常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-09 17:00:07 细胞资源库平台 访问量:113
来自法国里昂第一大学 Claude Bernard 大学 CNRS UMR 5261 研究所 Fabien Le Grand 团队发表在《STAR Protocols》题为《Protocol for cell proliferation and cell death analysis of primary muscle stem cell culture using flow cytometry》的实验方案,聚焦 MuSCs 研究的技术痛点。MuSCs 是骨骼肌损伤修复的核心细胞,其增殖与凋亡平衡直接决定修复效率,但传统检测方法存在局限:免疫染色法操作复杂,TUNEL assay 因 MuSCs 对培养环境敏感、易脱落,导致凋亡检测偏差;且缺乏同时分析同一来源 MuSCs 增殖与死亡的标准化流程。此前研究虽证实 EdU(检测 S 期增殖)、PI(区分坏死 / 活细胞)、YO-PRO-1(早凋亡标记)可分别用于细胞功能检测,却未形成针对 MuSCs 的整合方案。因此,本研究建立从 MuSCs 分离、纯度验证到流式同步检测的完整 protocol,确保结果可靠且可重复。
本方案旨在提供原代肌肉干细胞(MuSCs)的分离、培养及同步分析细胞增殖与死亡的标准化流程。方法:从 8-12 周龄 B6 小鼠后肢肌肉(腓肠肌、胫骨前肌等)分离 MuSCs,经胶原酶 II/Dispase 消化、MACS 负选富集,胶原 I 包被培养皿接种;通过 PAX7 免疫染色(≥80% 阳性为合格)验证纯度;细胞死亡分析用活细胞染色(PI 标记坏死 / 晚凋亡,YO-PRO-1 标记早凋亡,H₂O₂做阳性对照),流式区分活细胞 / 早凋亡 / 晚凋亡 / 坏死细胞;细胞增殖分析用 EdU 标记 S 期细胞,结合 PI 染色分析细胞周期(G0/G1、S、G2/M 期)。结果:可从同一批 MuSCs 同步获得增殖(各周期比例)与死亡(各凋亡阶段比例)数据,纯度验证确保细胞特异性,流式检测重复性高。结论:本方案为 MuSCs 功能研究(如基因敲除对其存活增殖的影响)提供标准化工具,适用于肌肉再生机制及相关疾病研究。
MuSCs 的分离、培养与纯度验证:实验经法国伦理委员会批准(APAFIS#34582-202111121631816 v3),取 8-12 周龄 B6 小鼠后肢肌肉,机械剪碎后用胶原酶 II(Mix I:800 U/mL,Mix II:300 U/mL+Dispase 3.3 U/mL)分步消化(37℃,1h+30min),29G 针头吹打后经 70μm/30μm 滤网过滤,MACS 缓冲液洗涤后用卫星细胞分离磁珠负选富集 MuSCs;胶原 I 包被(0.1g/L)培养皿接种,用含 20% FBS、bFGF 的 Ham’s F-10 培养基培养,2 天换液一次至 70% 汇合;纯度验证采用 PAX7 免疫染色:4% 多聚甲醛(PFA)固定 10min,透化液处理后封闭 1h,PAX7 一抗(1:2 稀释)4℃孵育 12h,Alexa Fluor 488 二抗(1:1000 稀释)室温孵育 1h,Hoechst 染核,荧光显微镜成像,ImageJ 计数 PAX7 阳性细胞比例(需≥80%)。
细胞增殖与死亡的流式分析:细胞死亡检测:活细胞用 20mM H₂O₂处理 20min 做阳性对照,收集培养液及胰酶消化的细胞,350×g 离心 5min,PBS 重悬后加 PI(终浓度 5μg/mL)37℃孵育 30min,洗涤后加 YO-PRO-1(终浓度 1μM)室温孵育 20min,30μm 滤网过滤,BD FACSCanto II 流式仪检测(Alexa Fluor 488 通道检测 YO-PRO-1,PE 通道检测 PI),设未染色、单染对照做补偿, gated 区分活细胞(PI⁻YO-PRO-1⁻)、早凋亡(PI⁻YO-PRO-1⁺)、晚凋亡(PI⁺YO-PRO-1⁺)、坏死(PI⁺YO-PRO-1⁻);细胞增殖检测:细胞培养至 70% 汇合前 1h 加 EdU(1:40 稀释),胰酶消化后 70% 冷乙醇固定,Click-iT EdU 试剂盒标记(Alexa Fluor 647),加 PI(5μg/mL)+RNase A(0.1μg/mL)4℃孵育 5min,流式检测(APC 通道检测 EdU,PE 通道检测 PI),分析细胞周期(G0/G1 期:EdU⁻PI 低,S 期:EdU⁺PI 中,G2/M 期:EdU⁻PI 高)。
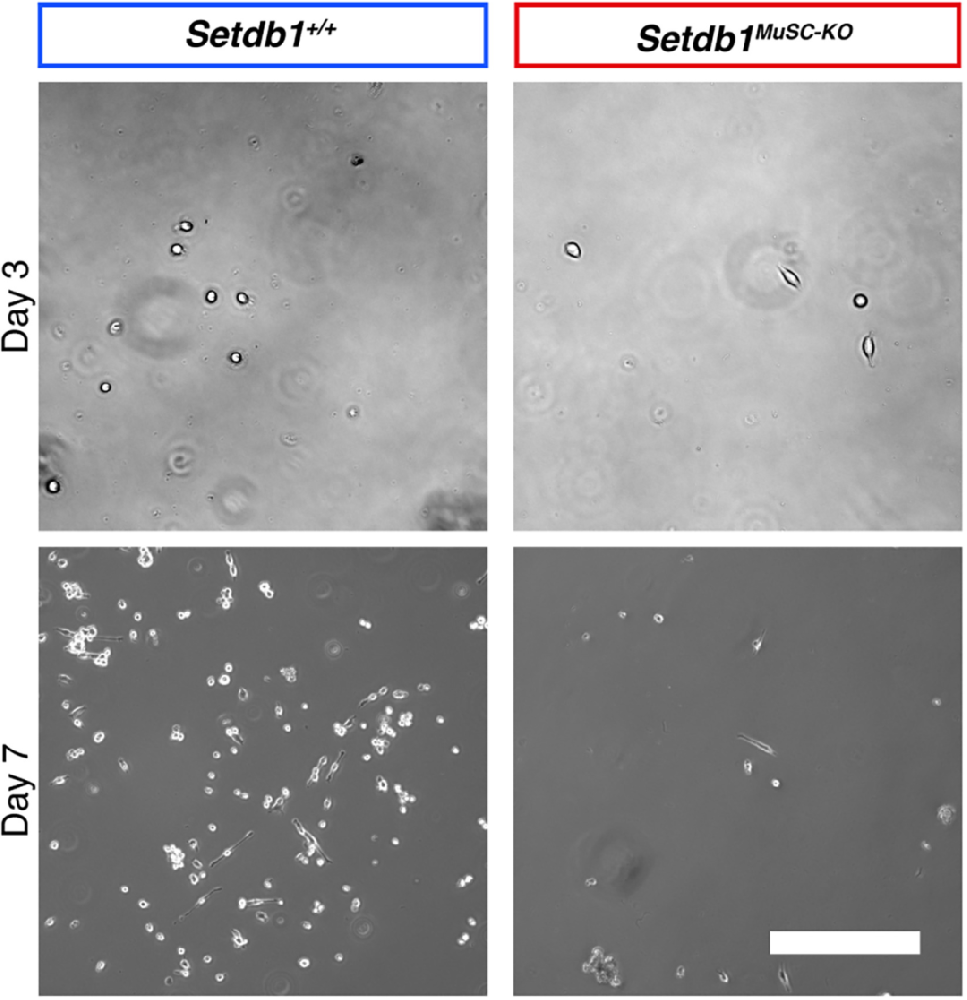
图1:MuSCs 增殖形态观察
该图为 Setdb1+/+(野生型)与 Setdb1MuSC-KO(MuSCs 特异性敲除)细胞在分离后 3 天和 7 天的增殖照片:两组细胞均呈梭形贴壁生长,7 天较 3 天细胞密度显著增加,Setdb1MuSC-KO 细胞增殖速度略慢于野生型;比例尺 100μm,证实本方案培养条件可支持 MuSCs 正常增殖,且基因敲除对增殖的影响可通过形态观察初步判断。
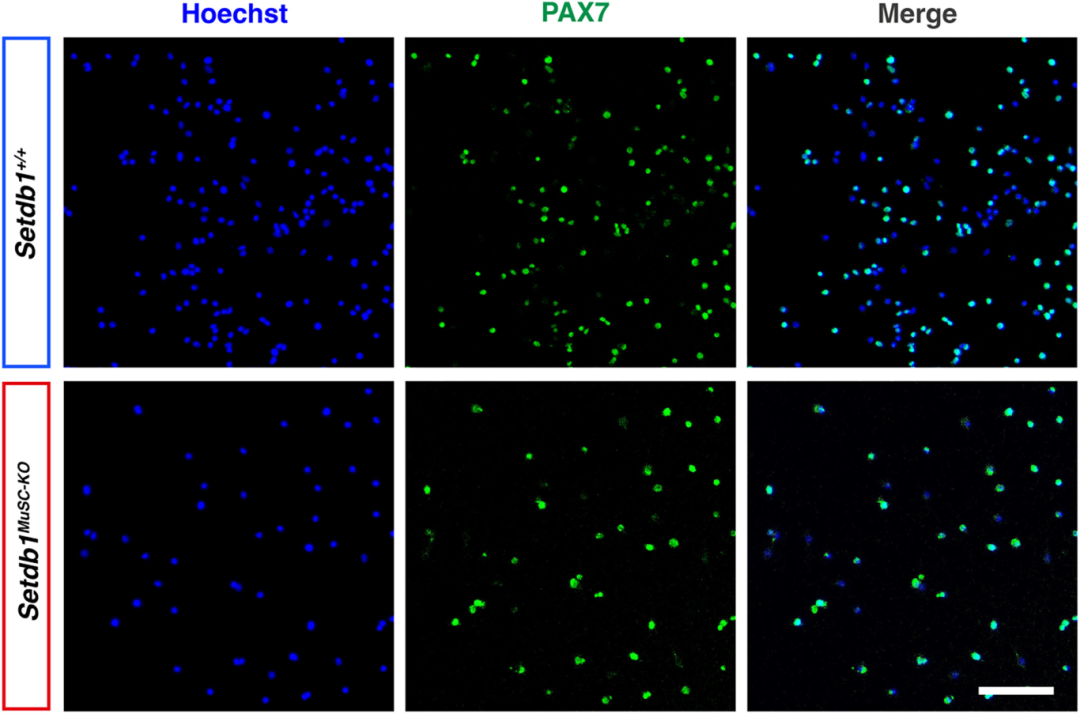
图2:PAX7 免疫染色验证 MuSCs 纯度
该图为 MuSCs 的 PAX7 免疫染色结果:左侧为 Hoechst 核染色(蓝色),中间为 PAX7 阳性信号(绿色),右侧为 Merge 图;PAX7 阳性信号集中在细胞核,与 Hoechst 共定位,证实培养细胞为 MuSCs;比例尺 100μm,结合 ImageJ 计数,可确保 PAX7 阳性细胞比例≥80%,排除成纤维细胞等杂细胞干扰,为后续功能检测提供细胞纯度保障。
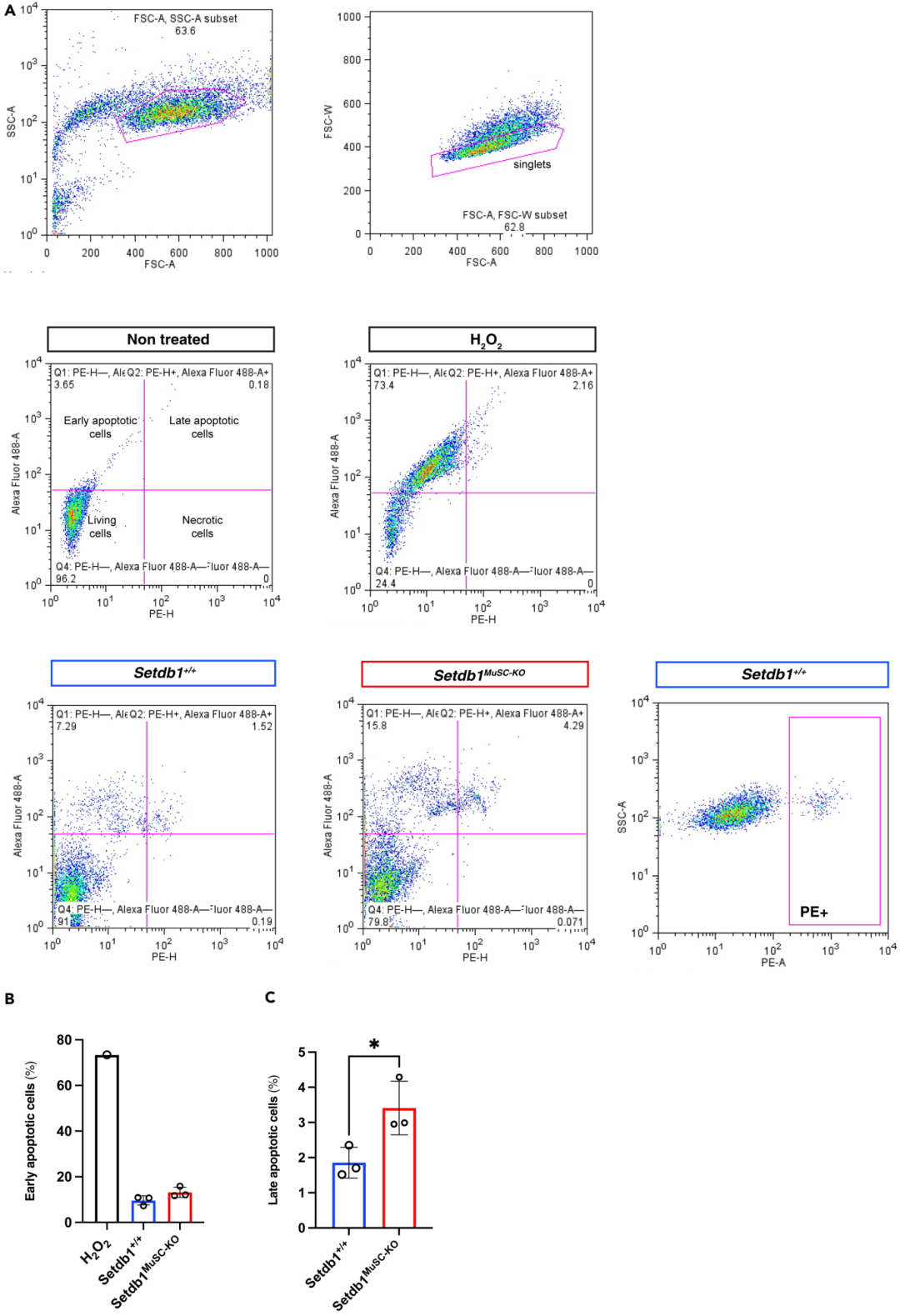
图3:MuSCs 细胞死亡的流式分析
该图为流式检测细胞死亡的典型结果:A 图为散点图(左:FSC-A/SSC-A gated 单细胞,右:YO-PRO-1/PI 双染),通过象限 gated 区分活细胞(Q4:PI⁻YO-PRO-1⁻)、早凋亡(Q1:PI⁻YO-PRO-1⁺)、晚凋亡(Q2:PI⁺YO-PRO-1⁺)、坏死(Q3:PI⁺YO-PRO-1⁻),H₂O₂处理组凋亡细胞比例显著升高;B 图为定量柱状图,显示 Setdb1MuSC-KO 组早凋亡(约 3%)、晚凋亡(约 2%)比例高于 Setdb1+/+ 组(早凋亡约 1%,晚凋亡约 0.5%),证实本方案可精准量化不同基因型 MuSCs 的凋亡差异。
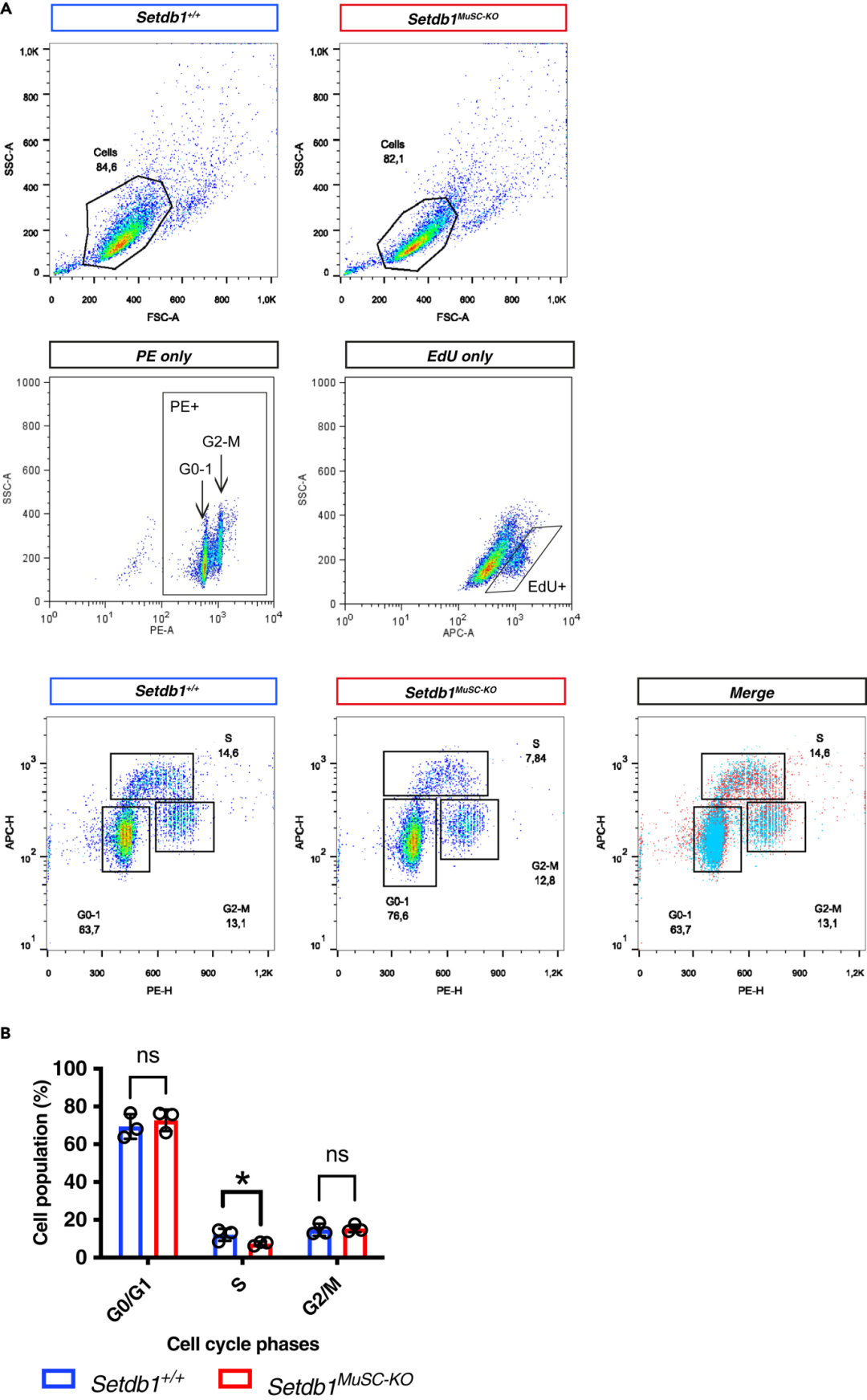
图4:MuSCs 细胞增殖的流式分析
该图为流式检测细胞增殖的典型结果:A 图为散点图(左:FSC-A/SSC-A gated 单细胞,右:EdU/PI 双染),通过信号强度区分 G0/G1 期(EdU⁻PI 低)、S 期(EdU⁺PI 中)、G2/M 期(EdU⁻PI 高),Setdb1MuSC-KO 组 S 期细胞比例(约 12.4%)低于 Setdb1+/+ 组(约 14.8%);B 图为定量柱状图,显示两组 G0/G1、G2/M 期比例无显著差异(ns),但 Setdb1MuSC-KO 组 S 期比例显著降低(*P<0.05),证实本方案可精准分析 MuSCs 的细胞周期分布,捕捉基因敲除对增殖的抑制效应。
本实验方案建立了从原代 MuSCs 分离、纯度验证到流式细胞术同步分析增殖与死亡的完整流程:通过 MACS 负选与 PAX7 染色确保细胞纯度(≥80%),用 PI/YO-PRO-1 活细胞染色区分凋亡阶段,EdU/PI 固定细胞染色分析细胞周期,解决传统方法检测偏差问题;方案重复性高,可从同一批 MuSCs 获得增殖与死亡双重数据,适用于研究基因调控(如 Setdb1)、药物处理等对 MuSCs 功能的影响;需注意细胞接种量(确保流式检测≥10000 个事件)、胶原包被质量(避免细胞脱落)及单染对照设置(确保补偿准确),为肌肉再生机制研究及相关疾病(如肌营养不良)的 MuSCs 功能评估提供标准化技术支撑。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:神经生物学中的原代细胞培养:小鼠胚胎后脑神经元培养的优化方案
下一篇:Nature 重磅!Ostα/β 结构解析揭示胆汁酸转运新机制