常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-08 08:00:12 细胞资源库平台 访问量:118
前列腺素 E₂(PGE₂)在脑缺血、炎症反应及血管生成中发挥关键作用,且与血脑屏障(BBB)破坏密切相关,此前研究已发现其通过 EP₂、EP₃、EP₄受体协同促进人脑内皮细胞(HBECs)迁移,但下游信号机制尚未明确;Rho 相关激酶(ROCK)是调控细胞迁移的关键分子,ROCK II 在脑等高表达,却未明确 HBECs 中 ROCK 亚型表达特征及 PGE₂如何通过 ROCK 调控迁移,故本研究聚焦上述机制空白。
本研究通过 RT-PCR、ELISA、Transwell 迁移实验、RNA 干扰、药理学抑制及小鼠主动脉环实验,探究 PGE₂诱导 HBECs 迁移的信号通路。结果显示:HBECs 仅表达 ROCK II;PGE₂(0.1nM 最适浓度)以剂量和时间依赖方式诱导 ROCK II 表达,15 分钟达峰值;抑制 ROCK II(Y27632 或 siRNA)或上游 PKA / 腺苷酸环化酶(H-89 或 ddA),可显著减弱 PGE₂诱导的 HBECs 迁移、MLC 磷酸化及 F-actin 聚合;ex vivo 实验中 ROCK II 抑制剂可抑制 PGE₂诱导的血管出芽。结论:PGE₂通过 “cAMP-PKA-ROCK II-MLC 磷酸化 - F-actin 聚合” 通路介导 HBECs 迁移,为脑血管疾病中异常血管生成提供潜在靶点。
实验经萨尔国王大学伦理委员会批准(KFU-REC-2024-MAY-ETHICS238),使用 25-30g 瑞士白化小鼠(乌拉坦麻醉);HBECs 购自 Cell Systems,用含 10% FBS 的内皮培养基培养(2-10 代细胞);通过 RT-PCR/ELISA 检测 ROCK 亚型,Transwell 实验(上室接种 1×10⁵细胞,下室加 PGE₂)检测迁移,RNA 干扰(转染 2nmol ROCK II siRNA)沉默 ROCK II,免疫印迹检测 MLC 磷酸化,NBD-phallacidin 染色观察 F-actin,主动脉环实验(包埋 Matrigel 培养 7 天)验证血管生成;所有实验重复≥5 次,数据以均值 ±SEM 表示,单因素 ANOVA+Bonferroni 多重比较分析。
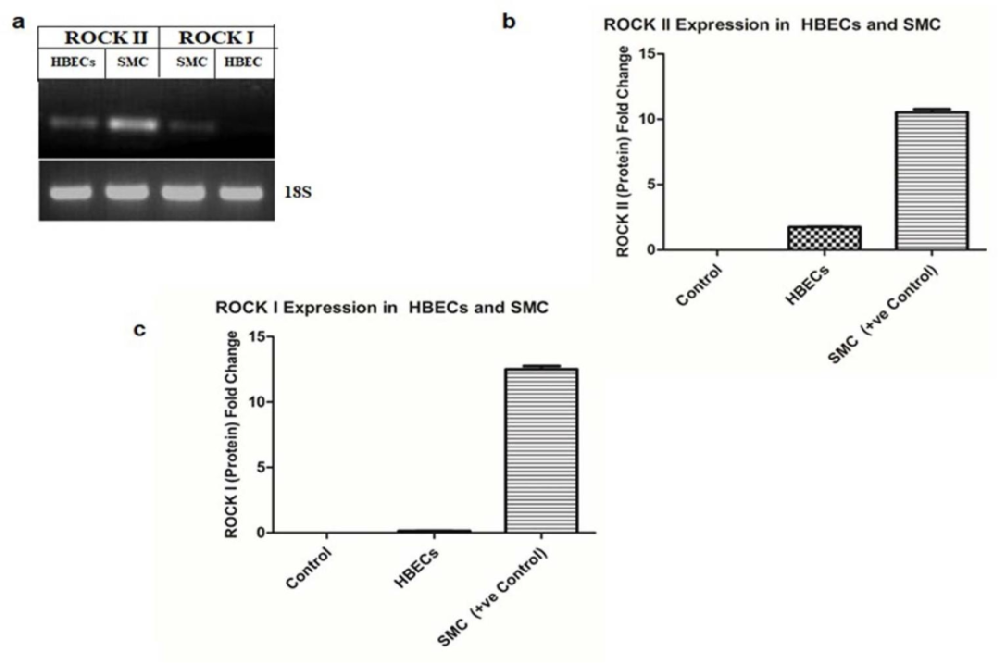
图1:HBECs 中 ROCK 亚型的表达特征
该图通过 RT-PCR(扩增 ROCK I/II mRNA,18S rRNA 为内参)和 ELISA(检测 ROCK I/II 蛋白),对比 HBECs 与平滑肌细胞(SMC)的 ROCK 表达,显示 HBECs 仅检测到 ROCK II,无 ROCK I 表达,而 SMC 同时表达两种亚型,证实 HBECs 特异性表达 ROCK II。
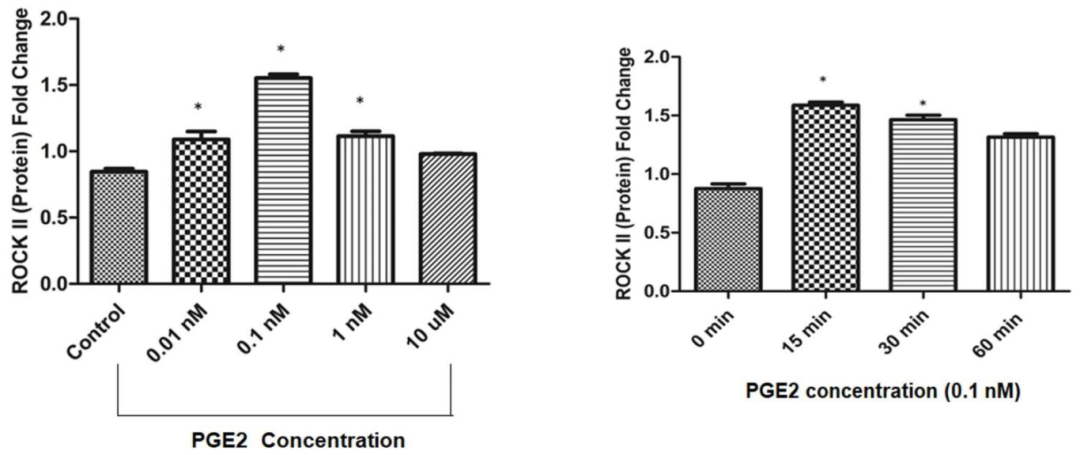
图2:PGE₂以剂量和时间依赖方式诱导 ROCK II 表达
该图显示,剂量依赖实验(0.01-10nM PGE₂)中 0.1nM PGE₂诱导 ROCK II 表达最强;时间依赖实验(0.1nM PGE₂处理 0-60 分钟)中 15 分钟 ROCK II 表达达峰,30 分钟后下降,明确 PGE₂诱导 ROCK II 的最适条件为 0.1nM、15 分钟。
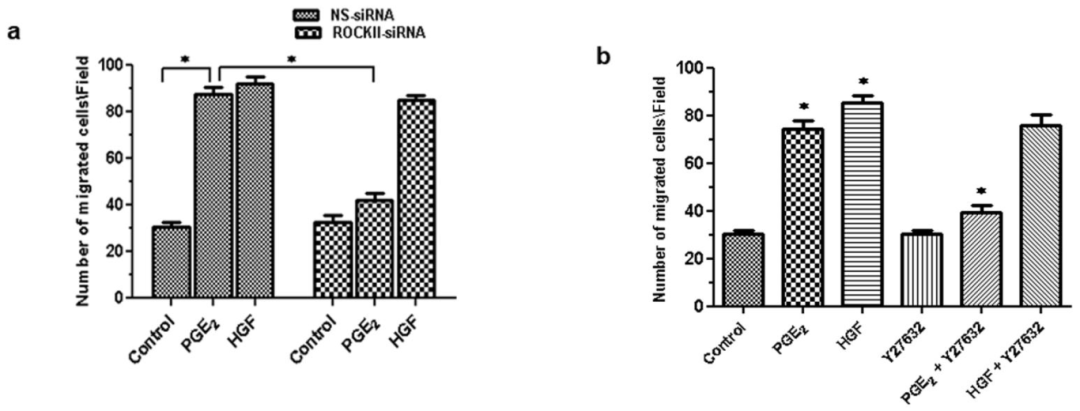
图3:ROCK II 是 PGE₂诱导 HBECs 迁移的关键分子
该图通过 RNA 干扰和药理学抑制实验,发现转染 ROCK II siRNA 或用 150nM Y27632(ROCK II 抑制剂)预处理,均显著减弱 PGE₂诱导的 HBECs 迁移,而 HGF(阳性对照)迁移不受影响,证实 PGE₂依赖 ROCK II 介导 HBECs 迁移。
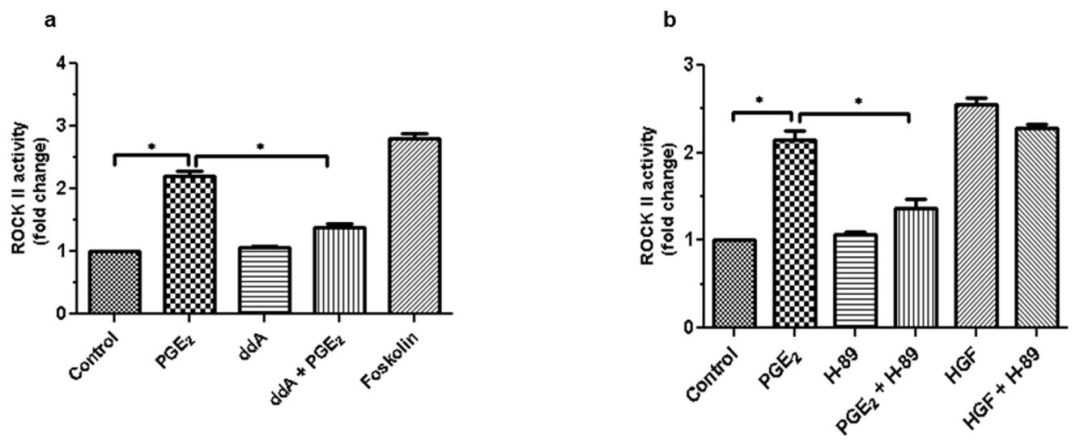
图4:PGE₂诱导 ROCK II 激活依赖 cAMP-PKA 轴
该图显示,用 1μM ddA(腺苷酸环化酶抑制剂)或 0.5μM H-89(PKA 抑制剂)预处理,均显著降低 PGE₂诱导的 ROCK II 活性;forskolin(腺苷酸环化酶激活剂)可激活 ROCK II,表明 PGE₂通过 cAMP-PKA 通路激活 ROCK II。
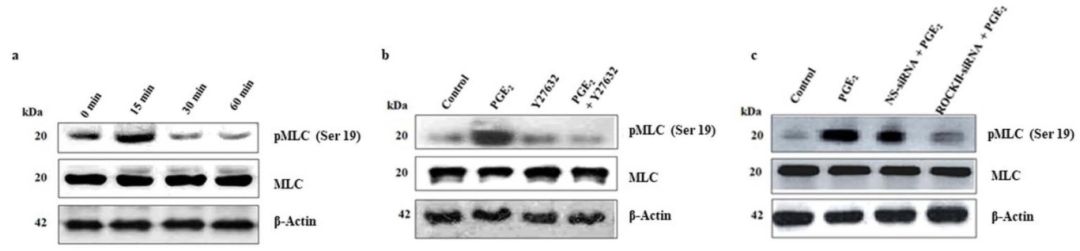
图5:PGE₂诱导 MLC 磷酸化依赖 ROCK II
该图通过免疫印迹(检测 phospho-MLC Ser19,总 MLC 和 β-actin 为内参),发现 PGE₂以时间依赖方式诱导 MLC 磷酸化,转染 ROCK II siRNA 或用 Y27632 预处理可显著减弱该效应,证实 PGE₂通过 ROCK II 介导 MLC 磷酸化。
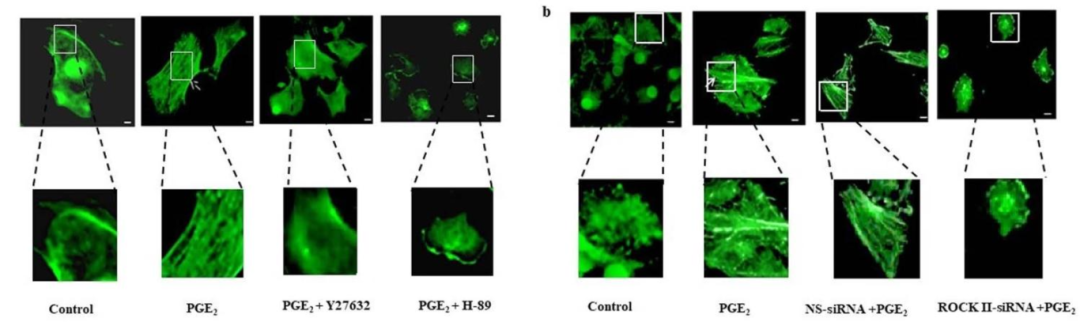
图6:PGE₂诱导 F-actin 聚合依赖 PKA-ROCK II 通路
该图通过 NBD-phallacidin 染色,显示用 Y27632、H-89 预处理或转染 ROCK II siRNA,均显著减少 PGE₂诱导的 F-actin 聚合,阴性对照 siRNA 无影响,表明 PGE₂通过 PKA-ROCK II 通路促进 F-actin 聚合。
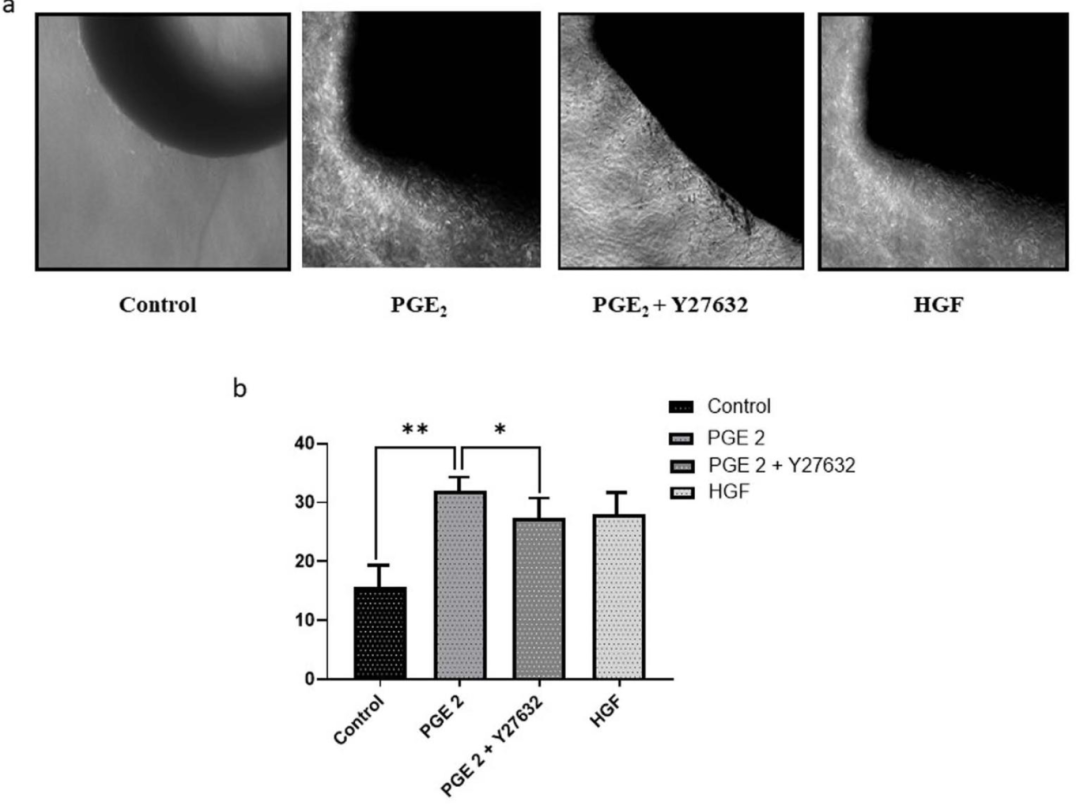
图7:PGE₂诱导血管生成依赖 ROCK II
该图通过 ex vivo 主动脉环实验,显示 PGE₂处理 7 天后主动脉环血管出芽显著增多,Y27632 预处理可抑制该效应;定量分析显示 PGE₂组出芽距离长于对照组,Y27632 组短于 PGE₂组(p<0.05),证实 PGE₂通过 ROCK II 介导血管生成。
本研究首次明确 HBECs 特异性表达 ROCK II,且 PGE₂通过 “cAMP-PKA-ROCK II-MLC 磷酸化 - F-actin 聚合” 通路介导 HBECs 迁移,ex vivo 主动脉环实验进一步验证该通路对血管生成的调控作用,填补了 PGE₂调控脑内皮细胞迁移的机制空白,为脑缺血、脑炎症等脑血管疾病中异常血管生成的靶向治疗提供理论依据;研究局限在于 HBECs 供体单一且缺乏在体动物模型验证,后续需扩大供体样本并结合动物实验深化机制转化。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:沙眼衣原体(Chlamydia trachomatis)与人原代宫颈内膜基质细胞互作的双 RNA 测序分析
下一篇:神经生物学中的原代细胞培养:小鼠胚胎后脑神经元培养的优化方案