常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-04 09:00:00 细胞资源库平台 访问量:129
登革病毒(DENV)是全球传播最快的蚊媒病毒,每年感染 1-4 亿人,WHO 已将其列为 “3 级紧急公共卫生事件”。然而,DENV 感染的发病机制仍不明确,且无获批抗病毒药物,现有研究模型存在显著缺陷:
动物模型:小鼠等动物与人类肝脏生理结构、免疫反应差异大,无法复现登革热重症肝损伤(如肝细胞坏死);
细胞系模型:Huh7 等永生细胞系缺乏肝脏细胞异质性和生理微环境,感染后仅出现轻微表型(如核碎裂),无法模拟临床重症病理;
原代肝细胞模型:来源有限、长期培养易失活,难以用于感染动态和药物筛选研究。
肝脏是 DENV 感染的关键靶器官,临床中重症患者常伴随肝损伤(转氨酶升高、肝细胞坏死),因此亟需一种能复现人类肝脏生理特征的体外模型。人多能干细胞(hPSC)衍生肝类器官(hPLO)因具备细胞异质性(肝细胞、胆管细胞、星状细胞)和肝脏功能(白蛋白分泌、尿素合成、CYP 酶活性),成为解决上述问题的理想选择。本研究构建 hPLO 模型,用于 DENV 感染建模、发病机制解析及抗病毒药物筛选。
来自中国军事医学科学院、首都儿科研究所的团队在《Nature Communications》(2025 年,Vol. 16)发表题为Recapitulating dengue virus infection with human pluripotent stem cell-derived liver organoids for antiviral screening的研究。
(1)研究方法
1.hPLO 的构建与鉴定
分化流程:hPSC(hiPSC、H1/H9 hESC)经 “定形内胚层(DE)→肝定向分化(HS)→3D 类器官形成” 分阶段诱导:
2D 阶段(D0-D10):用 Activin A、CHIR99021 诱导 DE,再用 bFGF、BMP4 诱导 HS;
3D 阶段(D10 后):HS 细胞嵌入 Matrigel,用含 Wnt3a、R-spondin1、EGF 的培养基培养,25 天形成可扩展 hPLO,50 天形成成熟 hPLO;
鉴定方法:免疫荧光(检测 AFP/ALB/HNF4A 等肝细胞标志物、KRT7/KRT19 胆管标志物)、功能实验(ICG 摄取释放、PAS 糖原染色、CYP3A4/CYP2C9 酶活性)、scRNA-seq(细胞组成分析)。
2.DENV-2 感染实验
感染条件:25 天 hPLO(更易感染,形态变化显著)经机械解离为 30-100μm 片段,以 1 PFU / 片段接种 DENV-2(TSV01 株);
检测指标:形态观察、Live/Dead 染色(细胞死亡)、RT-qPCR(病毒 RNA)、空斑实验(病毒滴度)、免疫荧光(DENV 抗原定位)、TEM(病毒颗粒)。
3.scRNA-seq 分析
样本:感染后 1、2、8 天的 hPLO 及对照,共 59029 个高质量细胞;
分析工具:UMAP 聚类、GSVA 富集、伪时间分析,重点解析细胞组成变化、病毒分布及差异表达基因(DEGs)。
4.抗病毒药物筛选与验证
筛选库:含 7DMA(广谱抗病毒药)、JNJ1802(已知抗 DENV 药)及线粒体保护剂 ORES(氧化白藜芦醇)、RTA 408(NRF2 激活剂);
验证:hPLO 中检测药物对病毒复制(RT-qPCR)、肝功能(ALB 分泌、CYP 活性)的恢复作用,AG6 小鼠(IFNα/γR-/-)中验证药物体内 efficacy。
(2)关键结果
1.hPLO 的构建与功能验证
细胞组成:含 4 种主要细胞类型 —— 肝细胞样细胞(表达 ALB/HNF4A)、增殖肝细胞样细胞(表达 MKI67/PCNA)、胆管细胞样细胞(表达 KRT7/KRT19)、肝星状细胞样细胞(表达 PDGFRB/COL3A1)(图 1n-o);
肝功能:可摄取并释放 ICG(7-14h 完全释放)、储存糖原(PAS 染色阳性)、分泌白蛋白(ALB)和尿素,CYP3A4/CYP2C9 酶活性与原代肝细胞(PHHs)相当(图 2g-k)。
2.hPLO 对 DENV-2 的易感性
形态变化:感染后 2 天,hPLO 从空心透明球体变为实心小体,6 天 90% 类器官失去健康形态(图 3b-c);
细胞死亡:感染后 4 天,Live/Dead 染色显示大量红色死亡细胞,对照几乎全为绿色活细胞(图 3d);
病毒复制:感染后 2-8 天,病毒 RNA 和滴度显著升高(RNA 增加 10³ 倍,滴度达 10⁶ PFU/mL),TEM 观察到病毒颗粒,DENV 抗原广泛分布于肝细胞样和增殖肝细胞样细胞(图 3e-g、3h-j)。
3.scRNA-seq 揭示感染机制
靶细胞:增殖肝细胞样细胞是主要感染靶细胞,感染后 8 天其比例下降 10%,而胆管 / 星状细胞比例分别增加 5%/10%(图 4d-g);
分子机制:感染后肝细胞样细胞中线粒体基因(MT-CO1/2/3、MT-CYB)表达下调,氧化应激相关基因(H19)上调,NRF2 通路下游抗氧化基因(GPX1、C1QBP)下调,提示线粒体损伤和氧化应激是核心发病机制(图 5a、5d);
免疫反应:胆管 / 星状细胞中炎症反应(IL-1β/TNFα)、I 型干扰素通路(MX1、ISG15)激活,而肝细胞样细胞免疫反应薄弱,导致易感性更高(图 5g-i)。
4.抗病毒药物筛选与验证
候选药物:ORES(10μM)和 RTA 408(0.2μM)可显著恢复 hPLO 健康形态(健康比例从 10% 升至 60%),降低病毒 RNA(下降 10²-10³ 倍)(图 6d-h、6j-m);
作用机制:激活 NRF2 通路,恢复下游抗氧化基因(HMOX1、GPX2)表达,减少氧化应激,保护线粒体功能,恢复肝糖原储存、CYP 活性及 ALB / 尿素分泌(图 6n-s);
体内验证:AG6 小鼠口服 ORES(60mg/kg)或 RTA 408(15mg/kg)后,肝脏和血清中 DENV RNA 显著降低(下降 50%-70%)(图 7d-e)。
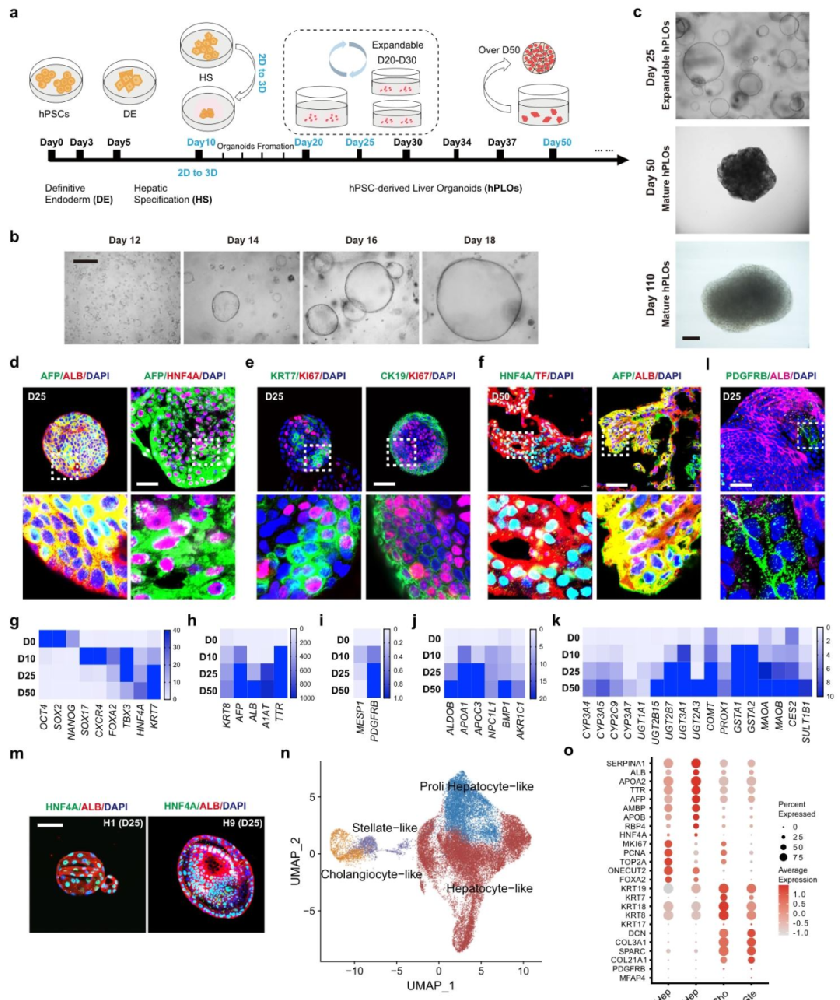
图 1:hPLO 的构建与细胞组成鉴定
该图核心是验证 hPLO 的成功构建及细胞异质性。(A)分化流程:hPSC→DE→HS→2D 到 3D 类器官(D10 启动 3D 培养,D25 可扩展,D50 成熟);(B-C)形态变化:D12-D18 从 20-30μm 空心球生长至 600-800μm,D25-D110 维持稳定形态;(D-F)免疫荧光:D25 hPLO 表达 AFP/ALB/HNF4A(肝细胞)、KRT7/KRT19(胆管细胞)、KI67(增殖),D50 表达成熟肝细胞标志物 TF;(G-K)基因表达热图:分化过程中干细胞标志物(OCT4)下调,肝脏标志物(ALB、CYP3A4)上调;(N-O)scRNA-seq:UMAP 聚类显示 4 种细胞类型,_dot 图验证各细胞标志物(如肝细胞样细胞的 SERPINA1、星状细胞的 PDGFRB)。图示证明 hPLO 具备肝脏细胞异质性和分化成熟特征。
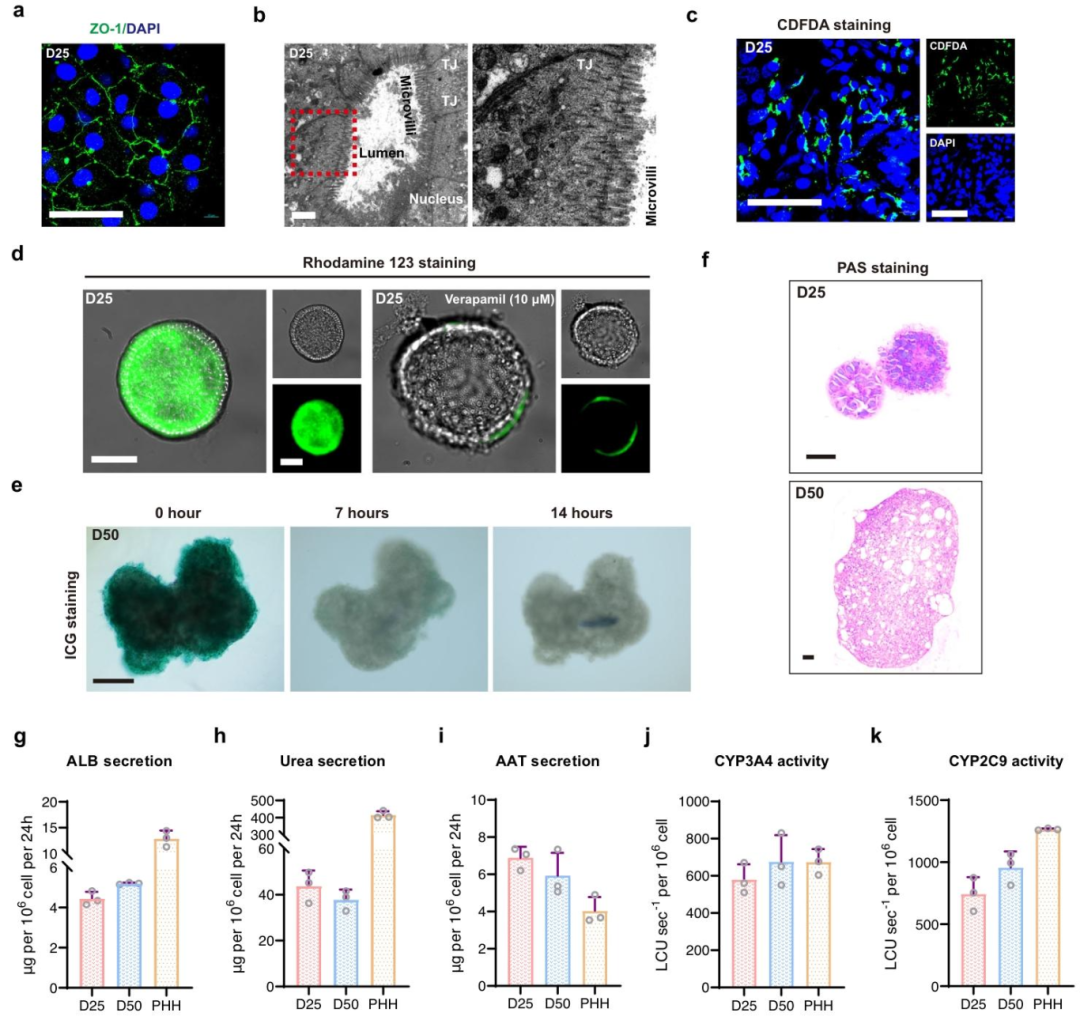
图 2:hPLO 的功能验证
该图证实 hPLO 的肝脏生理功能。(A-B)超微结构:TEM 观察到胆管细胞间紧密连接(ZO-1 阳性)和微绒毛,符合胆管结构;(C-F)功能实验:CDFDA 染色显示胆汁 canaliculi 形成(MRP2 活性),Rhodamine 123 转运实验证实 MDR1 活性(Verapamil 可抑制),ICG 7-14h 完全释放,PAS 染色显示糖原储存;(G-K)定量功能:D25/D50 hPLO 的 ALB / 尿素 / AAT 分泌量、CYP3A4/CYP2C9 活性与原代肝细胞相当。图示 hPLO 具备完整肝脏代谢和转运功能。
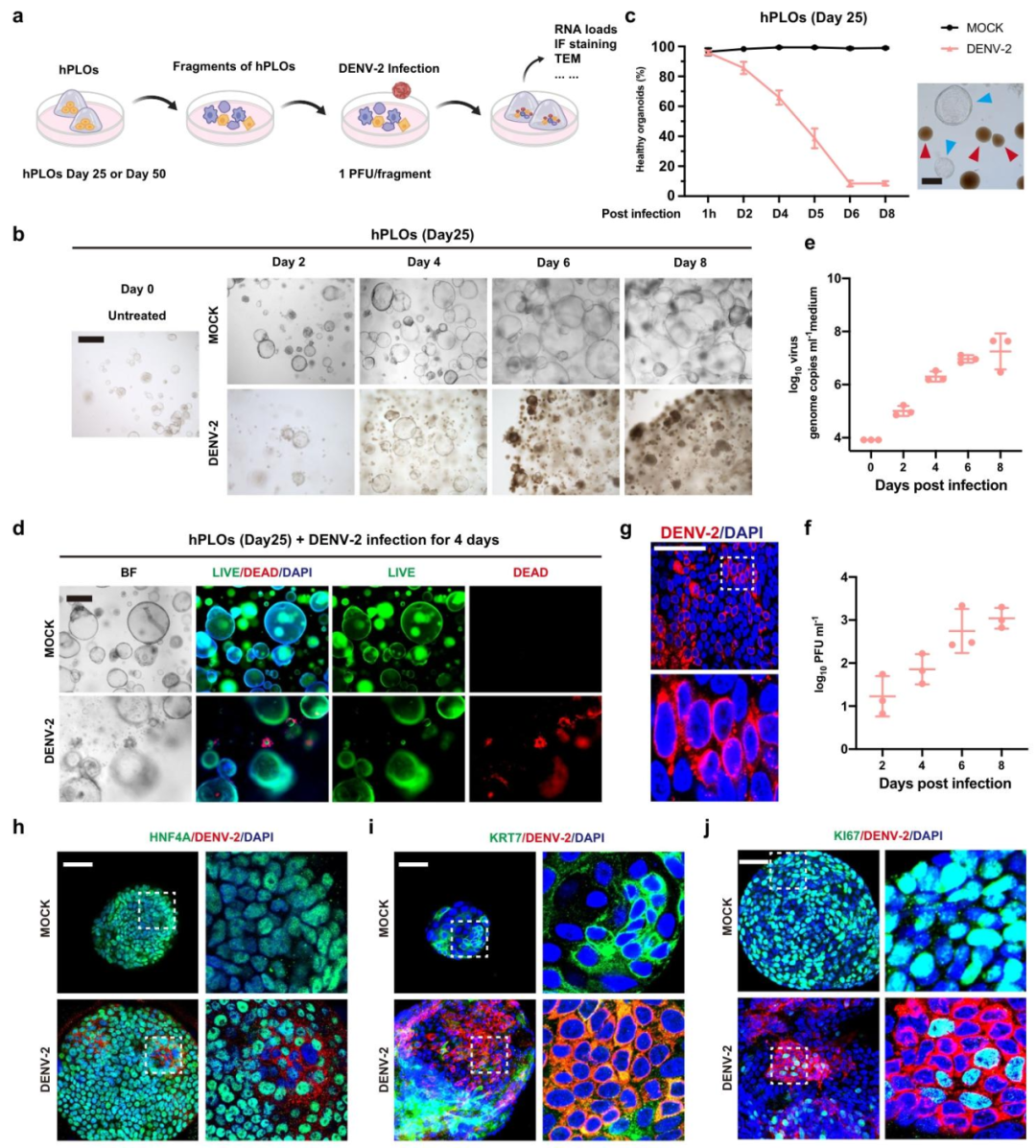
图 3:hPLO 感染 DENV-2 后的表型与病毒复制
该图直观展示感染后的病理变化。(A)实验设计:hPLO 片段接种 DENV-2(1 PFU / 片段);(B-C)形态量化:感染后 6 天 90% hPLO 变为实心小体,对照无变化;(D)Live/Dead 染色:感染组红色死亡细胞显著增多;(E-F)病毒定量:病毒 RNA 和滴度随时间升高;(G-J)免疫荧光:DENV 抗原(绿)与 HNF4A(肝细胞,红)、KI67(增殖,红)共定位,证实感染靶细胞。图示 hPLO 可复现 DENV 感染的临床病理特征。
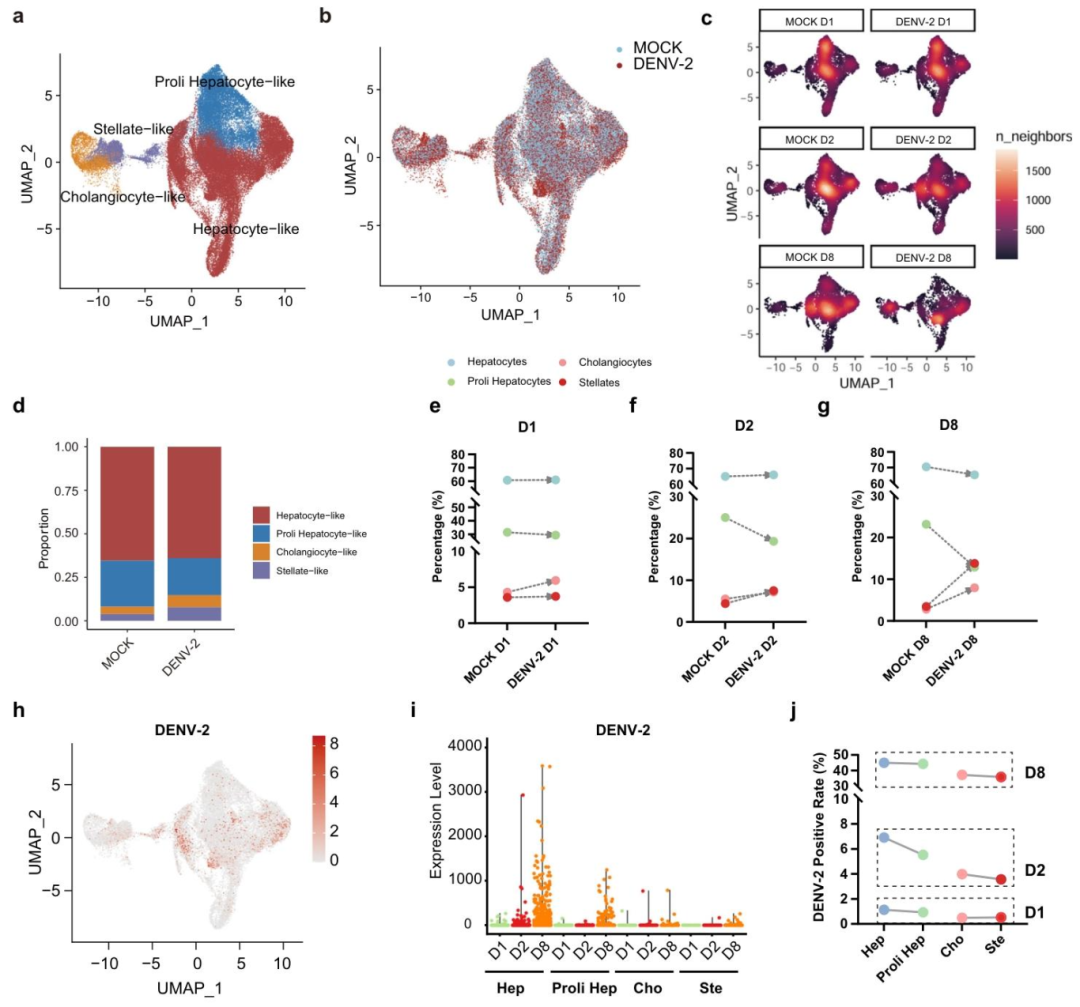
图 4:scRNA-seq 的细胞聚类与感染动态
该图解析感染对细胞组成的影响。(A-B)UMAP 聚类:对照与感染组细胞分布差异显著,感染后 8 天变化最明显;(C)密度图:感染后 2 天细胞组成开始改变,8 天差异扩大;(D-G)细胞比例:增殖肝细胞样细胞比例下降 10%,胆管 / 星状细胞比例升高;(H-J)病毒分布:感染后 8 天 45% 肝细胞样 / 增殖肝细胞样细胞呈 DENV 阳性,胆管 / 星状细胞阳性率 35%。图示增殖肝细胞样细胞是主要靶细胞,感染导致细胞组成失衡。
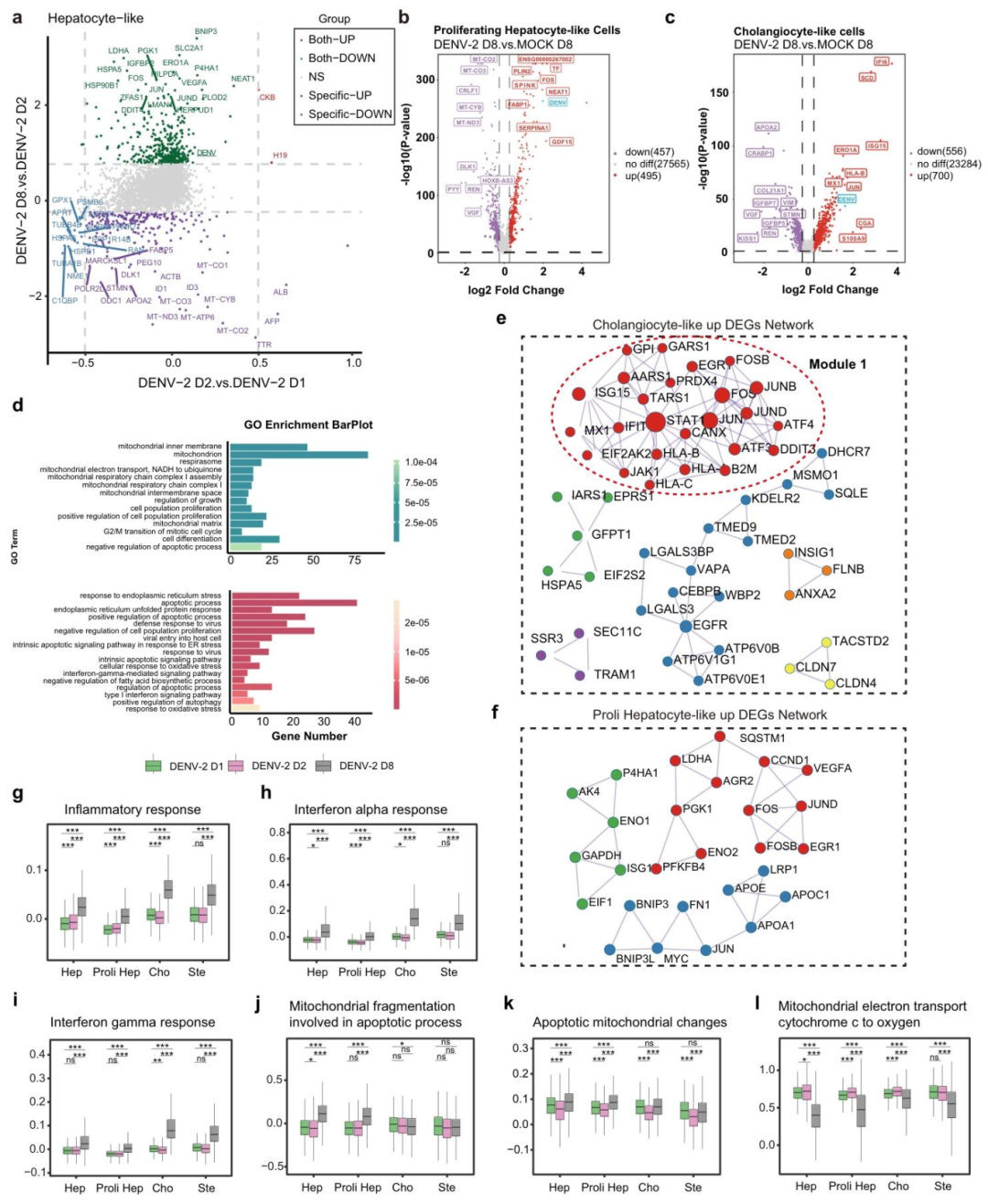
图 5:感染后的发病机制(线粒体损伤与免疫反应)
该图揭示感染的分子机制。(A)DEG 分析:感染后肝细胞样细胞线粒体基因下调,氧化应激基因上调;(B-C)火山图:增殖肝细胞样细胞中 PLIN2(抗病毒)、NEAT1(线粒体应激)上调,线粒体基因下调;胆管细胞中 IFN 通路基因(IFI6、ISG15)上调;(D)GO 富集:增殖肝细胞样细胞上调基因富集 “病毒感染 / 凋亡”,下调基因富集 “线粒体呼吸链”;(G-L)功能评分:胆管 / 星状细胞炎症 / 干扰素评分高,肝细胞样细胞线粒体损伤评分高。图示线粒体损伤和免疫失衡是核心机制。
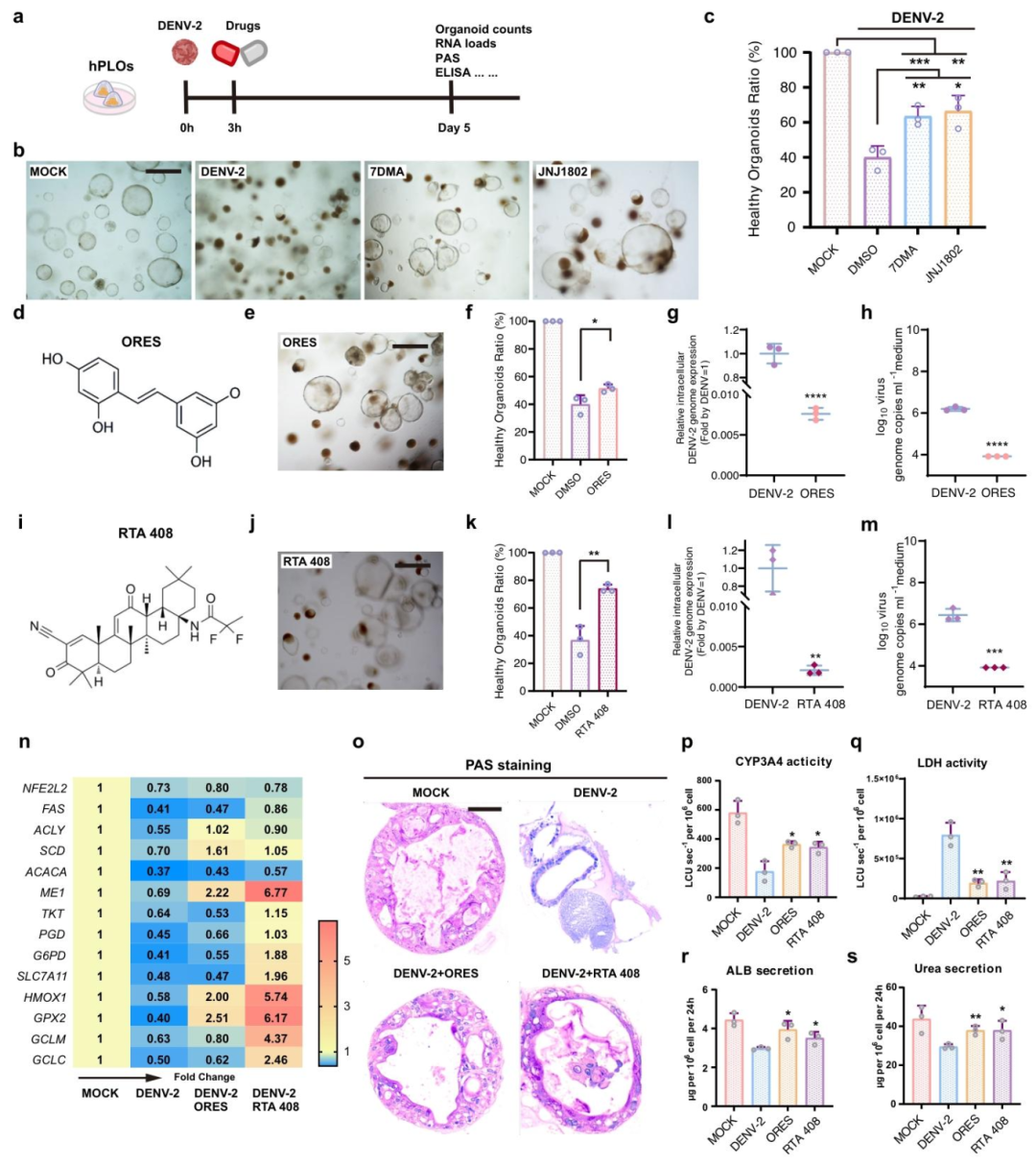
图 6:抗病毒药物筛选与功能恢复
该图展示药物筛选结果。(A)筛选流程:hPLO 感染后加药,检测形态、病毒量、肝功能;(B-C)阳性药验证:7DMA/JNJ1802 可恢复 hPLO 形态;(D-H)ORES 效果:10μM ORES 使健康类器官比例升至 60%,病毒 RNA 下降 10³ 倍;(I-M)RTA 408 效果:0.2μM RTA 408 同理;(N-S)机制验证:药物激活 NRF2 通路,恢复糖原储存、CYP 活性及 ALB / 尿素分泌。图示 ORES 和 RTA 408 是有效抗 DENV 药物。
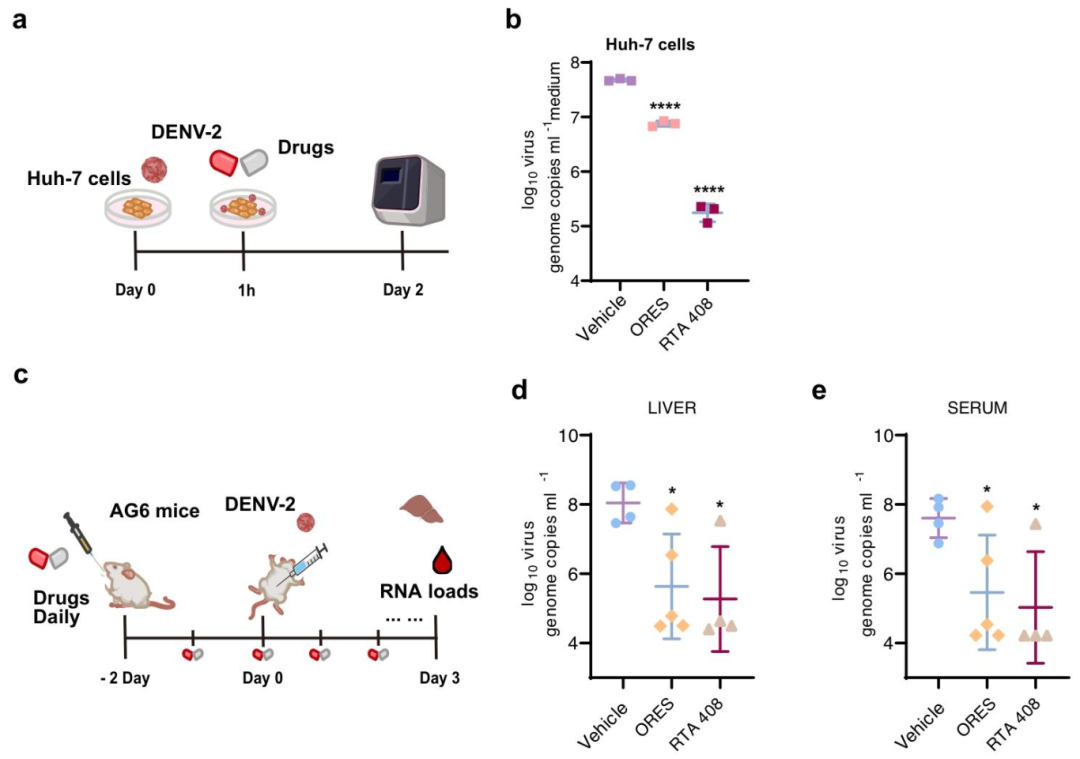
图 7:细胞与动物模型的药物验证
该图验证药物的体外 / 体内 efficacy。(A-B)Huh7 细胞:ORES/RTA 408 显著降低病毒 RNA;(C)动物实验设计:AG6 小鼠预处理 2 天,感染后给药 5 天;(D-E)体内效果:药物处理组肝脏 / 血清病毒 RNA 下降 50%-70%。图示药物在细胞和动物模型中均有效。
本研究首次构建了具备生理相关性的 hPSC 衍生肝类器官(hPLO)模型,解决了 DENV 感染研究中模型缺乏人体相关性的核心问题,核心创新点如下:
模型优势:hPLO 含 4 种肝脏细胞类型,具备完整肝功能,对 DENV-2 高度易感,可复现重症肝损伤(形态变化、细胞死亡),优于传统细胞系和动物模型;
机制突破:通过 scRNA-seq 发现增殖肝细胞样细胞是 DENV 主要靶细胞,线粒体损伤和 NRF2 通路抑制是关键发病机制,为 DENV 肝损伤提供新靶点;
药物发现:筛选出 ORES 和 RTA 408 两种 NRF2 激活剂,可通过抗氧化、保护线粒体发挥抗 DENV 作用,在 AG6 小鼠中验证有效,为临床治疗提供候选药物。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:单细胞 RNA 测序解析人类胎儿肾脏发育的分子图谱与先天性肾病关联