常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-02 17:04:17 细胞资源库平台 访问量:124
中脑类器官是模拟人脑中脑发育(如多巴胺能神经元生成)和研究中脑相关疾病(如帕金森病)的核心模型,但传统病毒感染技术存在三大痛点:① 病毒载量大导致细胞毒性高,破坏类器官结构完整性;② 无法精准靶向中脑特定功能区域(如管状脑室区 VZ,中脑神经发生的关键区域);③ 操作依赖复杂设备或多人协作,通量低,难以满足高通量研究需求。
现有中脑类器官分化方案虽能生成多巴胺能神经元,但缺乏与病毒精准递送结合的标准化流程。本研究团队开发了一套 “hPSC 分化中脑类器官→病毒注射设备组装→靶向显微注射→感染细胞可视化” 的完整 protocol,解决传统方法的靶向性差、毒性高问题,同时明确操作细节(如设备参数、类器官选择标准),为中脑疾病建模和基因编辑研究提供实用工具。
来自中国南京医科大学等机构的 Mengdan Tao、Yan Liu 团队在《STAR Protocols》(2025 年,Vol. 6)发表了题为Protocol for differentiating human pluripotent stem cells into midbrain organoids for targeted microinjection of viruses的研究。
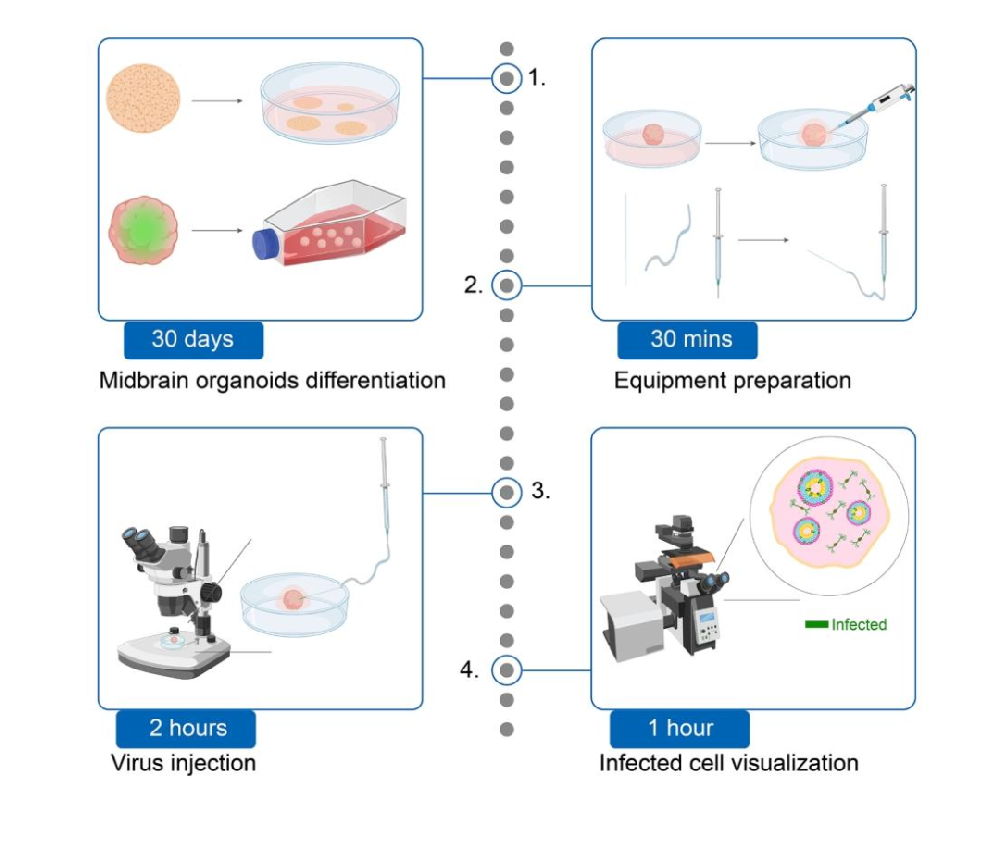
研究方法:
1.hPSC 培养与中脑类器官分化(30 天):
预准备:vitronectin 包被 6 孔板(0.5μg/cm²,4℃孵育≥12h),hPSC(ihtc-03、H9 等)用 Essential 8 培养基培养至 70-80% 融合;
分阶段诱导:
D0:换神经诱导培养基(含 2μM SB431542、2μM DMH1、0.4μM CHIR99021),启动神经分化;
D2-D8:每 2 天换半量培养基,维持上述因子,促进中脑前体形成;
D9:dispase(1U/mL)消化 7-10min,收集细胞团转移至培养瓶(T12.5/T25/T75,按类器官数量选择),培养基加 0.4μM CHIR99021、2μM SAG;
D11-D19:D11 起加 100μg/mL FGF8b,D14 起维持 FGF8b+SAG,促进中脑区域化;
D20-D30:换培养基为 FGF8b+20μg/mL SHHC25,诱导多巴胺能神经元成熟。
2.病毒注射设备准备与操作:
设备组装:用 Sutter P1000 拉针仪将玻璃毛细管拉制成 50μm 直径针尖(参数:Heat 510、Vel 135、Pressure 200),组装 2mL 注射器(清洗用)、10μL 微量注射器(注射用)、硅胶管(15-20cm),UV 消毒 30min;
类器官选择:D30 选择形态规则、边缘光滑的类器官(排除不规则、有破损的),单个置于培养皿,保留 30-50μL 培养基防干燥;
靶向注射:两人协作 —— 一人显微镜下将针尖插入类器官核心,另一人缓慢推注 0.2μL AAV9 病毒(滴度 1.0×10¹²GC/mL,含 hSyn 启动子靶向神经元),注射后用含 B27 的培养基恢复培养 30min。
3.检测与验证:
免疫荧光:检测中脑标志物(FOXA2、OTX2,中脑前体)、神经元标志物(DCX,新生神经元)、多巴胺能神经元标志物(TH);
共聚焦成像:488nm 激发光观察 GFP⁺感染细胞,量化共表达比例(如 GFP⁺与 OTX2⁺/TH⁺细胞重叠率)。
关键结果:
类器官保真度:D30 中脑类器官高表达中脑前体标志物 FOXA2(78.19±3.23%)和 OTX2(84.76±1.45%),D60 多巴胺能神经元(TH⁺)占比达 71.24±2.54%,复现中脑发育轨迹;
注射效率:病毒靶向注射后,类器官结构完整,细胞死亡率 < 5%;D30 感染细胞中,41.23% GFP⁺细胞共表达 OTX2(中脑前体),39.52% 共表达 TH(多巴胺能神经元),实现精准靶向;
设备可靠性:玻璃毛细管针尖通过率 > 90%,无堵塞时注射成功率达 85%,且病毒载量较传统浸泡法降低 60%,细胞毒性显著降低。
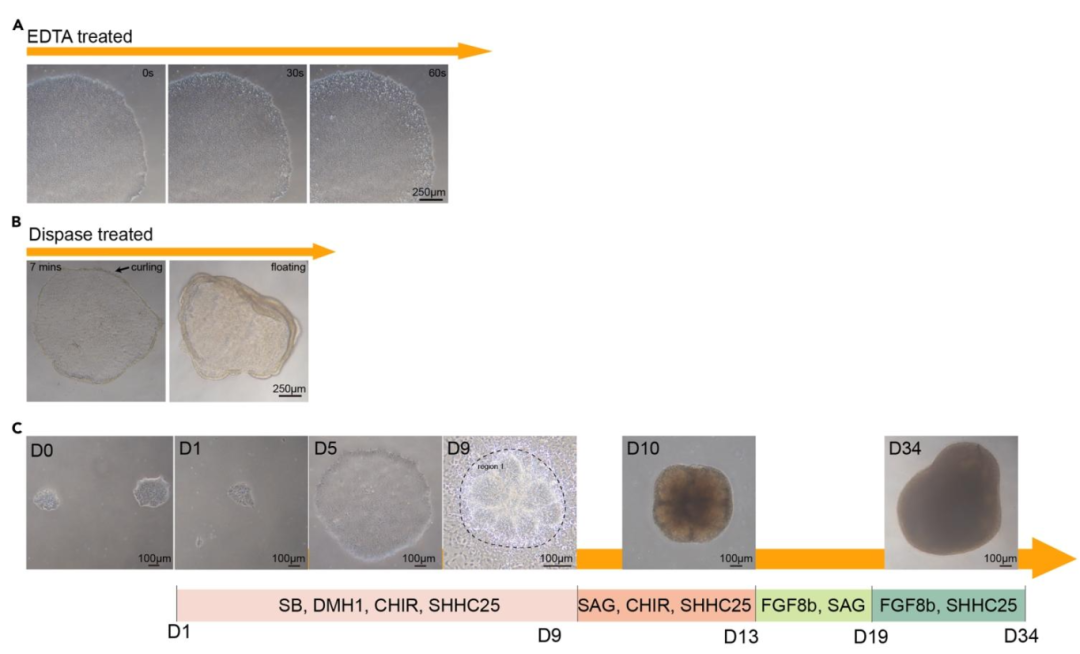
图 1:hPSC 分化为中脑类器官的时间线与关键阶段形态
该图展示分化全流程及核心阶段验证。(A)hPSC 消化:EDTA 处理 1min 后,细胞克隆松散但未脱离,边缘清晰(40×);(B)D9 神经干细胞:dispase 处理 7min 后,细胞团边缘卷曲,形成玫瑰结样结构(rosette),为神经前体特征(100×);(C)分化时间线:D0(hPSC 贴壁)→D1(启动分化)→D5(神经前体聚集)→D9(转移至培养瓶)→D10(悬浮生长)→D34(成熟类器官,呈球形,边缘光滑),标注各阶段关键诱导因子(如 SB431542、FGF8b)。图示明确分化各阶段的 “形态 - 因子” 对应关系,为类器官质量控制提供依据。

图 2:病毒注射设备组装与操作流程
该图详解设备关键部件与注射步骤。(A)2mL 注射器组装:连接硅胶管和玻璃毛细管,推注时可见水流(验证通畅),用于设备清洗;(B)10μL 微量注射器组装:针尖锋利,连接后用于病毒注射;(C)类器官选择:左侧 “差类器官” 形态不规则、边缘破损,右侧 “好类器官” 球形规则、边缘光滑(D30,100×);(D-F)注射过程:(D)类器官单个置于皿中,保留少量培养基;(E-F)显微镜下针尖插入类器官核心,缓慢推注病毒(箭头示针尖位置)。图示设备组装的关键细节(如针尖直径、管路连接)和类器官选择标准,避免因设备故障或类器官质量导致注射失败。
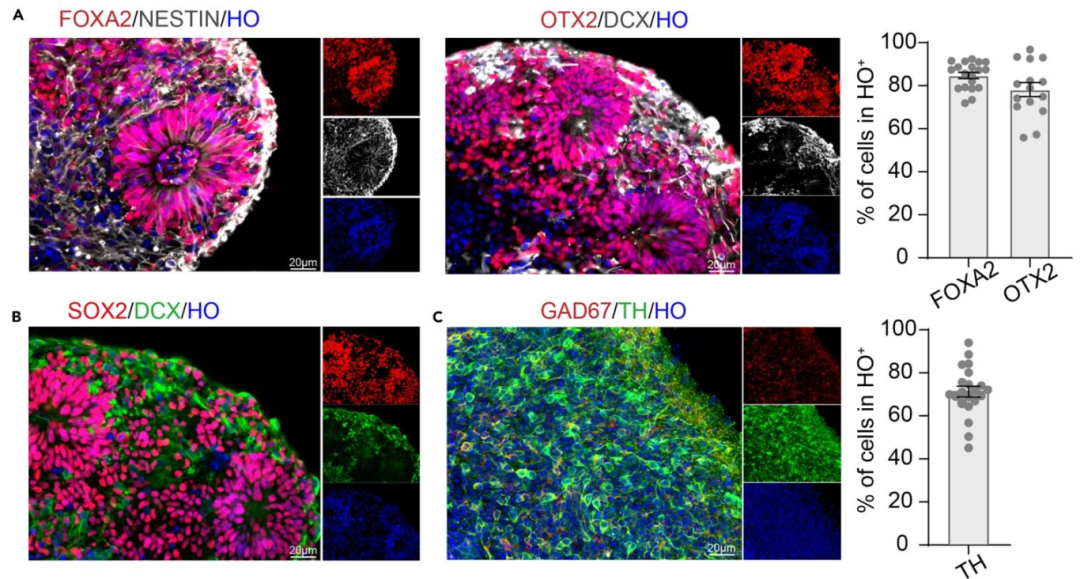
图 3:中脑类器官不同阶段的免疫荧光验证
该图证实类器官的中脑特异性。(A)D30:左图 FOXA2(中脑前体,红)与 NESTIN(神经干细胞,绿)共定位,右图 OTX2(中脑区域化标志物,红)与 DCX(新生神经元,绿)共定位,量化显示 FOXA2⁺/OTX2⁺细胞占比超 75%;(B)D30:SOX2(干细胞,红)与 DCX(绿)共表达,证实神经发生持续进行;(C)D60:TH(多巴胺能神经元,红)与 GAD67(GABA 能神经元,绿),量化 TH⁺细胞占比 71.24±2.54%。图示类器官从 “前体” 到 “功能神经元” 的分化有效性,为后续病毒靶向提供合格模型。
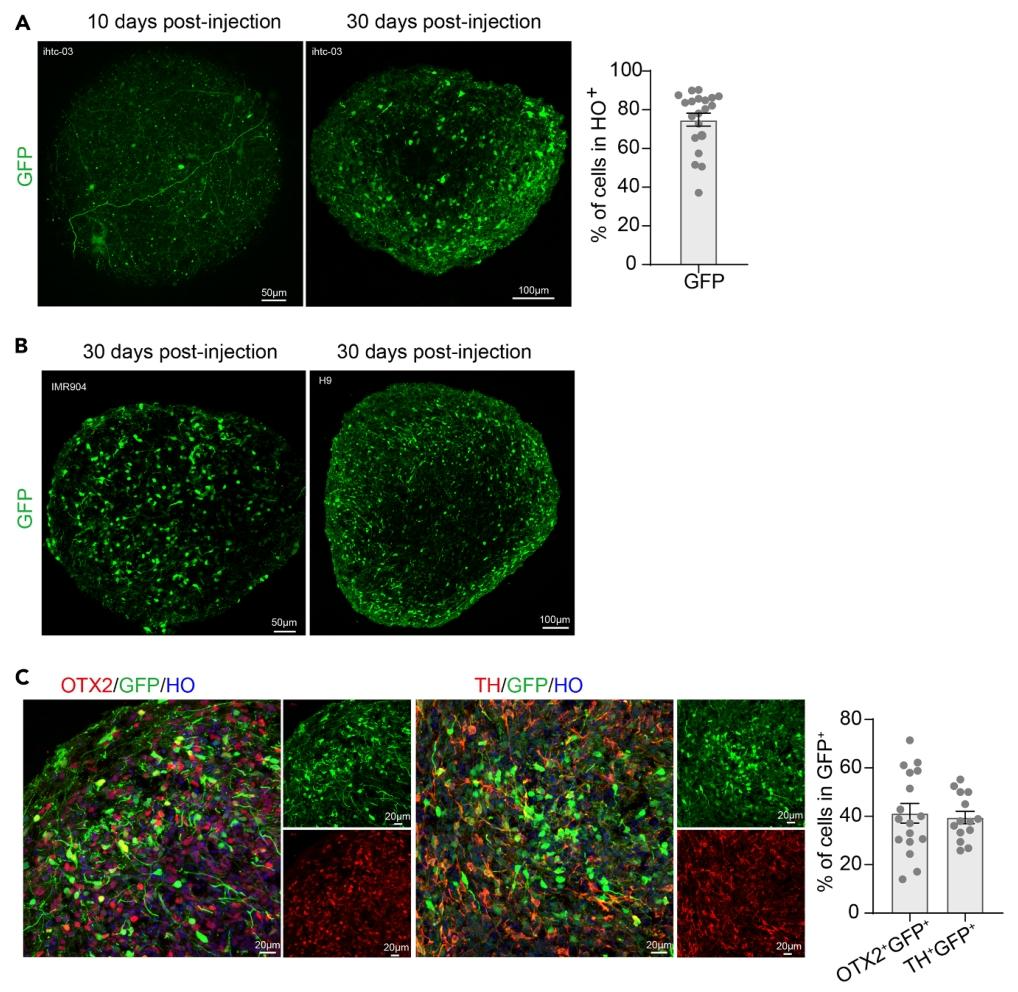
图 4:病毒感染细胞的可视化与量化
该图验证注射效率与靶向性。(A)感染时间动态:注射后 10 天 GFP⁺细胞散在分布,30 天 GFP⁺细胞密集,量化显示 GFP⁺细胞占比随时间升高;(B)不同细胞系验证:H9、IMR904 来源类器官均能有效感染,GFP⁺细胞形态正常;(C)靶向性验证:左图 GFP⁺(绿)与 OTX2⁺(红)共定位,右图 GFP⁺与 TH⁺(红)共定位,量化显示 41.23% GFP⁺细胞共表达 OTX2,39.52% 共表达 TH。图示病毒可精准靶向中脑前体和多巴胺能神经元,符合实验设计目标。
本研究建立了一套 “分化 - 注射 - 验证” 一体化的中脑类器官病毒靶向递送 protocol,核心创新在于:① 分阶段诱导确保中脑类器官高保真度(D60 TH⁺神经元占比超 70%);② 定制化注射设备(50μm 针尖 + 微量注射器)降低病毒载量(0.2μL / 个),减少细胞毒性,同时实现核心区域靶向;③ 明确类器官选择标准和操作细节(如两人协作、培养基保留量),提升可重复性。
局限性包括:① 操作需两人协作,通量低(一次仅处理少量类器官);② 类器官脱离培养基时间短(需 30min 内完成注射),易引发细胞应激;③ 未验证对其他病毒血清型(如 LV)的适用性。未来可通过自动化注射设备提升通量,优化培养基配方延长类器官体外存活时间,拓展病毒类型适配范围。
该 protocol 为中脑疾病(如帕金森病)的基因编辑建模、多巴胺能神经元功能研究提供标准化工具,尤其适合需要精准靶向中脑特定区域的实验设计。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:TNFα 通过 ACSL1/JNK/ERK/NF-κB 信号通路诱导单核细胞中基质金属蛋白酶 - 9 的表达
下一篇:人诱导多能干细胞衍生胰腺类器官的构建及其在胰腺发育与疾病研究中的应用