常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-01 17:14:36 细胞资源库平台 访问量:155
患者来源类器官(PDOs)是精准肿瘤学的重要预临床模型,但现有方案多依赖手术切除标本,难以覆盖无法手术的晚期或局部进展期患者。临床中,内镜超声引导细针活检(EUS-FNB)、经皮肝活检(PLB)等微创活检标本,以及腹水、胸腔积液等液体标本更易获取,却因细胞量少、成分复杂(含免疫细胞、红细胞),缺乏标准化 PDO 构建流程。本研究建立了一套适用于多模态标本(手术组织、微创活检、体液)的 PDO 生成与应用 protocol,涵盖标本运输、肿瘤细胞分离、培养、生物保藏及高通量药物筛选,解决了非手术患者 PDO 建模的技术瓶颈,推动 PDO 在多样化临床场景中的转化应用。
来自韩国国家癌症中心的团队在《STAR Protocols》(2025 年,Vol. 6)发表了题为Protocol for generation and utilization of patient-derived organoids from multimodal specimen的研究。
研究方法:
标本类型与处理流程:
手术组织:切除后去除正常组织(如脂肪、肌肉),剪碎(0.5×0.5 cm),用 Miltenyi 肿瘤解离试剂盒 + gentleMACS Octo 解离仪(37℃,30-40 min,按肿瘤硬度选程序),离心洗涤后用基底膜提取物(BME)包埋,24 孔板每孔 40μL dome 接种;
微创活检(EUS-FNB/PLB/ 穿刺活检):标本用转移培养基洗涤,无菌剪刀切碎,加少量解离酶(Enzyme H/R/A)37℃旋转孵育 15 min,红细胞裂解(按需)后 BME 包埋;
液体活检(腹水 / 胸腔积液):400×g 离心 10 min,Ficoll 密度梯度离心分离单核细胞层(含肿瘤细胞),洗涤后 BME 包埋。
培养体系优化:
基础培养基:Advanced DMEM/F12+ B-27、GlutaMAX 等;
癌症特异性补充剂:口腔癌加毛喉素,胰腺癌 / 胆管癌加胃泌素,结直肠癌加 SB202190+N2,确保不同癌症 PDO 的增殖能力。
保藏与质量控制:
冻存:对数期 PDO 用含 5% DMSO、10% 热灭活 FBS 的冻存液,-80℃过夜后转液氮;
复苏:37℃水浴 1 min,洗涤后 BME 包埋,加 50μM Y-27632(前 3 天);
质控:解冻后 7 天用 LIVE/DEAD 染色测活力(≥60% 为合格),STR 分析验证遗传一致性,支原体 PCR 检测污染。
高通量药物筛选:
384 孔板接种(1000 细胞 / 孔,含 10% BME),培养 3 天后加 2× 药物浓度(5 个剂量 + 对照,4 复孔),孵育 5 天后用 CellTiter-Glo 3D 测活力,计算 IC50 和 AUC。
关键结果:
多标本适配性:成功从 6 种癌症(口腔癌、胰腺癌、结直肠癌等)的多模态标本生成 PDO,手术组织 PDO 建立成功率约 70%,活检标本约 50%,液体标本约 40%;
形态与遗传一致性:PDO 保留原发肿瘤形态(如胆管癌呈葡萄状,结直肠癌呈囊性),STR 分型与原组织匹配率 > 95%;
药物筛选有效性:384 孔板筛选的 Z'- 因子 > 0.5,IC50 与患者临床响应趋势一致(如 KRAS 突变胰腺癌对 MEK 抑制剂敏感);
长期保藏:液氮保存 24-36 个月的 PDO 解冻后活力仍达 60%-80%,可正常传代。
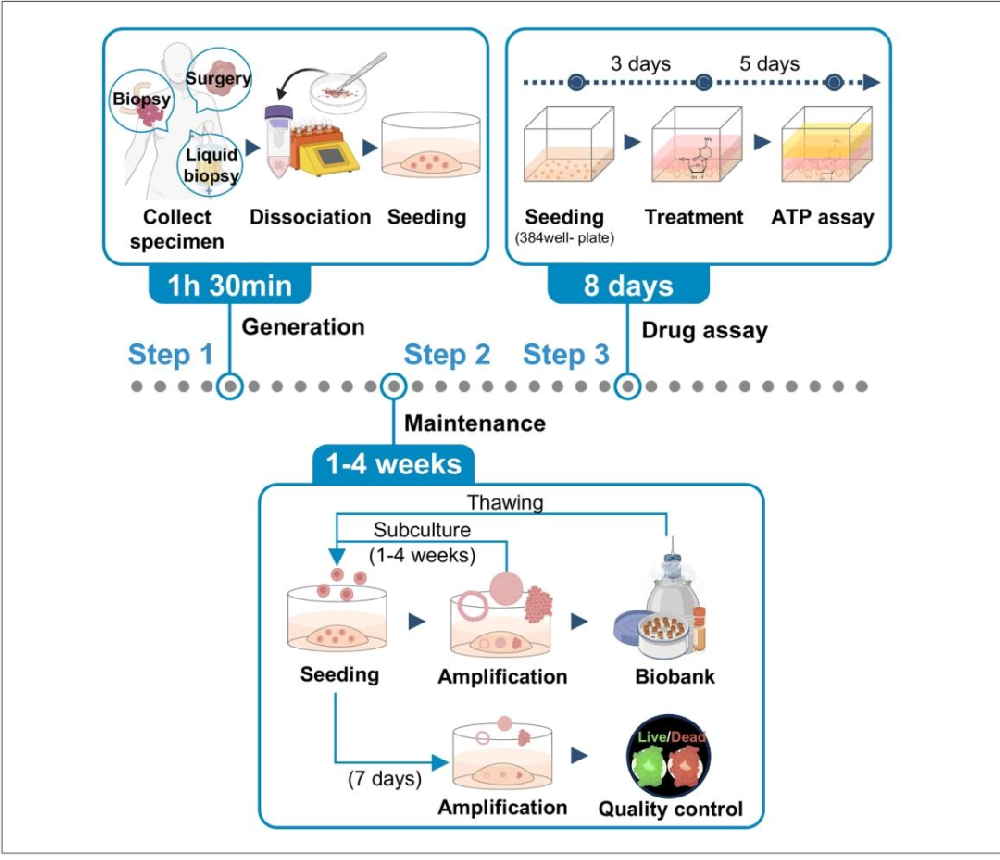
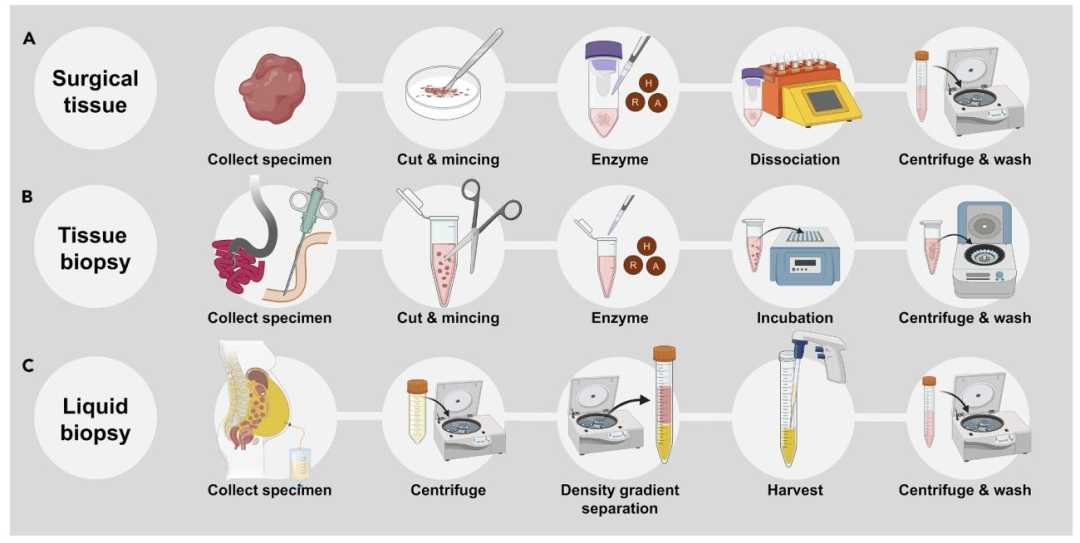
图 1:多模态标本处理流程示意图
该图展示不同标本的 PDO 构建核心步骤。(A)手术组织:剪碎→酶解 + 机械解离→离心洗涤;(B)活检标本:剪碎→酶孵育→离心洗涤;(C)液体活检:离心→Ficoll 密度梯度分离→离心洗涤。图示清晰区分三类标本的关键差异(如液体标本需密度梯度分离),为标准化操作提供可视化指南。
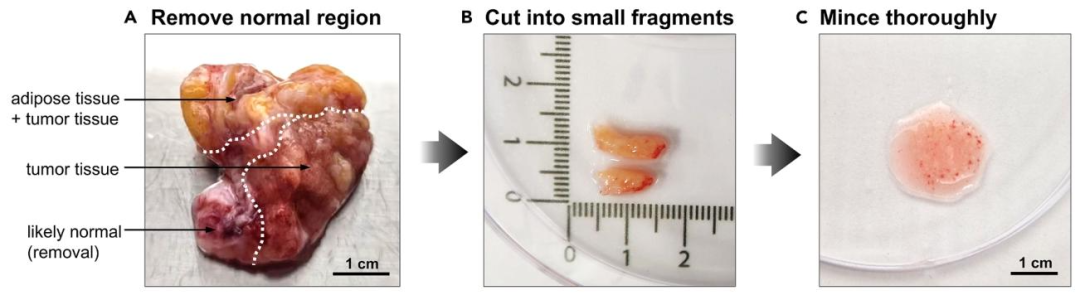
图 2:手术组织标本处理步骤
该图细化手术组织的预处理。(A)去除正常组织(如脂肪),保留肿瘤区域;(B)肿瘤切成 0.5×0.5 cm 小块;(C)剪至糊状以提高酶解效率。图示强调 “去正常化” 和 “充分剪碎” 对肿瘤细胞得率的重要性,避免非肿瘤细胞干扰 PDO 形成。
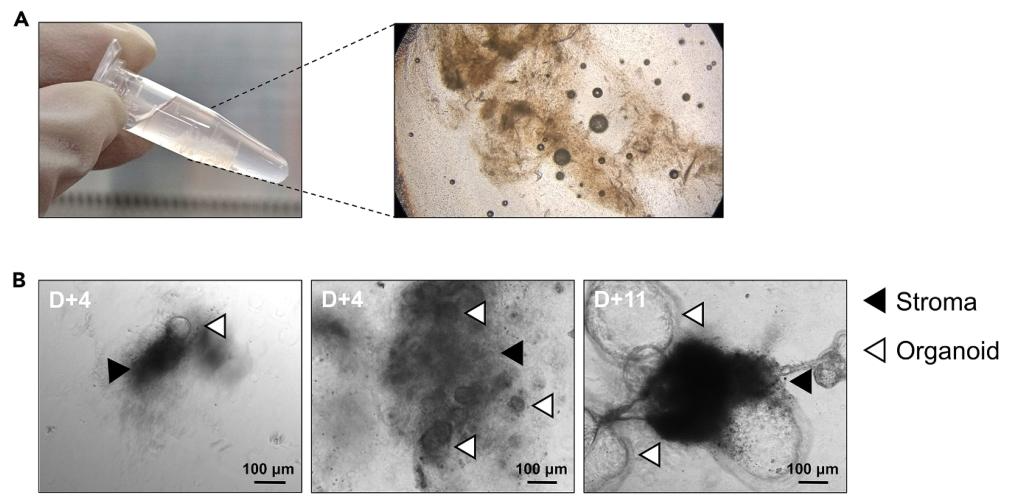
图 3:PDO 在基质中的生长景观
该图显示 PDO 与基质成分的关系。(A)酶解后残留的纤维成分与肿瘤细胞;(B)肿瘤细胞在基质中形成 PDO(白色箭头),基质组织(黑色箭头)作为支撑。图示说明省略过滤步骤可减少肿瘤细胞损失(尤其标本量少时),且基质不影响 PDO 生长。
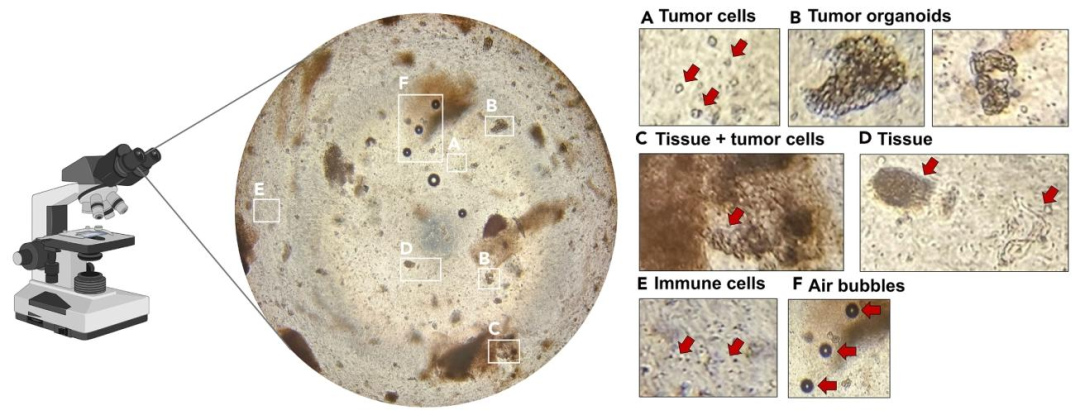
图 4:BME 内细胞分布观察
展示 BME 中可能出现的成分:(A)单肿瘤细胞(PDO 形成基础);(B)类器官雏形(细胞早期聚集);(C)组织碎片间肿瘤细胞(无需过滤避免损失);(D)退化分化组织;(E)干扰性免疫细胞;(F)需移除的大气泡。助力快速识别有效肿瘤成分与干扰因素。
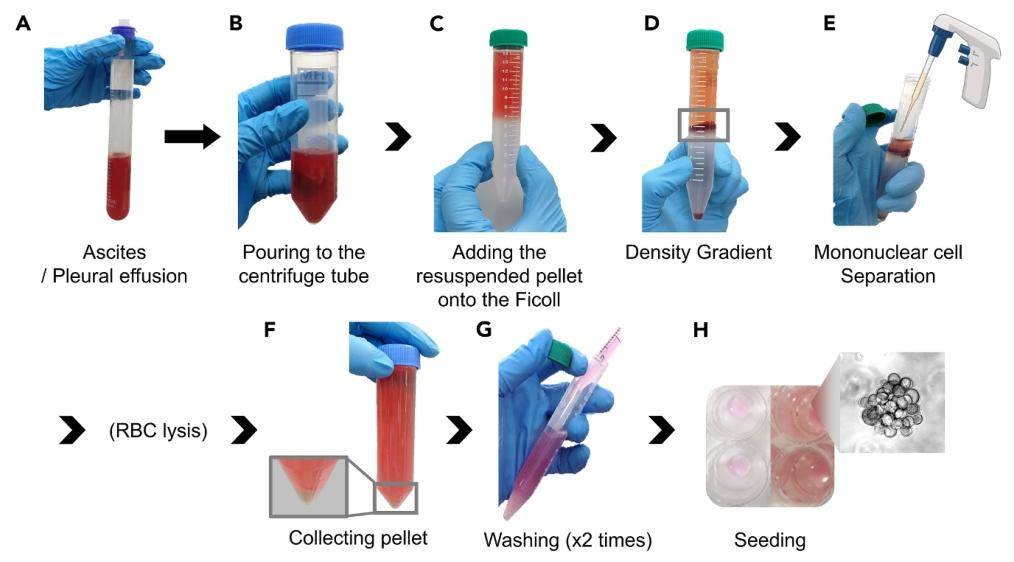
图 5:液体活检标本的肿瘤细胞分离流程
该图详解体液中肿瘤细胞的获取。(A-B)腹水 / 胸腔积液离心获细胞 pellet;(C)将细胞悬液铺于 Ficoll 层(避免混合);(D-E)离心后吸取单核细胞层(含肿瘤细胞);(F-H)洗涤后 BME 包埋。图示关键在于 “梯度离心的层间不混合” 和 “单核细胞层的精准吸取”,确保肿瘤细胞纯度。
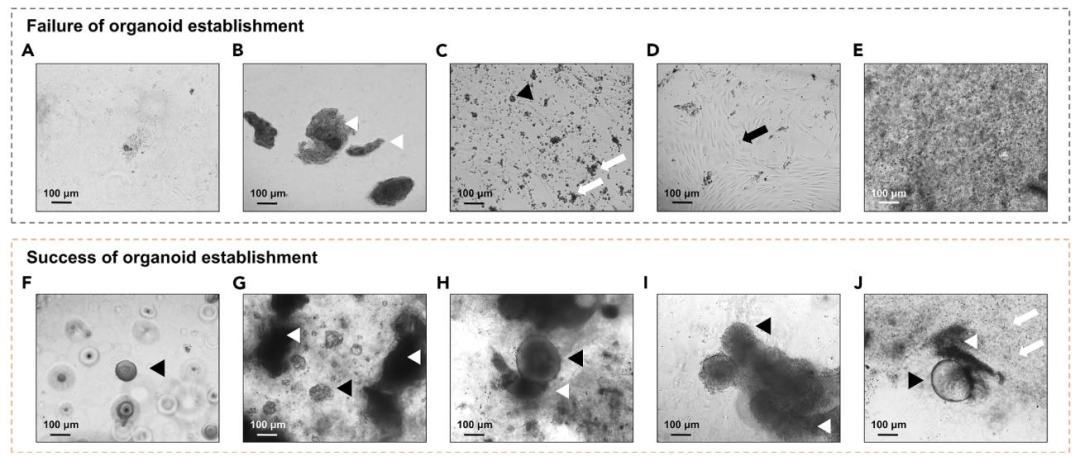
图 6:PDO 建立成功与失败的形态对比
该图提供结果判断标准。(A-E)失败案例:无肿瘤细胞生长(A)、分化组织碎片(B)、免疫细胞过多(C)、成纤维细胞过度生长(D)、细胞接种过密(E);(F-J)成功案例:PDO 增殖(F-G)、基质中 PDO(H)、组织碎片转化为 PDO(I)、免疫细胞与 PDO 共存(J)。图示帮助研究者快速识别培养状态,及时调整操作(如成纤维细胞过度时需分离传代)。
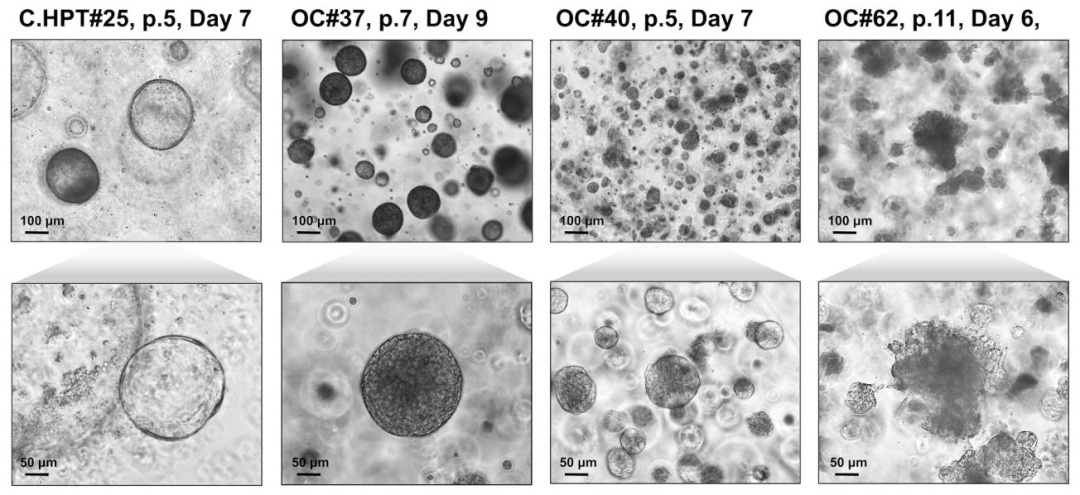
图 7:可传代 PDO 的典型形态
该图展示适用于传代的 PDO 特征。不同癌症 PDO(如口腔癌 HPT#25、胆管癌 OC#62)直径达 150-300 μm,密度约 50% 视野覆盖,形态致密或囊性。图示提供传代时机判断依据(如葡萄状 PDO 直径≥150 μm、囊性 PDO≥300 μm 时传代)。
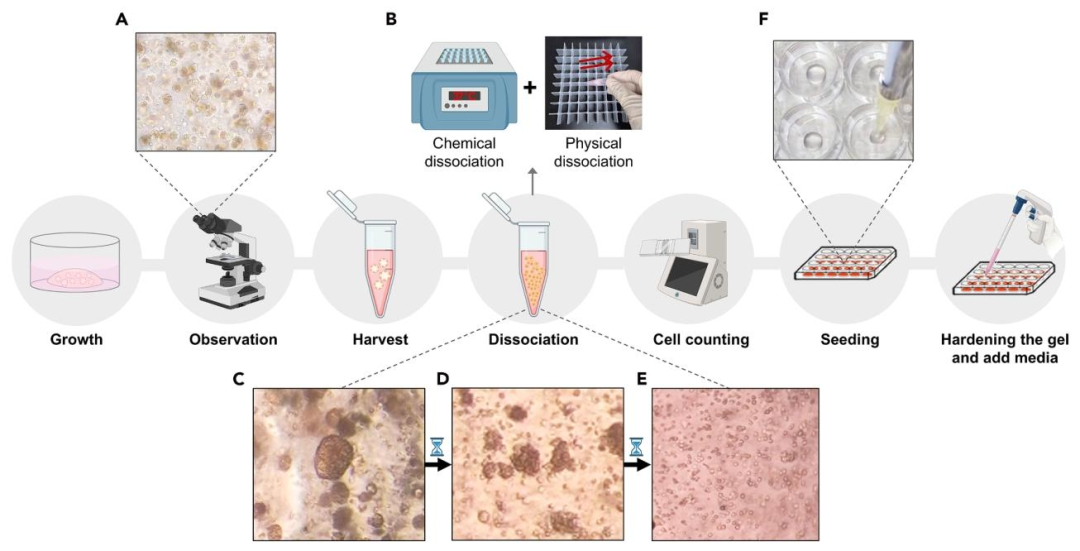
图 8:类器官传代实操步骤
展示传代全流程:(A)显微镜观察筛选待传代类器官;(B)收获类器官后,通过物理刮擦(管壁摩擦)+ 化学酶解(TrypLE)实现解离;(C-E)逐步解离为单细胞;(F)计数后按密度(3×10³-5×10³ 细胞 / 40μL BME)接种,凝胶凝固后加培养基。明确解离关键(刮擦提升效率、避免酶解损伤)与接种标准,保障传代后类器官稳定生长。
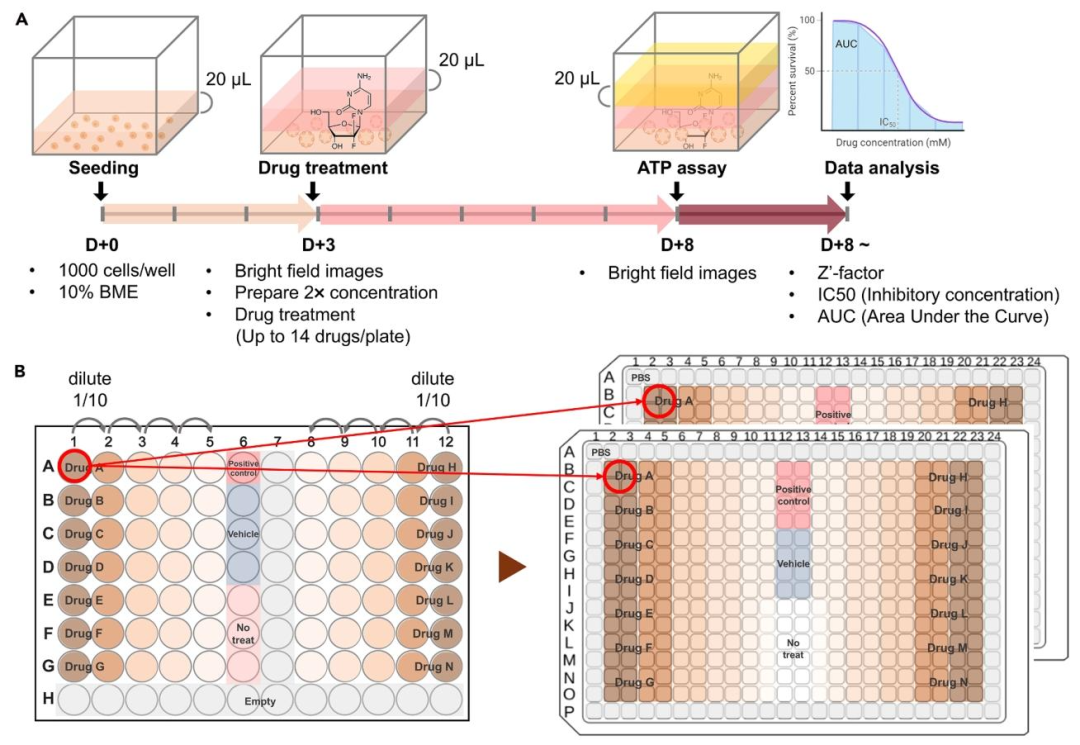
图 9:高通量药物筛选实验设计
该图呈现药物筛选的操作流程与布局。(A)时间线:接种→培养 3 天→加药→培养 5 天→活力检测;(B)384 孔板布局:14 种药物,每种 5 个剂量 + 对照,4 复孔,边缘孔加 PBS 防蒸发。图示确保筛选的高通量与重复性,Z'- 因子 > 0.5 验证实验可靠性。
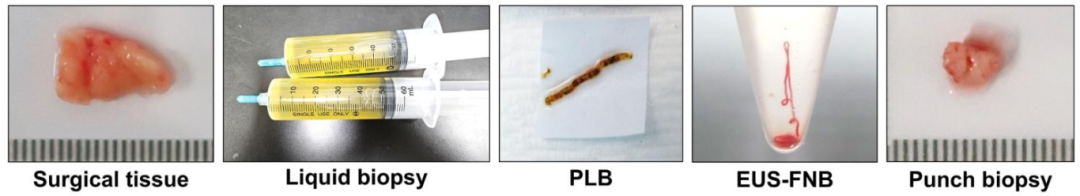
图 10:多模态标本的实物与 PDO 对应
该图展示不同标本类型的来源。包括手术组织、液体活检(腹水 / 胸腔积液)、PLB、EUS-FNB、穿刺活检,图示直观体现本 protocol 的标本覆盖范围,尤其突出微创和体液标本的临床可及性。
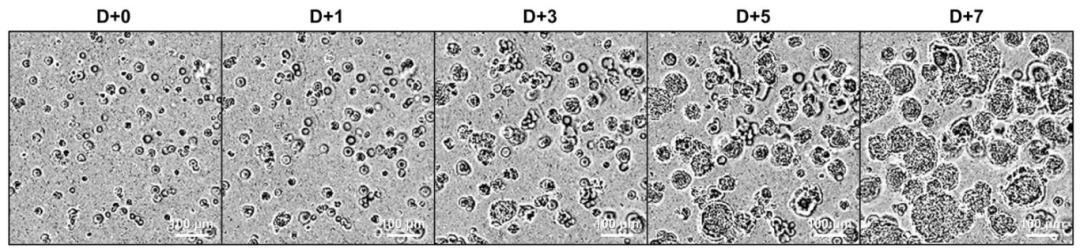
图 11:PDO 传代后生长时序
记录传代后动态:(1 天)单细胞 / 小细胞团;(3 天)早期类器官(直径~50μm);(5 天)形态清晰(如结直肠癌呈囊性);(7 天)达传代标准(直径 150-200μm,密度 50% 视野覆盖)。明确生长规律与传代时机。
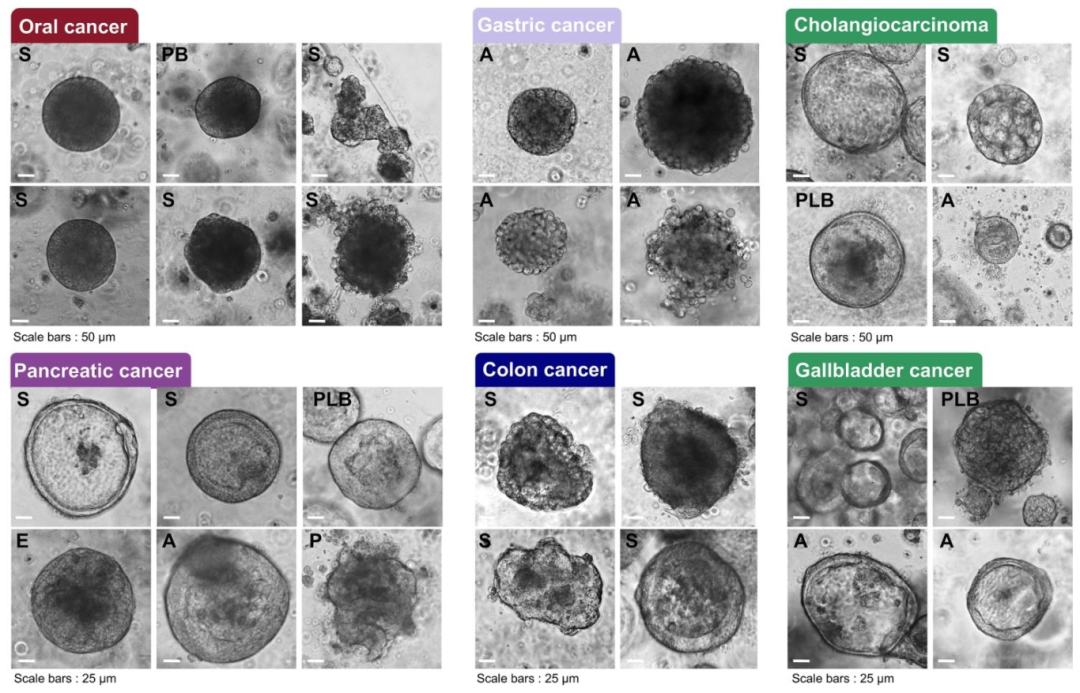
图 12:不同癌症 PDO 的形态差异
该图呈现癌症特异性形态。口腔癌 PDO 呈致密状,胃癌呈囊性,胆管癌呈葡萄状,胰腺癌呈不规则状,且标注标本来源(如 PLB、腹水)。图示说明 PDO 形态与癌症类型的关联性,可作为初步鉴定依据。
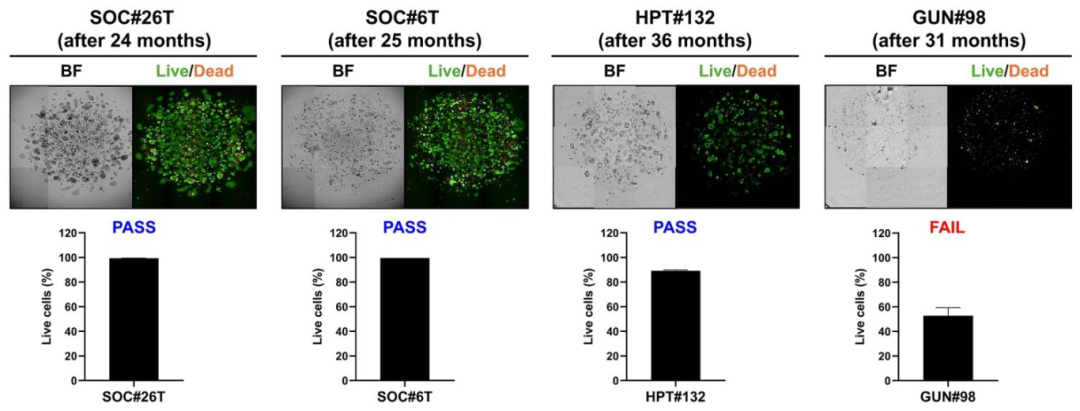
图 13:冻存 PDO 的复苏质量控制
该图验证长期保藏效果。冻存 24-36 个月的 PDO 解冻后,LIVE/DEAD 染色显示活细胞(绿色)占比 60%-80%,活力量化结果与形态一致(如 SOC#26T 活力 80%,GUN#98 活力 < 60% 判定为失败)。图示确立冻存 PDO 的质控标准,保障生物库的可靠性。
本研究建立了首套覆盖多模态标本(手术、微创活检、体液)的 PDO 标准化 protocol,核心创新在于:1)针对不同标本特性优化处理流程(如活检的温和酶解、液体标本的密度梯度分离),突破非手术患者的建模限制;2)提供癌症特异性培养配方,确保 PDO 的增殖与形态保真;3)整合冻存 - 复苏 - 质控体系,支持 PDO 生物库建设;4)开发 384 孔高通量药物筛选方法,适配临床精准用药需求。
局限性包括:1)标本中肿瘤细胞占比 < 10% 时成功率显著下降;2)口腔癌、胰腺癌标本易受微生物污染;3)未覆盖血液系统肿瘤。未来可结合磁珠分选富集肿瘤细胞、添加抗生素减少污染,拓展至更多癌症类型。
该 protocol 为 PDO 在临床转化中的普及提供了实用工具,尤其适合无法手术的晚期患者,可实现 “标本获取 - 建模 - 药物筛选” 的全流程标准化,推动精准肿瘤学从 “手术标本依赖” 向 “多场景适配” 升级。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:RPA1 通过抑制 DNA 损伤诱导的 PANoptosis 保护肢体发育研究
下一篇:TNFα 通过 ACSL1/JNK/ERK/NF-κB 信号通路诱导单核细胞中基质金属蛋白酶 - 9 的表达