常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-02-28 09:00:00 细胞资源库平台 访问量:169
顺铂作为广泛使用的化疗药物,其疗效受个体基因背景影响显著,但在生理相关的 3D 模型中系统解析基因 - 药物相互作用的研究仍较匮乏。传统 2D 细胞系模型难以复现组织架构和微环境,导致许多生理相关的基因功能被忽略;而 3D 类器官虽能保留组织复杂性,却缺乏高效的基因组编辑工具进行高通量筛选。
本研究通过在人胃类器官中建立大规模 CRISPR 筛选平台(包括敲除、干扰(CRISPRi)、激活(CRISPRa)及单细胞技术),首次实现了对顺铂药物反应相关基因的系统挖掘,填补了 3D 模型中基因功能与药物敏感性研究的空白,为解析胃癌化疗耐药机制和开发个性化疗法提供了新工具。
来自美国 MD 安德森癌症中心的团队在《Nature Communications》(2025 年,Vol. 16)发表了题为Large-scale CRISPR screening in primary human 3D gastric organoids enables comprehensive dissection of gene-drug interactions的研究。
研究方法:
类器官模型构建:从人胃组织建立 TP53/APC 双敲除(DKO)的癌前胃类器官,作为均一遗传背景的筛选模型;
CRISPR 筛选平台:建立 CRISPR-KO、诱导性 CRISPRi(干扰)和 CRISPRa(激活)系统,针对 1952 个 DNA/RNA 结合蛋白基因设计 sgRNA 文库,在类器官中进行顺铂敏感性筛选;
单细胞分析:结合 Perturb-seq 技术,将 sgRNA 扰动与单细胞转录组关联,解析基因扰动对顺铂反应的单细胞水平影响;
机制验证:通过基因敲除 / 过表达、功能实验(如 EdU 增殖检测、ATAC-seq)验证关键基因(如 GMDS、TAF6L)的作用。
关键结果:
筛选平台有效性:成功在 3D 胃类器官中实现高效 CRISPR 筛选,sgRNA 覆盖率 > 1000×,重复实验一致性高,验证了 68 个影响细胞生长的基因;
顺铂敏感性基因:发现 41 个基因敲除可增强顺铂敏感性,包括已知 DNA 修复基因(如 ERCC6、BRCA1)和新基因(如 ELOF1、ZNF677);
单细胞机制解析:顺铂处理后,NER 通路基因(如 ERCC4)敲除细胞的转录组呈现通路特异性聚类,而未处理时异质性显著,证实药物处理可驱动功能相关基因的转录组趋同;
岩藻糖基化关联:NER 基因(如 ERCC4)敲除与顺铂联合处理可协同抑制 GMDS(岩藻糖合成关键酶),减少细胞岩藻糖基化,而 GMDS 过表达增强顺铂敏感性,提示岩藻糖基化下调是细胞的保护性机制;
TAF6L 的作用:TAF6L 敲除显著增强顺铂敏感性,其通过维持染色质可及性促进顺铂处理后的细胞增殖恢复,ATAC-seq 显示其敲除导致启动子区域开放峰减少,尤其自身启动子的自调控显著。
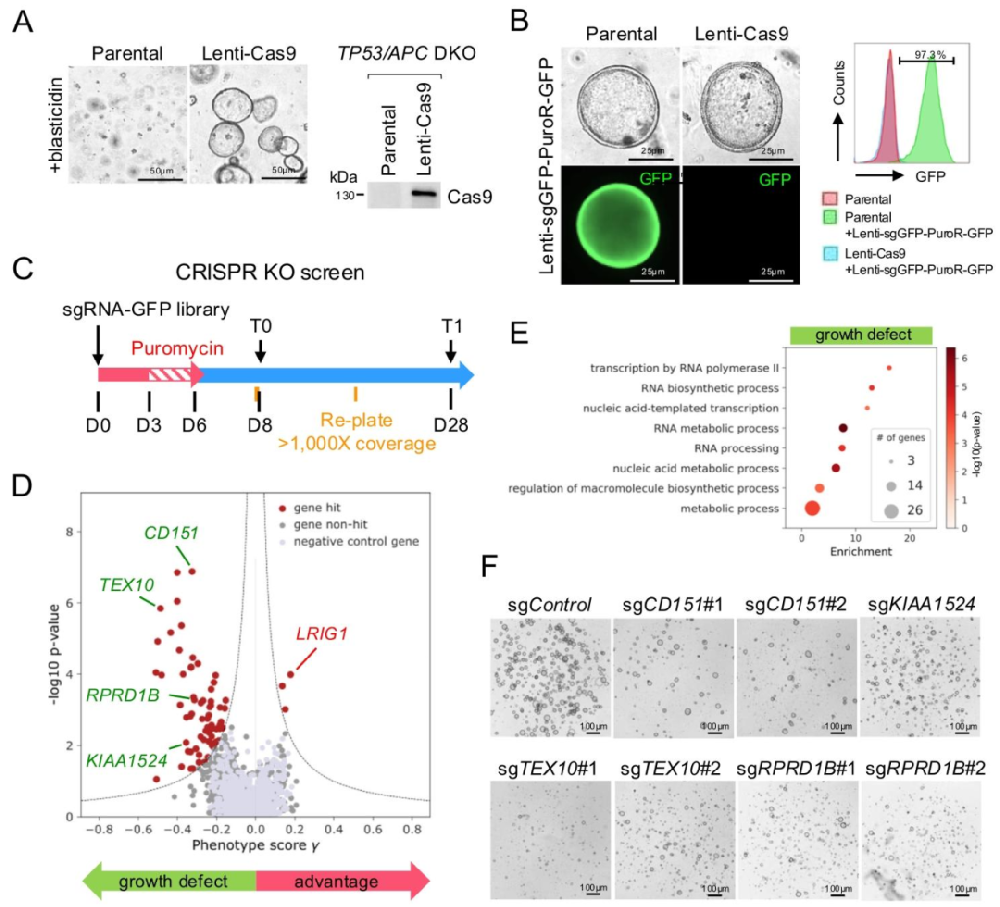
图 1:CRISPR-KO 筛选在胃类器官中的建立
该图验证敲除筛选的可行性。(A)构建稳定表达 Cas9 的 TP53/APC DKO 类器官,Western blot 证实 Cas9 表达;(B)GFP 靶向 sgRNA 实验显示 > 95% 细胞 GFP 阴性,证明 Cas9 活性高效;(C)筛选时间线:sgRNA 文库转导后 2 天(T0)和 28 天(T1)测序,覆盖度 > 1000×;(D)火山图显示 68 个生长缺陷基因(如 CD151)和少数生长优势基因(如 LRIG1);(E)GO 分析显示生长缺陷基因富集转录、RNA 加工等通路;(F)单个 sgRNA 验证显示 4 个基因敲除均重现生长缺陷表型。图示证实 3D 类器官中大规模 CRISPR-KO 筛选的可靠性。
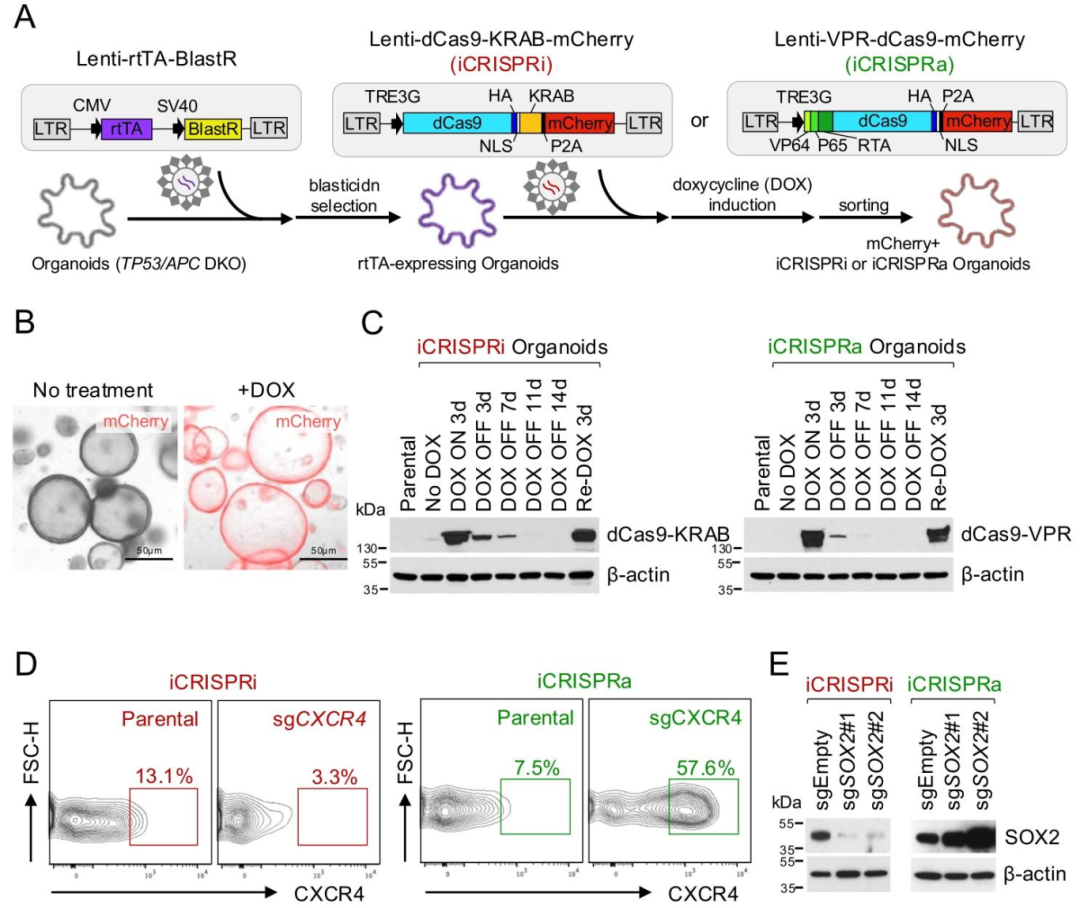
图 2:诱导性 CRISPRi 和 CRISPRa 系统的建立
该图展示基因表达调控工具的有效性。(A)系统构建流程:通过慢病毒依次导入 rtTA 和 dCas9-KRAB(iCRISPRi)或 dCas9-VPR(iCRISPRa),多西环素诱导表达;(B)诱导后类器官形态正常,mCherry + 细胞比例高;(C)Western blot 证实 dCas9 融合蛋白的诱导表达及撤药后的降解;(D)iCRISPRi-sgCXCR4 使 CXCR4 + 细胞比例从 13.1% 降至 3.3%,iCRISPRa-sgCXCR4 则升至 57.6%;(E)SOX2 的表达被 iCRISPRi 抑制、被 iCRISPRa 激活。图示验证诱导系统可精准调控内源性基因表达。
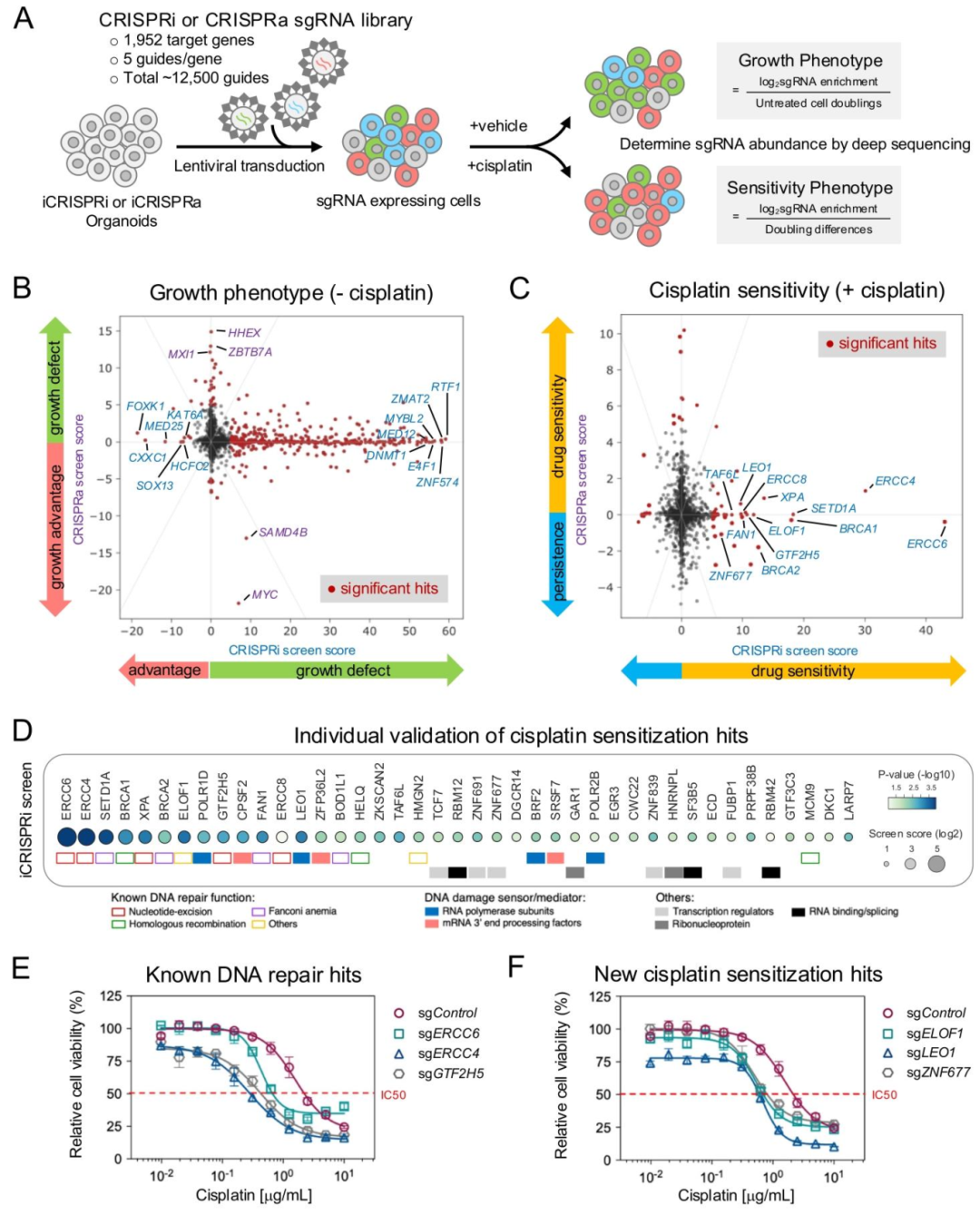
图 3:顺铂敏感性的 CRISPRi/a 筛选结果
该图呈现药物敏感性基因的筛选发现。(A)筛选策略:对比顺铂处理与未处理组的 sgRNA 丰度,计算药物敏感性评分;(B)无顺铂时,iCRISPRa 筛选发现 MYC 等生长优势基因,iCRISPRi 发现 384 个生长缺陷基因;(C)顺铂处理后,iCRISPRi 筛选得到 41 个敏感基因(如 ERCC6、LEO1),iCRISPRa 得到 9 个敏感基因;(D)热图显示敏感基因涵盖 NER、HRR 等 DNA 修复通路;(E-F)单个基因验证:ERCC4、ELOF1 等敲除显著降低顺铂 IC50,证实筛选可靠性。
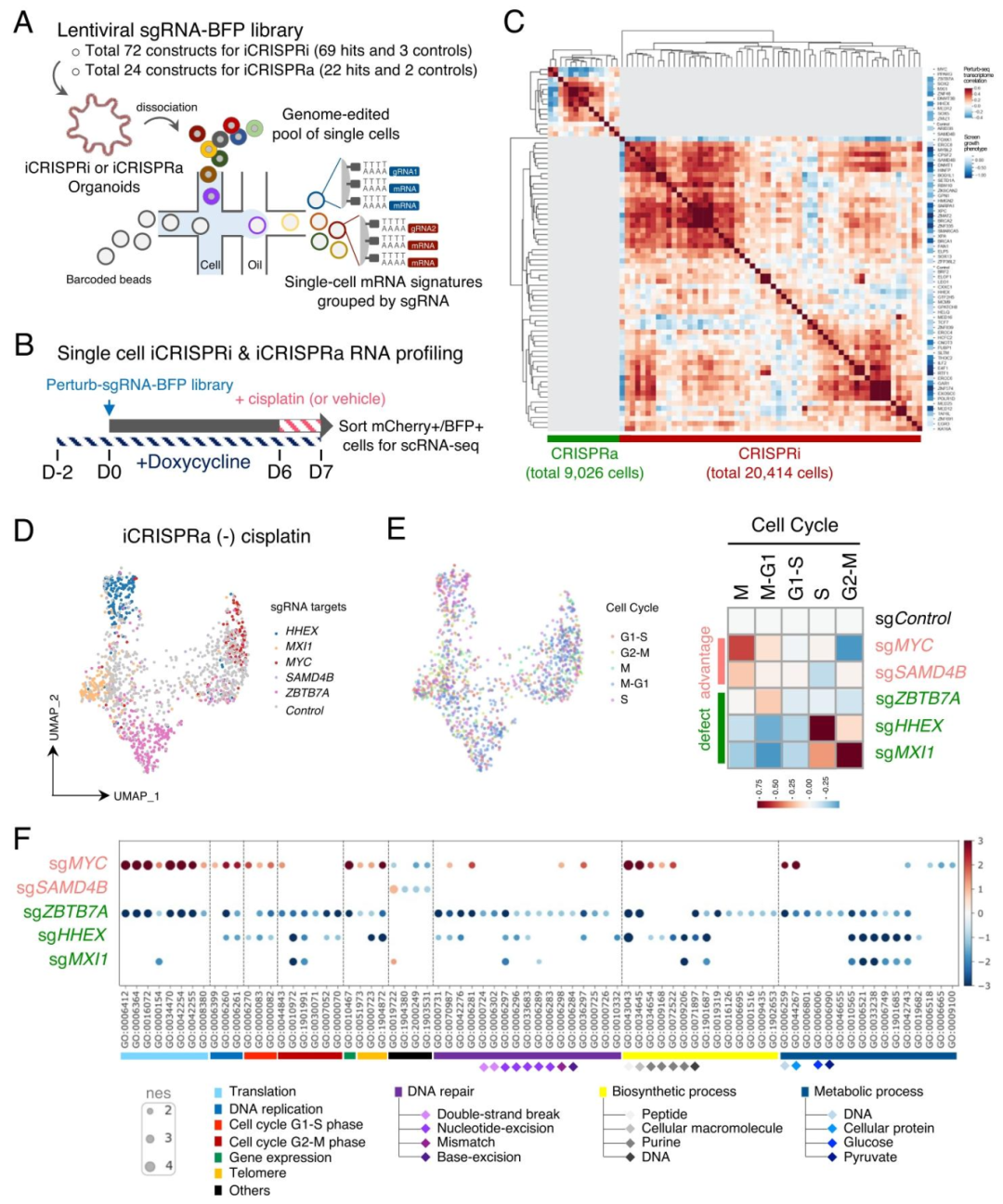
图 4:单细胞 Perturb-seq 解析基因 - 药物互作
该图揭示单细胞水平的转录组变化。(A)Perturb-seq 流程:sgRNA 文库转导类器官,顺铂处理后分选 mCherry+/BFP + 细胞进行 scRNA-seq;(B)时间线:多西环素诱导后转导 sgRNA,6 天后药物处理并测序;(C)热图显示 sgRNA 扰动的转录组聚类,功能相关基因聚为一类;(D)UMAP 显示 MYC、SAMD4B 等基因扰动的细胞集群分离;(E)细胞周期分析:MYC 激活使 M 期细胞增加,HHEX 激活导致 S 期阻滞;(F)GSEA 显示 MYC 激活富集 DNA 复制、细胞周期通路,HHEX 激活则抑制这些通路。图示证实单细胞技术可关联基因型与表型。
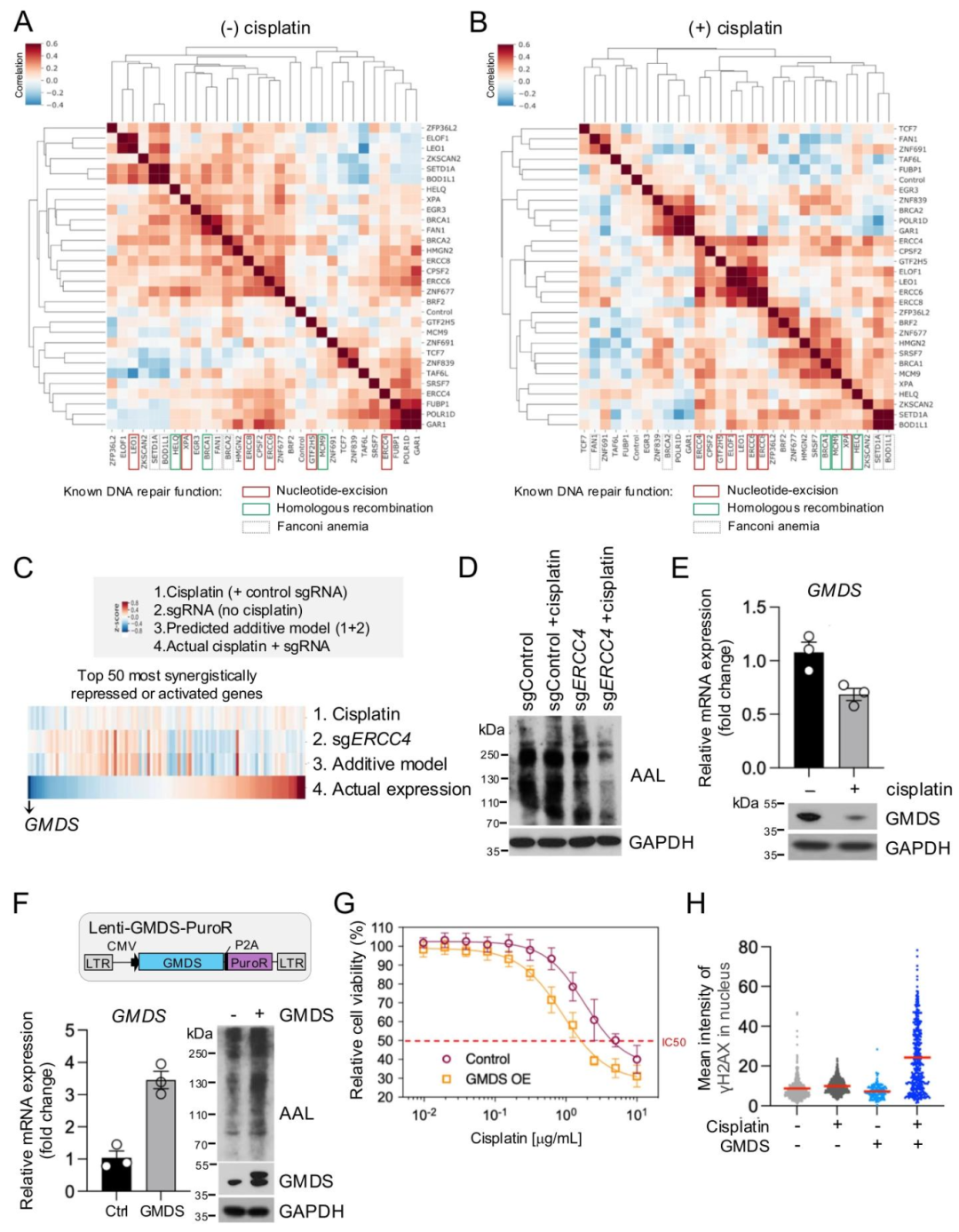
图 5:岩藻糖基化与顺铂敏感性的关联
该图解析 GMDS 的作用机制。(A-B)无顺铂时 NER/HRR 基因敲除细胞转录组异质,顺铂处理后 NER 基因敲除细胞转录组趋同;(C)协同效应分析:ERCC4 敲除 + 顺铂处理显著下调 GMDS,实际表达低于 additive 模型预测;(D)Western blot 显示该组合减少岩藻糖基化(AAL 染色);(E)顺铂处理单独下调 GMDS 蛋白;(F)GMDS 过表达恢复岩藻糖基化;(G)GMDS 过表达显著降低顺铂 IC50;(H)γH2AX 染色显示 GMDS 过表达增加 DNA 损伤。图示证实 GMDS 下调通过减少岩藻糖基化保护细胞。
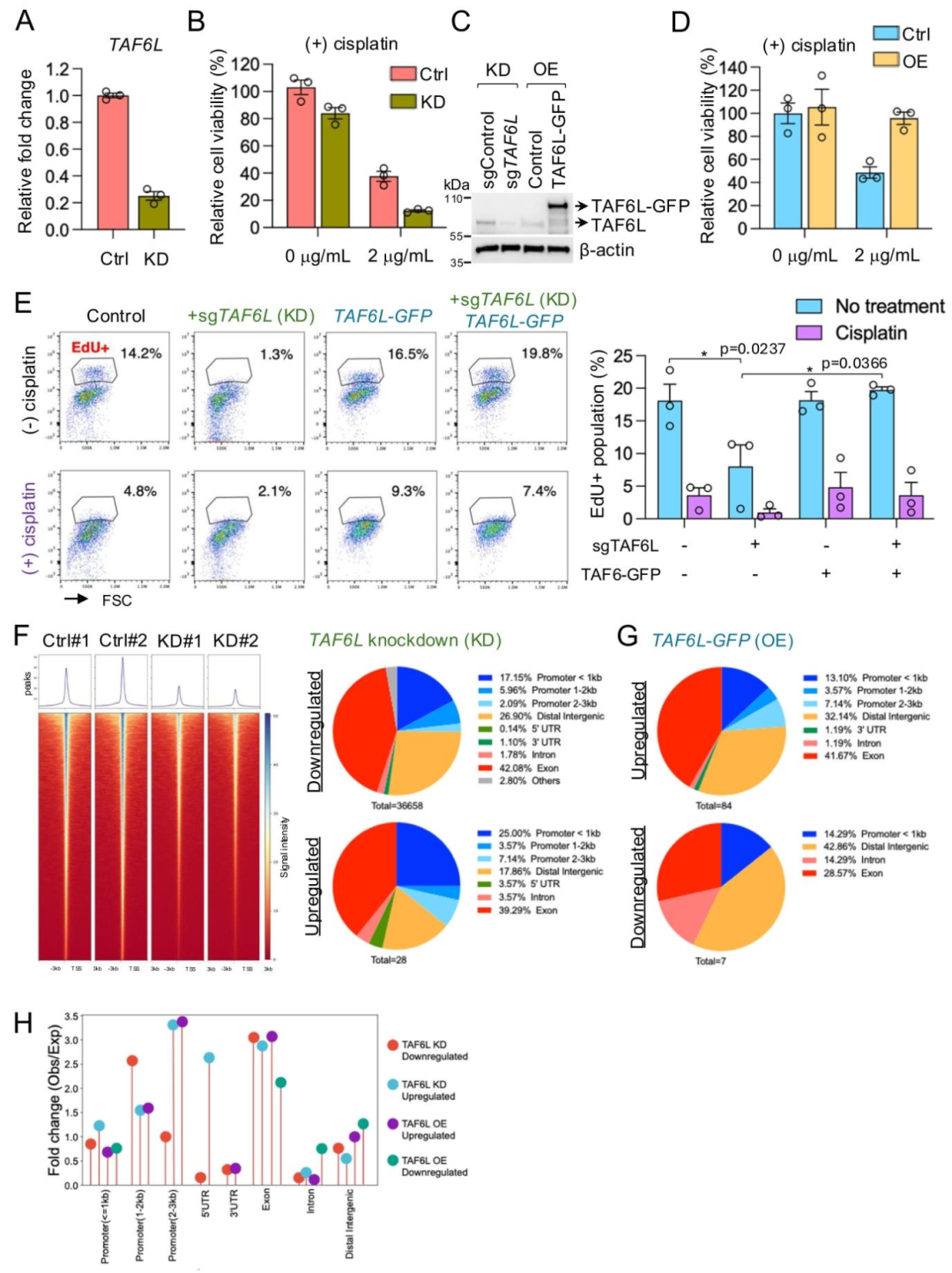
图 6:TAF6L 调控顺铂处理后的细胞恢复
该图验证 TAF6L 的功能。(A)qPCR 显示 TAF6L 敲除效率达 85%;(B)敲除显著降低顺铂处理后的细胞活力;(C)Western blot 证实 TAF6L 敲除和过表达;(D)过表达提高顺铂处理后的活力;(E)EdU 实验:TAF6L 敲除使顺铂处理后 EdU + 细胞从 3.6% 降至 1%,过表达则恢复至 4.8%;(F-G)ATAC-seq:敲除导致 36658 个开放峰减少(主要在启动子),过表达无显著变化;(H)开放峰在启动子区域富集,敲除后显著减少。图示证实 TAF6L 通过维持染色质可及性促进细胞恢复。
本研究在人胃类器官中建立了大规模 CRISPR 筛选平台,系统解析了顺铂药物反应的基因调控网络。核心发现包括:成功在 3D 类器官中实现 CRISPR-KO、CRISPRi 和 CRISPRa 的高通量筛选,鉴定出 41 个顺铂敏感基因(涵盖 NER、HRR 等通路);通过单细胞 Perturb-seq 发现药物处理可驱动功能相关基因的转录组趋同;首次揭示岩藻糖基化与顺铂敏感性的关联,GMDS 下调通过减少岩藻糖基化保护细胞;发现 TAF6L 通过维持染色质可及性调控顺铂处理后的细胞增殖恢复。
创新点在于:首次在 3D 胃类器官中实现多模态 CRISPR 筛选,结合单细胞技术解析基因 - 药物互作;发现岩藻糖基化这一全新顺铂耐药机制;证实 TAF6L 作为新的化疗反应调控因子。局限性包括模型为癌前状态(与晚期肿瘤有差异)、CRISPRa 重复性较低、缺乏体内验证。未来可扩展至患者来源类器官,结合体内模型验证靶点,探索岩藻糖基化抑制剂与顺铂的联合应用。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:引导编辑精准纠正 iPSC 中的 G6PD Viangchan 突变研究