常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-02-26 17:18:05 细胞资源库平台 访问量:122
英文标题:Supramolecular lipid nanoparticle reprograms tumor microenvironment by cucurbit[7]uril-based host–guest recognition for STING-activating cancer immunotherapy
中文标题:通过基于葫芦[7]脲的主客体识别重构肿瘤微环境以增强STING激活的癌症免疫疗法的超分子脂质纳米粒子
发表期刊:《Materials Today》
影响因子:22
作者单位:
清华大学化学系生物有机磷化学与化学生物学教育部重点实验室;浙江理工大学浙江省纤维材料与制备技术重点实验室;山西医科大学环境病原微生物与感染防控教育部重点实验室
作者信息:
Yunxuan Feng, Yuan Yu, Xinyang Yu, Mengyao Li, Jiaqi Lei, Yongcan Li, Zhida Liu, Shaolong Qi, Guocan Yu
1.靶向cGAS-STING通路为癌症免疫治疗提供了新机遇,但其在治疗实体瘤(尤其是"冷肿瘤")中的临床疗效仍不理想。
2."冷肿瘤"的特征是T细胞浸润稀少、免疫原性低以及免疫抑制性的肿瘤微环境,这严重阻碍了细胞毒性T淋巴细胞(CTLs)的激活、增殖和浸润。
3.小分子STING激动剂在体内代谢快、清除迅速;同时,肿瘤内高浓度的内源性多胺会显著抑制cGAS活性,进一步削弱基于STING的免疫治疗效果。
4.研究创新点:本研究开发了一种名为MC7-LNP的超分子脂质纳米粒子系统。它基于葫芦[7]脲的主客体识别和金属配位作用,同时负载STING激动剂MSA-2和铜离子,旨在重构免疫抑制性TME,提高肿瘤免疫原性,并将"冷肿瘤"转变为"热肿瘤"。
1.化学合成:
合成脂质修饰的葫芦[7]脲衍生物CB[7]-lipid(通过Huisgen环加成反应)。
合成树枝状可电离脂质G0-C14。
2.纳米粒子制备(MC7-LNP):
使用微流控混合装置,将含有G0-C14、胆固醇、DSPC、ALC-0159、CB[7]-lipid和MSA-2的乙醇相,与含有mRNA和铜离子的水相(柠檬酸盐缓冲液)混合制备。
对所得混合物进行透析纯化。
3.表征分析:
使用核磁共振(¹H NMR, 2D NOESY)、质谱(MALDI-TOF, LCMS-IT/TOF)、等温滴定量热法(ITC)分析主客体相互作用及结合常数。
使用动态光散射(DLS)测定粒径和PDI,zeta电位仪测表面电位,透射电镜(TEM)观察形貌。
使用高效液相色谱(HPLC)测定载药量。
使用荧光共振能量转移(FRET)评估胶体稳定性。
4.体外实验:
使用共聚焦激光扫描显微镜(CLSM)和流式细胞术(FCM)研究细胞摄取、内体逃逸、ROS产生、细胞凋亡等。
使用蛋白质印迹(Western Blot)分析干扰素分泌、多胺生物合成和铜死亡相关蛋白表达。
使用酶联免疫吸附测定(ELISA)检测细胞因子(如IFN-α, IFN-β, cGAMP)水平。
5.体内动物实验:
建立C57BL/6小鼠B16黑色素瘤皮下移植瘤模型。
将荷瘤小鼠随机分组,瘤内注射不同制剂(PBS、CuSO₄、IL-12蛋白、MSA-2、LNP@CB[7]-lipid、LNP@MSA-2、MC7-LNP、MC7-LNP@mRNAIL-12)。
监测肿瘤体积、小鼠生存率。
通过FCM、免疫荧光、H&E染色分析肿瘤组织、引流淋巴结中的免疫细胞浸润(CD8⁺ T细胞、DC成熟度、M2巨噬细胞、Tregs等)及细胞因子水平。
使用电感耦合等离子体质谱(ICP-MS)评估铜在主要器官的蓄积。
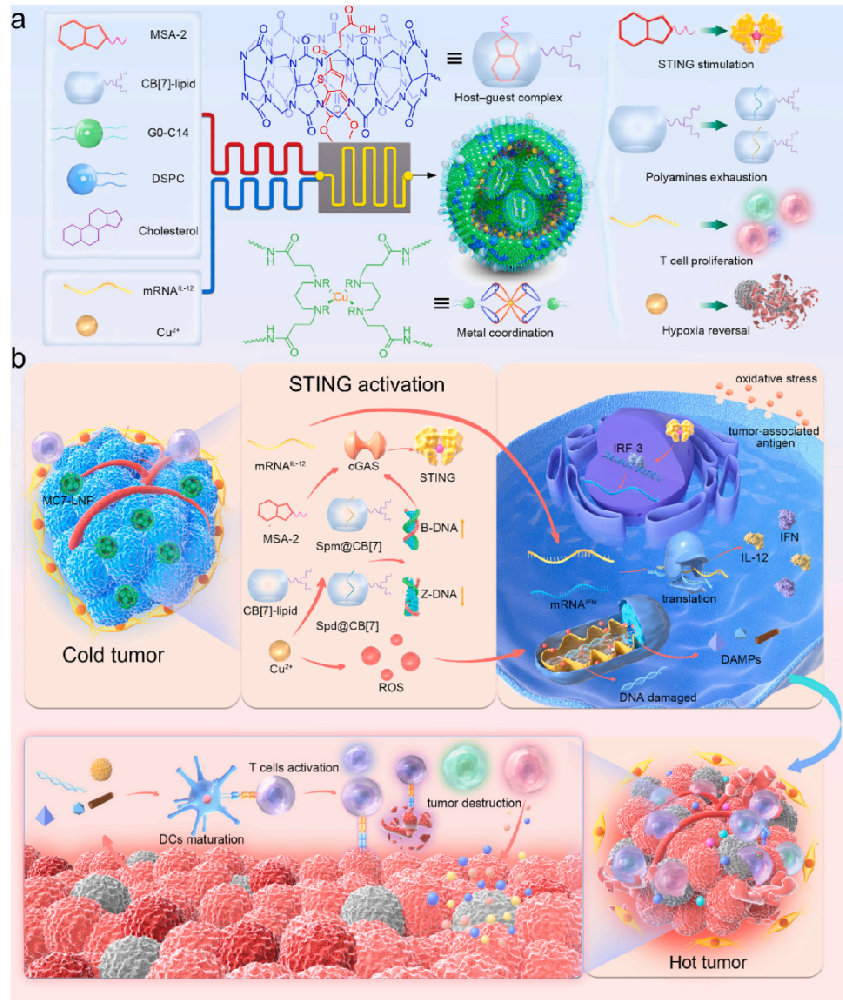
图1. MC7-LNP系统设计原理及作用机制示意图
a)MC7-LNP的化学成分和合成策略示意图。基于主客体识别和金属配位的驱动,通过微流控装置进行超分子自组装制备MC7-LNP。 b) MC7-LNP通过持续的STING刺激、多胺清除和缺氧缓解来重构免疫抑制性TME。当与mRNA结合时,这种协同策略极大地促进了CTL活化和免疫活性细胞因子的分泌,从而有效地将"冷肿瘤"转变为"热肿瘤"。
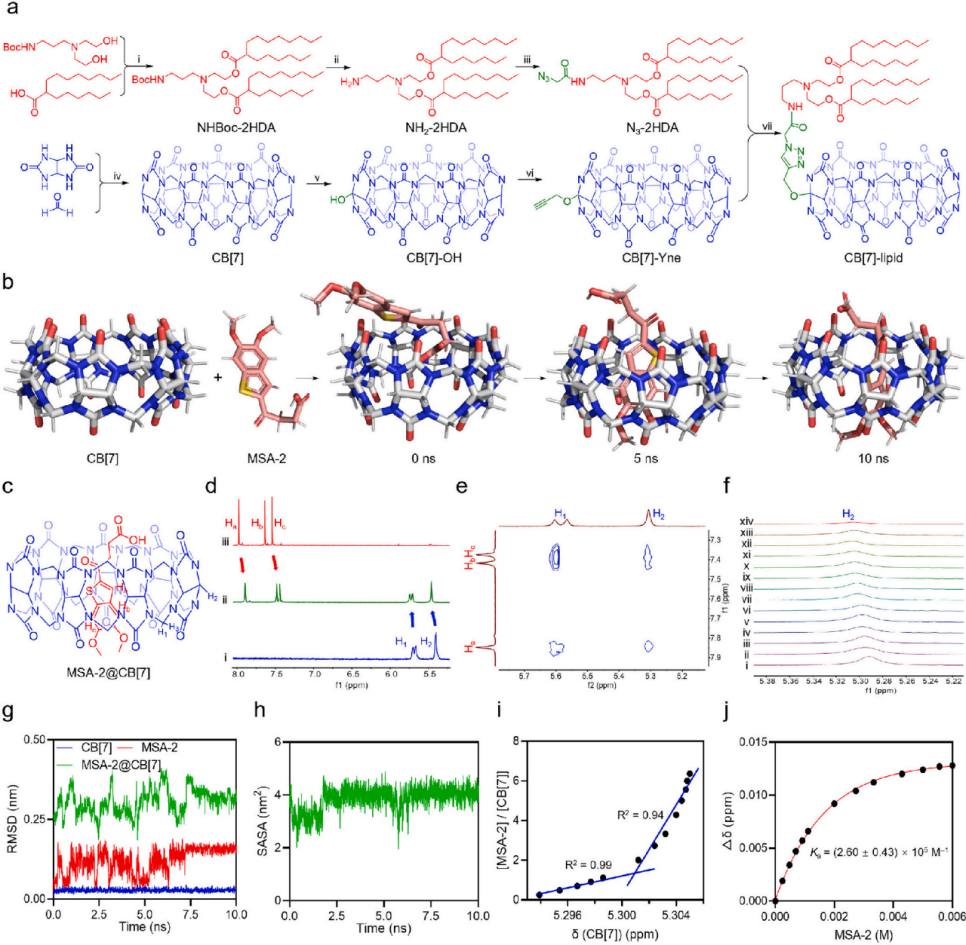
图2. 化学合成与主客体识别
a) CB[7]-lipid的合成路线。 b) MSA-2和CB[7]之间主客体结合的分子动力学模拟。 c) MSA-2和CB[7]形成的主客体复合物的化学结构。 d) CB[7]、MSA-2 + CB[7]、MSA-2的¹H NMR谱图。e) MSA-2和CB[7]的2D NOESY谱图。 f) ¹H NMR滴定谱图。 g) 模拟过程的RMSD变化。h) 分子动力学模拟期间的SASA变化。 i) 随着MSA-2与CB[7]摩尔比的增加,CB[7]上质子H₂的化学位移变化。 j) 通过¹H NMR滴定确定MSA-2和CB[7]之间Ka值的非线性拟合图。
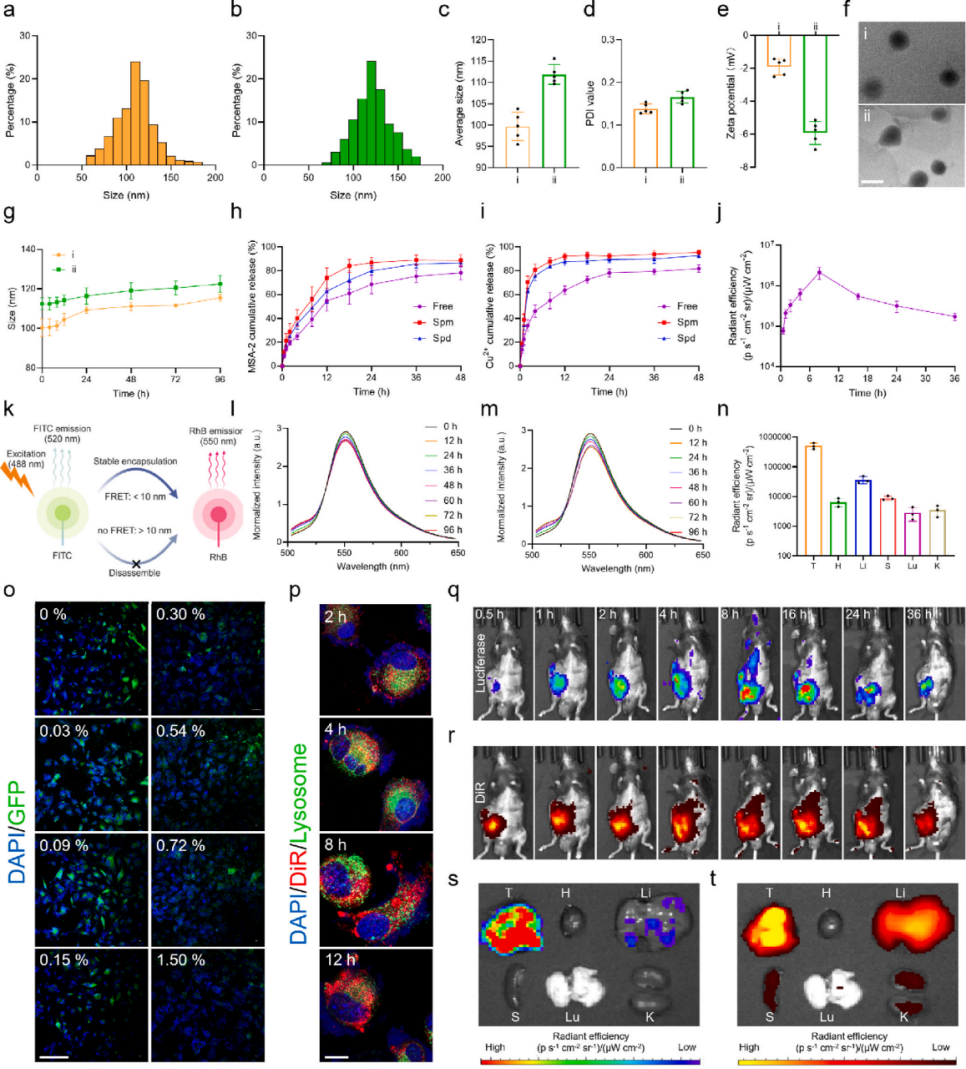
图3. MC7-LNP的制备与表征
a) DLS测定的MC7-LNP粒径分布图。b) DLS测定的MC7-LNP@mRNALuci粒径分布图。 c) MC7-LNP和MC7-LNP@mRNALuci的平均粒径。 d) MC7-LNP和MC7-LNP@mRNALuci的PDI值。 e) MC7-LNP和MC7-LNP@mRNALuci的Zeta电位。 f) MC7-LNP和MC7-LNP@mRNALuci的TEM图像。比例尺 = 100 nm。 g) MC7-LNP和MC7-LNP@mRNALuci在PBS缓冲液中4°C下储存时的粒径变化。 h) 有无多胺存在时,MSA-2在不同时间点的累积释放曲线。 i) 有无多胺存在时,铜离子在不同时间点的累积释放曲线。 j) 图3q中生物发光信号的定量分析。 k) FITC和RhB标记的LNP用于FRET检测的简图。 l) FITC和RhB标记的MC7-LNP在PBS中的归一化荧光强度。 m) FITC和RhB标记的MC7-LNP@mRNALuci在DMEM培养基中的归一化荧光强度。 n) 图3s中主要器官生物发光信号的定量分析。 o) 用含有不同浓度铜离子的MC7-LNP@mRNAGFP处理后B16细胞的CLSM图像。比例尺 = 100 μm。 p) B16细胞与DiR标记的MC7-LNP在不同时间点孵育后的CLSM图像。比例尺 = 10 μm。 q) 注射后36小时主要器官的离体生物发光图像。 r) 注射后36小时主要器官的离体荧光图像。 s) 瘤内注射DiR标记的MC7-LNP@mRNALuci后小鼠的体内生物发光图像。 t) 瘤内注射DiR标记的MC7-LNP@mRNALuci后小鼠的体内荧光图像。 缩写:T,肿瘤;H,心脏;Li,肝脏;S,脾脏;Lu,肺;K,肾脏。
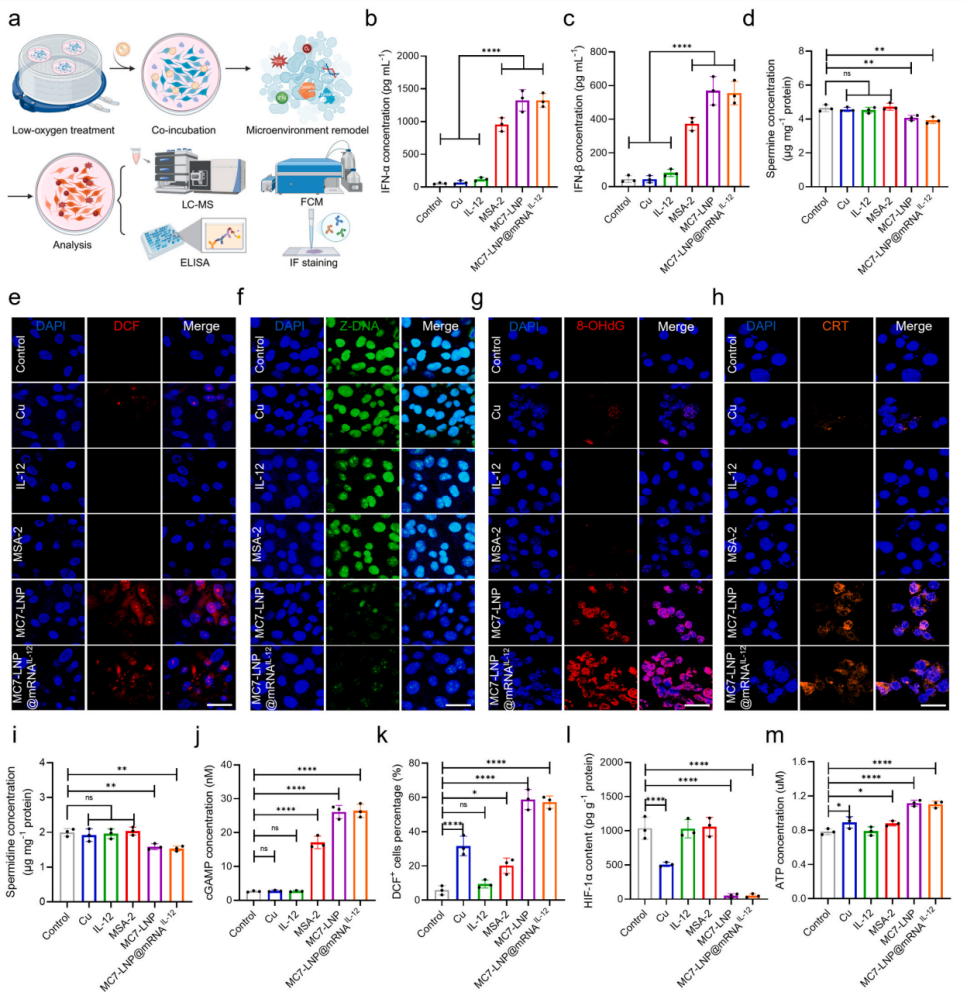
图4. MC7-LNP对免疫抑制性TME的重构
a) TME重构和实验分析的示意图。 b) 不同处理24小时后细胞内IFN-α的浓度。 c) 不同处理24小时后细胞内IFN-β的浓度。 d) 不同处理24小时后细胞内Spm含量的测定。 e) DCF荧光的CLSM图像。 f) Z-DNA荧光的CLSM图像。 g) 检测氧化性DNA损伤的8-OHdG荧光CLSM图像。 h) 研究应激反应的CRT荧光CLSM图像。 i) 不同处理24小时后细胞内Spd含量的测定。 j) B16细胞与不同制剂孵育24小时后的细胞内cGAMP浓度。 k) 不同处理后,通过FCM分析的DCF⁺ B16细胞百分比。 l) 不同处理后细胞内HIF-1α的浓度。 m) 不同处理后上清液中ATP的浓度。 所有比例尺 = 20 μm。
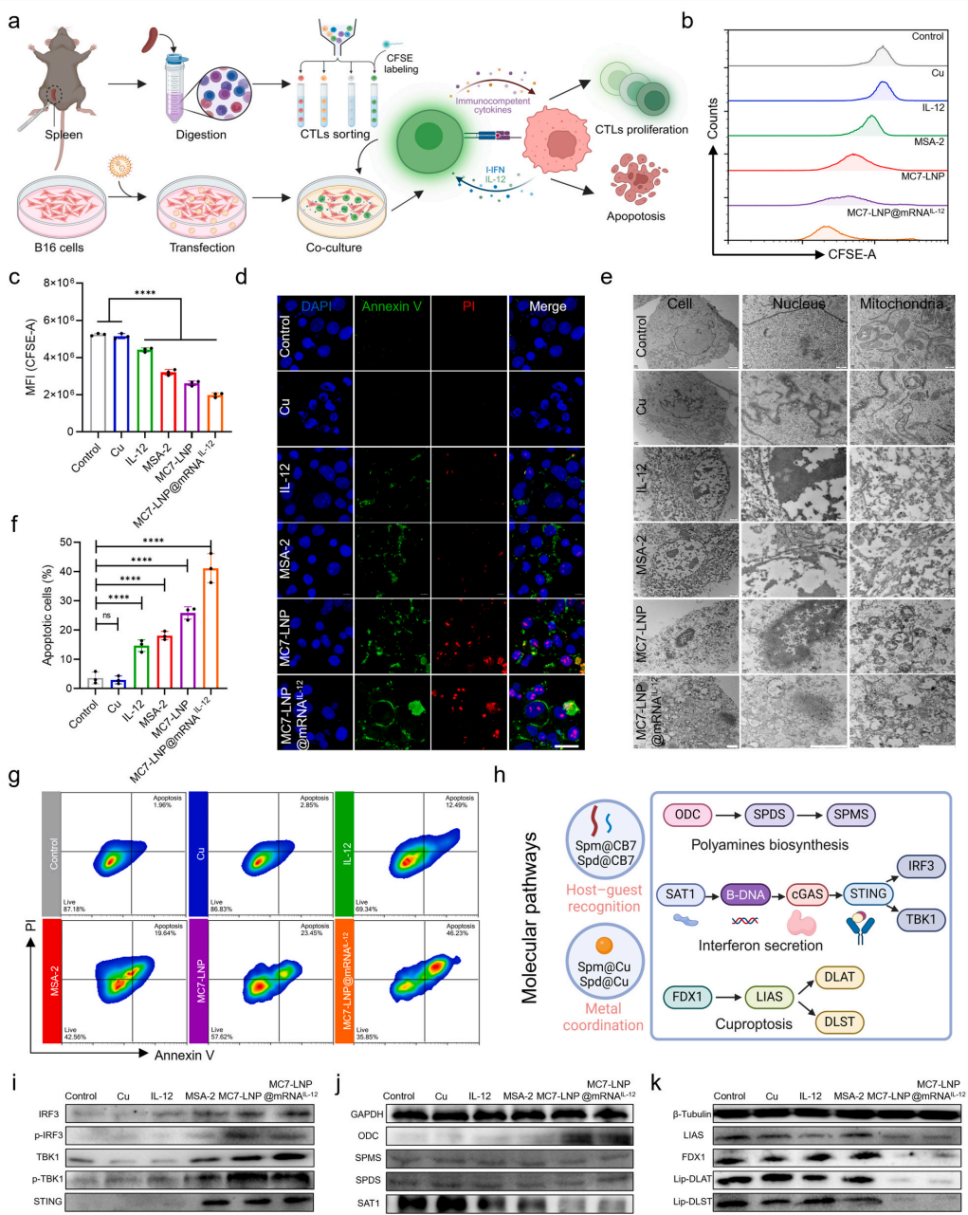
图5. TME重构后的T细胞活力恢复
a) 用于研究CTL活化的CTLs分选及体外共培养的系统方案。 b) CFSE标记的CTLs的代表性荧光直方图。 c) 图5b中CFSE-A的平均荧光强度。 d) B16细胞与CTLs共培养24小时后的CLSM图像。比例尺 = 20 μm。 e) 不同制剂处理的B16细胞的TEM图像。每组第一张图显示细胞全貌,后续图像为放大视图。比例尺 = 2 μm。 f) 图5g中凋亡B16细胞的统计计数。 g) 用于确定细胞凋亡的B16细胞FCM等高线图。 h) 涉及干扰素分泌、多胺生物合成和铜死亡的超分子调控机制。 i-k) 参与各通路的不同蛋白质的Western Blot分析:干扰素分泌(i)、多胺生物合成(j)、铜死亡(k)。
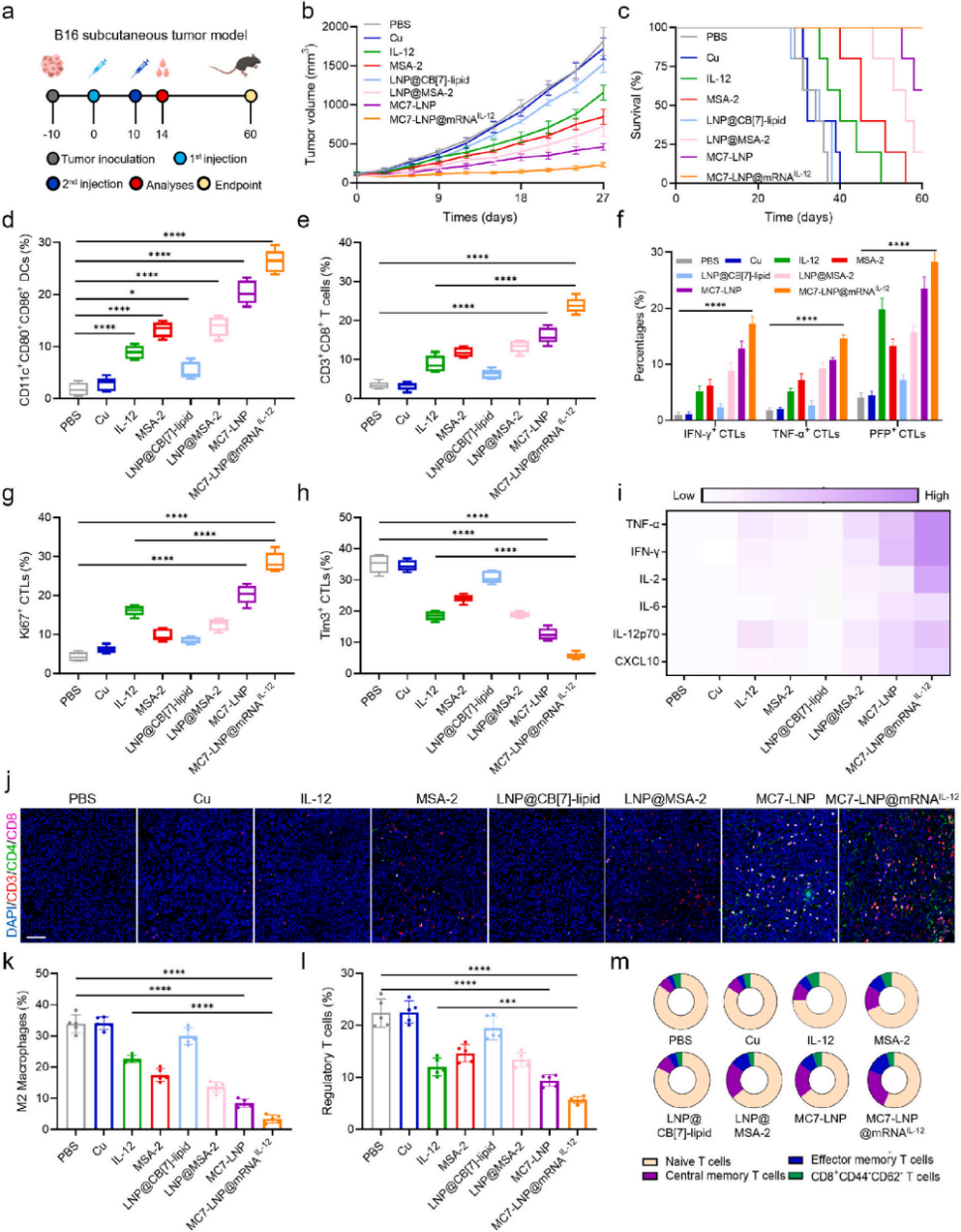
图6. 黑色素瘤模型中CTLs应答研究
a) B16皮下肿瘤模型的简要描述。 b) 不同处理后小鼠的肿瘤体积变化。 c) 不同处理后小鼠的生存率曲线。 d) TDLNs的FCM分析以评估DC成熟度。 e) 瘤内CD3⁺CD8⁺ T细胞的百分比。 f) 瘤内CTLs的FCM分析以确定T细胞类型。 g) CD8⁺Ki67⁺ T细胞的百分比。 h) CD8⁺Tim3⁺ T细胞的百分比。 i) 肿瘤组织中细胞因子的浓度。 j) 肿瘤组织的免疫荧光染色以研究T细胞活化。比例尺 = 100 μm。 k) 瘤内M2巨噬细胞的比例。 l) 瘤内调节性T细胞的比例。 m) TDLNs中记忆T细胞的比例。
1.成功构建多功能超分子纳米平台: 开发了基于CB[7]主客体识别和金属配位的MC7-LNP系统,实现了MSA-2和铜离子的高效共负载与控释。
2.有效重构免疫抑制性TME:
清除多胺: CB[7]可高效结合并清除肿瘤内的免疫抑制性多胺(精胺、亚精胺),解除其对cGAS-STING通路的抑制。
缓解缺氧/诱导氧化应激: 铜离子催化产生活性氧,缓解肿瘤缺氧,同时诱导DNA损伤和损伤相关分子模式(DAMPs)释放,显著提升肿瘤细胞免疫原性。
持续激活STING通路: 主客体复合物实现了MSA-2的缓释,延长了STING通路的激活时间。
3.协同增强抗肿瘤免疫:
当与编码IL-12的mRNA联用时(MC7-LNP@mRNAIL-12),该系统在体外和体内均能强烈激活CTLs,促进其增殖、细胞因子分泌(如IFN-γ, GZM-B),并减少耗竭标志物(Tim3)表达。
显著促进树突状细胞成熟,降低M2巨噬细胞和调节性T细胞比例,逆转免疫抑制微环境。
显著抑制肿瘤生长: 在B16黑色素瘤模型中,MC7-LNP@mRNAIL-12治疗能最有效地抑制肿瘤生长,延长小鼠生存期,并诱导免疫记忆形成。
4.展示良好生物安全性: 瘤内给药未引起主要器官的明显病理损伤或异常铜蓄积。
文献意义:
本研究创新性地将超分子主客体化学与脂质纳米粒技术相结合,为解决STING激动剂在实体瘤治疗中的瓶颈(如快速代谢、免疫抑制微环境)提供了一个多功能的协同治疗平台。它不仅显著增强了STING通路的激活效率和持久性,还通过主动重塑TME,将"冷肿瘤"转化为"热肿瘤",为基于STING的癌症免疫疗法的发展提供了新的思路和强有力的实验依据。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:突破 “不可成药” 靶点!新型分子胶降解剂精准狙击 c-Myc 癌蛋白
下一篇:多组学驱动的基因组尺度代谢模型提高 HEK293 细胞的病毒载体产量