常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-02-25 09:00:00 细胞资源库平台 访问量:60
B 细胞是体液免疫的核心细胞,参与抗体产生、细胞因子分泌及抗原提呈,其活化、类别转换重组(CSR)、体细胞高频突变(SHM)等过程的机制研究对理解免疫应答及相关疾病至关重要。小鼠模型虽已揭示 B 细胞功能调控的关键通路,但人鼠 B 细胞生物学存在显著差异 —— 例如 BTK 缺陷在人类中导致 B 细胞发育完全阻断,而小鼠仍能产生前体 B 细胞;人类拥有 IgA1/IgA2 亚型,小鼠仅单一 IgA,且人类特有的 FcαRI 等受体影响体液免疫效应,这些差异限制了小鼠研究结果向人类的转化。此前虽有基于 CD40L 表达饲养细胞与细胞因子(BAFF、IL-4、IL-21)的人原代 B 细胞培养系统,但各组分对 B 细胞活力、增殖及抗体分泌的独立作用与相互作用尚不明确,且缺乏系统优化策略。
为此,来自丹麦奥胡斯大学医学院生物医学系、美国纽约基因组中心、哈佛大学医学院机构的 团队在《Scandinavian Journal of Immunology》上发表题为 “Multiparametric Optimization of Human Primary B-Cell Cultures Using Design of Experiments” 的原创研究,采用实验设计(DOE)框架,系统解析 CD40L、BAFF、IL-4、IL-21 对人原代 B 细胞功能的调控作用,建立标准化培养体系,为人类 B 细胞生物学研究及体外抗体生产提供关键工具。
本研究旨在建立并优化模拟 T 细胞依赖活化的人原代 B 细胞体外共培养系统,通过实验设计(DOE)框架解析关键调控因子的作用及相互作用。研究团队通过慢病毒转染构建工程化饲养细胞(人真皮成纤维细胞 NHDF、小鼠基质细胞 MS-5,经 hTERT 永生化),分别表达 CD40L 或细胞因子(BAFF、IL-4、IL-21);从健康供体血沉棕黄层纯化 CD19 + 泛 B 细胞或 naive B 细胞,设计 6 组 DOE 实验(全因子设计或 Box-Behnken 设计),调控 CD40L 饲养细胞密度 / 表达水平、重组细胞因子浓度(BAFF 10-100ng/mL、IL-4 0.1-10ng/mL、IL-21 1-250ng/mL)或细胞因子分泌饲养细胞密度,通过流式细胞术检测 B 细胞活力 / 增殖 / 表型,TRIFMA 检测抗体分泌。结果显示:BAFF 对 B 细胞功能影响微弱,IL-21 作用温和;CD40L(低表达饲养细胞高密度利于增殖,高表达促进抗体分泌)和 IL-4(高浓度抑制活力,却是 IgE CSR 的必需因子)是核心调控因子,且二者存在负相互作用;工程化饲养细胞可替代重组细胞因子传递信号,重组因子则更具浓度调控灵活性。该系统成功实现人原代 B 细胞的活化(CD38+CD95hi)、分化(记忆样 / 浆母细胞样)及多亚型抗体分泌,为深入研究人 B 细胞生物学及体外生产人源抗体提供标准化平台。
工程化饲养细胞构建:用慢病毒载体将 hTERT(细胞永生化)、CD40L、BAFF、IL-4、IL-21 分别转入 NHDF 或 MS-5 细胞,经潮霉素(hTERT)或嘌呤霉素(CD40L / 细胞因子)筛选获得稳定克隆;通过流式检测 CD40L 膜表达,ELISA 检测 BAFF/IL-4/IL-21 分泌水平,选择低 / 高 CD40L 表达克隆(N.40-low、N.40-high)及高细胞因子分泌克隆(N.BAFF、N.IL4、N.IL21)备用。
原代人 B 细胞纯化:从健康供体血沉棕黄层分离 PBMC(Ficoll 密度梯度离心),用 MACS 磁珠法(Naive B 细胞分离试剂盒或 CD19 磁珠)获取 CD19 + 泛 B 细胞或 CD19+CD27-IgD+ naive B 细胞;流式验证纯度(>90%)后,用含 90% FBS+10% DMSO 的冻存液保存,或直接用于实验。
DOE 实验设计与共培养:设计 6 组 DOE 实验(全因子设计用于二水平分析,Box-Behnken 设计用于三水平优化):DOE1-2 调控 CD40L 饲养细胞密度 / 表达水平及重组细胞因子浓度,DOE3-5 比较重组因子与细胞因子分泌饲养细胞的效果,DOE6 分析时间动态(Day0-14);Day-1 接种饲养细胞,Day0 接种 B 细胞(1×10³-2.8×10⁴细胞 / 孔),Day3/5 换液(补充 IL-21/BAFF,DOE3 中 Day5 换液不补 IL-4),培养至目标时间点检测。
功能与表型检测:流式细胞术(PI 染色)检测 B 细胞活力,计数活细胞数量评估增殖;通过 CD38、CD95、CD27、IgD 抗体检测 B 细胞活化(CD38+CD95hi)与分化(记忆样 IgD-CD27+、浆母细胞样 CD38hi);TRIFMA 检测上清中 IgG、IgE、IgM、IgA、IgG1、IgG3 水平;用 FlowSOM 和 UMAP 分析 B 细胞分化聚类模式。
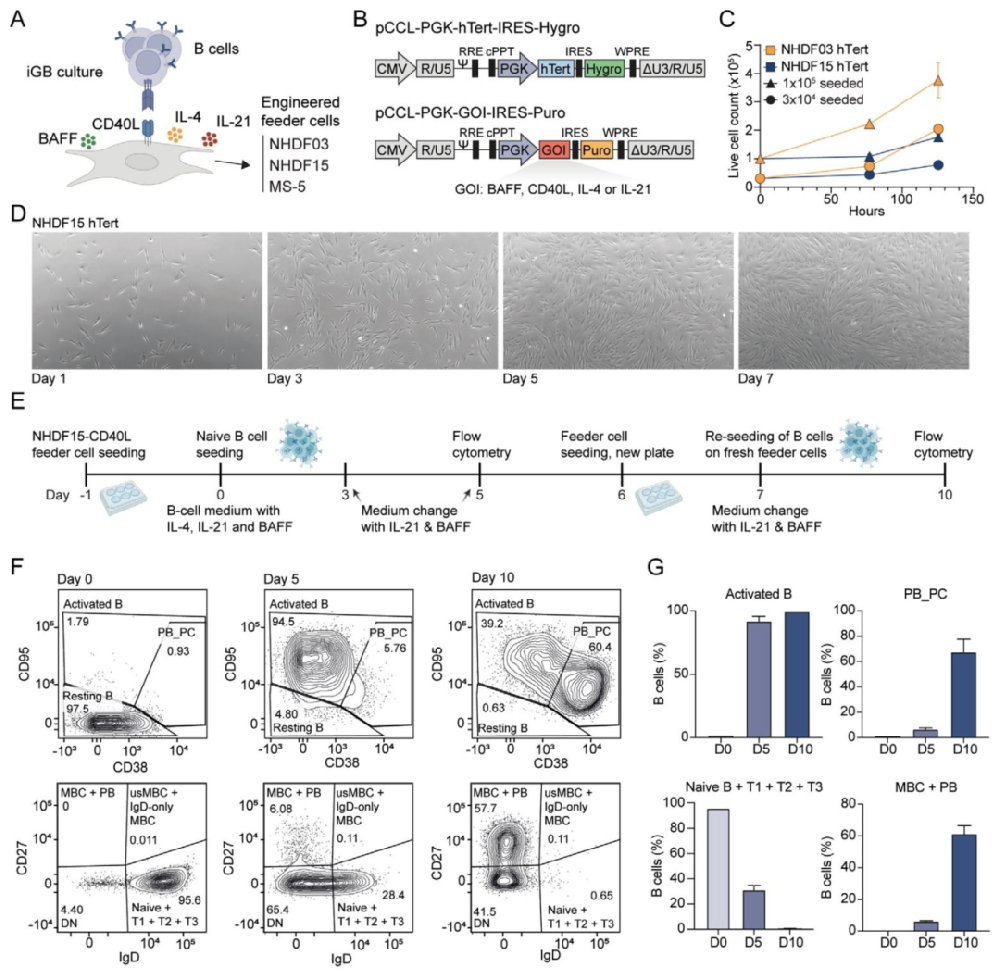
图1:人原代 B 细胞共培养系统的建立
内容:图 1A 为诱导生发中心样 B 细胞(iGB)共培养示意图,naive B 细胞接种于 CD40L 表达饲养细胞,补充 BAFF/IL-4/IL-21 以模拟 T 细胞依赖活化;图 1B 展示慢病毒载体结构,用于构建 hTERT 永生化(含潮霉素抗性)及 CD40L / 细胞因子表达(含嘌呤霉素抗性)饲养细胞;图 1C 显示 hTERT 修饰的 NHDF03(倍增时间 48h)和 NHDF15(倍增时间 64h)生长曲线,证实 NHDF15 增殖更慢,更适合共培养;图 1D 为 NHDF15-hTERT 细胞在 Day1、3、5、7 的相差显微镜图像,显示其贴壁生长及接触抑制特性;图 1E 为共培养时间线(Day-1 接种饲养细胞,Day0 接种 B 细胞,Day7 传代至新饲养细胞,Day5/10 进行流式检测);图 1F-G 为流式结果,Day0 naive B 细胞以 CD38 低、IgD + 为主,Day5 分化为活化 B 细胞(CD38+CD95hi,占比 94.5%),Day10 进一步分化为记忆样(IgD-CD27+,占比 60.4%)和浆母细胞样(CD38hi,占比 39.2%)细胞,证实工程化饲养细胞可有效支持人 naive B 细胞的活化与分化。
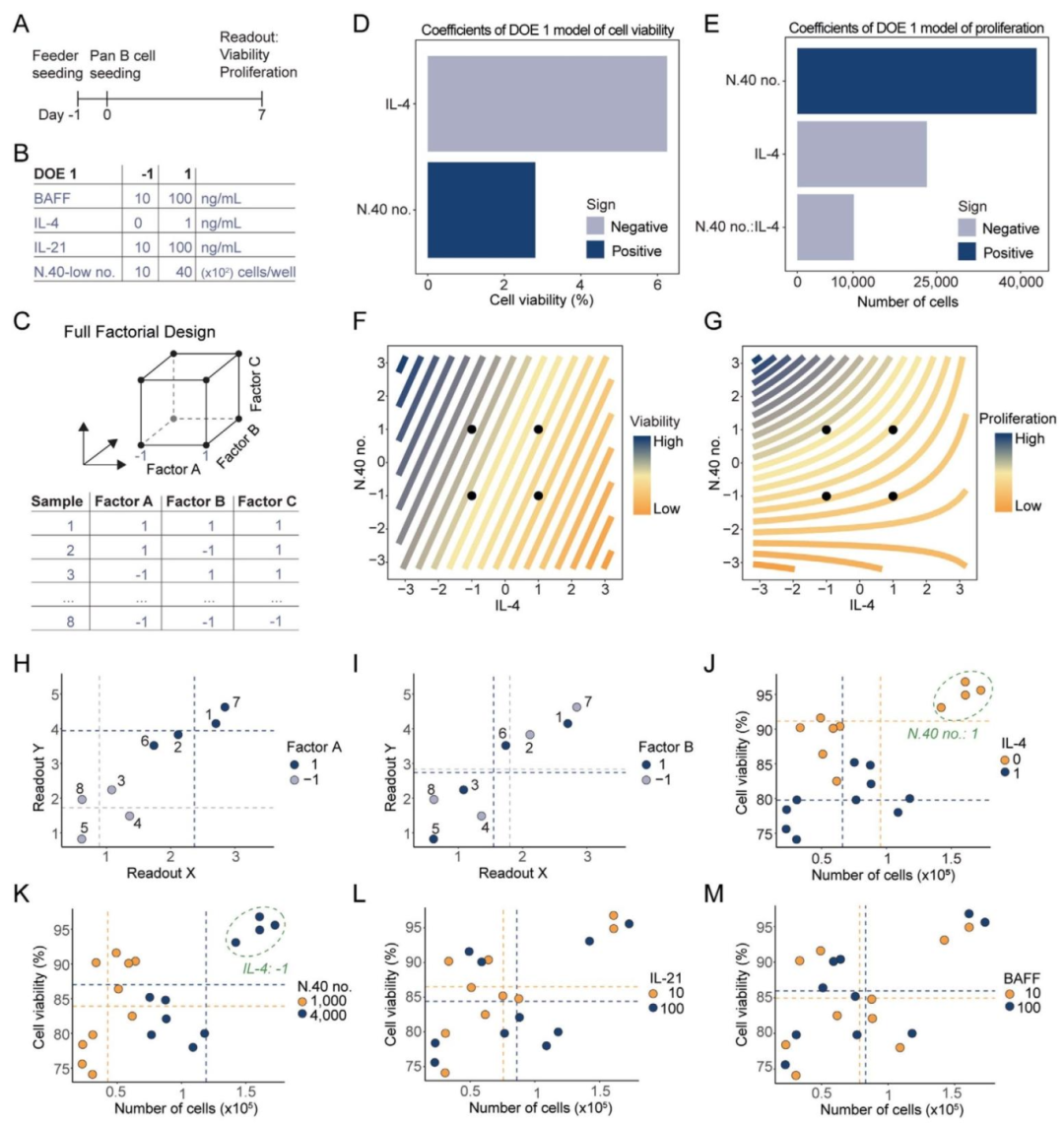
图2:IL-4 和 CD40L 对 B 细胞活力与增殖的调控(DOE1)
内容:图 2A 为 DOE1 时间线(Day-1 接种 N.40-low 饲养细胞,Day0 接种泛 B 细胞,Day7 检测活力与增殖);图 2B 为 DOE1 因子水平设置:CD40L 饲养细胞密度(10-40×10³ 细胞 / 孔)、BAFF(10-100ng/mL)、IL-4(0-1ng/mL)、IL-21(10-100ng/mL);图 2C 为三因子全因子设计示意图,每个因子的高低水平组合覆盖所有可能条件;图 2D-E 帕累托图显示,IL-4(负效应)和 N.40-low 密度(正效应)是影响 B 细胞活力(图 2D)和增殖(图 2E)的显著因子(p<0.05),BAFF 与 IL-21 无显著作用;图 2F-G 等高线图显示 IL-4 与 N.40-low 密度存在负相互作用 —— 高 IL-4 + 高饲养细胞密度时,B 细胞活力与增殖均下降;图 2J-M 散点图进一步验证:1ng/mL IL-4 使 B 细胞活力下降超 10%(图 2J),N.40-low 密度 40×10³ 细胞 / 孔时 B 细胞数量是 10×10³ 的 2 倍以上(图 2K),而 BAFF(图 2L)和 IL-21(图 2M)在测试浓度范围内无显著影响。
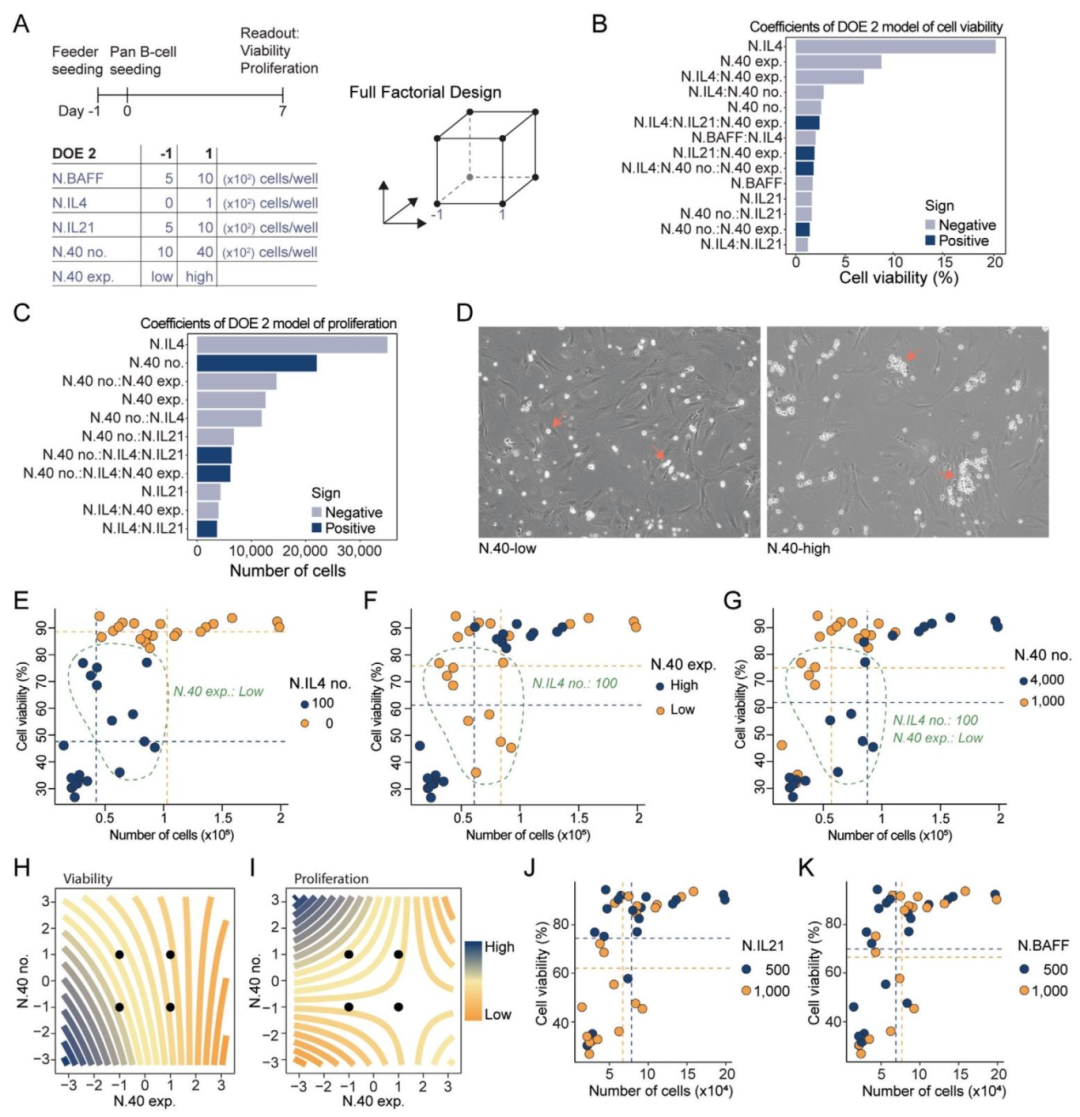
图3:饲养细胞传递细胞因子对 B 细胞的影响(DOE2)
内容:图 3A 为 DOE2 设计,调控 N.BAFF(5-10×10² 细胞 / 孔)、N.IL4(0-1×10² 细胞 / 孔)、N.IL21(5-10×10² 细胞 / 孔)、N.40 密度(1-4×10³ 细胞 / 孔)及 N.40 表达水平(低 / 高);图 3B-C 帕累托图显示,IL-4(N.IL4,负效应)、N.40 密度(正效应)及 N.40 表达水平(负效应)是影响活力(图 3B)和增殖(图 3C)的核心因子,且 N.40 密度与表达水平存在负相互作用;图 3D 相差显微镜图像显示,N.40-high 饲养细胞组的 B 细胞更易形成小簇,而 N.40-low 组细胞分布更均匀;图 3E 显示仅接种 100 个 N.IL4 细胞,即可使 B 细胞活力 / 增殖分别下降 40%/50%;图 3F-G 显示 N.IL4 存在时,N.40-low 组的 B 细胞活力(图 3F)和增殖(图 3G)均高于 N.40-high 组,且 N.40 低密度利于活力、高密度利于增殖;图 3H-I 等高线图明确最优条件:活力最优为 N.40 低密度 + 低表达,增殖最优为 N.40 高密度 + 低表达;图 3J-K 证实 N.BAFF 与 N.IL21 无显著影响。
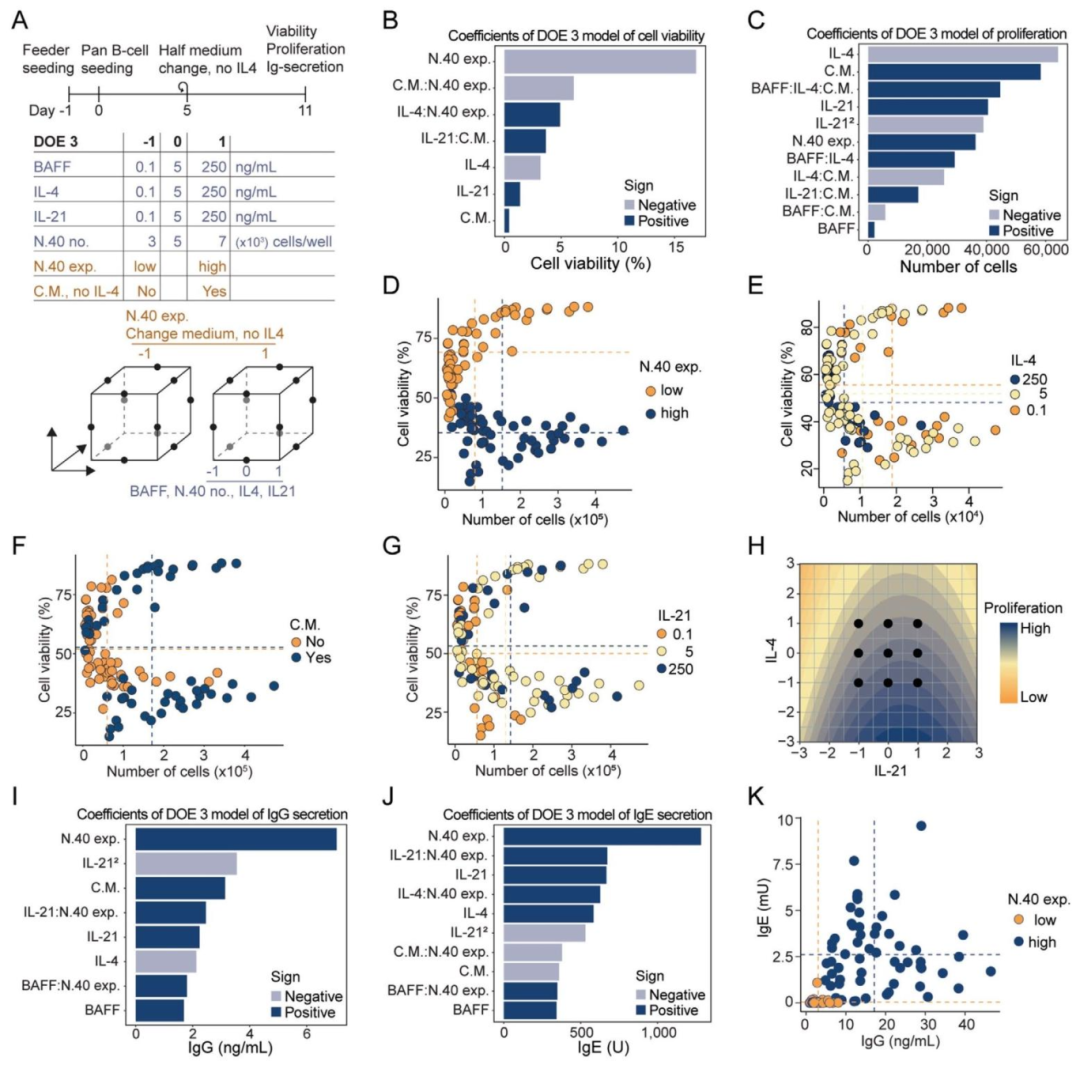
图4:Box-Behnken 设计优化抗体分泌(DOE3)
内容:图 4A 为 DOE3 时间线(Day0 接种 B 细胞,Day5 换液不补 IL-4,Day11 检测),采用三水平 Box-Behnken 设计,调控 N.40 表达水平(低 / 高)、IL-4(0.1-10ng/mL)、IL-21(1-250ng/mL)及换液操作;图 4B-C 帕累托图显示,CD40L 表达水平、IL-4(负效应)及 Day5 换液(正效应)是影响活力(图 4B)和增殖(图 4C)的显著因子,IL-21 呈非线性效应(模型预测最优浓度 172ng/mL);图 4D-E 显示 N.40-low 组活力高于 N.40-high,IL-4 0.1ng/mL 时增殖最优;图 4F 显示 Day5 换液(不补 IL-4)可提升 B 细胞活力;图 4G-H 显示 IL-21 172ng/mL 时增殖最高;图 4I-J 帕累托图显示,CD40L 表达水平是影响 IgG(4 倍升高)和 IgE(10 倍升高)分泌的最显著因子;图 4K 显示 N.40-high 组 IgG/IgE 分泌显著高于 N.40-low,且高 IL-4 促进 IgE、抑制 IgG,BAFF 无显著作用。
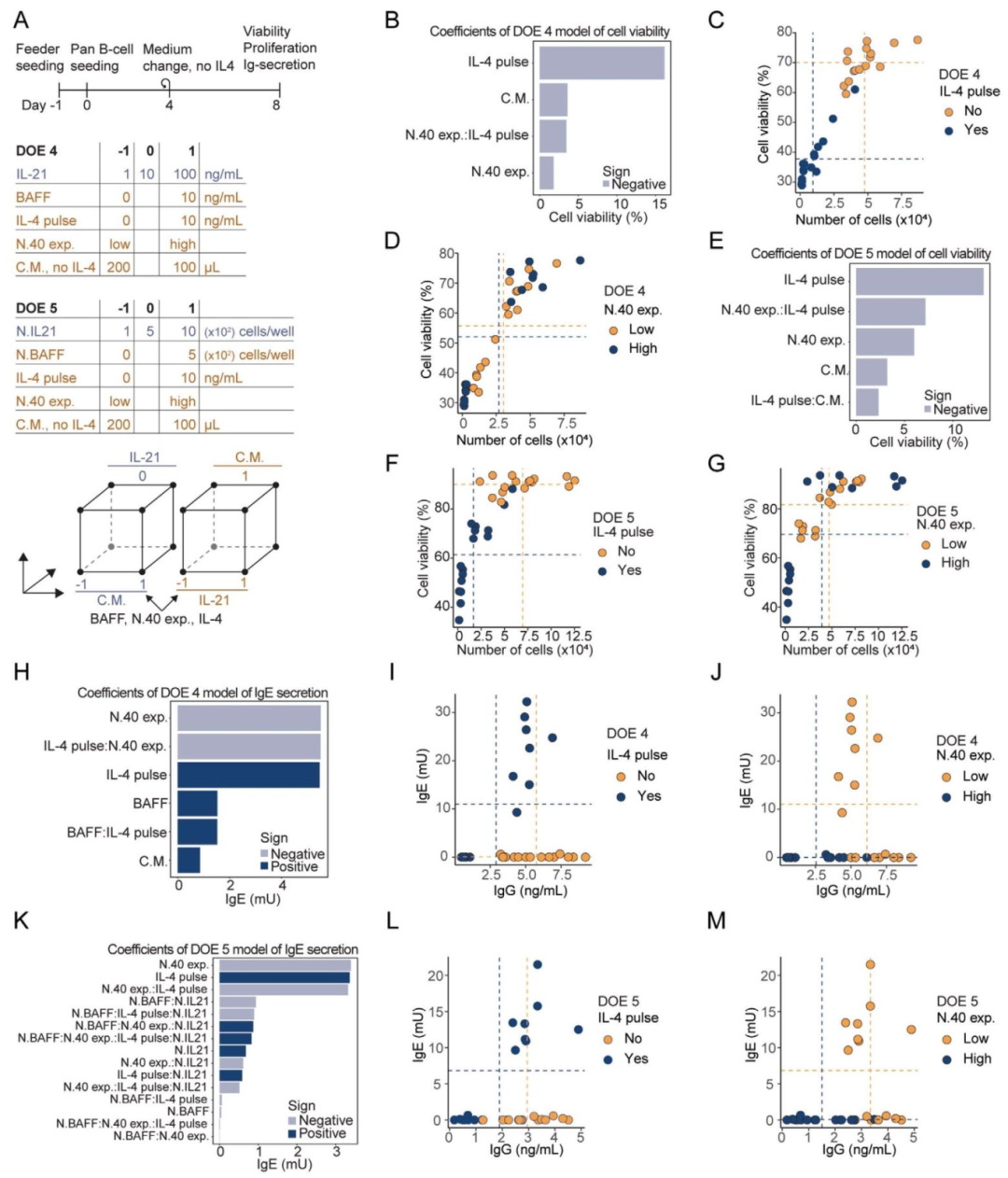
图5:细胞因子传递方式的比较(DOE4/5)
内容:图 5A 为 DOE4/5 时间线(Day0 接种 B 细胞,Day8 检测),DOE4 调控重组细胞因子(BAFF 0-10ng/mL、IL-4 0-10ng/mL、IL-21 1-100ng/mL),DOE5 调控细胞因子分泌饲养细胞密度;图 5B-E 帕累托图显示,IL-4(负效应)和 N.40 表达水平(与 IL-4 存在负相互作用)是影响活力(图 5B、5E)和增殖(图 5C、5F)的核心因子,与前序实验一致;图 5H-K 显示 IL-4 是 IgE 分泌的必需因子 —— 仅 IL-4 存在时检测到 IgE,且 N.40-high 组 IgG 分泌更高;图 5M 显示 DOE5 中,细胞因子分泌饲养细胞与重组因子效果一致,最高增殖倍数达 125 倍(N.IL21 5×10² 细胞 / 孔 + N.40-high 组),证实饲养细胞可有效替代重组因子传递 BAFF/IL-21 信号。
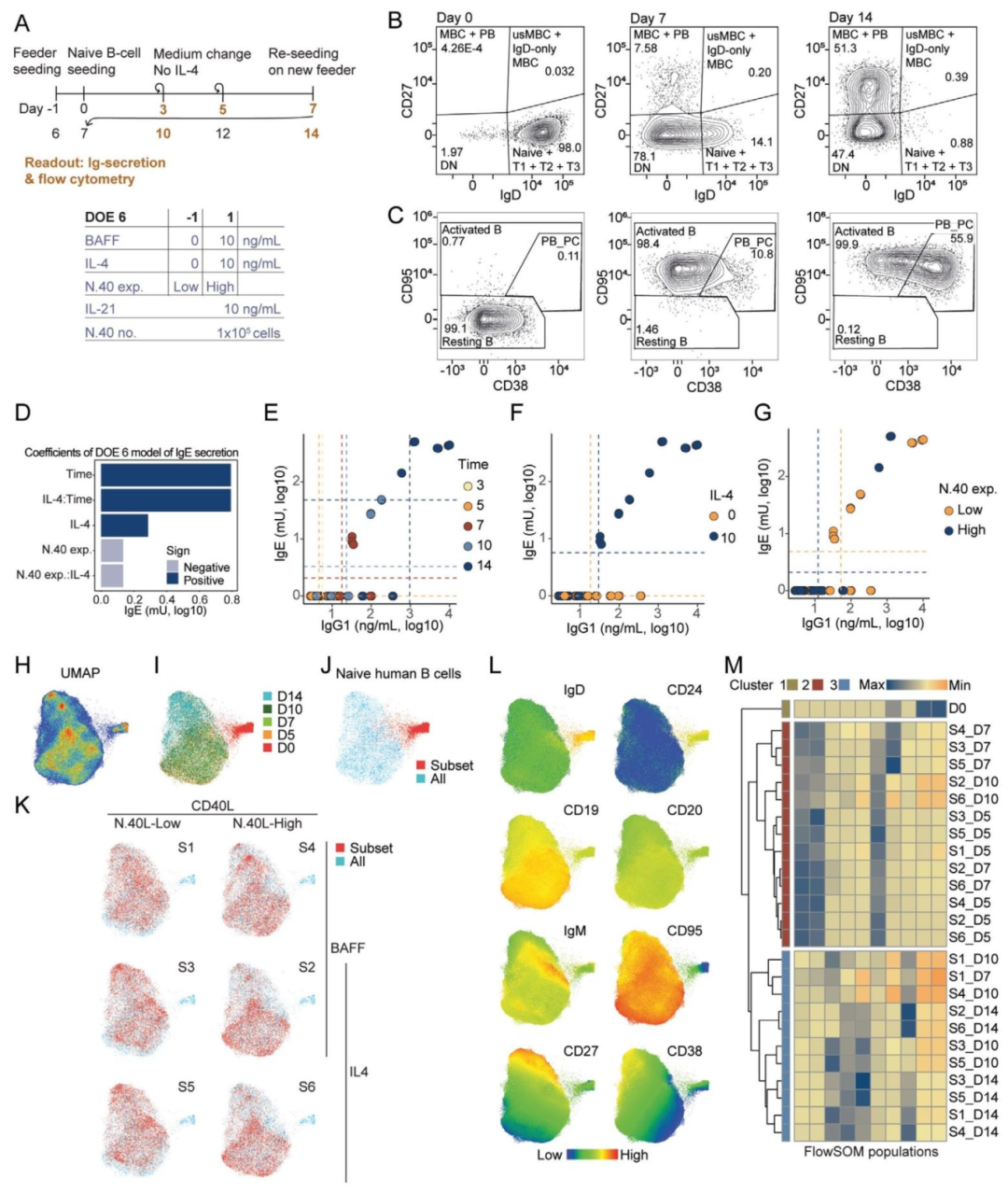
图6:B 细胞分化与抗体分泌的时间动态(DOE6)
内容:图 6A 为 DOE6 设计(调控 BAFF 0-10ng/mL、IL-4 0-10ng/mL、N.40 表达水平),Day0-14 多时间点检测;图 6B-C 流式结果显示,Day0 naive B 细胞(IgD+CD27-)随培养时间分化:Day5 出现活化 B 细胞(CD38+CD95+),Day10 分化为记忆 B 细胞(IgD-CD27+)和浆细胞(CD38hi),Day14 浆细胞比例进一步升高;图 6D 帕累托图显示,时间、IL-4、N.40 表达水平是 IgE 分泌的显著因子;图 6E-G 显示 IgG1 分泌随时间升高(Day14 达峰值),IL-4 促进 IgE 分泌(N.40-low 组 Day10 IgE 最高,N.40-high 组 Day14 追上);图 6H-M 为 UMAP 和 FlowSOM 分析,显示 B 细胞聚类主要由培养时间驱动(Day0 与 Day14 聚类完全分离),IL-4+N.40-high 组分化速度较慢,IL-4-N.40-low 组分化最快,BAFF 无显著影响,证实时间是 B 细胞默认 CSR(向 IgG1/IgG3/IgA)的关键驱动因素。
本研究通过实验设计(DOE)框架,首次系统解析了人原代 B 细胞体外培养的关键调控因子及相互作用,核心结论如下:1. 因子重要性排序:CD40L 和 IL-4 是核心调控因子(CD40L 调控增殖与抗体分泌,IL-4 调控 IgE CSR 但抑制活力),IL-21 作用温和(长期培养最优浓度 172ng/mL),BAFF 无显著影响;2. 关键相互作用:CD40L 与 IL-4 存在负相互作用 —— 高 IL-4 + 高 CD40L 对 B 细胞功能更不利,低 CD40L 表达 + 高饲养细胞密度是平衡活力与增殖的最优组合;3. 细胞因子传递方式:工程化饲养细胞可替代重组因子传递 BAFF/IL-21 信号,效果相当,而重组因子更易灵活调控浓度;4. 分化与分泌动态:培养时间是 B 细胞向 IgG1/IgG3/IgA 默认 CSR 的关键因素,IL-4 与 CD40L 共同调控 IgE CSR 的速率(低 CD40L 组更快)。该系统为解析人 B 细胞特有的生物学过程(如 RNA 编辑、抗体亚型转换)提供标准化工具,也为体外生产人源治疗性抗体(如自身免疫病或感染性疾病相关抗体)奠定基础,同时证实 DOE 框架在多参数细胞培养优化中的高效性,可推广至其他原代细胞培养体系的开发。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:鱿鱼(Euprymna berryi)原代细胞的分离、培养与转染实验方案
下一篇:TXNIP 缺陷患者原代细胞中 NRF2 激活与乙醛酸酶 1(GLO1)上调的关联