常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-02-02 09:00:38 细胞资源库平台 访问量:173
在生物医学研究和药物开发领域,生物发光成像技术因其高信噪比而被广泛应用于细胞测定和动物成像研究。然而,传统的荧光素酶种类有限,限制了同时成像多个分子和细胞事件的能力。为了突破这一限制,科学家们开发了一种新型的ATP非依赖性荧光素酶——NanoLuc(NL),它源自深海虾Oplophorus gracilirostris,并经过工程改造以增强蛋白质稳定性。NanoLuc作为一种小型(19 kDa)、高亮度的荧光素酶,其亮度是传统萤火虫或海肾荧光素酶的100倍,并且使用furimazine作为底物产生明亮的辉光型发光。NanoLuc的意义在于其为双报告基因生物发光分子成像提供了新的可能。它不仅可以在活体小鼠的表层和深层组织中成像,而且其生物发光随时间的变化可以用来定量肿瘤生长,甚至在少量血清中也能检测到分泌的NL。此外,NanoLuc与萤火虫荧光素酶的结合使用,为在完整细胞和活体小鼠中定量TGF-β信号传导的两个关键步骤提供了一种新型双荧光素酶成像策略,从而在正常生理、疾病和药物开发中扩展了信号转导的成像能力。NanoLuc的作用不仅体现在其高灵敏度和高稳定性上,它还具有更小的尺寸,这使得在标记细胞和蛋白质时对样本的侵入性更小,有助于保持细胞或组织的天然状态。NanoLuc的快速反应、低背景发光和多样灵活等特点,使其在生物学和医学研究中具有广泛的应用前景。因此,NanoLuc作为一种新的报告基因,不仅增强了我们对生物过程的理解和疾病机理的研究,而且在开发潜在治疗方法和疗法方面发挥了重要作用。
英文标题:Nanobody-assisted nanoluciferase fragment complementation for in situ measurement and visualization of endogenous protein-protein interaction
中文标题:纳米抗体辅助的纳米荧光素酶片段互补技术用于内源性蛋白质相互作用的原位检测与可视化
发表期刊:《Biosensors and Bioelectronics》
影响因子:10.5
作者单位:
1.Shenzhen Bay Laboratory, Shenzhen, 518132, China
2.State Key Laboratory of Crop Stress Biology for Arid Areas, College of Life Sciences, Northwest A&F University, Yangling, 712100, Shanxi, China
3.Key Laboratory for Biorheological Science and Technology of Ministry of Education, State and Local Joint Engineering Laboratory for Vascular Implants, College of Bioengineering, Chongqing University, Chongqing, 400030, China
4.Department of Biology, School of Life Sciences, Southern University of Science and Technology, Shenzhen, 518055, China
5.Beijing National Laboratory for Molecular Sciences, College of Chemistry and Molecular Engineering, Peking University, Beijing, 100871, China
6.Biomedical Pioneering Innovation Center (BIOPIC), Peking University, Beijing, 100871, China
作者信息:
Qianqian Li,Huijuan Liu
蛋白质相互作用(PPI)是细胞生理过程的核心,异常 PPI 与疾病密切相关,但现有检测方法存在局限:免疫沉淀依赖细胞裂解丢失空间信息,邻近标记需外源表达融合蛋白,邻近连接 assay(PLA)操作繁琐、成本高。本研究整合纳米抗体(高特异性、小尺寸)与纳米荧光素酶片段互补(NanoBiT,高信号背景比)的优势,开发纳米抗体辅助的 PPI 原位检测技术(NanaPPI),实现内源性 PPI 的快速、灵敏、低成本检测,同时保留空间定位信息,适用于新 PPI 鉴定、抑制剂筛选及临床生物标志物检测。
核心原理:当内源性蛋白质发生相互作用时,针对两种蛋白的一抗(鼠源 / 兔源)分别招募融合纳米荧光素酶小片段(SF)和大片段(LgBiT)的二抗纳米抗体,使 SF 与 LgBiT 互补形成完整酶,产生发光信号。关键实验包括:1)探针优化:筛选 SF 与 LgBiT 的最佳组合(SF128/LgBiT),验证纳米抗体特异性;2)方法验证:检测已知低丰度 PPI(SFPQ/NONO、YAP1/TEAD4、p53/MDM2),对比 PLA 和 HTRF 方法;3)原位可视化:利用发光显微镜观察固定细胞及肿瘤组织切片中 PPI 的空间定位;4)功能应用:评估抑制剂( Verteporfin)对 YAP1/TEAD4 的干扰,鉴定应激颗粒中 YTHDF2/G3BP1、m⁶A/G3BP1 等新 PPI;5)数据处理:通过免疫染色验证定位,归一化发光强度量化 PPI 水平,统计分析采用 t 检验和 Pearson 相关系数。
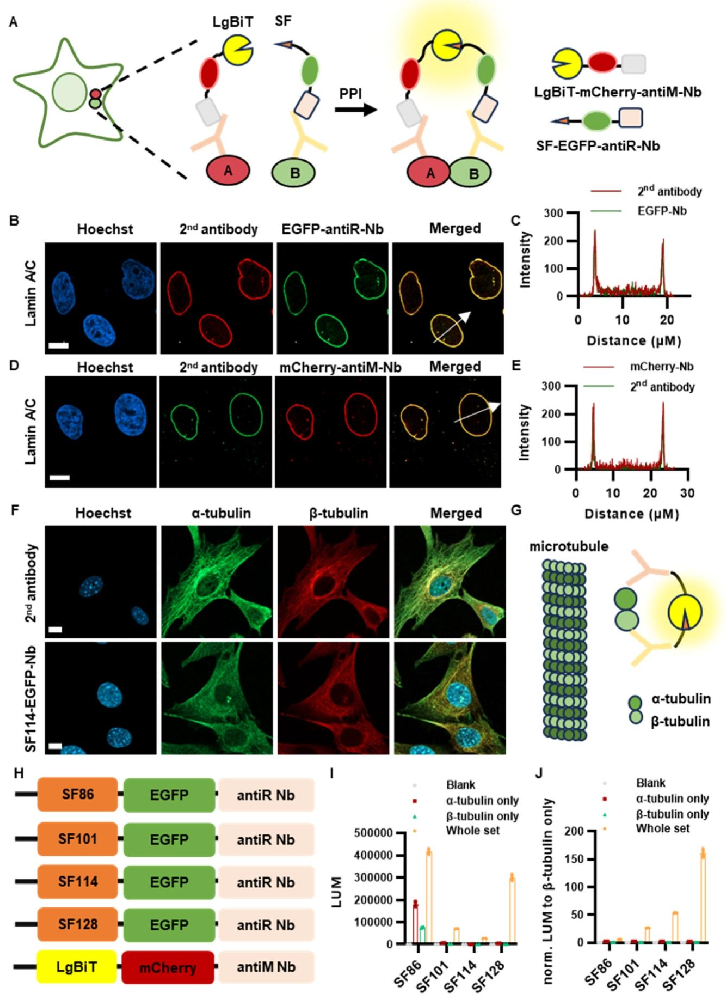
图 1:NanaPPI 技术设计与优化
NanaPPI 由一抗、融合 SF/LgBiT 的二抗纳米抗体组成(图 1A);纳米抗体特异性经免疫染色验证,可精准识别靶蛋白(Lamin A/C、H3K27me3 等)(图 1B-E);以 α/β- 微管蛋白 PPI 为模型,确定 SF128/LgBiT 组合的信号背景比(SBR)最高(图 1G-J),显著优于 HTRF 方法。
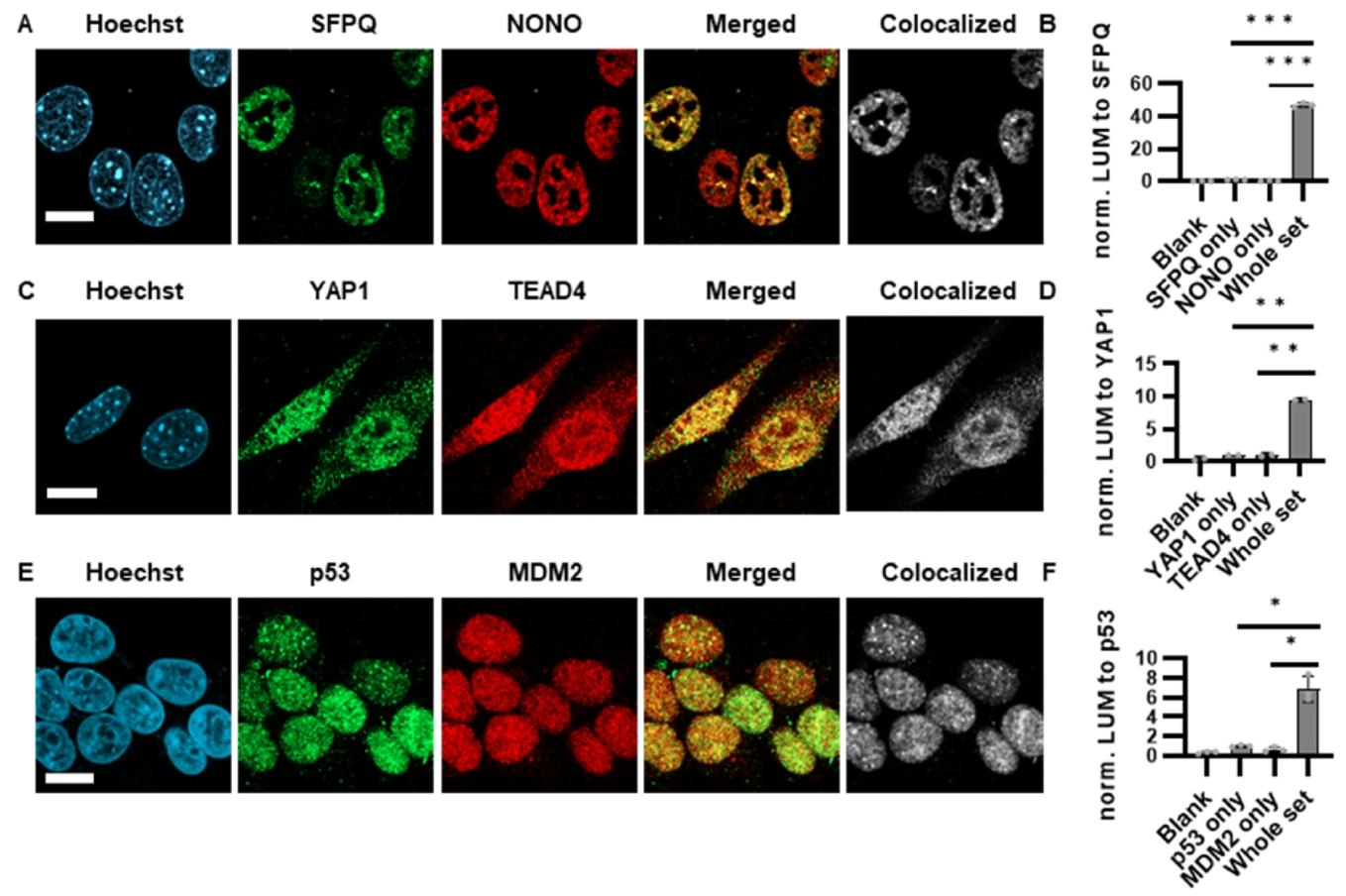
图 2:检测低丰度内源性 PPI
成功检测 SFPQ/NONO( paraspeckle 核心复合物)、YAP1/TEAD4(Hippo 通路关键 PPI)、p53/MDM2(肿瘤治疗靶点)等低丰度 PPI(图 2A-E);发光信号比单一抗体对照组高 6-40 倍,证实技术高灵敏度(图 2B、D、F)。
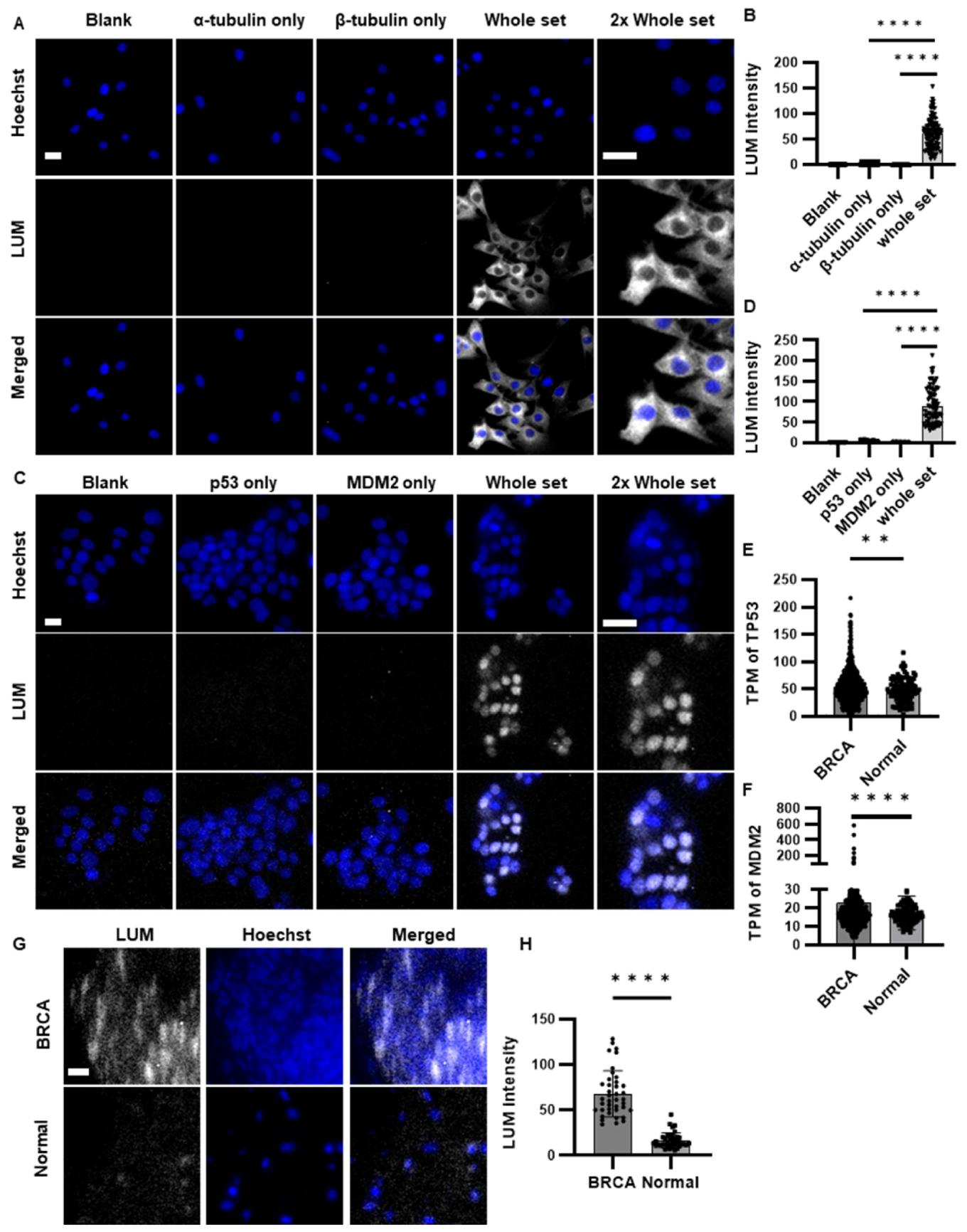
图 3:细胞与组织水平的 PPI 可视化
在 C2C12 细胞中,α/β- 微管蛋白 PPI 的发光信号定位于细胞质,与微管分布一致(图 3A-B);p53/MDM2 PPI 的发光信号集中在细胞核(图 3C-D);临床乳腺癌组织切片中 p53/MDM2 PPI 信号显著高于正常乳腺组织(图 3G-H),与 TCGA 数据库中基因表达水平一致(图 3E-F)。
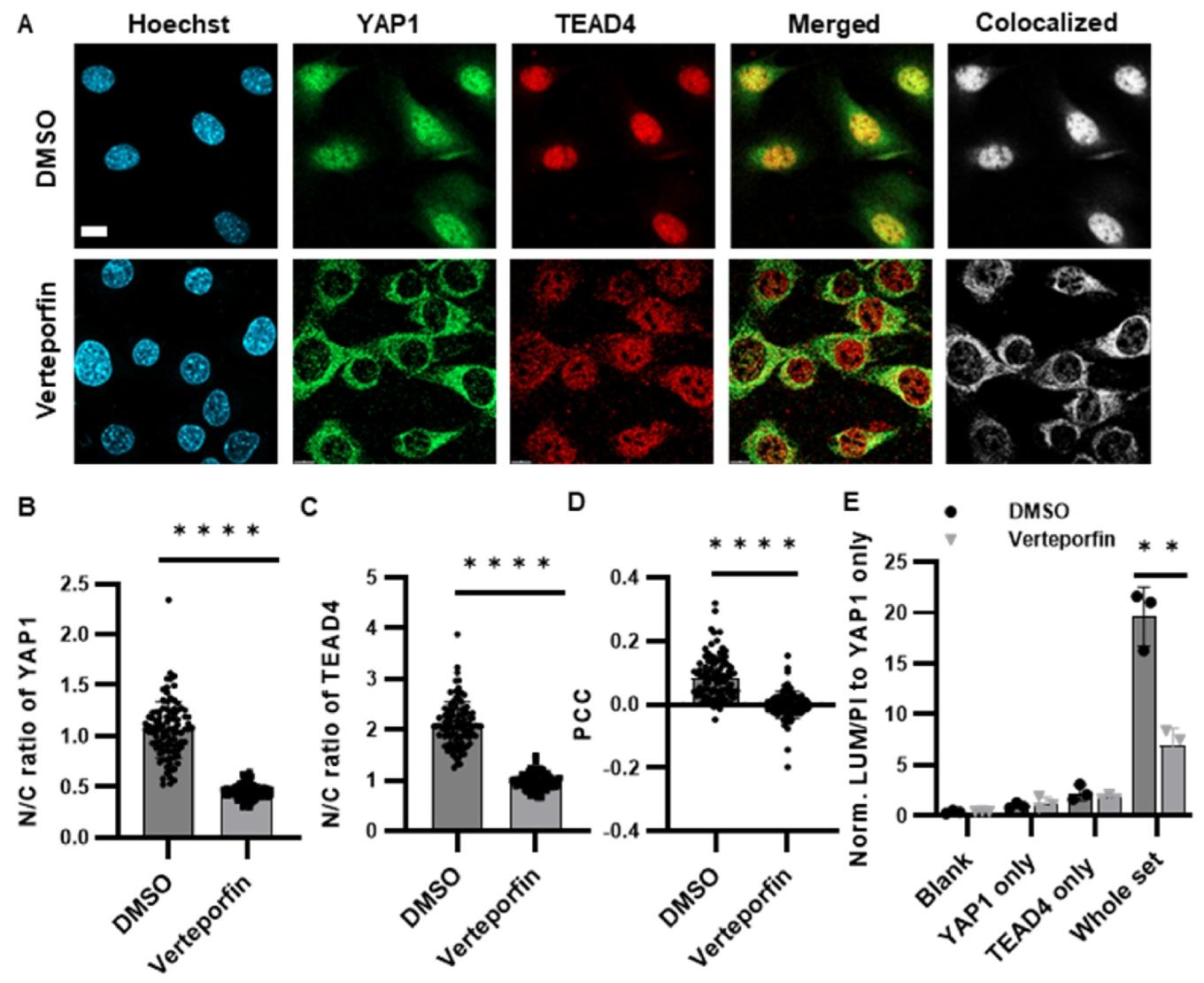
图 4:PPI 抑制剂筛选与细胞类型差异分析
Verteporfin 处理后,YAP1/TEAD4 的核质分布改变、共定位系数下降(图 4A-D),NanaPPI 检测到 PPI 水平降低 50%(图 4E),验证技术用于抑制剂筛选的可行性;乳腺癌细胞 MCF-7 的 α/β- 微管蛋白 PPI 水平显著低于正常乳腺细胞 MCF-10A(图 S6),提示 PPI 可作为疾病标志物。
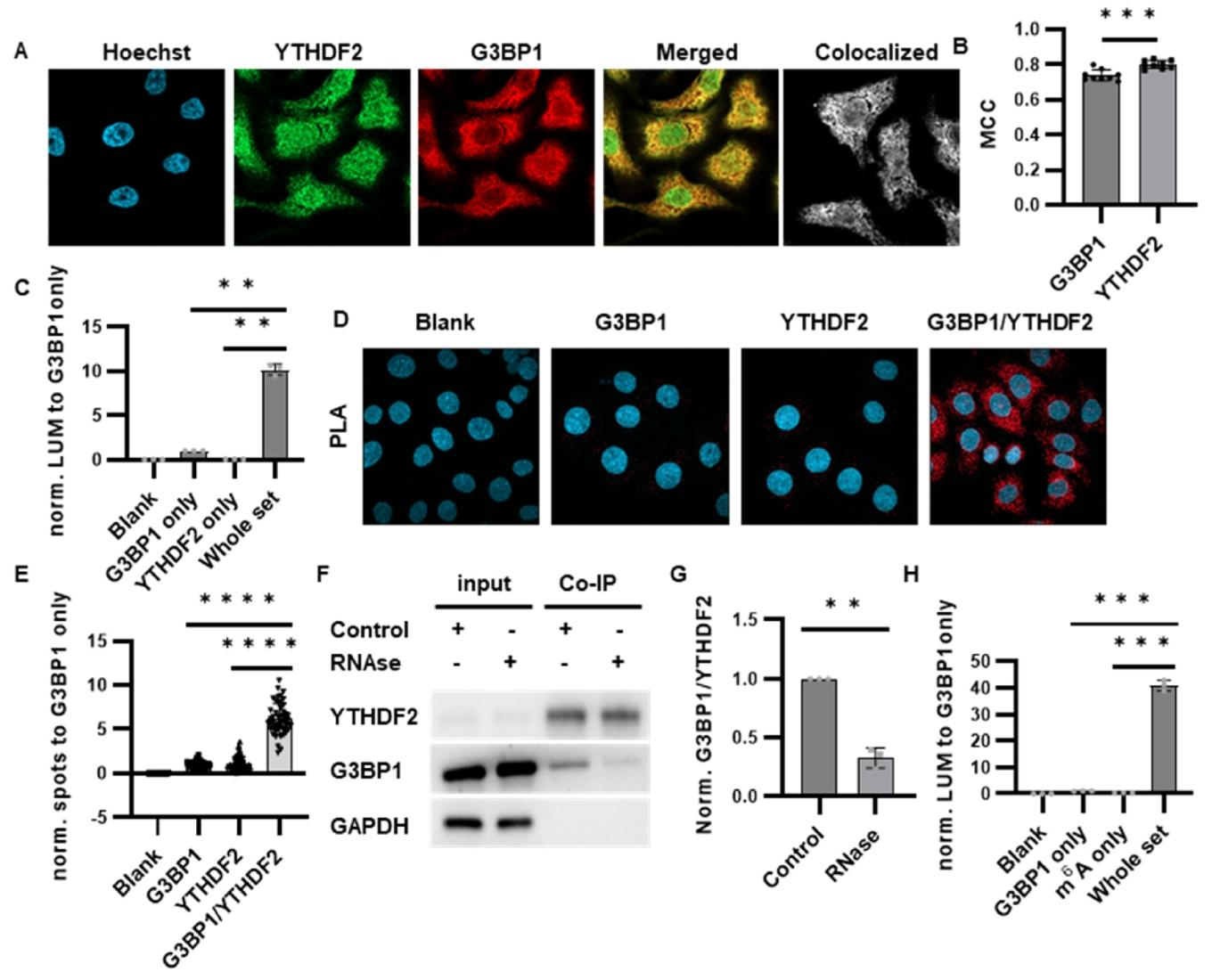
图5 :YTHDF2/G3BP1 及 m⁶A/G3BP1 新 PPI 的鉴定
免疫染色结果:HeLa 细胞中 YTHDF2 与 G3BP1 主要定位于细胞质,且存在明显共定位,Manders 共定位系数(MCC)证实二者空间邻近(图 5A-B)。
NanaPPI 检测:YTHDF2 与 G3BP1 在生理状态下即存在显著相互作用,发光信号显著高于单一抗体对照组(图 5C),信号背景比与 PLA 相当。
PLA 验证:YTHDF2/G3BP1 相互作用产生的斑点数量远高于空白或单一抗体对照组,进一步证实该 PPI 的真实性(图 5D-E)。
免疫沉淀验证:YTHDF2 抗体下拉实验中可检测到 G3BP1,RNase 处理后结合信号显著降低,表明二者相互作用依赖 RNA(图 5F-G)。
m⁶A/G3BP1 相互作用:NanaPPI 首次检测到 m⁶A 修饰与 G3BP1 的内源性相互作用,突破体外研究中 G3BP1 偏好未修饰 RNA 的认知(图 5H)。
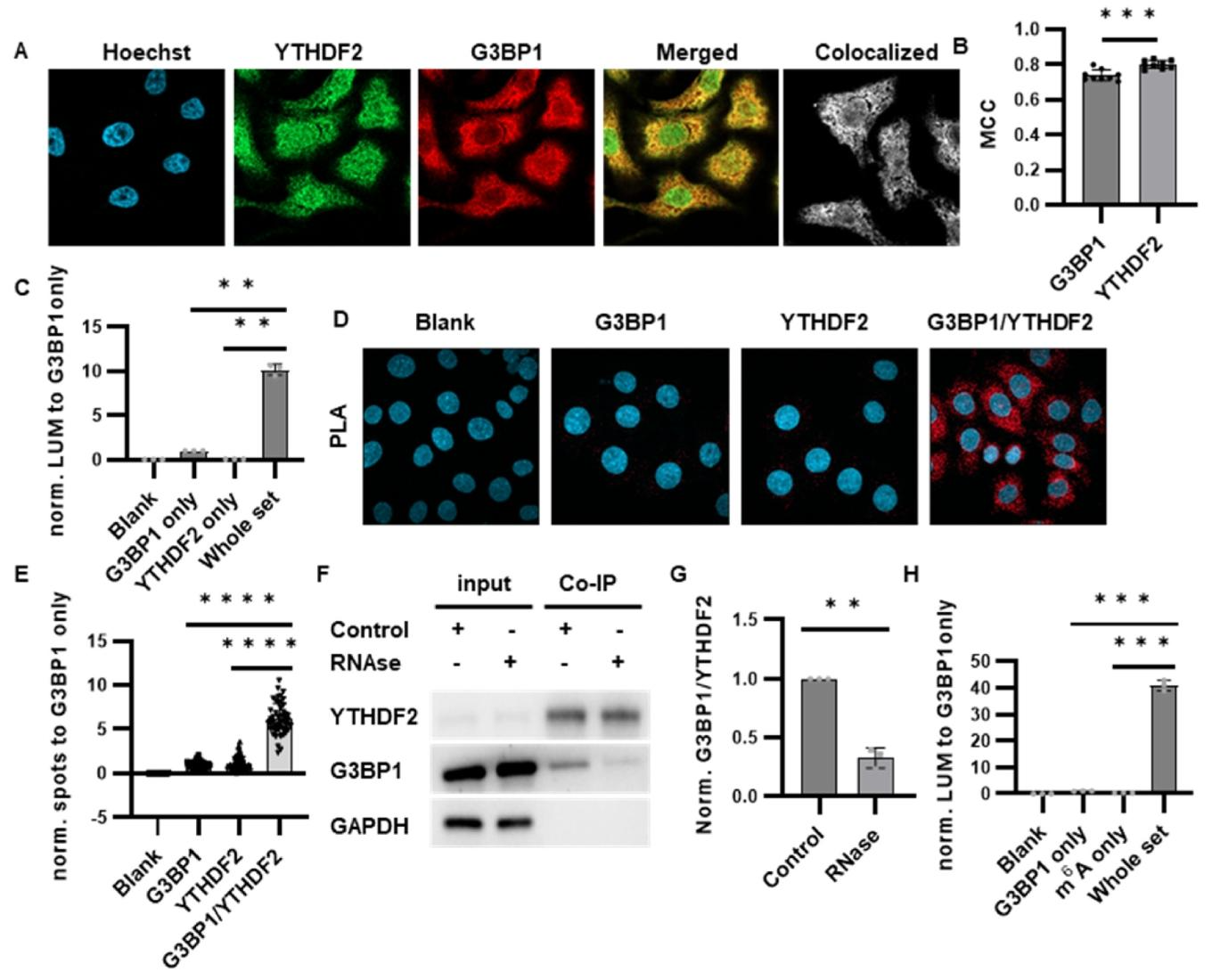
图6 :亚砷酸盐应激下 PPI 的动态变化及机制
应激诱导共定位:NaAsO2 处理后,YTHDF2 与 G3BP1 共定位系数(PCC)显著升高,形成应激颗粒(SG)特征性凝聚体(图 6A-B);m⁶A 与 G3BP1 的共定位也同步增强(图 6C-D)。
NanaPPI 量化:应激状态下,YTHDF2/G3BP1 和 m⁶A/G3BP1 的发光信号均显著高于生理状态,证实应激可强化二者相互作用(图 6E-F);而 PLA 因 DNA 扩增子拥挤,无法有效区分应激颗粒内的 PPI 信号(图 S7)。
YTHDF2 介导机制:siRNA 敲低 YTHDF2 后,NaAsO2 诱导的 m⁶A/G3BP1 相互作用显著减弱,表明 YTHDF2 作为 m⁶A 阅读器,介导 m⁶A 修饰 mRNA 向应激颗粒富集(图 6G)。
本研究开发的 NanaPPI 技术实现了内源性 PPI 的原位高灵敏检测,核心结论如下:1)技术优势:信号背景比与 PLA 相当,但操作更简便、检测更快、成本更低,无需外源表达,保留空间信息;2)核心性能:可检测低丰度 PPI,实现固定细胞及组织切片中 PPI 的可视化,量化抑制剂对 PPI 的干扰及生理 / 病理状态下的 PPI 差异;3)创新发现:鉴定 YTHDF2/G3BP1、m⁶A/G3BP1 等新 PPI,揭示 YTHDF2 在应激颗粒中富集 m⁶A 修饰 mRNA 的机制;4)应用前景:适用于新 PPI 鉴定、PPI 抑制剂高通量筛选及临床疾病的 PPI 生物标志物检测。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:报告基因假阳性预警!查尔酮对 FLuc 的抑制竟依赖 A/B 环取代模式
下一篇:双层(清洁-治愈)水凝胶中光控时空顺序释放MXenes/NO气体促进MRSA生物膜感染的糖尿病溃疡伤口愈合