常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-25 17:28:47 细胞资源库平台 访问量:205
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:Targeting IL-6/STAT3 signaling abrogates EGFR-TKI resistance through inhibiting Beclin-1 dependent autophagy in HNSCC
中文标题:靶向 IL-6/STAT3 信号通过抑制 Beclin-1 依赖的自噬逆转头颈部鳞状细胞癌(HNSCC)的 EGFR-TKI 耐药
发表期刊:《Cancer Letters》
影响因子:10.1
作者单位:
Cell Signalling Research Group, School of Life Sciences, University of Nottingham, Nottingham, UK
作者信息:
1.Department of Maxillofacial and Otorhinolaryngological Oncology, Tianjin Medical University Cancer Institute & Hospital, Tianjin, 300060, China
2.National Clinical Research Center for Cancer, Tianjin, 300060, China
3.Tianjin’ s Clinical Research Center for Cancer, Tianjin, 300060, China
4.Key Laboratory of Cancer Prevention and Therapy, Tianjin, 300060, China
5.Key Laboratory of Basic and Translational Medicine on Head & Neck Cancer, Tianjin, 300060, China
6.National Key Laboratory of Druggability Evaluation and Systematic Translational Medicine, Tianjin, 300060, China
7.Department of Genetics, School of Basic Medical Sciences, Tianjin Medical University, Tianjin, 300070, China
作者:
Yu Wang,Qianqian Zhou
头颈部鳞状细胞癌(HNSCC)中 EGFR 过表达率达 80%-90%,但 EGFR 酪氨酸激酶抑制剂(TKI)临床疗效有限,耐药是主要障碍。现有研究表明,平行信号通路代偿激活可能介导耐药,但具体机制不明。IL-6/STAT3 通路调控多种肿瘤相关通路,EGFR-TKI 治疗后 STAT3 可能代偿激活,但该通路是否与 EGFR-TKI 耐药相关、具体机制如何尚未明确。本研究旨在探究 IL-6/STAT3 通路在 HNSCC 的 EGFR-TKI 耐药中的作用及机制,验证靶向该通路联合 EGFR-TKI 的治疗效果,为耐药 HNSCC 提供新的治疗策略。
采用 HNSCC 细胞系(UM1、Detroit 562、SCC25 等)及 NSCLC 细胞系(A549、PC9)作为对照;药物包括 EGFR-TKI(吉非替尼、厄洛替尼)、STAT3 抑制剂(Stattic)、JAK 抑制剂(Solcitinib、Fedratinib)、抗 IL-6 单抗(Siltuximab)及西妥昔单抗。通过 CCK-8、集落形成实验检测细胞活力;流式细胞术分析凋亡和细胞周期;WB、IF 检测蛋白表达与定位;ChIP、双荧光素酶报告基因验证 STAT3 与下游靶点结合;GFP-LC3、mRFP-GFP-LC3 质粒转染检测自噬 flux;构建细胞来源异种移植(CDX)和患者来源异种移植(PDX)小鼠模型,评估联合治疗的体内疗效。采用 CompuSyn 软件计算药物协同指数(CI),统计学分析采用 Student’s t 检验或 ANOVA,P<0.05 为差异有统计学意义。
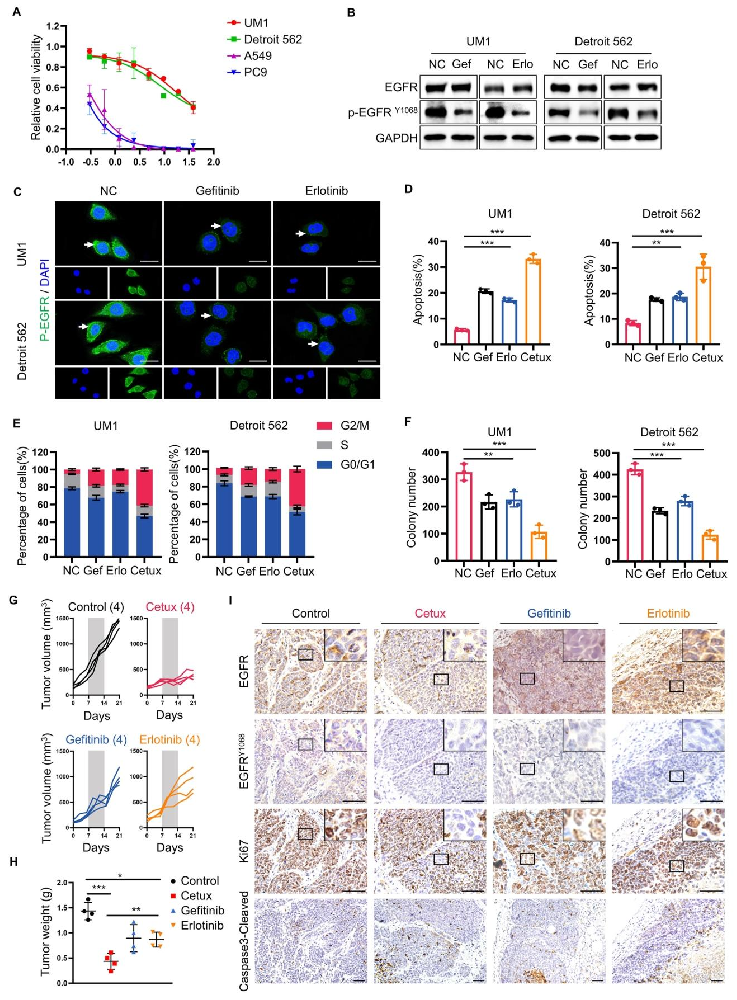
图 1:HNSCC 对 EGFR-TKI 治疗反应差
EGFR-TKI(吉非替尼、厄洛替尼)对 HNSCC 细胞的抑制效果显著弱于 NSCLC 细胞,且诱导凋亡、阻滞周期的能力不及西妥昔单抗(图 1D、E)。体内 CDX 模型中,EGFR-TKI 治疗组肿瘤体积、重量下降不明显,Ki-67 阳性细胞比例高,cleaved caspase-3 阳性细胞少,而西妥昔单抗疗效更优(图 1G、H、I),证实 HNSCC 对 EGFR-TKI 存在固有耐药。
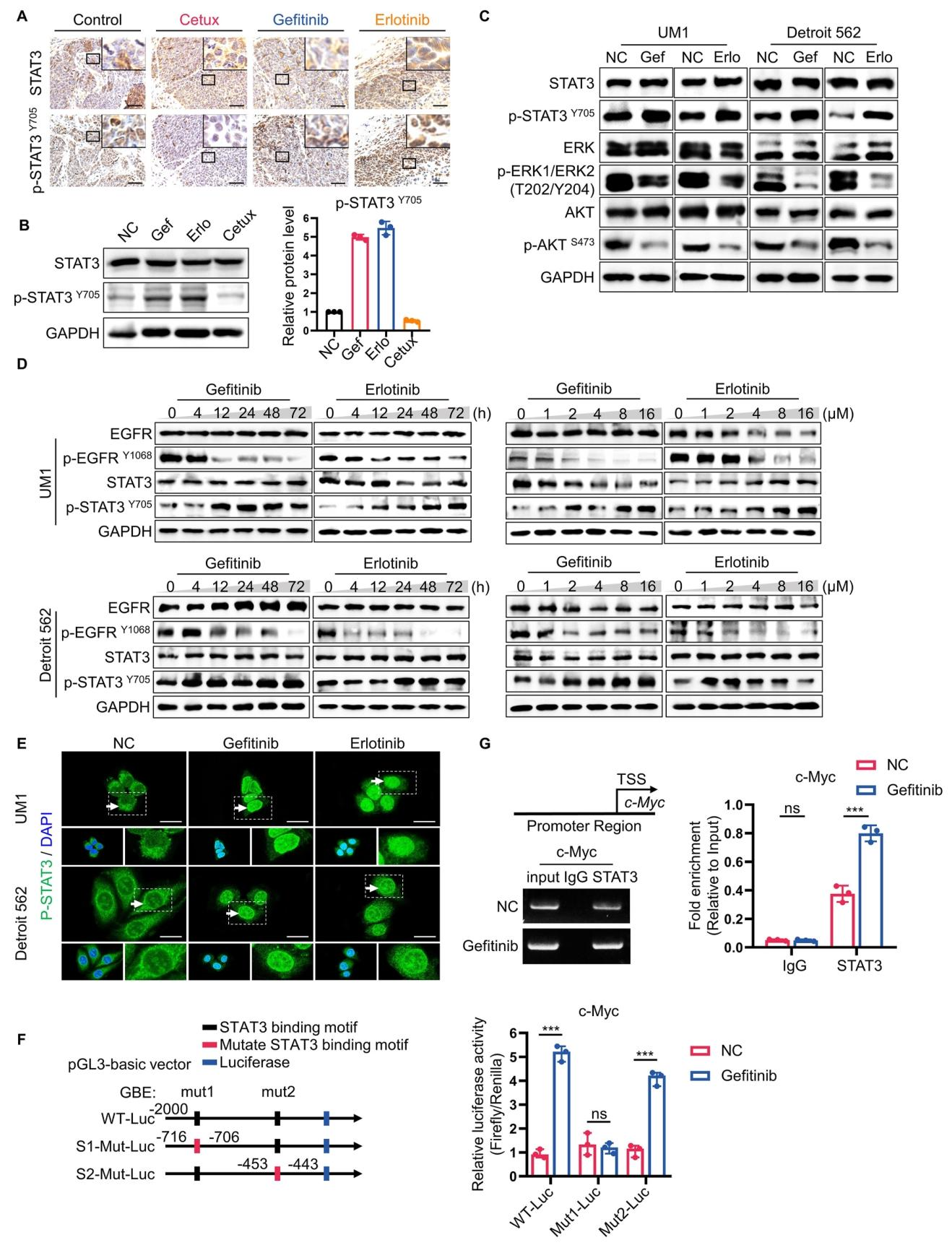
图 2:STAT3 在 EGFR-TKI 耐药 HNSCC 中异常激活
EGFR-TKI 处理后,HNSCC 细胞中 p-STAT3(Tyr705)表达呈时间和浓度依赖性升高,且在 TKI 治疗后的肿瘤组织中也显著上调(图 2A、B、C、D)。IF 显示 TKI 诱导 p-STAT3 核定位增加(图 2E);双荧光素酶报告基因和 ChIP 实验证实,STAT3 可直接结合 c-Myc 启动子并激活其转录(图 2F、G),表明 STAT3 激活是 EGFR-TKI 耐药的关键事件。
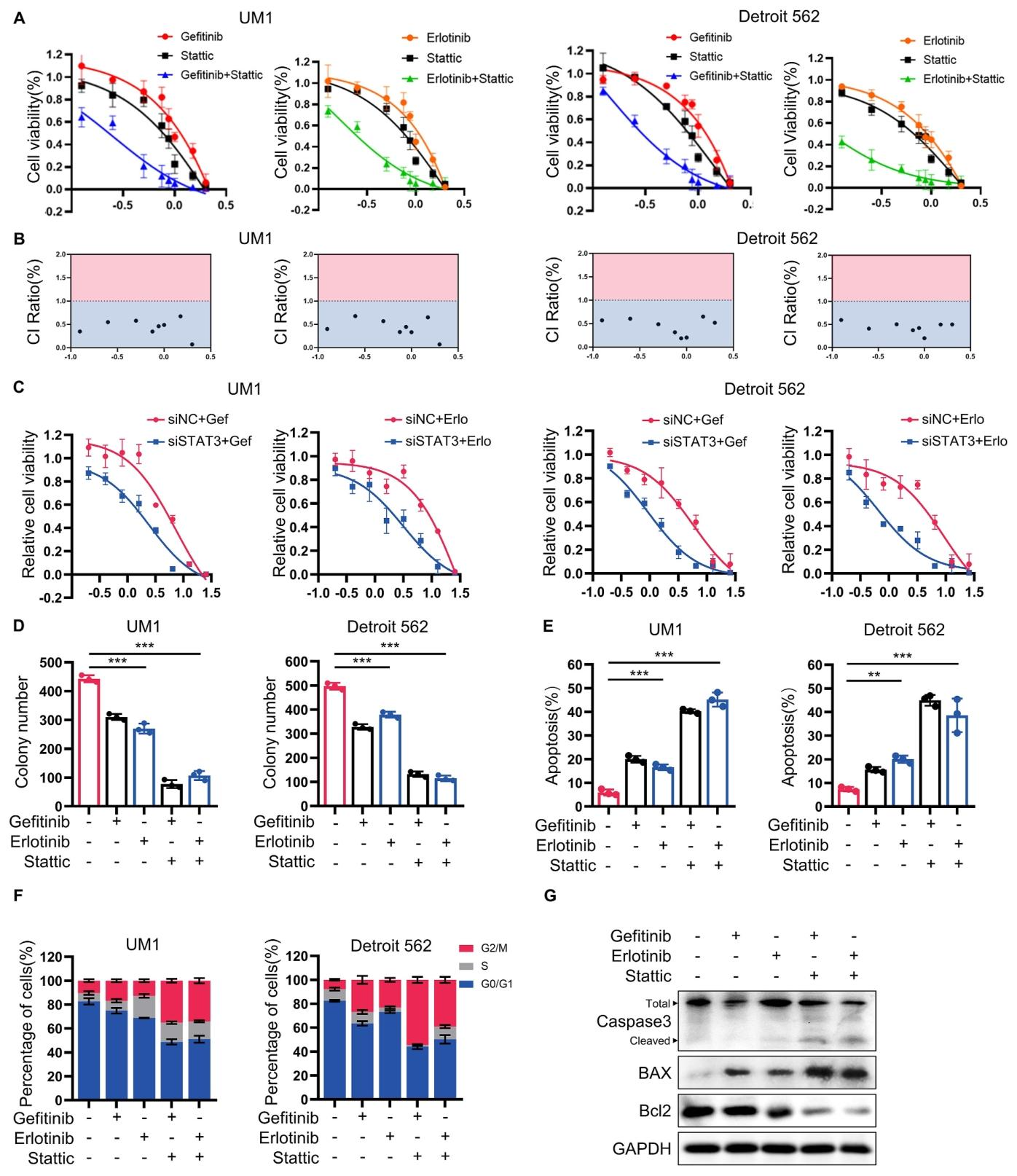
图 3:靶向 STAT3 可逆转 EGFR-TKI 耐药
STAT3 抑制剂 Stattic 与 EGFR-TKI 联合治疗的协同指数 CI<1,呈显著协同效应(图 3B);联合治疗显著抑制 HNSCC 细胞活力、集落形成,诱导凋亡和 G2/M 周期阻滞(图 3A、D、E、F),并上调 cleaved caspase-3、BAX 表达,下调 Bcl-2(图 3G)。siRNA 沉默 STAT3 也可增强 EGFR-TKI 的抑制效果(图 3C),证实 STAT3 是逆转耐药的关键靶点。
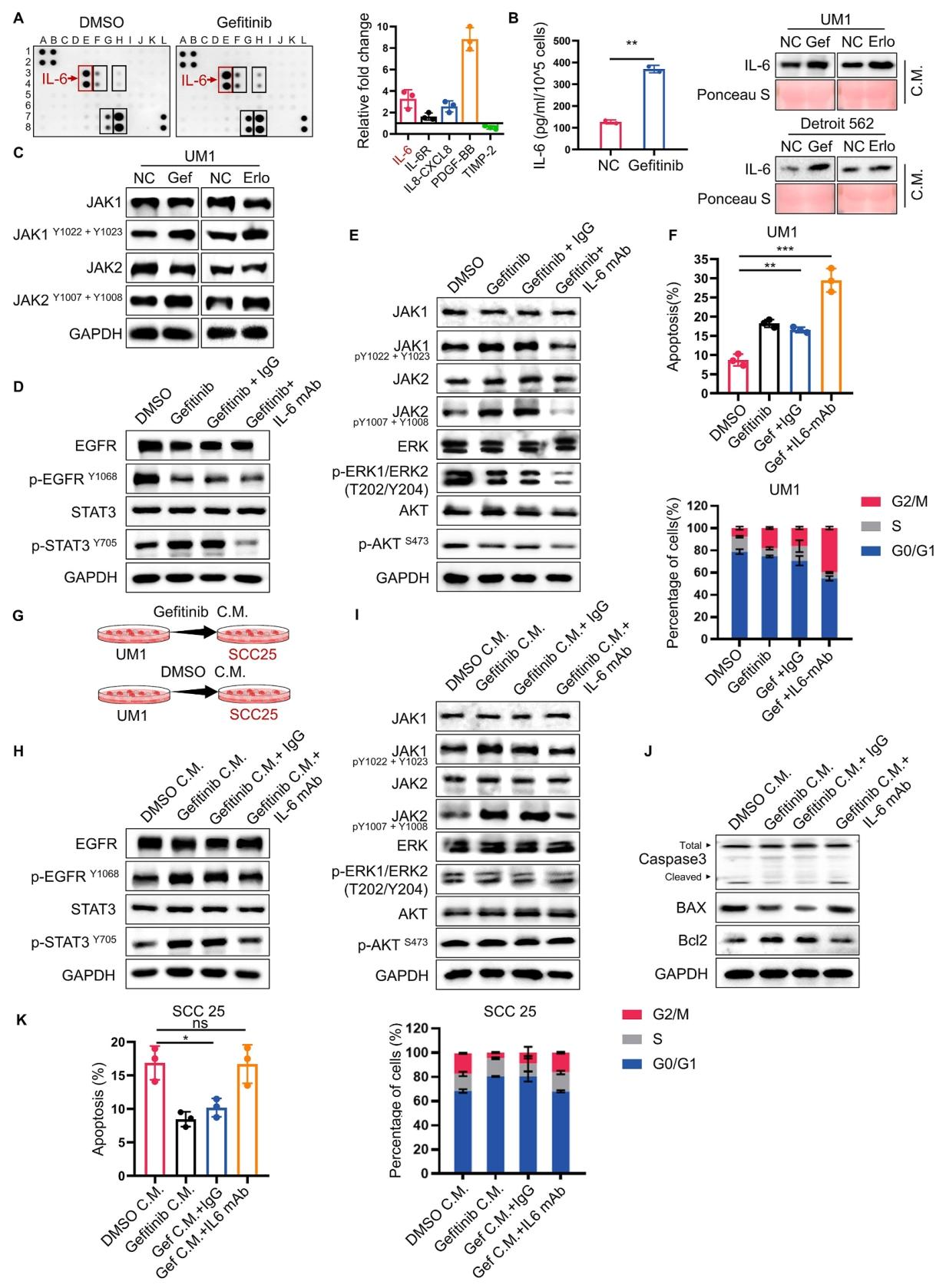
图 4:IL-6 分泌激活 JAK/STAT3 通路介导耐药
细胞因子抗体芯片显示,EGFR-TKI 治疗后 HNSCC 细胞分泌 IL-6 显著增加(图 4A、B);IL-6 通过激活 JAK1/2,进而促进 STAT3 磷酸化(图 4C、D)。中和 IL-6(Siltuximab)或抑制 JAK1/2 可显著减弱 STAT3 激活,增强 EGFR-TKI 诱导的凋亡和周期阻滞(图 4E、F),且耐药细胞的条件培养基可通过 IL-6 诱导敏感细胞耐药(图 4G-K),证实 IL-6/STAT3 轴是耐药的核心驱动通路。
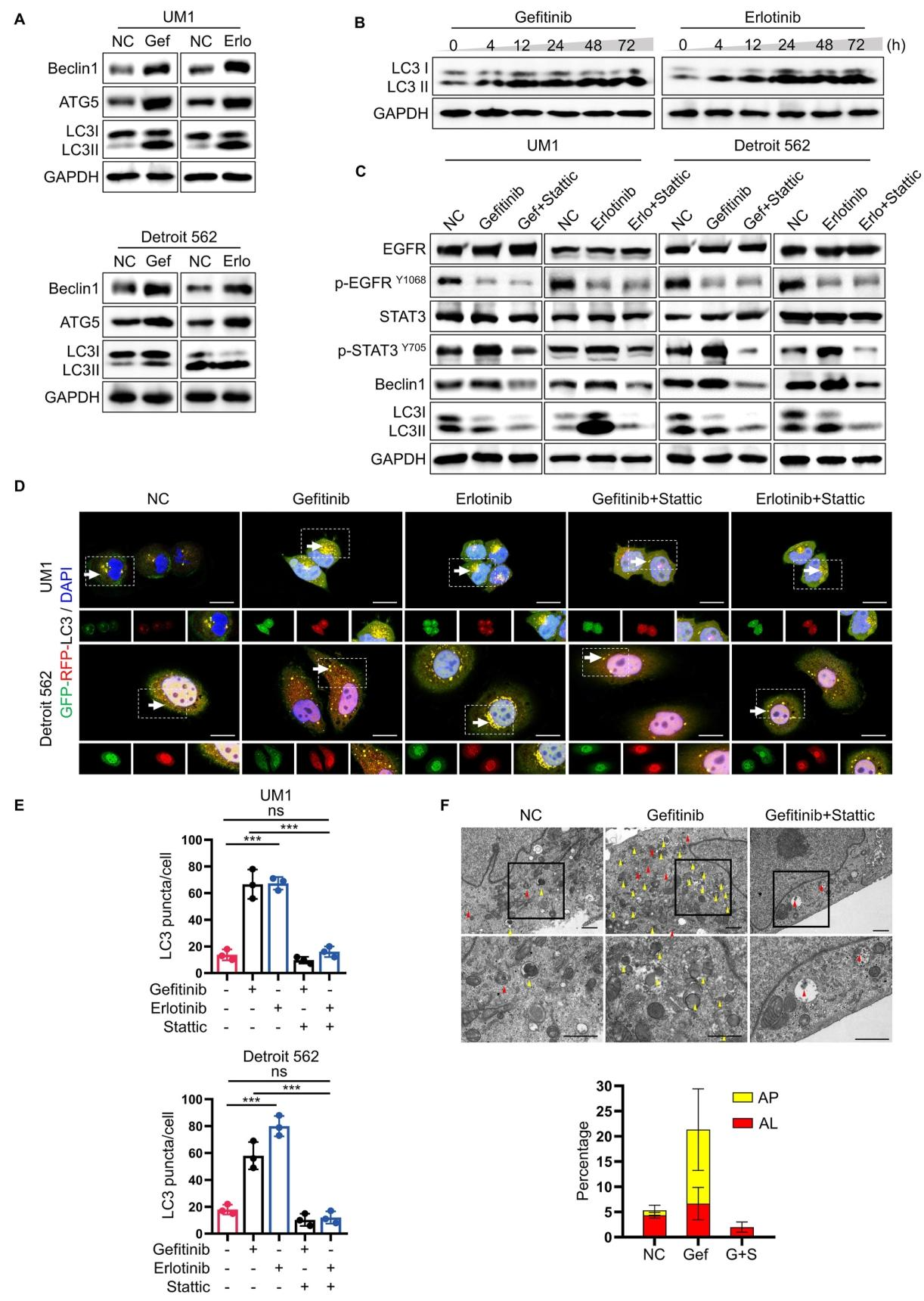
图 5:自噬参与 IL-6/STAT3 介导的耐药
EGFR-TKI 治疗后,HNSCC 细胞中 Beclin-1、ATG5 表达上调,LC3-II/LC3-I 比值升高,自噬 flux 激活(图 5A、B);自噬抑制剂 3-MA 可增强 TKI 敏感性。联合 STAT3 抑制剂与 EGFR-TKI 可显著抑制自噬相关蛋白表达,减少自噬体(黄色 puncta)和自噬溶酶体(红色 puncta)形成(图 5C、D、E),电镜进一步证实联合治疗可减少自噬体和自噬溶酶体数量(图 5F),表明 STAT3 通过激活自噬介导耐药。
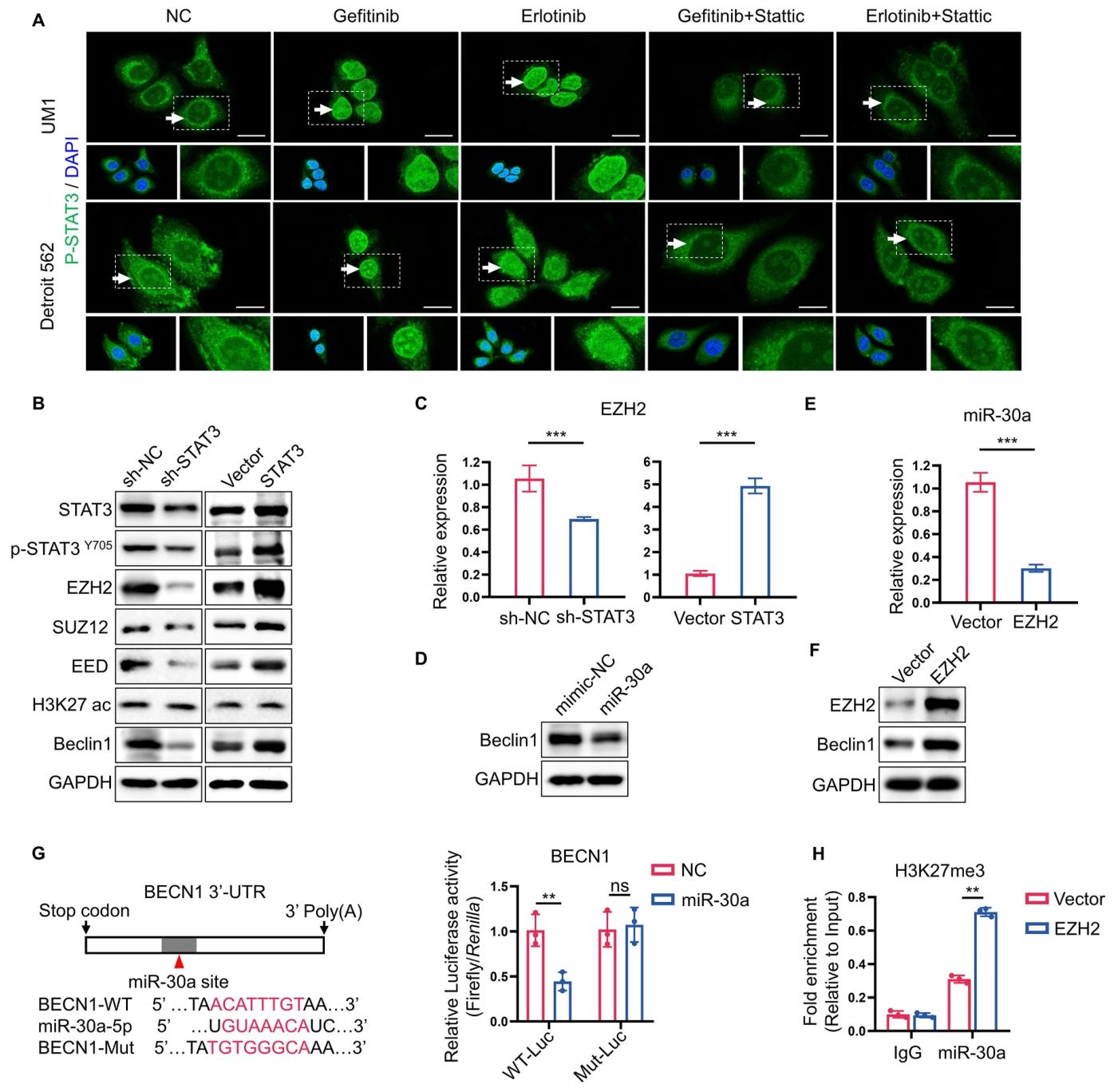
图 6:STAT3 通过 EZH2/miR-30a/Beclin-1 轴调控自噬
STAT3 激活可上调 EZH2 表达(图 6B、C);EZH2 通过 H3K27me3 修饰沉默 miR-30a(图 6E、H);miR-30a 可直接结合 Beclin-1 的 3’UTR 并抑制其表达(图 6G)。外源性过表达 miR-30a 可下调 Beclin-1,而 EZH2 过表达则上调 Beclin-1(图 6D、F),证实 STAT3→EZH2→miR-30a→Beclin-1 是调控自噬的关键分子轴。
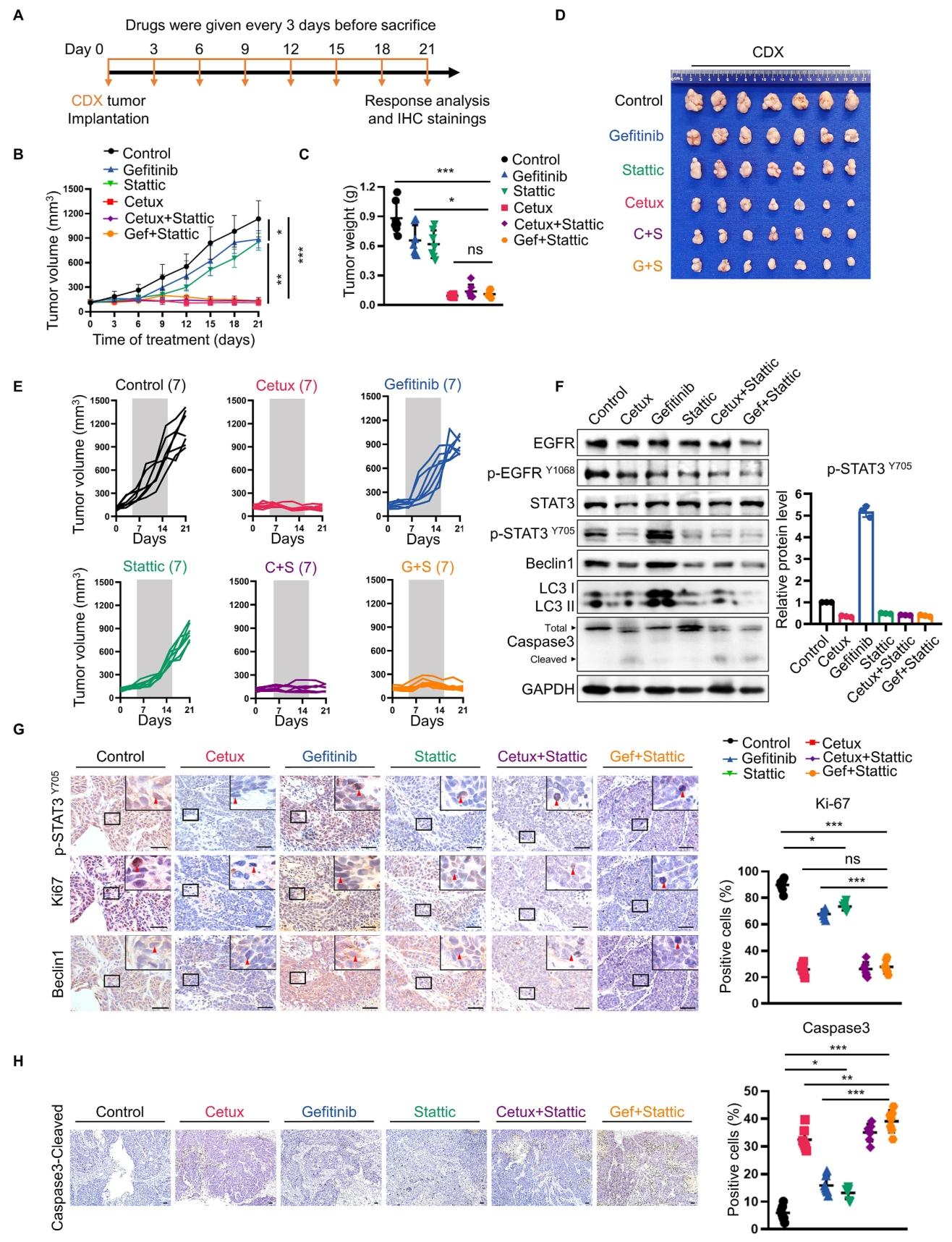
图 7:CDX 模型中联合治疗显著抑瘤
CDX 模型中,Stattic 与吉非替尼联合治疗组肿瘤体积和重量显著小于单药组(图 7B、C、D),且无明显体重下降(图 S9A)。联合治疗可显著降低 p-STAT3、Beclin-1、LC3-II 表达,增加 cleaved caspase-3 表达,减少 Ki-67 阳性细胞(图 7F、G、H),其疗效与西妥昔单抗相当,证实联合治疗的体内有效性。
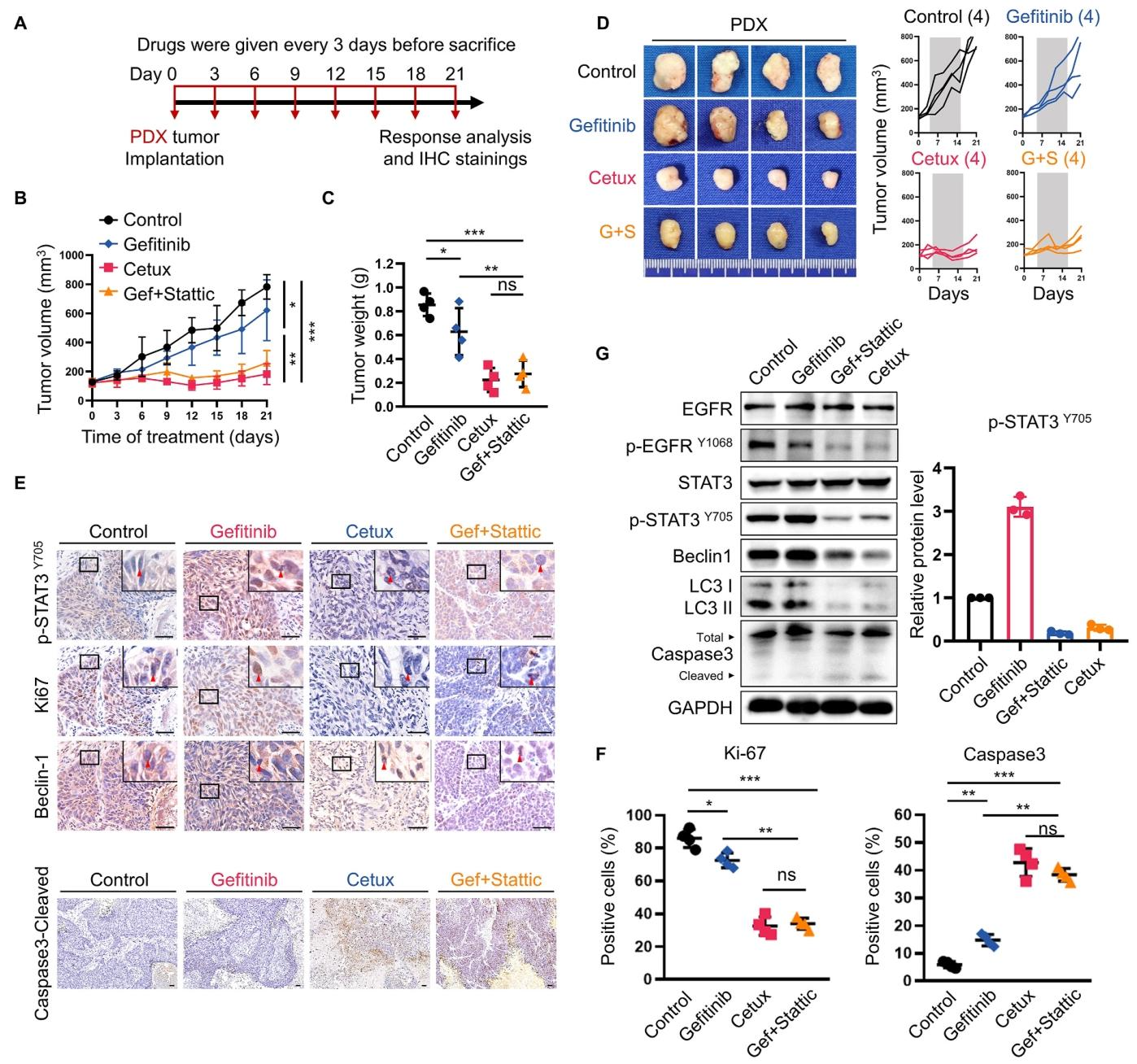
图 8:PDX 模型验证联合治疗的临床潜力
PDX 模型中,Stattic 与吉非替尼联合治疗同样显著抑制肿瘤生长(图 8B、C、D),降低 p-STAT3、Beclin-1 表达,减少 Ki-67 阳性细胞,增加凋亡相关蛋白表达(图 8E、F、G),与 CDX 模型结果一致,证实联合治疗对临床来源肿瘤的抑制效果,具有临床转化潜力。
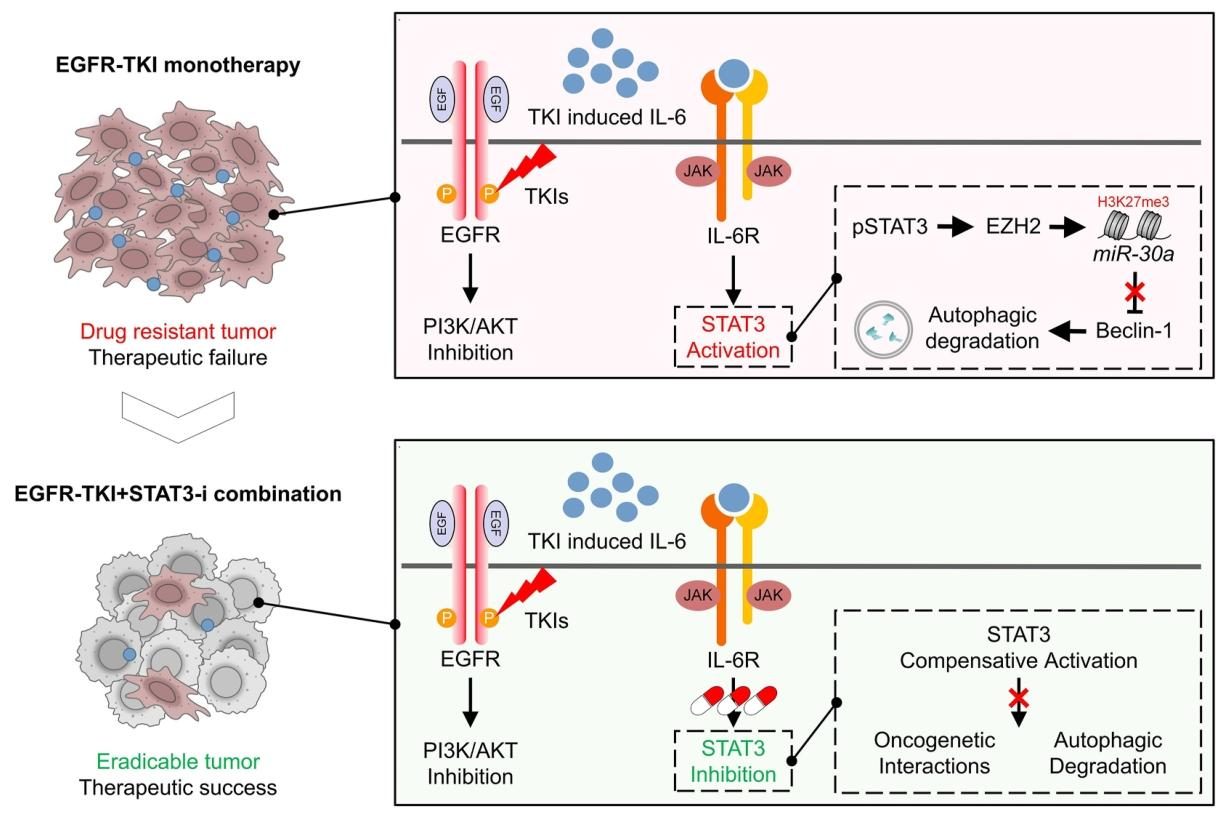
图 9:机制示意图
EGFR-TKI 治疗诱导 HNSCC 细胞分泌 IL-6,激活 JAK/STAT3 通路;p-STAT3 上调 EZH2,通过表观沉默 miR-30a 解除对 Beclin-1 的抑制,激活自噬 flux,促进肿瘤细胞存活并介导耐药;靶向 STAT3 联合 EGFR-TKI 可阻断该通路,抑制自噬,诱导肿瘤细胞凋亡,逆转耐药(图 9)。
本研究首次明确 IL-6/STAT3 通路通过调控 Beclin-1 依赖的自噬介导 HNSCC 的 EGFR-TKI 耐药。核心机制为:EGFR-TKI 治疗后,HNSCC 细胞代偿性分泌 IL-6,激活 JAK/STAT3 通路,STAT3 上调 EZH2 并表观沉默 miR-30a,进而上调 Beclin-1 表达并激活自噬,促进肿瘤细胞存活;靶向 STAT3(Stattic)或中和 IL-6 可阻断该通路,抑制自噬,与 EGFR-TKI 产生协同抑瘤效应,在 CDX 和 PDX 模型中均显著逆转耐药。该研究揭示了 HNSCC 的 EGFR-TKI 耐药的关键机制,提出 IL-6/STAT3 / 自噬通路作为治疗靶点,为临床耐药 HNSCC 提供了可转化的联合治疗策略,STAT3 也可作为预测耐药的生物标志物。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:MiR-140-5p 通过靶向 TLR4 守护巨噬细胞