常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-22 17:28:22 细胞资源库平台 访问量:154
儿童炎症性肠病(pediatric IBD)是一种以肠道慢性炎症为特征的疾病,全球发病率持续上升,但病因及 optimal 治疗策略仍不明确。与成人 IBD 相比,儿童 IBD 表型更独特,更常与罕见单基因突变相关,这些突变可导致肠上皮屏障功能异常或黏膜免疫细胞功能缺陷。目前已发现超过 100 个基因与早发性 IBD 相关,但多数基因在肠上皮中的作用及突变致病机制仍不清楚。
患者来源的肠道上皮类器官(IEOs)作为模拟肠道上皮结构和功能的 3D 模型,能克服动物模型和永生细胞系的局限性,为研究 IBD 的上皮缺陷提供了生理相关性更高的平台。本研究通过建立大规模 pediatric IBD 患者的 IEOs,结合转录组分析,探究上皮表型与遗传驱动因素的关联,为个性化治疗提供靶点。
来自荷兰乌得勒支大学医学中心、美国西奈山伊坎医学院的团队在《bioRxiv》(2025 年预印本)发表了题为A collection of patient-derived intestinal organoid lines reveals epithelial phenotypes associated with genetic drivers of pediatric inflammatory bowel disease的研究。
类器官构建:从 94 名 pediatric IBD 患者(含单基因突变患者,如 TTC7A、STXBP2、LRBA 等)和 46 名非 IBD 对照的肠道活检样本中建立 140 个 IEOs 系,成功率 IBD 为 74%、对照为 66%;
实验处理:对 58 个 IEOs 系(38 名患者、20 名对照)进行细菌裂解物刺激(0h、6h、72h),通过 RNA-seq 分析转录组变化;
数据分析:采用差异表达基因(DEGs)分析、加权基因共表达网络分析(WGCNA)鉴定与疾病及基因突变相关的基因模块。
IEOs 长期生长能力下降:尽管初始生成率较高,但冻存复苏后仅 44% 的 IBD 类器官和 45% 的对照类器官能持续扩增,IBD 类器官完全无法生长的比例(38%)高于对照(23%);
细菌刺激诱导炎症反应:无论疾病状态或基因突变,IEOs 暴露于细菌抗原后均上调促炎基因(如 CXCL8、NFKB2)及通路(IL-17、NF-κB),模拟 IBD 炎症状态;差异基因表达:IBD 类器官在刺激后显著上调 SERPINA1(编码 α1 - 抗胰蛋白酶,具有抗炎作用)和 LIFR(白血病抑制因子受体,参与免疫调节),这两个基因与肠上皮先天免疫反应相关;
共表达网络特征:WGCNA 未发现 IBD 整体的一致转录特征,但特定基因型(TTC7A、STXBP2、LRBA)与对照存在差异。其中,STXBP2 和 LRBA 突变体共享 IL-1 信号通路和 SLC30 介导的锌转运通路的上调,提示共同致病机制;TTC7A 突变体则与 HOX 基因模块表达降低相关,HOX 基因参与肠道发育模式形成。
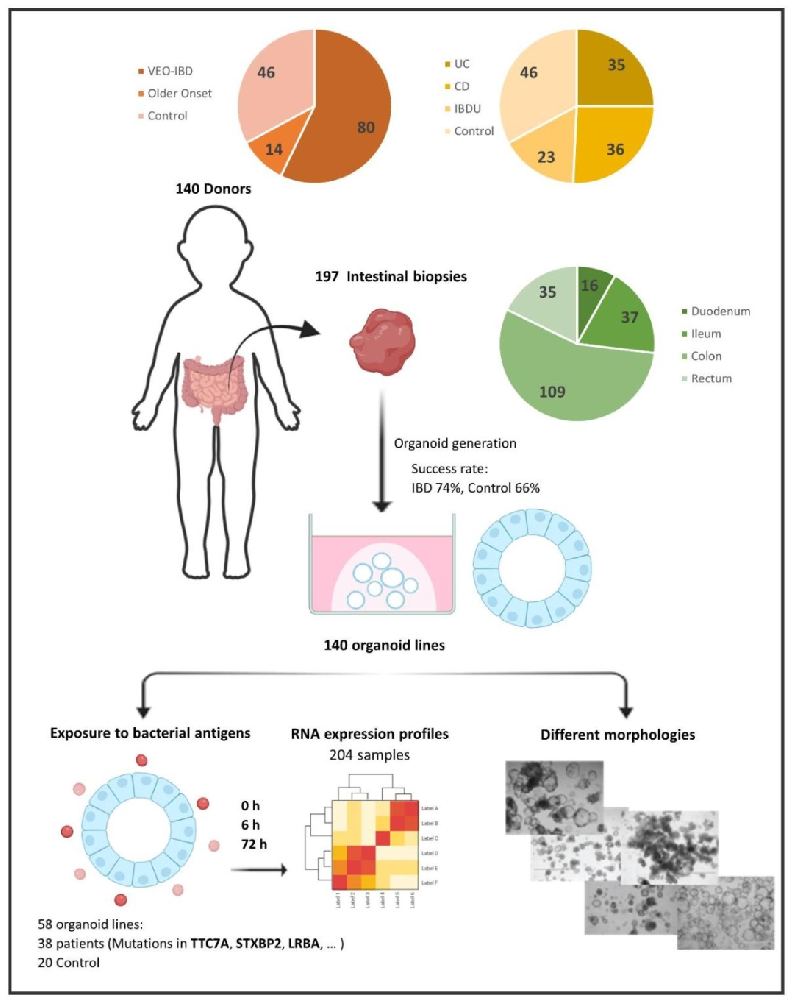
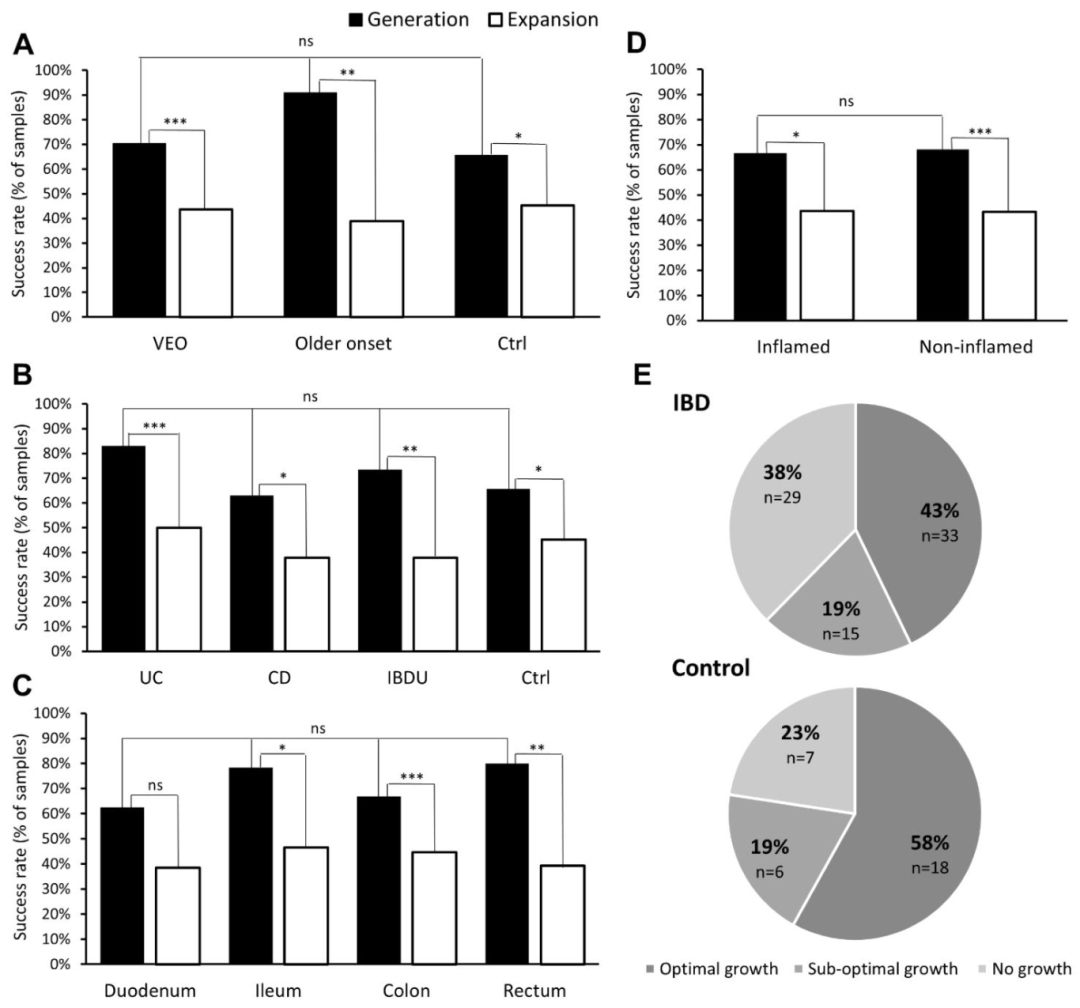
图 1:肠道类器官的生成与长期扩增能力
该图展示不同组别类器官的生成率和扩增率。(A-D)柱状图显示,IBD(包括 VEO-IBD 和晚发型)与对照的初始生成率无显著差异(IBD 74% vs 对照 66%),且不受疾病亚型(UC、CD、IBDU)、肠道位置(十二指肠、回肠、结肠、直肠)或活检炎症状态影响;但冻存复苏后,所有组别的持续扩增率均下降(VEO-IBD 44%、晚发型 IBD 39%、对照 45%),IBD 类器官完全无法生长的比例(38%)高于对照(23%)。(E)饼图显示 IBD 类器官的最优生长比例(43%)低于对照(58%),证实 IBD 上皮细胞的长期增殖能力受损。
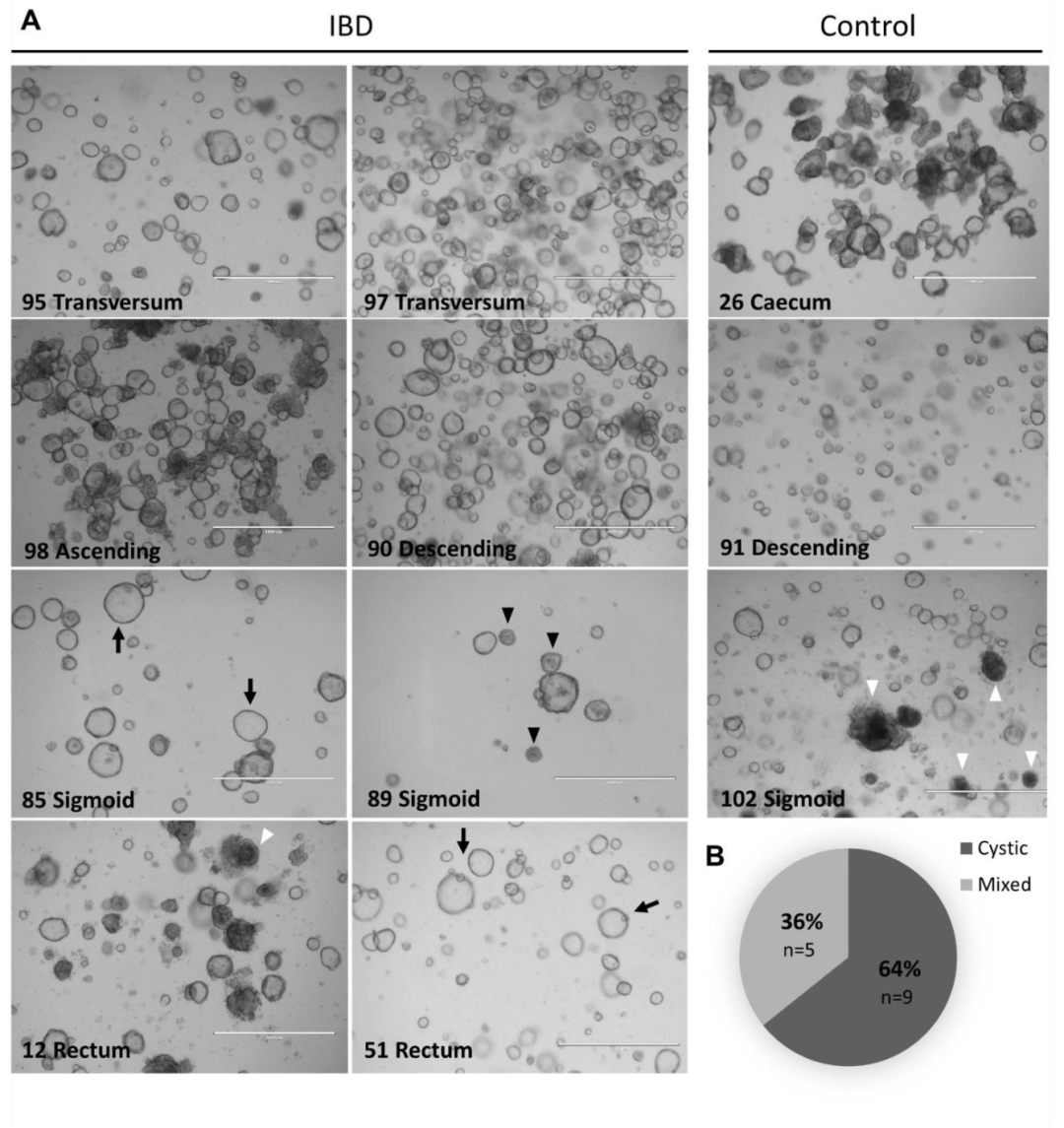
图 2:IBD 与对照类器官的形态差异
该图呈现不同供体类器官的形态学特征。(A)明场图像显示,即使来自同一肠道区域(如横结肠、降结肠),不同供体的类器官在大小、融合度和结构上存在显著差异:部分 IBD 类器官呈典型囊状结构,部分则表现为塌陷或聚集状;(B)统计显示 64% 的 IBD 类器官为单纯囊状形态,36% 为囊状与非囊状的混合形态,提示供体特异性的形态异质性,且与疾病状态无直接关联。
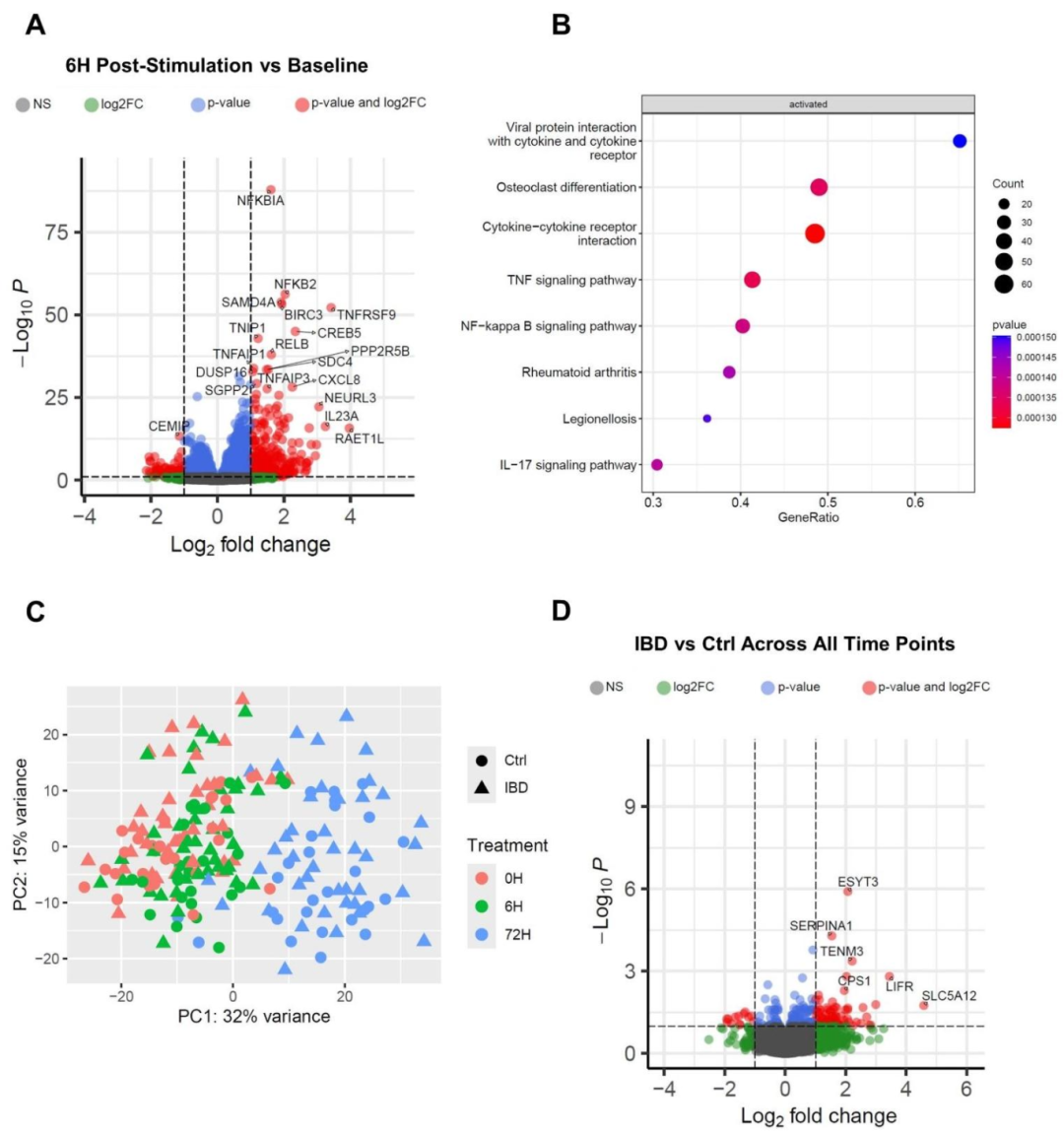
图 3:细菌刺激诱导的炎症反应
该图通过转录组分析展示类器官对细菌抗原的应答。(A)火山图显示,刺激 6 小时后,IBD 和对照类器官均显著上调 CXCL8、NFKB2 等促炎基因;(B)通路富集分析证实 IL-17、NF-κB、TNF 等炎症通路激活;(C)PCA 分析显示,样本聚类主要由刺激时间(0h、6h、72h)驱动,而非疾病状态;(D)火山图显示,IBD 类器官在各时间点均上调 SERPINA1、LIFR 等基因,提示疾病特异性的免疫应答特征。
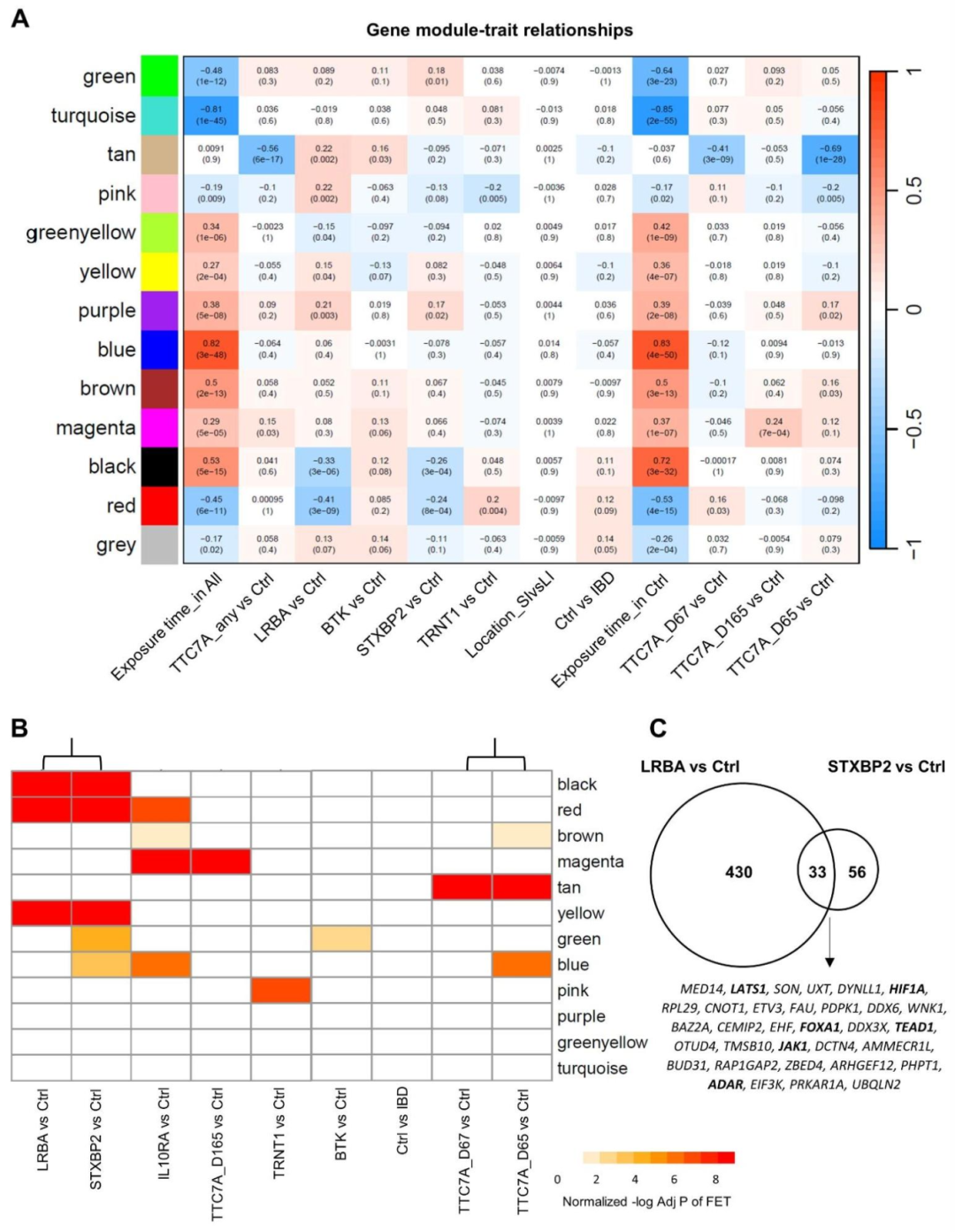
图 4:基因共表达网络与基因型关联
该图通过 WGCNA 分析基因模块与表型的关联。(A)热图显示,细菌刺激时间是模块表达的主要驱动因素(如紫色模块富集促炎基因,6 小时表达达峰),而疾病状态(IBD vs 对照)无显著关联;但特定基因型(如 TTC7A、STXBP2、LRBA)与模块表达相关(如 TTC7A 突变体与 tan 模块负相关,该模块含 HOX 基因)。(B)热图显示不同基因型的差异基因在特定模块中富集,如 STXBP2 和 LRBA 突变体均富集于黄色模块(含 IL-1 信号和锌转运相关基因)。(C)韦恩图显示 STXBP2 和 LRBA 突变体的差异基因存在重叠(如 HIF1A、JAK1),提示共同通路参与致病。
本研究建立了目前最大的 pediatric IBD 患者肠道类器官库,证实 IEOs 可有效模拟细菌刺激诱导的炎症反应,且能保留患者特异性上皮表型。关键发现包括:IBD 类器官的长期增殖能力下降;SERPINA1 和 LIFR 在炎症应答中上调,可能成为治疗靶点;特定单基因突变(TTC7A、STXBP2、LRBA)与独特的转录模块相关,其中 STXBP2 和 LRBA 通过 IL-1 信号和锌转运通路参与致病。该研究为解析儿童 IBD 的遗传驱动机制提供了新工具,支持基于基因型的个性化治疗开发。局限性包括样本量有限、未排除表观遗传 “记忆” 的影响,未来需结合基因编辑验证突变的直接作用。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:上皮细胞分泌的细胞外基质 niche 驱动肠道类器官形成研究