常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-14 09:00:00 细胞资源库平台 访问量:217
原发性硬化性胆管炎(PSC)是一种慢性肝病,以肝内胆管进行性炎症和纤维化为特征,典型表现为 “洋葱皮样” 胆管周围纤维化,终末期需肝移植,缺乏有效治疗手段。其发病与免疫失调、遗传因素及胆管病理密切相关,其中辅助性 T 细胞 17(Th17)及其分泌的 IL-17A 被认为是驱动纤维化的关键因素 ——IL-17A 可刺激胆管上皮分泌趋化因子(如 CCL20),招募更多 Th17 细胞,形成促纤维化正反馈。间充质干细胞来源的外泌体(EVMSC)具有免疫调节和抗纤维化潜力,但其在 PSC 中的具体机制尚不明确。本研究通过人肝多谱系类器官(Mulorgs)和 Mdr2-/- 小鼠模型,探究 EVMSC 通过调控 Th17 分化减轻胆管周围纤维化的作用及机制。
来自浙江大学医学院附属第一医院的团队在《Journal of Nanobiotechnology》期刊发表了题为Mesenchymal stem cell-derived extracellular vesicles attenuate periductal fibrosis by inhibiting Th17 differentiation in human liver multilineage organoids and Mdr2−/− mice的研究。
建立含胆管细胞、肝细胞和肝星状细胞(HSCs)的人肝多谱系类器官(Mulorgs),诱导为 IL-17A 驱动的纤维化类器官(FibHOs);
采用 Mdr2-/- 小鼠(PSC 模型)验证体内疗效。
EVMSC 富集 hsa-miR-7977,靶向 NFKBIZ(编码 IκBζ),抑制其翻译,减少 IL-17A 及下游 Th17 分化、IL-17 信号通路相关基因表达;
抑制 Th17 细胞分化和迁移至胆管周围纤维化区域,降低肝内 IL-17A 水平,减少 HSCs 激活和胶原沉积。
EVMSC 在 Mdr2-/- 小鼠中富集于肝纤维化区域,降低肝重 / 体重比、血清转氨酶及纤维化相关基因(Col3a1、Acta2 等)表达;
显著减少小鼠肝内 IL-17A + 细胞数量,体外抑制 CD4+T 细胞向 Th17 分化(抑制率 25.07%);
FibHOs 中,EVMSC 降低 IL-8、CCL20 等炎症因子及 COL1A1 等纤维化标志物表达;
miR-7977 富集的 EVMSC(EVhigh)可改善 Mdr2-/- 小鼠胆管周围纤维化,减少纤维化区域 IL-17A + 细胞比例(降低 50.42%)。
图 1:MSC 来源的 EVs 显著改善 Mdr2-/- 小鼠肝脏状况
内容:(A)EVMSC 表征:纳米颗粒追踪分析(NTA)显示其粒径分布(约 125.7nm)和浓度;冷冻电镜证实膜完整性;Western blot 检测到 TSG101、Hsp70、CD63 等 EV 标志物。(B)处理示意图:8 周龄 FVB.Mdr2 小鼠每周尾静脉注射 EVMSC,12 周龄分析,Mdr2+/+ 小鼠为对照。(C)EVMSC 生物分布:DiR 标记的 EVMSC(红色)在 Mdr2-/- 小鼠肝内富集,尤其在胆管周围和纤维化区域;共定位分析显示 EVMSC 与 Alb + 肝细胞、CK7 + 胆管细胞、α-SMA+HSCs 及 CD45 + 免疫细胞共定位(DAPI 染核)。(D)肝重 / 体重比:12 周龄 Mdr2-/-+EV 组显著低于 Mdr2-/- 组(n=5,P<0.05)。(E)肝组织 P21(细胞衰老标志物)表达:Mdr2-/-+EV 组显著降低(n=3)。(F)HE 染色显示 Mdr2-/-+EV 组汇管区纤维化改善。(G)SA-β-gal(衰老)和 CK19(胆管细胞)染色:Mdr2-/-+EV 组胆管衰老减轻。(H)血清转氨酶(AST、ALT、ALP):Mdr2-/-+EV 组显著降低(n=5,P<0.05)。(I)Western blot 显示 Mdr2-/-+EV 组 cleaved-caspase-3/caspase-3、cleaved-caspase-9/caspase-9 比值降低。(J)肝组织及血清中 Ccl20、Ccl2 等细胞因子水平:Mdr2-/-+EV 组显著降低(n=5,P<0.05)。
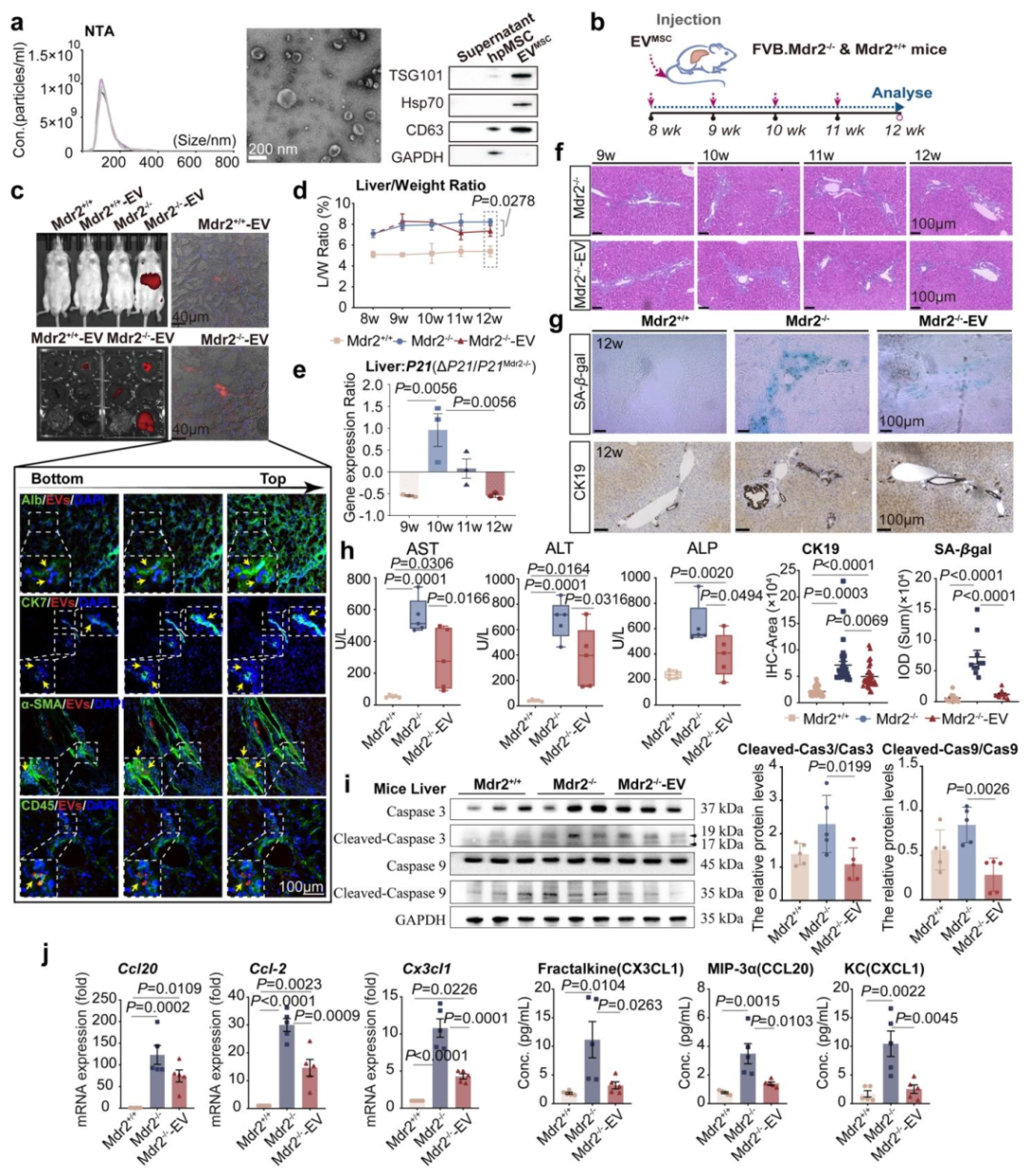
图 2:EVMSC 减轻 Mdr2-/- 小鼠肝纤维化并抑制 Th17 分化
内容:(A)qRT-PCR 显示 Mdr2-/-+EV 组肝组织纤维化相关基因(Acta2、Col3a1 等)及血清 TGF-β1 水平显著降低(n=5,P<0.05)。(B)天狼星红染色(胶原)、α-SMA 免疫荧光(HSCs 激活)、Desmin 免疫组化(HSCs 标志物):Mdr2-/-+EV 组阳性区域减少。(C)Image-Pro Plus 定量分析上述染色结果(n=15,P<0.05)。(D)KEGG 富集分析显示 Mdr2-/-+EV 组下调通路中 Th17 分化通路显著富集。(E)Th17 分化通路基因表达趋势:Mdr2-/- 组上调,Mdr2-/-+EV 组下调。(F)12 个 Th17 分化相关基因在 Mdr2-/- 组上调、Mdr2-/-+EV 组下调。(G)qRT-PCR 显示 Mdr2-/-+EV 组肝内免疫细胞 Il-17a mRNA 降低(n=10,P<0.05)。(H)IL-17A 免疫组化:Mdr2-/-+EV 组胆管周围 IL-17A + 细胞(红箭头)减少。(I)流式细胞术显示 EVMSC 体外抑制 CD4+IL17A+ T 细胞比例(2-15ng/mL 浓度下抑制率 16.5%-25.03%,n=9)。(J)qRT-PCR 显示 EVMSC 降低 Th17 细胞 IL-17A 表达(抑制率 15.56%,n=9,P<0.05)。
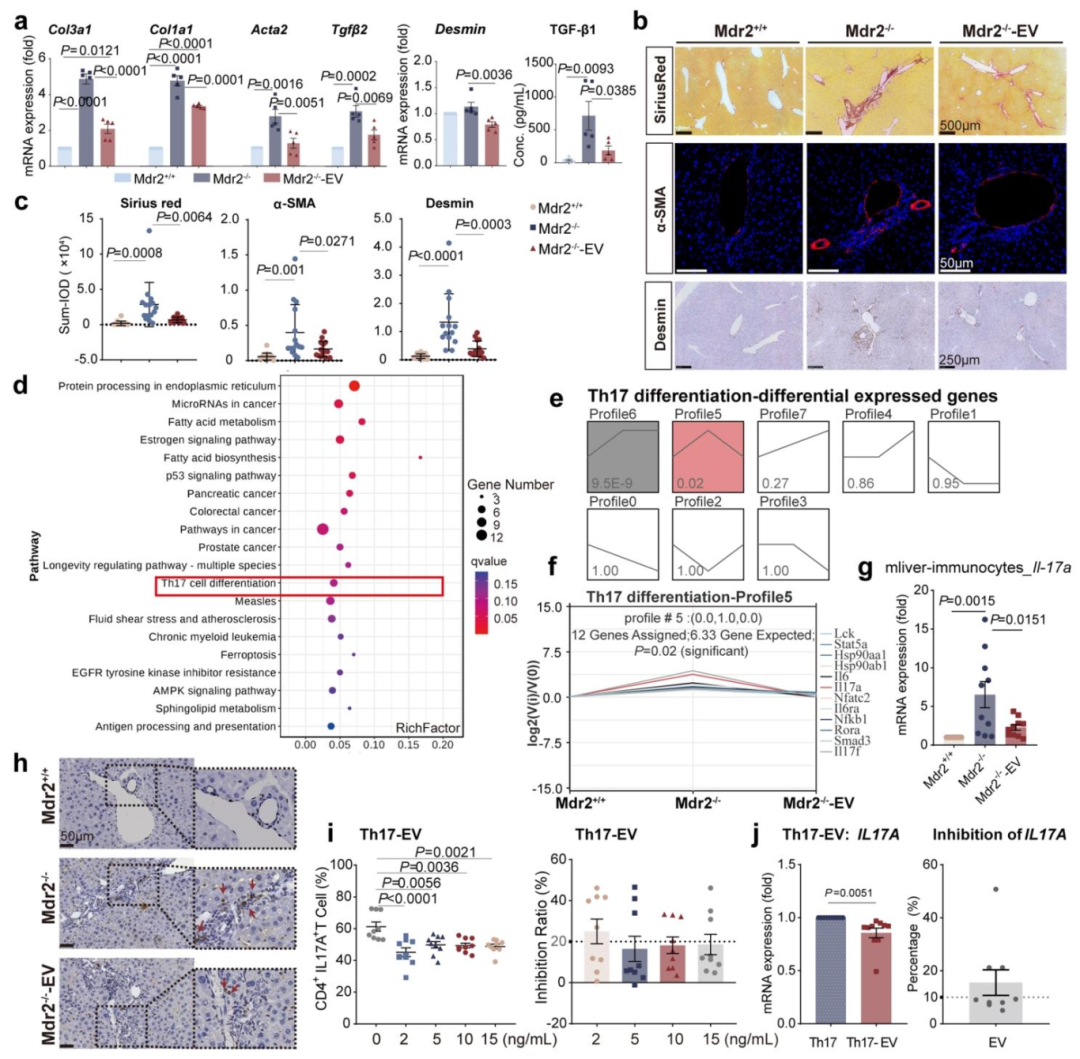
图 3:EVMSC 逆转 IL-17A 诱导的纤维化类器官(FibHOs)
内容:(A)Mulorgs 及 FibHOs 建立示意图:胆管细胞类器官(Chorgs)、肝细胞类器官(Heporgs)与 HSCs 共培养形成 Mulorgs,经 IL-17A 处理为 FibHOs。(B)免疫荧光显示 Mulorgs 中 Desmin+(红)和 GFAP+(绿)HSCs 分布(Z-stack 扫描)。(C)免疫荧光显示 Mulorgs 中 CK18 + 肝细胞(绿)、CK19 + 胆管细胞(红)、GFAP+HSCs(品红)的 3D 和 2D 分布(DAPI 染核)。(D)qRT-PCR 显示 IL-17A(250-400ng/mL)剂量依赖性上调 FibHOs 中 COL1A1、TGFB1 等纤维化基因(n=5,P<0.05)。(E)ELISA 及 LEGENDplex 检测显示 IL-17A 上调 FibHOs 分泌 IL-8、IL-6、CCL20 等(n=3-5,P<0.05)。(F)qRT-PCR 显示 EVMSC 下调 FibHOs 中 COL1A1 等纤维化基因(n=3,P<0.05)。(G)EVMSC 降低 FibHOs 分泌 IL-8、CCL20 等(n=3,P<0.05)。(H)3D 免疫荧光显示 EVMSC 处理后 FibHOs 中 α-SMA(绿)和胶原 I+III(红)减少(Dil 染膜,DAPI 染核)。(I)Masson 染色显示 EVMSC 处理组 FibHOs 胶原(蓝)减少。
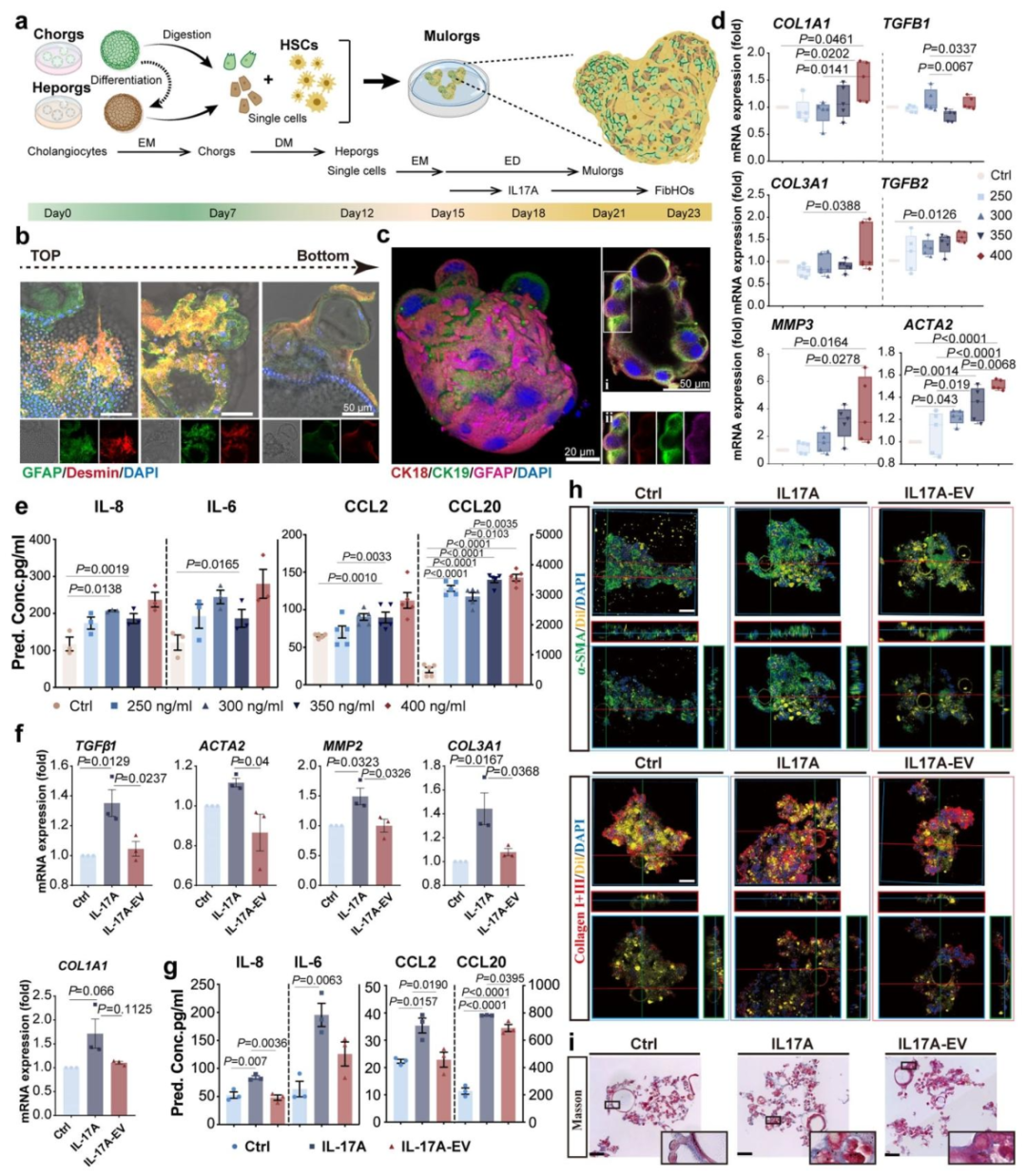
图 4:EVMSC 来源的 miR-7977 靶向 NFKBIZ 抑制 Th17 分化
内容:(A)GO 富集分析显示 Mdr2-/- 与 Mdr2-/-+EV 组肝组织差异基因富集于转录调控相关功能。(B)EVMSC 中 miRNA 靶基因 GO 富集于 “RNA 诱导沉默复合体” 等通路。(C)EVMSC 中高表达的 6 种 miRNA(如 hsa-miR-7977)。(D)TargetScan 分析显示 hsa-miR-7977 靶向 Th17 分化相关转录因子数量最多。(E)hsa-miR-7977 与 NFKBIZ 3'UTR 结合序列示意图。(F)荧光素酶报告实验证实 hsa-miR-7977 与野生型(WT)NFKBIZ 3'UTR 结合,突变型(MUT)无结合(n=3,P<0.05)。
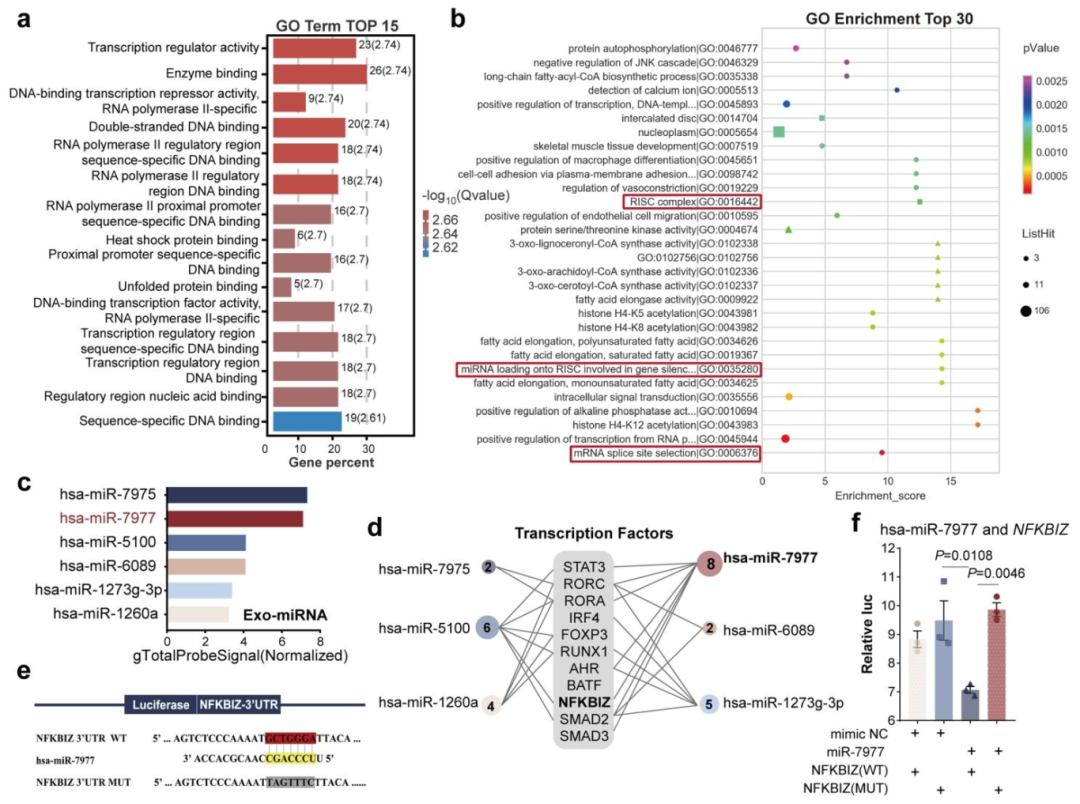
图 5:EV 来源的 miR-7977 通过减少 IκBζ 抑制 Th17 分化及 IL-17A 表达
内容:(A)流式细胞术显示 miR-7977 模拟物减少 CD4+IL-17A+ T 细胞比例(平均抑制率 31.12%,n=5,P<0.05)。(B)qRT-PCR 显示 EVMSC 或 miR-7977 模拟物下调 Th17 细胞中 NFKBIZ 表达(抑制率分别为 26.58%、30.32%,n=5,P<0.05)。(C)Western blot 显示 EVMSC 或 miR-7977 模拟物降低 IκBζ 蛋白水平(抑制率分别为 37.75%、52.09%),升高 p-eIF2α/eIF2α 比值(n=5)。(D)qRT-PCR 显示 miR-7977 模拟物下调 IL-17A 表达(抑制率 50.66%,n=5,P<0.05)。(E)KEGG 分析显示 IκBζ 靶基因富集于 IL-17 信号、Th17 分化等通路。(F)ChIP-seq 显示 Th17miR 组(miR-7977 处理)IL-17A 基因峰减少。
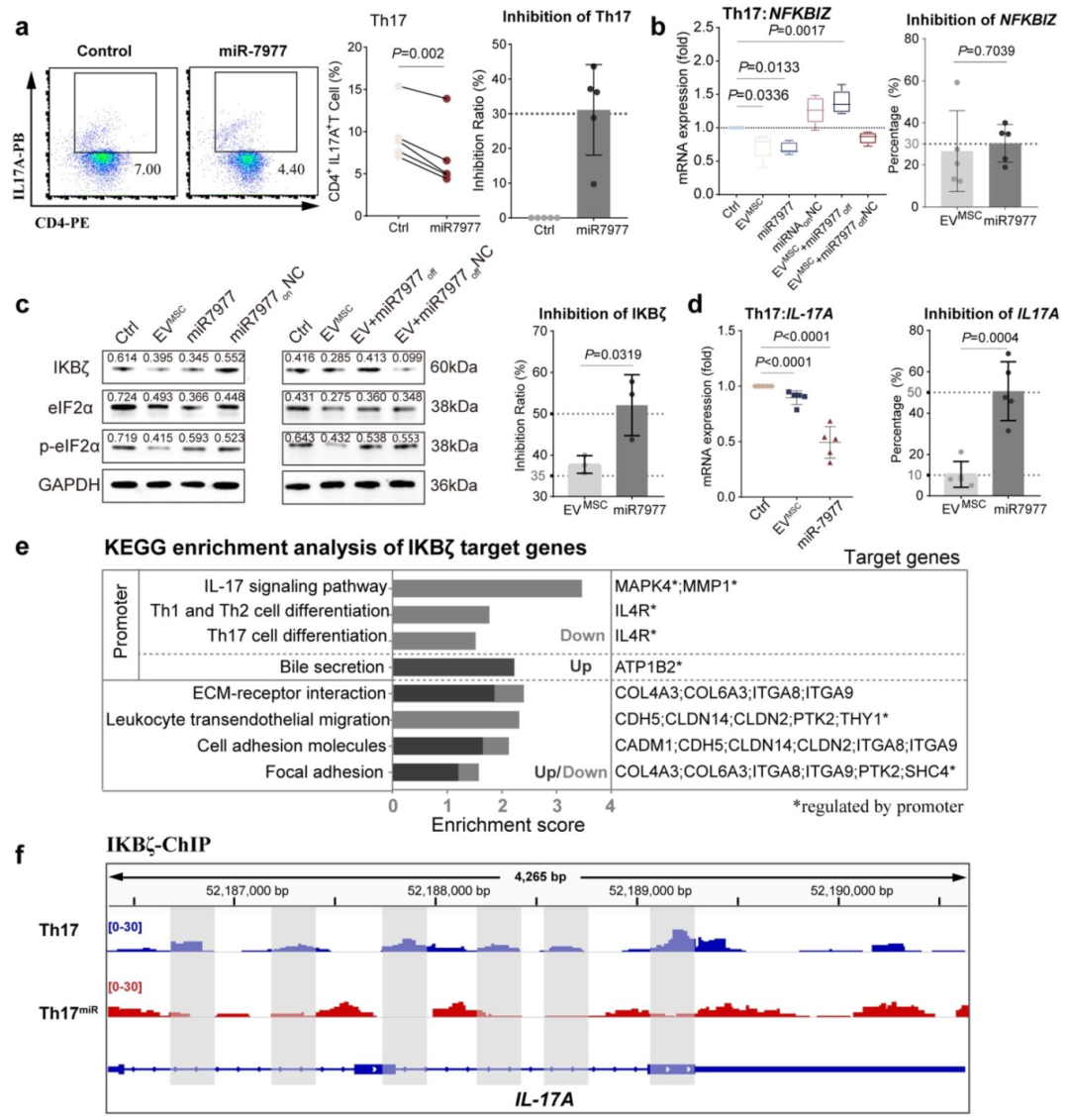
图 6:EVhigh 有效改善 Mdr2-/- 小鼠胆管周围纤维化微环境
内容:(A)EVhigh(高 miR-7977)和 EVlow(低 miR-7977)的制备与表征:qRT-PCR 证实 miR-7977 水平,NTA 显示粒径和浓度(n=3-5,P<0.05)。(B)流式细胞术显示 EVhigh 抑制 Th17 分化(抑制率 25.07%,n=5,P<0.05)。(C)天狼星红和 Masson 染色显示 Mdr2-/-+EVhigh 组胶原沉积显著减少(n=5,P<0.05)。(D-E)CK19(胆管细胞)和 α-SMA(HSCs)免疫组化:Mdr2-/-+EVhigh 组阳性区域减少。(F)Image-Pro Plus 定量上述染色结果(n=30,P<0.05)。(G)qRT-PCR 显示 Mdr2-/-+EVhigh 组 Col3a1、Acta2 等纤维化基因下调(n=5,P<0.05)。
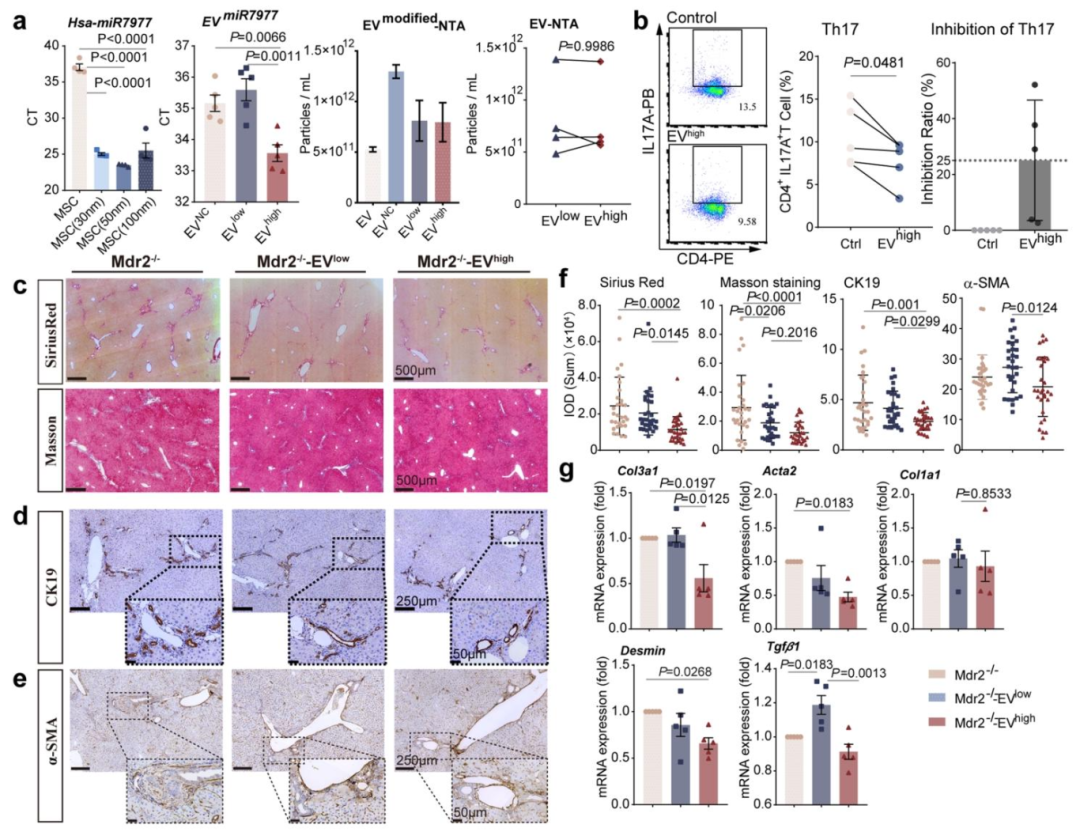
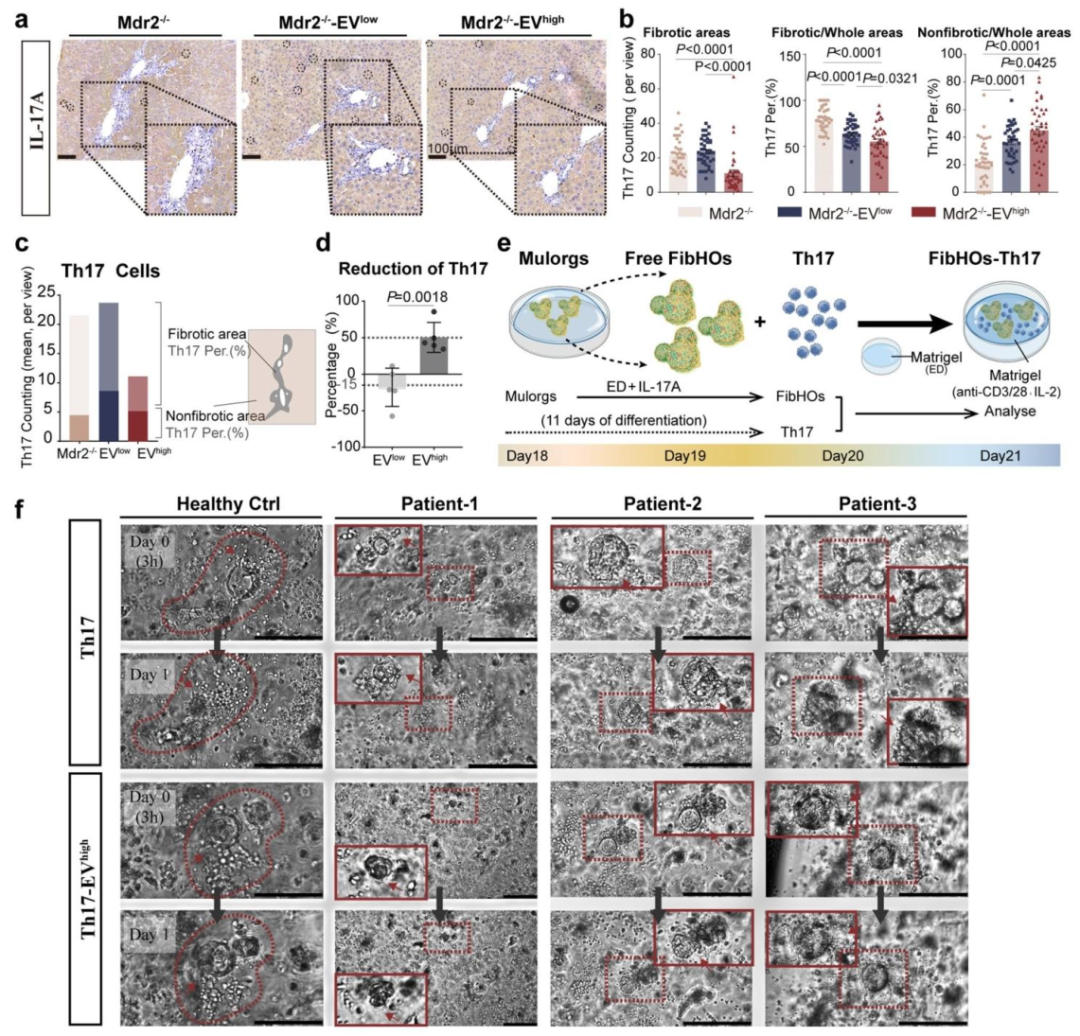
图 7:EVhigh 通过抑制 Th17 分化和迁移改善 PSC 的 Th17 相关纤维化微环境
内容:(A)IL-17A 免疫组化显示 Mdr2-/-+EVhigh 组纤维化区域 IL-17A + 细胞减少(虚线框为非纤维化区)。(B-C)纤维化及非纤维化区域 IL-17A + 细胞数量和比例定量(n=40,P<0.05)。(D)Mdr2-/-+EVhigh 组肝内 IL-17A + 细胞比例降低 50.42%,EVlow 组升高 17.88%(n=5,P<0.05)。(E)FibHOs 与 Th17 细胞共培养示意图。(F)光镜显示 Th17 细胞 3h 向 FibHOs 迁移、24h 聚集,Th17-EVhigh 组迁移减少;健康对照 FibHOs 与 Th17 共培养结构破坏,与 Th17-EVhigh 共培养形态保持;PSC 来源 FibHOs 与两者共培养形态变化小(比例尺 100μm)。
本研究证实,间充质干细胞来源的外泌体(EVMSC)通过其富集的 hsa-miR-7977 靶向 NFKBIZ,抑制 IκBζ 翻译,从而减少 IL-17A 表达及 Th17 细胞分化与迁移,减轻 Mdr2-/- 小鼠和人肝多谱系类器官(Mulorgs)中的胆管周围纤维化。EVhigh(高 miR-7977)可显著降低纤维化相关基因表达、HSCs 激活及炎症因子水平,为原发性硬化性胆管炎(PSC)及 Th17 相关疾病提供了新的治疗靶点和策略。局限性包括单一动物模型及类器官微环境模拟不完全,未来需结合更多临床样本和复杂模型验证。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:基于 DNA - 丝素蛋白水凝胶缓释系统的软骨类器官加速软骨再生研究
下一篇:靶向 B7-H3 的嵌合抗原受体 T 细胞在结直肠癌类器官和肝异种移植模型中的显著细胞毒性研究