常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-03 09:00:19 细胞资源库平台 访问量:304
小胶质细胞是中枢神经系统(CNS)的固有免疫细胞,老年小胶质细胞存在 “炎症衰老” 特征,与阿尔茨海默病等神经退行性疾病密切相关。但传统小胶质细胞培养多依赖新生或年轻小鼠,无法模拟老年细胞特性。美国北卡罗来纳大学夏洛特分校 Kristen E. Funk 团队在《Current Protocols》(2025, 5:e70199)发表优化方案:以 18 月龄老年 C57BL/6J 小鼠皮层为材料,通过胶原酶消化 + Percoll 梯度纯化,在含 GM-CSF 的培养基中成功培养小胶质细胞,可维持 30 天且保留老年细胞激活特征,为衰老神经生物学及神经退行性疾病研究提供关键模型。
本研究旨在建立可靠的老年小鼠小胶质细胞原代培养方法,解决传统模型的局限。方法:1. 取 8 周成年与 18 月龄老年小鼠皮层,经心脏灌流、解剖分离后,用胶原酶消化 + 机械研磨处理;2. Percoll 梯度离心纯化小胶质细胞,接种于 PDL 包被的非组织培养板,用含 GM-CSF 的培养基培养;3. 免疫荧光(Iba1/TMEM119)与流式细胞术(CD45/CD11b/P2RY12)鉴定纯度及激活状态。结果:每只小鼠可获~1×10⁶ viable 细胞,纯度 > 95%,可培养 30 天,老年小胶质细胞 MHC I/II、CD68 等激活标志物水平显著高于成年细胞。结论:该方案可高效制备老年小胶质细胞,为研究衰老相关小胶质细胞功能提供可靠工具。
小胶质细胞作为 CNS 的固有巨噬细胞,参与神经发育、突触重塑及损伤修复,在衰老过程中会出现 “炎症衰老”—— 基础炎症水平升高、吞噬功能下降,且激活标志物(CD45、MHC II)表达增加,这与阿尔茨海默病等神经退行性疾病的发病密切相关。传统小胶质细胞培养多采用新生或年轻小鼠,虽易培养但无法复现老年细胞的病理特征;而老年小鼠小胶质细胞因分离难度大、存活依赖特定因子(如 GM-CSF),可靠培养方案稀缺。现有研究表明 18 月龄小鼠相当于人类~60 岁,是研究衰老相关神经疾病的理想模型,因此亟需建立老年小鼠小胶质细胞培养方法,填补衰老神经生物学研究的模型缺口。
1.细胞模型与材料准备:采用 8 周龄成年与 18 月龄老年 C57BL/6J 小鼠(符合 IACUC 伦理规范),培养板用 10μg/ml PDL(硼酸盐缓冲液配制)包被≥1 小时,晾干备用;制备专用培养基(微胶质细胞生长培养基:DMEM/F12+10% FBS+1% 抗真菌抗生素;加 GM-CSF 至终浓度 5ng/ml 用于老年细胞培养),胶原酶消化缓冲液(含胶原酶 D、TLCK、DNase I)现配现用。
2.皮层分离与细胞纯化:小鼠经异氟烷麻醉后,心脏灌流冷 PBS 去除血液,解剖分离皮层(去除嗅球、小脑及中脑);皮层剪碎后用胶原酶消化缓冲液室温摇床孵育 1 小时,70μm 滤网过滤 + 注射器活塞研磨,500×g 离心 10 分钟;沉淀用 37% 等渗 Percoll 重悬,1200×g 无刹车离心 30 分钟,吸取底部细胞团即为纯化小胶质细胞。
3.培养与维护:纯化细胞用含 GM-CSF 的培养基重悬,以 5×10⁵ cells / 孔接种 12 孔板,37℃ 5% CO₂培养;前 3 天每天全量换液,之后每周两次;细胞达 80% 汇合时用 0.05% 胰酶消化,1:2 传代,传代后次日换液去除残留胰酶,总培养周期可达 30 天。
4.鉴定与功能检测:培养 24 天时,免疫荧光染色 Iba1(小胶质细胞特异性)、TMEM119(小胶质细胞标志物)及 GFAP/NeuN(排除星形胶质细胞 / 神经元污染);培养 28 天时,流式细胞术检测 CD45/CD11b/P2RY12(纯度鉴定)及 MHC I/II、CD68(激活状态),对比成年与老年细胞差异。
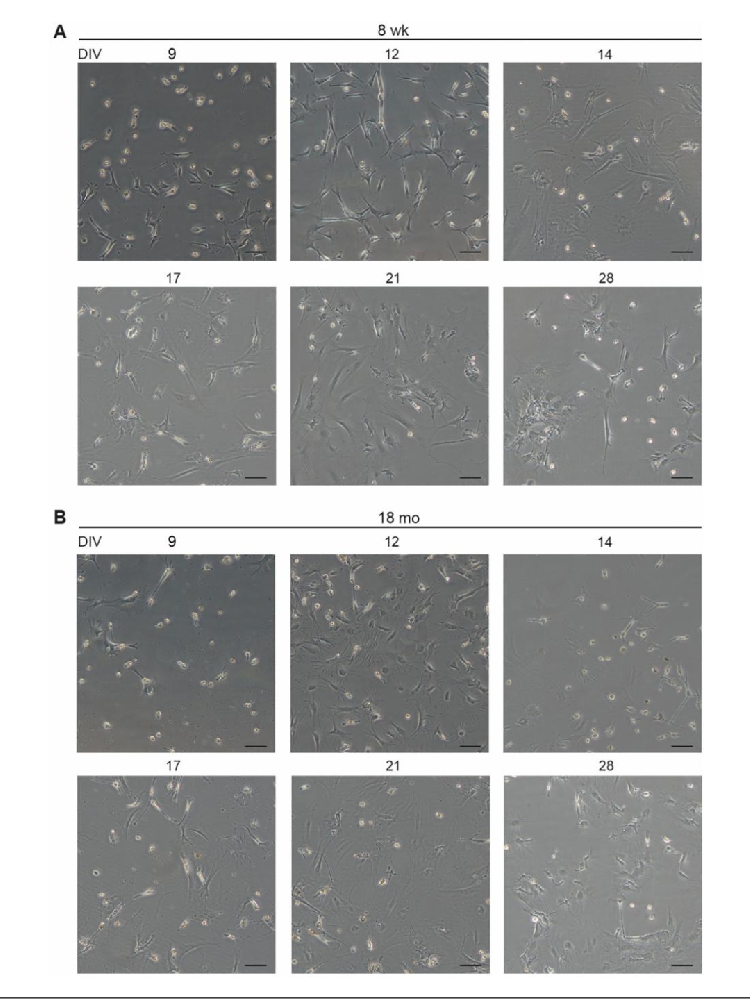
Fig1:成年与老年小胶质细胞培养过程中的形态变化
该图为 8 周成年(A)与 18 月龄老年(B)小鼠小胶质细胞培养 28 天的明场图像(20× 放大):培养 9 天时,成年细胞已可见明显分支状形态,老年细胞仍有较多未分化细胞;12 天时两者均达到成熟状态,呈典型小胶质细胞形态;17-21 天时,细胞分支增多,维持稳态下的分支状表型;28 天时,两者均转为阿米巴样形态(激活态),且老年细胞成熟速度显著慢于成年细胞,提示老年小胶质细胞在体外仍保留衰老相关的增殖与分化延迟特征,与体内老年小胶质细胞功能下降的表型一致。
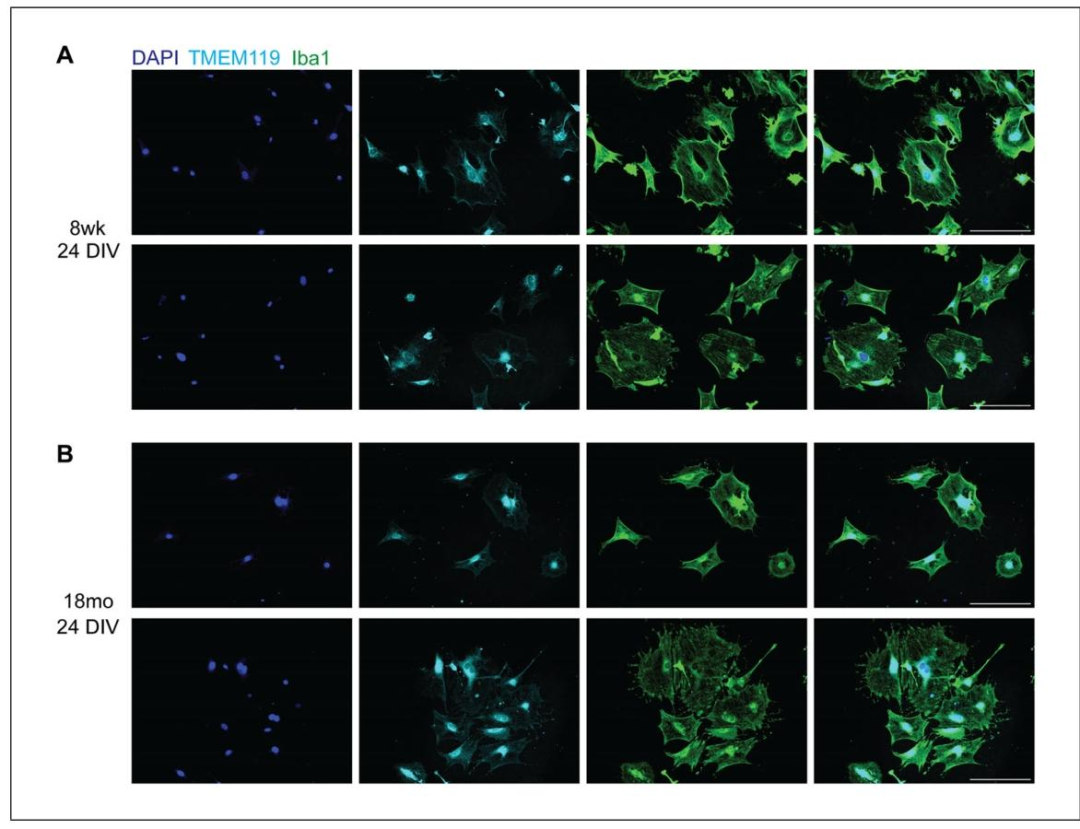
Fig2:成年与老年小胶质细胞的纯度鉴定(免疫荧光)
该图为培养 24 天的免疫荧光结果(40× 放大):成年(A)与老年(B)小胶质细胞均呈 Iba1(绿色)与 TMEM119(浅蓝色)双阳性,DAPI(深蓝色)标记细胞核,无 GFAP(星形胶质细胞)与 NeuN(神经元)染色信号;merged 图像显示几乎所有细胞核均对应 Iba1/TMEM119 阳性细胞,纯度 > 95%,证实该培养方案可获得高纯度小胶质细胞,且无其他神经细胞污染,为后续功能实验排除杂细胞干扰。
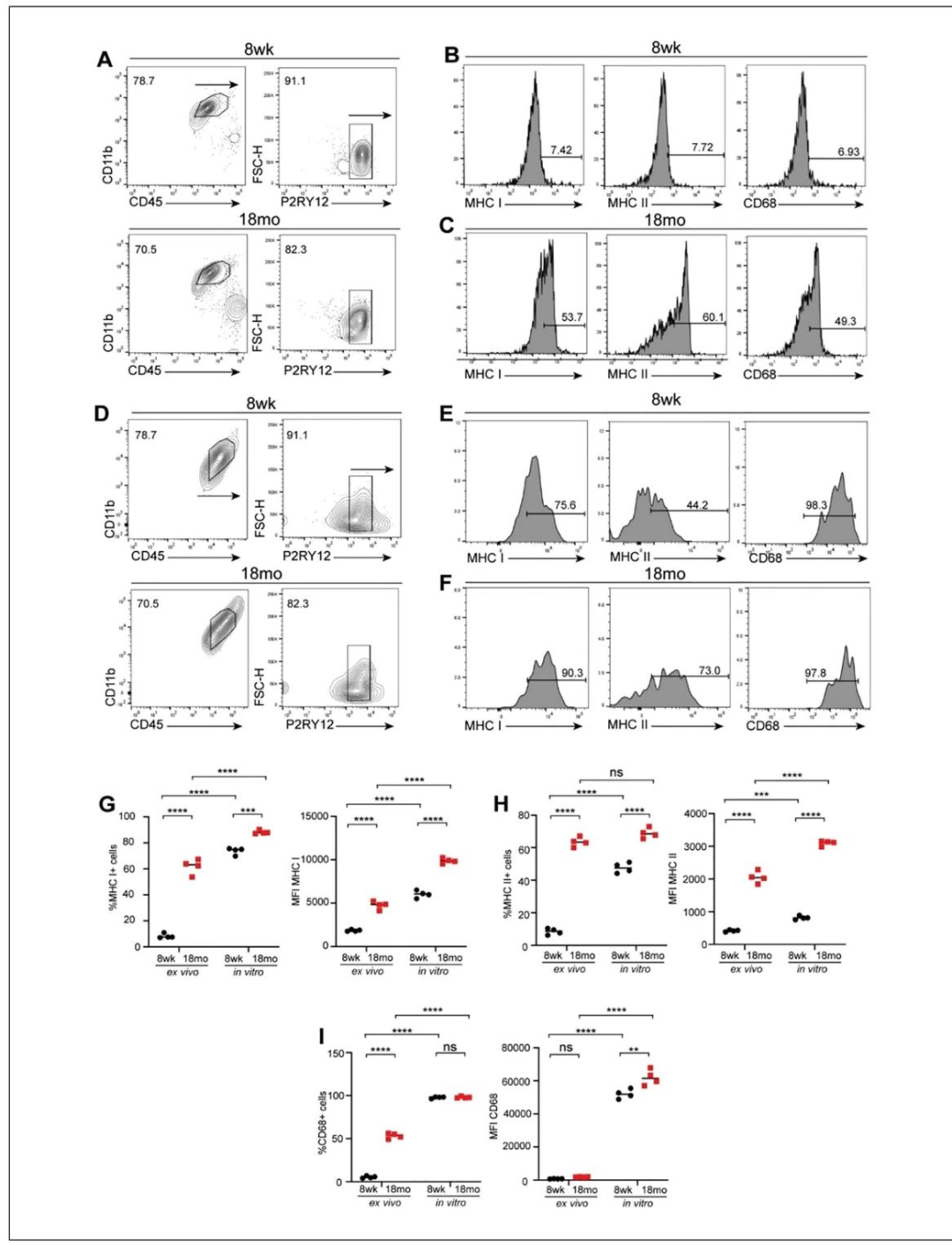
Fig3:成年与老年小胶质细胞的激活状态对比(流式细胞术)
该图通过流式分析新鲜分离(A-C)与体外培养 28 天(D-I)的小胶质细胞激活状态:新鲜分离的老年小胶质细胞(B、C)MHC I/II、CD68 表达已高于成年细胞;体外培养后,两者激活标志物水平均升高,但老年细胞(F、H、I)仍显著高于成年细胞(E、G);同时流式门控显示培养细胞中 CD45⁺CD11b⁺P2RY12⁺小胶质细胞比例 > 90%,进一步证实纯度。结果表明体外培养可保留老年小胶质细胞的高激活特征,与体内 “炎症衰老” 表型一致,适合研究衰老相关小胶质细胞功能。
本研究建立的老年小鼠小胶质细胞培养方案具有三大优势:1. 高效性:每只小鼠可获~1×10⁶ viable 细胞,纯度 > 95%;2. 稳定性:添加 GM-CSF 可维持细胞存活 30 天,支持长期实验;3. 生理相关性:体外培养的老年小胶质细胞保留 “炎症衰老” 特征,激活标志物水平显著高于成年细胞。该方案填补了老年小胶质细胞模型的空白,为研究衰老相关神经退行性疾病的小胶质细胞机制提供可靠工具,也可用于药物筛选(如调控小胶质细胞激活的化合物)。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:可编程巨噬细胞极化纳米颗粒用于MRI引导的肺转移瘤早期检测与治疗
下一篇:猪视网膜色素上皮(RPE)单眼原代培养方案:为年龄相关性黄斑变性(AMD)研究提供标准化模型