常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-10-25 09:20:04 细胞资源库平台 访问量:311
肝脏通过肝细胞执行关键的代谢功能,包括糖异生、糖原合成、尿素循环、脂肪生成、胆汁酸合成、蛋白质生产和药物代谢。肝功能严重受损会导致肝衰竭,这是一种威胁生命的状况,需要移植治疗。随着抗病毒疗法的进步,肝衰竭的病因从病毒性肝炎转向与现代生活方式相关的代谢性肝病,特别是代谢功能障碍相关脂肪性肝病,如果不治疗,可进展为代谢功能障碍相关脂肪性肝炎、肝硬化和肝衰竭。尽管代谢功能障碍相关脂肪性肝病的增加引起了重大健康关注,但代谢性肝病的预防取得的成功有限,部分原因是缺乏能够忠实再现代谢功能的人类肝细胞模型。
在体外分离的肝细胞会迅速丧失扩增能力,与其在体内强大的再生潜力形成鲜明对比。现有的培养方法,如经典的夹层培养和最近开发的基于五种小分子抑制剂的培养,能暂时维持原代人肝细胞(PHHs)的功能,但会影响其扩增能力。肝细胞培养研究探索了部分克服这一限制的策略。肝细胞分化方案从可扩增的非肝细胞资源中产生肝细胞样细胞,包括胆管细胞、多能干细胞或直接重编程的成纤维细胞。然而,它们的不成熟性妨碍了成人肝功能的分析。小分子抑制剂(如GSK-3和ROCK抑制剂)的使用促进了人成人肝细胞的扩增,但总是伴随着胆管导管分化的化生变化,这一过程最近被重新定义为"古质形成",将高功能细胞重编程为能增殖的细胞,将能量从细胞功能转向复制。类器官培养可以繁殖功能性小鼠成体肝细胞和人胎儿肝母细胞,但其应用于人成体肝细胞受到限制。因此,研究者们缺乏确保长期扩增和人成体肝细胞功能的策略,这对再生医学、药物发现和毒理学中基于人肝细胞的应用构成了实质性障碍。
近期,发表在Nature期刊上的一篇题为Generation of human adult hepatocyte organoids with metabolic functions的研究论文开发了一种新的人类成人肝细胞类器官培养系统,解决了体外扩增与功能性之间的权衡关系。通过OSM-STAT3信号通路的激活,研究者能够长期培养人类成人肝细胞,同时维持其肝脏特性和功能能力。
1,人类肝细胞类器官的建立和特性。研究团队基于肝细胞癌基因组学分析结果,设计了包含EGF、HGF、FGF10、Wnt/R-spondin、TGFβ家族抑制剂、IL-6和PKA激活剂的扩增培养基。该培养基促进了形成具有厚单层结构且表达肝细胞标记物(白蛋白和HNF4α)的小囊性类器官,称为人肝细胞类器官(HHOs)。研究发现,白介素6超家族细胞因子oncostatin M(OSM)通过STAT3信号通路显著增强了HHOs的扩增和长期培养潜力,使HHOs能够在至少3个月内指数级增长,并维持6个月以上的生长。通过流式细胞术分选的单个肝细胞能够形成类器官,形成效率为10-30%,与其他人类组织干细胞相当。全基因组测序证实了HHOs的基因组稳定性。
2,OSM和YAP信号通路对HHOs生长的影响。OSM处理不仅促进了HHOs的增殖,还诱导了类上皮基底极性的形成,使类器官与富含层粘连蛋白的细胞外基质(Matrigel)相互作用,进一步促进类器官生长。转录组和ChIP-seq分析确认,OSM-STAT3激活上调了细胞粘附相关基因。有趣的是,尽管YAP激活在肝细胞增殖中被认为是关键驱动因素,但其对OSM诱导的HHO增殖的影响较小。LATS抑制剂(LATSi)诱导的YAP激活与OSM协同增强了HHO扩增,但导致胆管化生。OSM抑制了由LATSi或单层培养诱导的化生和上皮-间充质转化反应,表明OSM-STAT3激活不仅通过与受体酪氨酸激酶和Wnt信号一起促进肝细胞增殖,还维持了肝脏谱系完整性,防止胆管化生。
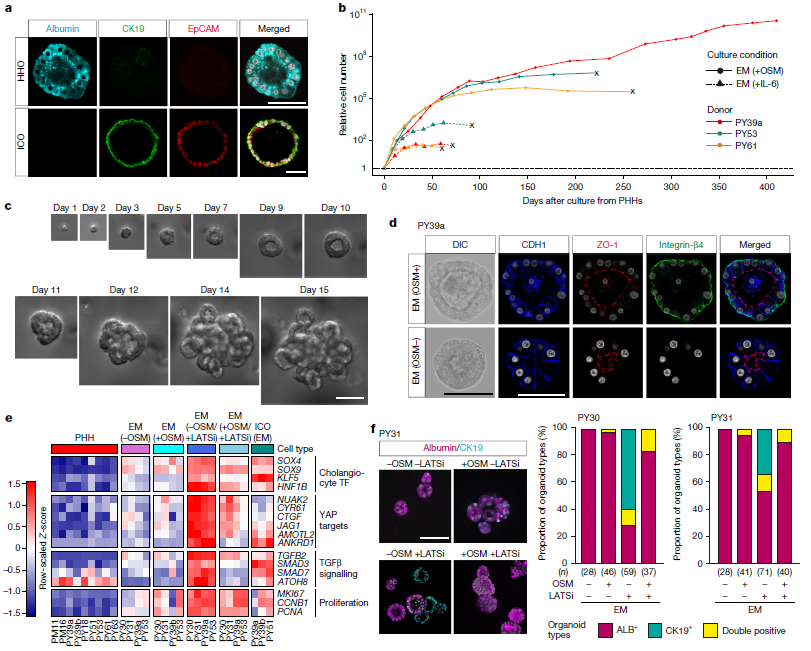
图 1 利用特定因子实现人类成体肝细胞类器官的扩增
3,HHOs的异种移植和分化。为评估HHOs的再生潜力,研究者将其移植到TK-NOG小鼠中。移植后8周,HHOs在肝脏中定植,形成胆小管结构,并沿周围门静脉至中央静脉轴表达不同的代谢标志基因,重建了代谢分区结构。HHOs的再殖能力与原代肝细胞相当,但扩增超过100万倍后降低。在体外分化条件下,去除OSM、Wnt/R-spondin和Noggin,并引入激素混合物(生长激素、催乳素和皮质醇)以及γ-分泌酶抑制剂(DAPT),形成了分化的HHOs(dHHOs)。加入Wnt/R-spondin(dHHO+WR)诱导中央静脉标记物表达,而在无葡萄糖培养基中"饥饿"处理促进了门静脉标记物和部分中央静脉标记基因的表达。转录组分析显示dHHOs与原代肝细胞在全球基因表达和肝脏特异性代谢功能方面高度相似。
4,HHOs的代谢功能和药物代谢能力。分化培养条件诱导了从类上皮到肝细胞样结构的形态学变化,dHHOs发展出胆管小管系统。dHHOs产生了多种胆汁酸,三酰甘油,并表现出药物代谢能力。生物质谱分析验证了dHHOs比原代肝细胞更高的胆汁酸产生,主要以甘氨酸或牛磺酸结合形式存在。dHHOs产生中等水平的三酰甘油,Wnt/R-spondin补充的dHHOs(dHHO+WR)积累脂滴并显示类似肝脂肪变性的特征。dHHOs表达主要细胞色素P450(CYP)基因,LC-MS/MS分析证实了主要CYP酶的基础活性。尽管不同个体间CYP活性有差异,但同一供体的dHHOs在长期培养中活性保持一致。dHHOs对药物诱导的CYP活性有反应,并保留了II期药物结合活性。对乙酰氨基酚(APAP)诱导的肝损伤模型表明,dHHO+WR对剂量依赖性细胞毒性反应敏感,且N-乙酰半胱氨酸(临床上用于APAP中毒的解毒剂)能阻断这种细胞毒性反应。
5,HHOs的门静脉肝细胞功能和蛋白合成能力。分化的HHOs表现出包括糖异生、尿素循环和β-氧化在内的门静脉肝细胞功能。同位素示踪证实了肝脏糖异生和独特的丙酮酸通量。15NH4Cl处理证实了氨转化为尿素的过程。dHHOs的最大呼吸能力高于eHHOs,表明氧化磷酸化增强。dHHOs产生了高水平的白蛋白,在50-150 μg/day/million cells范围内,与人体内估计的产生率相当。分化培养基还诱导了与止血系统相关的基因表达,包括F2、F7、F9和F10。维生素K补充增加了因子IX活性。编码肝细胞源性先天性免疫蛋白的基因,如SERPINA1(α1-抗胰蛋白酶)和C3(补体3),在eHHOs和dHHOs中高表达。研究团队还成功建立了基因编辑流程,生成了靶向G6PC和OTC基因的敲除HHOs,这些基因分别负责糖原贮积病和X-连锁尿素循环障碍。
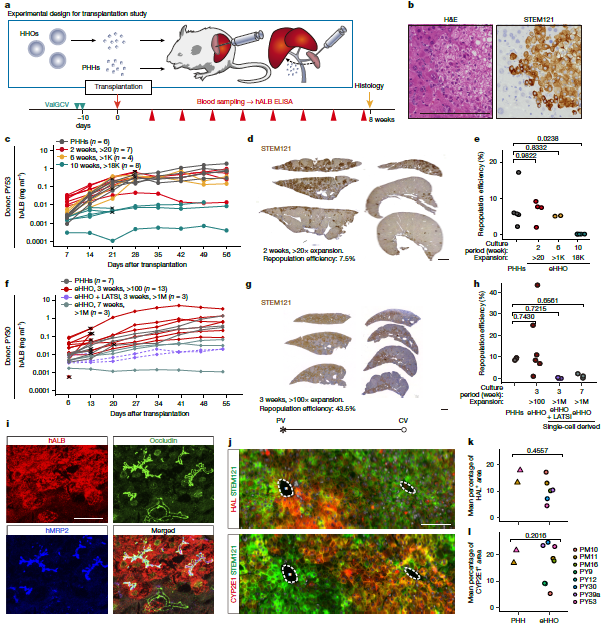
图 2 人类肝细胞类器官(HHOs)对小鼠肝脏的重新填充
该研究方法允许生成大量功能性肝细胞,为药物毒性筛选、代谢性疾病建模和再生医学开辟了新的可能性。dHHOs表现出了多种肝脏特异性功能,包括糖代谢、脂质代谢、药物代谢和蛋白质合成,这些功能接近或超过了体外培养的原代肝细胞性能。特别是,dHHOs在长期培养后仍保持这些功能,这一特性在以前的人肝细胞模型中尚未实现。此外,基因编辑流程的建立为遗传性代谢性肝病的人体模型提供了重要工具。总的来说,HHO技术代表了一种新的器官培养系统,协调了肝细胞的扩增性和功能性。其优点扩展到提供一个稳定、可重复和经济有效的平台,用于探索人类肝脏代谢,超越了原代肝细胞的局限性。此外,HHOs在再生医学中的潜在应用为应对肝衰竭开辟了新的视野。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:建立双向潜能人肺类器官培养系统及产生成熟肺泡和气道类器官的分化方法