常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-09-03 17:39:39 细胞资源库平台 访问量:237
唾液腺纤维化是一种以细胞外基质异常沉积和肌成纤维细胞激活为特征的疾病,会导致唾液腺不可逆的功能障碍。其主要由慢性炎症、衰老、干燥综合征以及口腔颌面部癌症的放射治疗等因素引起,给患者带来口干、味觉减退、龋齿等严重并发症,严重影响患者的口腔健康和生活质量。目前的治疗方法无法有效逆转纤维化,迫切需要新的治疗策略。
2025年5月27日,发表在Journal of Translational Medicine上题为Saliva-derived extracellular vesicles: a promising therapeutic approach for salivary gland fibrosis的研究旨在探究唾液源性细胞外囊泡(sEV)对唾液腺纤维化的治疗潜力。
通过体外实验,发现 sEV 能显著抑制 TGF-β 诱导的人类唾液腺成纤维细胞(hSGFs)和唾液腺类器官的纤维化活动,包括迁移、胶原蛋白产生和肌成纤维细胞激活。生物信息学分析揭示 sEV 源性 miRNA 对纤维化相关通路具有协同调节作用,其中 STAT3 被确定为关键介质。在体内实验中,局部 sEV 给药减少了唾液腺纤维化,保持了腺泡结构,并抑制了成纤维细胞中 STAT3 的核转位。研究表明 sEV 通过调节 STAT3 信号通路发挥强大的抗纤维化作用,为唾液腺纤维化提供了一种有前景的无细胞治疗策略。
1) 慢性腮腺炎组织的纤维化变化。通过苏木精-伊红(HE)染色,正常组织显示出清晰的腺泡和导管结构,而CS组织则表现为腺泡细胞萎缩、炎症细胞浸润增加和胶原纤维大量沉积。Masson三色染色进一步揭示了CS组织中胶原纤维主要沉积在萎缩的腺泡周围,形成特征性的漩涡状模式。半定量分析证实,CS组织的胶原含量显著高于正常组织(P < 0.01)。此外,通过免疫荧光共定位分析α-平滑肌肌动蛋白(αSMA)和波形蛋白(Vimentin),发现CS组织中存在αSMA和Vimentin的共定位,表明肌成纤维细胞的激活及其在胶原沉积中的作用。这些结果表明,CS组织中显著的胶原纤维沉积和肌成纤维细胞激活是纤维化的关键特征。
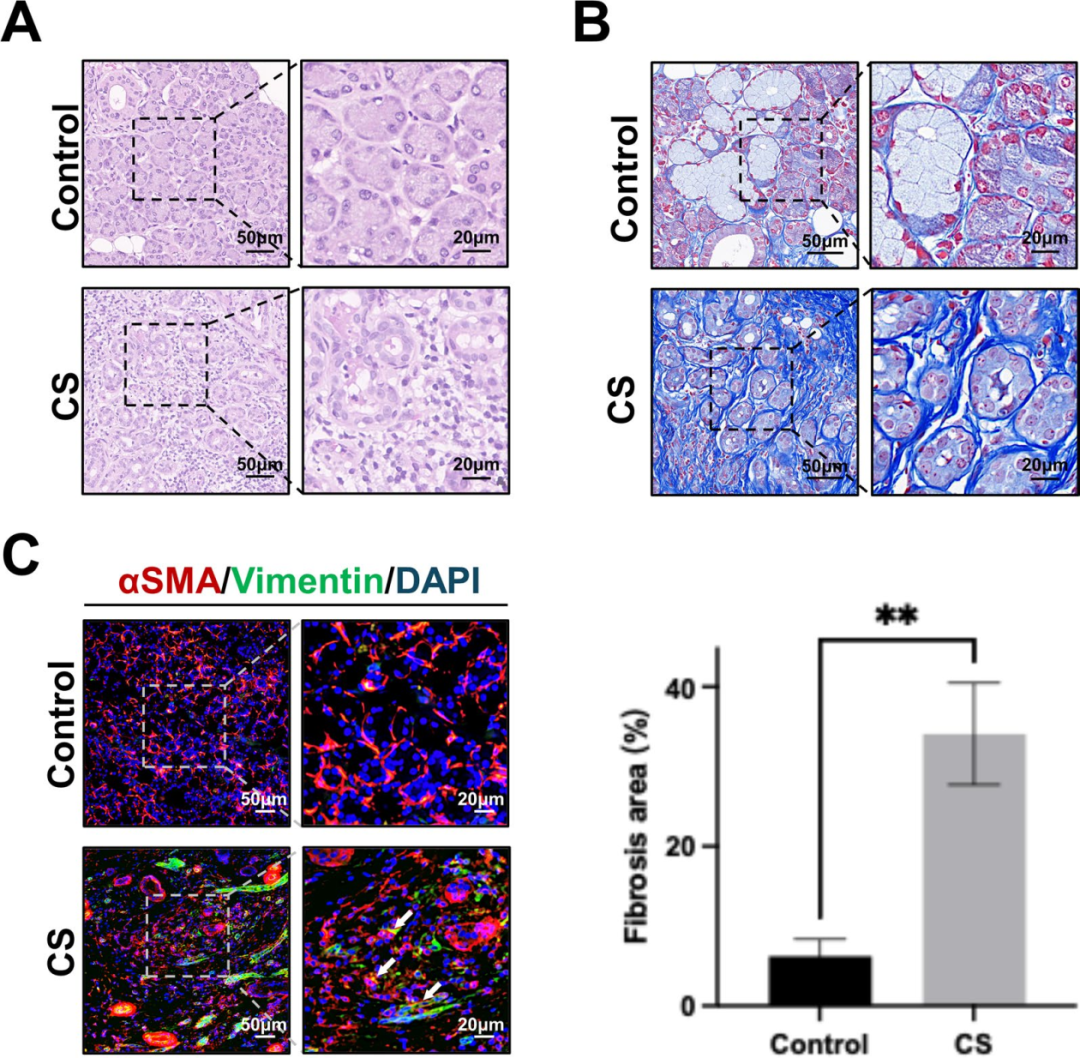
图1展示了正常和慢性腮腺炎(CS)组织的组织学变化。
2) 唾液源性细胞外囊泡(sEV)的特征。通过透射电子显微镜(TEM)观察到sEV呈圆形,直径约为150纳米。纳米颗粒跟踪分析(NTA)确认sEV的直径小于300纳米。Western blot检测到sEV中存在CD9、Alix和TSG101等细胞外囊泡特异性标志物,而内质网标志物Calnexin未被检测到,这证实了sEV的成功分离。这些结果表明,从唾液样本中成功分离出sEV,其形态和大小符合细胞外囊泡的特征,且不含非囊泡成分。
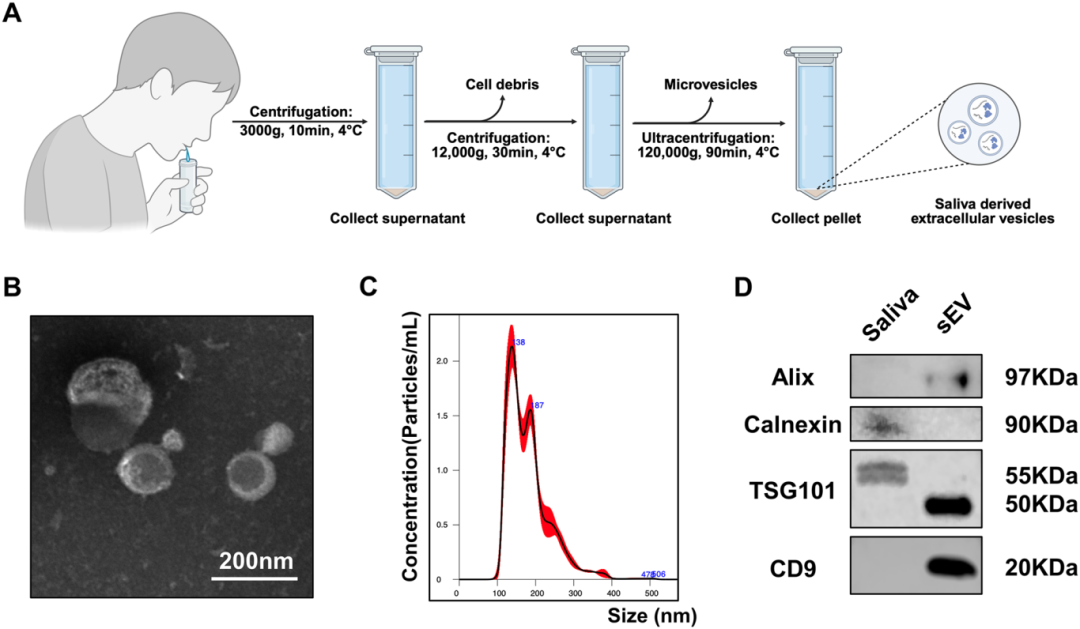
图2展示了唾液源性细胞外囊泡(sEV)的分离和鉴定过程。
3) sEV抑制人唾液腺成纤维细胞(hSGFs)的纤维化活性。细胞计数试剂盒8(CCK8)实验显示,10 µg/mL的sEV显著降低了hSGFs的活性(P < 0.0001),因此选择此浓度进行后续实验。免疫荧光分析证实hSGFs有效摄取了sEV。在划痕试验中,TGF-β处理显著增强了hSGFs的迁移能力,而sEV处理则有效抑制了这种效果(P < 0.01)。进一步的实验中,细胞在TGF-β存在或不存在sEV的情况下培养24小时,Western blot分析显示TGF-β上调了Col1A1和αSMA的表达,而sEV处理显著逆转了这种效应。这些结果表明,sEV通过抑制hSGFs的迁移和胶原蛋白产生,有效抑制了TGF-β诱导的纤维化活性。
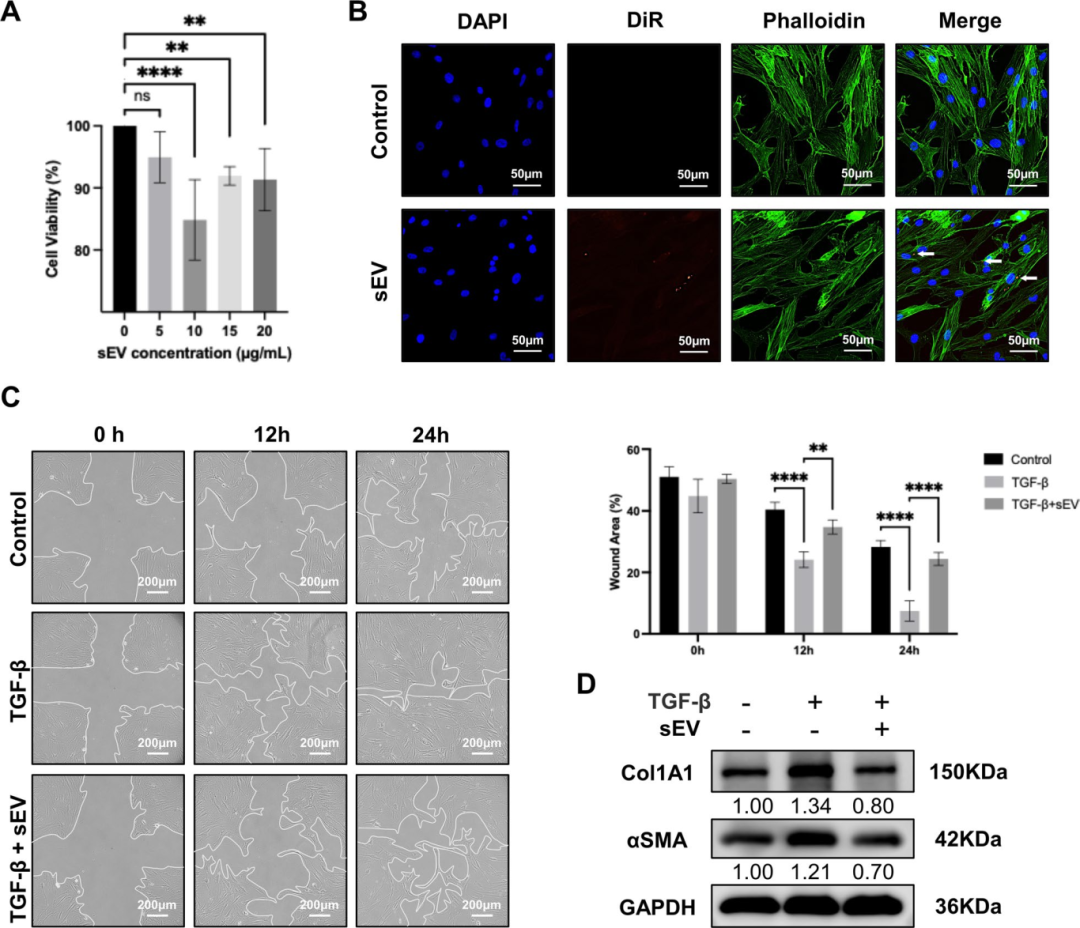
图3评估了sEV对人唾液腺成纤维细胞(hSGFs)纤维化活性的影响。
4) sEV中miRNA的抗纤维化功能。通过网络分析,研究者从10名供体中选取了表达量最高的30种miRNA进行分析。分析发现hsa-let-7b-5p、hsa-let-7a-5p、hsa-miR-92a-3p、hsa-let-7f-5p和hsa-miR-26b-5p是关键miRNA,它们在网络中具有最高的连接度和中介中心性。基因集富集分析(GSEA)进一步揭示了这些miRNA与抗纤维化途径的显著关联,并涉及转录因子(TF)网络。这些结果表明,sEV中的miRNA通过协同调节TF介导的基因网络发挥抗纤维化作用。
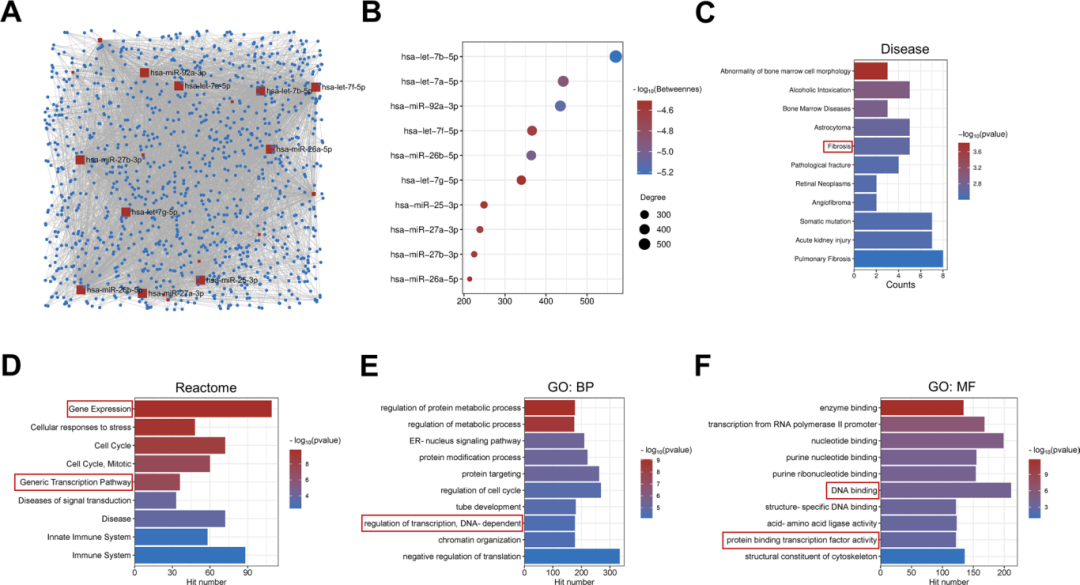
图4探讨了sEV中miRNA的抗纤维化作用。
5) RNA测序和靶向转录因子预测表明sEV通过STAT3抑制纤维化。火山图展示了TGF-β处理组与TGF-β+sEV处理组之间的差异表达基因(DEGs)。基因本体(GO)分析显示,sEV处理影响了与“细胞外基质”和“含胶原的细胞外基质”相关的基因。热图确认了sEV处理组中Col1A1和αSMA表达的下调。通过整合目标-TF数据库与RNA-seq数据,研究者预测了可能调节Col1A1和ACTA2的TF,确定了SP1、GATA3和STAT3为潜在调节因子。然而,RNA-seq分析显示sEV处理下调了STAT3的表达,而SP1和GATA3的表达未发生变化。这些结果表明,sEV通过下调STAT3的表达发挥其抗纤维化作用。
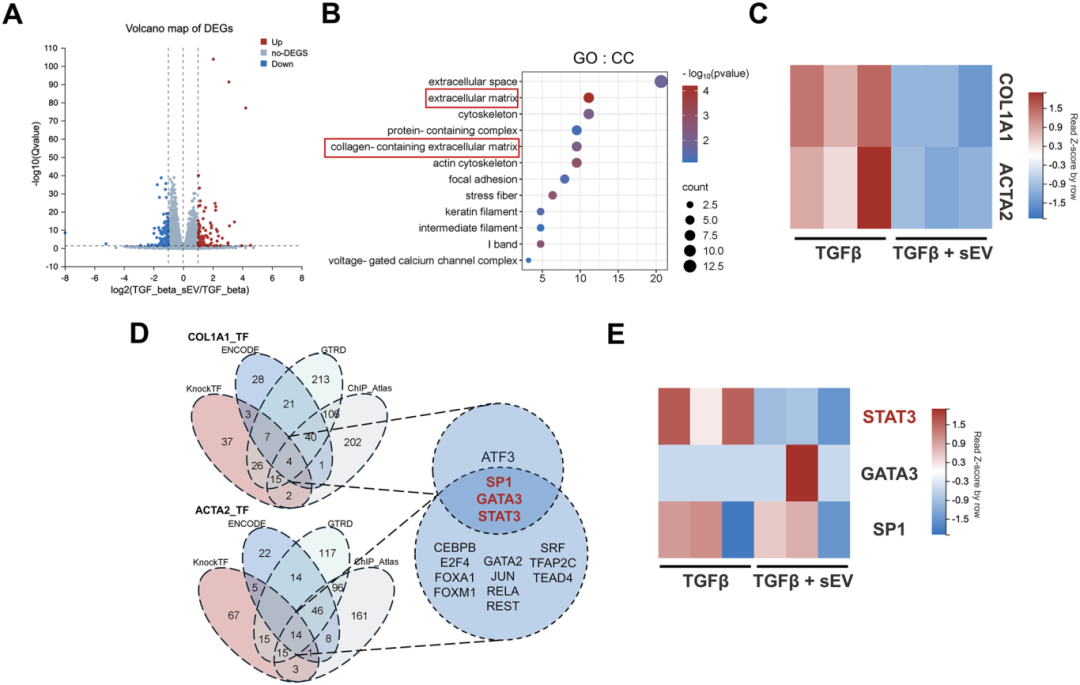
图5通过RNA测序和转录因子(TF)预测分析,探讨了sEV对唾液腺纤维化的影响及其潜在机制。
6) sEV通过STAT3抑制hSGFs的纤维化能力。划痕试验显示,1 µM的STAT3激活剂Colivelin恢复了被sEV抑制的hSGFs的迁移能力(P < 0.01)。Western blot分析进一步揭示,sEV处理显著降低了Col1A1和αSMA的表达,同时下调了p-STAT3和STAT3的表达,而STAT3的激活则逆转了这些效应。这些结果表明,STAT3是sEV抗纤维化作用的关键介质,其激活可以抵消sEV对hSGFs纤维化能力的抑制作用。
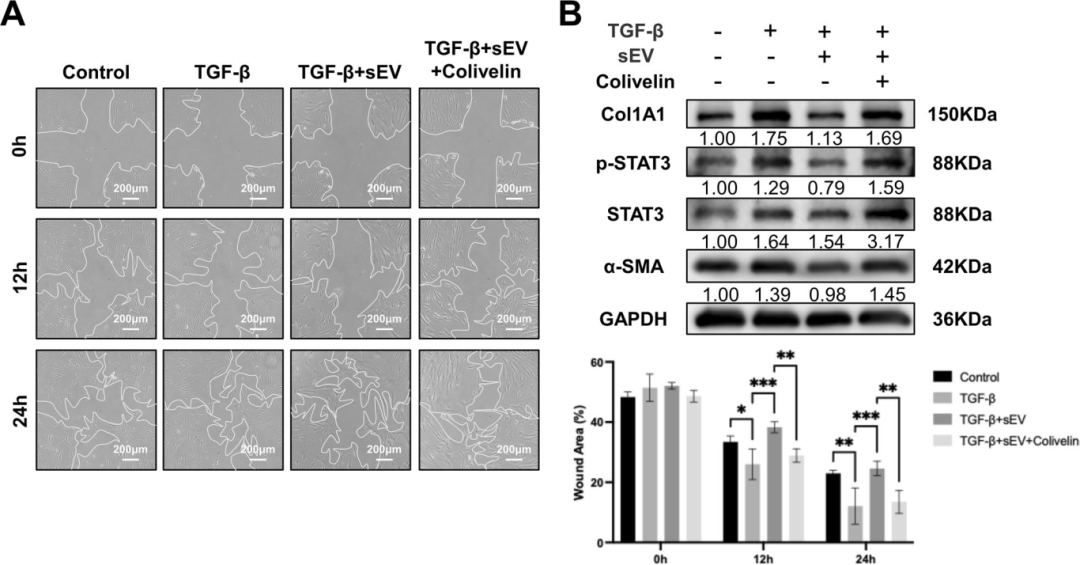
图6进一步验证了STAT3在sEV抗纤维化作用中的关键作用。
7) sEV通过STAT3抑制唾液腺类器官模型中的纤维化。类器官模型用PBS、TGF-β、TGF-β+sEV或TGF-β+sEV+Colivelin处理。结果显示,sEV处理显著抑制了TGF-β诱导的纤维化,表现为减少的αSMA和波形蛋白阳性区域。免疫荧光染色显示,sEV处理抑制了p-STAT3和αSMA的共定位,而Colivelin的添加则恢复了这些纤维化标志物的表达。这些结果进一步证实了STAT3在sEV抗纤维化作用中的关键作用,并表明sEV可以通过抑制STAT3的活性来减轻唾液腺类器官模型中的纤维化。
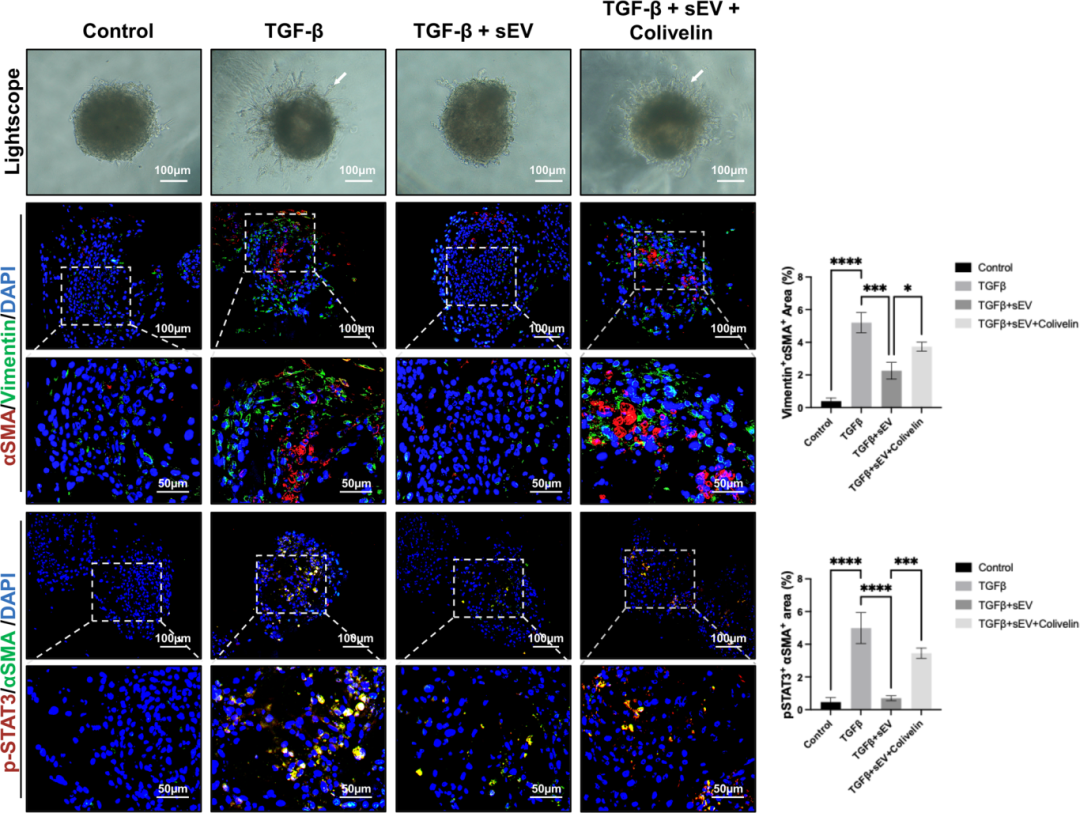
图7展示了sEV在唾液腺类器官模型中通过STAT3抑制纤维化的效果。
8) 小鼠Wharton’s导管结扎模型中sEV的抗纤维化作用。实验中,通过在结扎近端的Wharton’s导管下方注射20 µg的sEV来评估其体内抗纤维化效果。在体成像显示,sEV在注射后7天仍可检测到。组织学分析显示,结扎组出现腺泡萎缩和胶原沉积,而sEV处理则部分恢复了唾液腺形态,并显著减少了纤维化区域(P < 0.05)。免疫组化染色进一步显示,sEV处理抑制了纤维化区域中成纤维细胞的p-STAT3核转位。这些结果表明,sEV在体内通过抑制STAT3的核转位发挥抗纤维化作用,为唾液腺纤维化的治疗提供了新的策略。
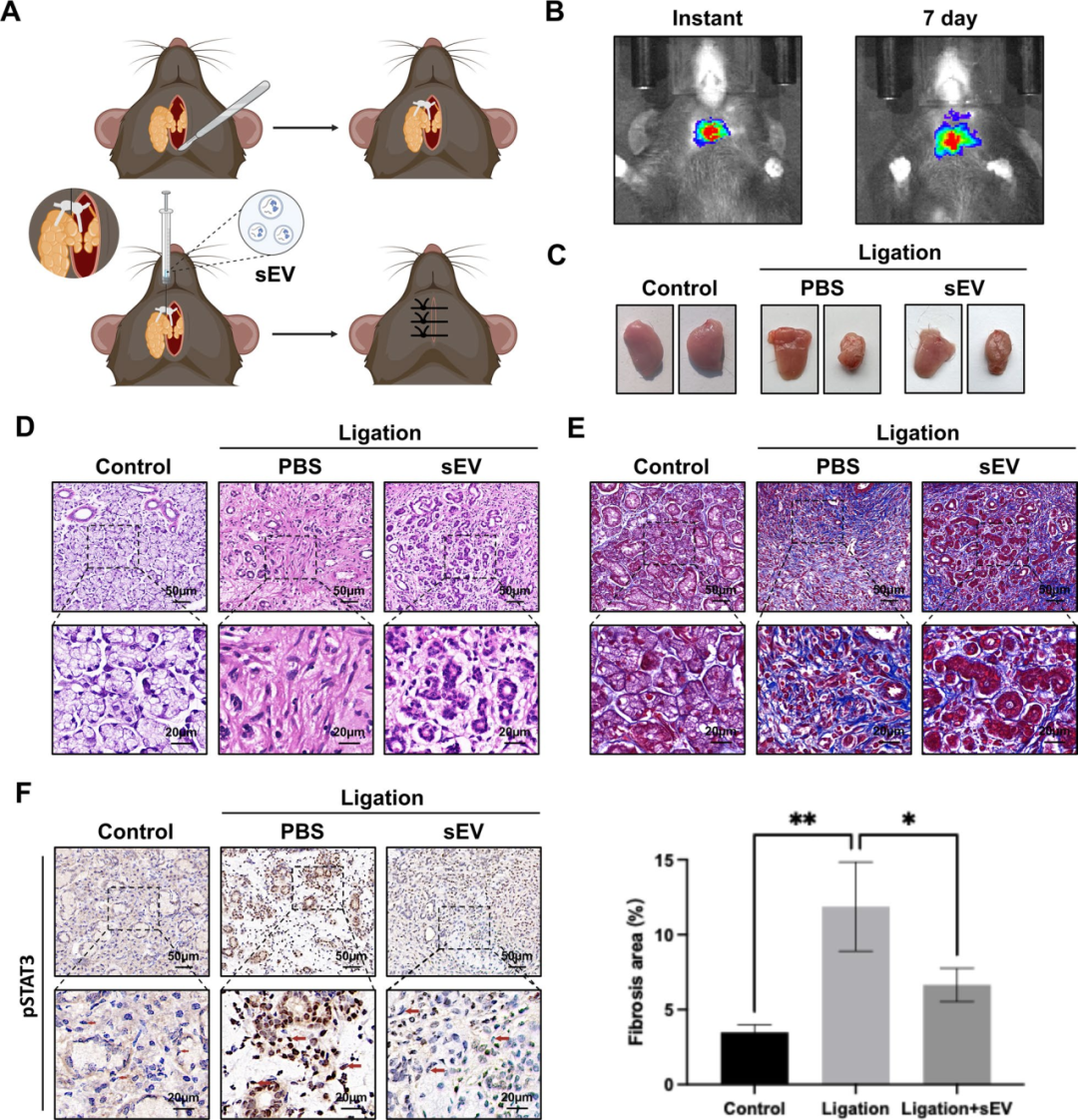
图8评估了sEV在小鼠Wharton’s导管结扎模型中对唾液腺纤维化的治疗效果。
本研究通过体外和体内实验,深入探究了唾液源性细胞外囊泡(sEV)对唾液腺纤维化的治疗效果。体外实验中,sEV显著抑制了TGF-β诱导的人类唾液腺成纤维细胞(hSGFs)的迁移、胶原蛋白产生和肌成纤维细胞激活。通过网络分析和RNA测序,发现sEV中的miRNA通过协同调节纤维化相关通路发挥作用,其中STAT3是关键介质。体内实验采用Wharton’s导管结扎模型,局部注射sEV可减轻唾液腺纤维化,保持腺泡结构,并抑制STAT3的核转位。这些结果表明,sEV通过调节STAT3信号通路发挥抗纤维化作用,为唾液腺纤维化的治疗提供了新的策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:miR-181a-5p在BMP4调控下的肠道细胞分化