常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-08-27 17:50:45 细胞资源库平台 访问量:306
乳腺癌是全球女性最常诊断的癌症类型,也是癌症相关死亡的主要原因之一。细胞外基质(ECM)在乳腺癌进展中发挥关键作用,癌细胞克服原有限制性表型的能力是维持适应性的必要进展。为了寻找新的乳腺癌治疗策略,有必要识别从原发肿瘤到转移进展过程中调节恶性表型的机制。然而,传统的二维(2D)单层细胞培养和动物模型在研究恶性表型的复杂机制方面存在固有局限性。
2D细胞培养在生理学上不相关,实验上不可靠,缺乏适当的细胞-ECM相互作用。动物模型除了昂贵、繁琐和耗时的问题外,许多不可控变量使得确定特定因子对肿瘤进展的影响变得困难。三维(3D)细胞培养技术的最新进展产生了类器官,能够反映体内组织的关键形态和功能特性,为更好地理解癌症生物学提供了平台。肿瘤类器官培养有潜力克服传统癌症模型的若干局限性,作为一个相对低成本且具有代表性的平台,在体外模拟癌症异质性和细胞-ECM相互作用。
在参与乳腺癌-基质相互作用的各种生物学线索中,表皮生长因子(EGF)在83%的人类乳腺癌中表达,被广泛认为是肿瘤发生和癌症进展的重要介质。EGF由基质细胞(如内皮细胞和成纤维细胞)分泌,主要定位于乳腺基质中。
近期,华中科技大学同济医学院刘熙秋团队发布在Materials Today Bio期刊,题为Matrix-bound EGF promotes malignant phenotypes of breast cancer organoids in the biomimetic ECM of alginate的研究旨在建立体外3D乳腺癌类器官模型,通过使用海藻酸冷凝胶模拟多孔ECM来重建肿瘤-基质微环境,特别是引入基质结合生长因子EGF的控制释放系统,研究其对恶性表型的影响。
1) 基质结合EGF仿生ECM的构建与表征。研究团队成功构建了基质结合EGF的仿生ECM系统。通过FTIR光谱分析证实了EGF与海藻酸冷凝胶之间的分子间相互作用,O-H吸收峰在3200-3500 cm⁻¹范围内的强度降低和轻微位移表明EGF蛋白的氨基与海藻酸钙中羟基之间存在潜在相互作用。SEM显示冷凝胶呈现疏松多孔的三维结构,有利于细胞生长和粘附,不同EGF浓度对孔径大小无显著影响。FITC标记的EGF可视化显示EGF能够附着并均匀分布在冷凝胶内壁上,600 ng/mL的EGF浓度被确定为最适浓度。释放动力学研究表明,约50%的基质结合EGF在初始48小时内释放,随后释放速率下降,7天后约40%的EGF仍保留在基质中,为持续的生长因子呈递提供了基础。
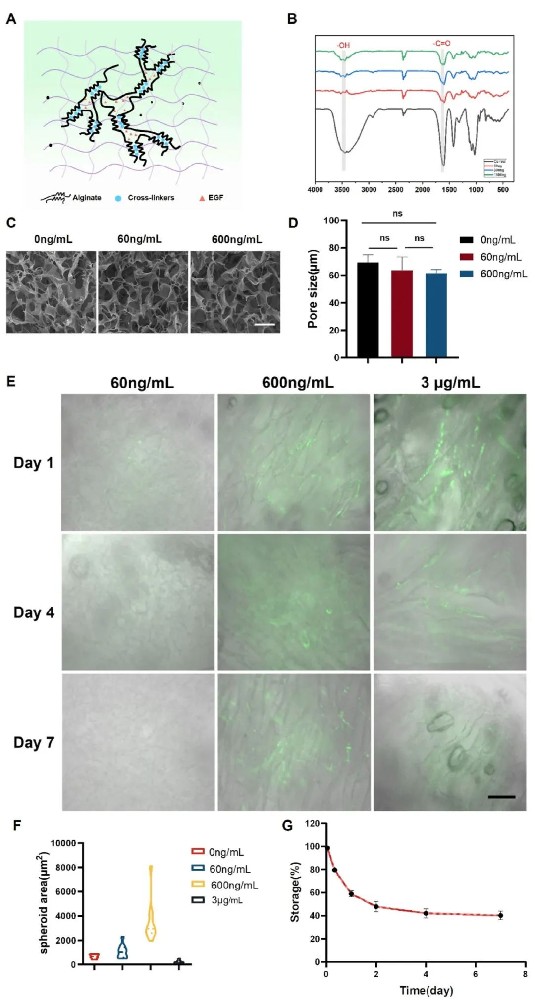
图1 基质结合EGF仿生ECM的构建与表征
2) 基质结合EGF对乳腺癌类器官恶性表型的影响。基质结合EGF显著改变了乳腺癌类器官的多种恶性表型。在细胞增殖方面,EGF(+)组的球体面积从EGF(-)组的2500 μm²显著扩展至近10000 μm²,Ki67阳性增殖指数从41.3% ± 3.8%显著增加至80.9% ± 3.3%。迁移实验显示,基质结合EGF处理后的乳腺癌细胞迁移活性显著增强,24小时和48小时后迁移细胞数分别约为130 ± 22和168 ± 24个/视野,而对照组仅为66 ± 14和100 ± 25个/视野。上皮-间质转化(EMT)分析表明,EGF(+)组中上皮标志物E-钙粘蛋白明显丢失,间质标志物波形蛋白表达增加。此外,基质结合EGF还赋予了乳腺癌细胞抗凋亡能力,TUNEL染色和Caspase-3免疫组化显示凋亡显著减少,流式细胞术分析证实凋亡细胞比例从26.6% ± 3.9%降至19.9% ± 3.8%。
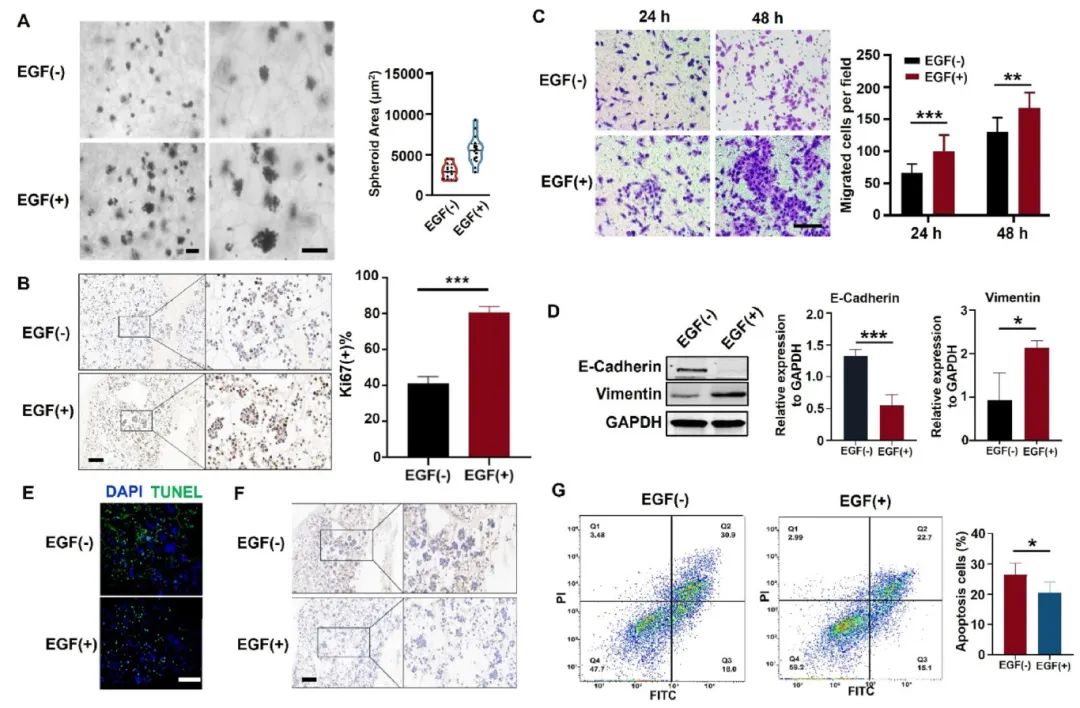
图2 基质结合表皮生长因子在仿生细胞外基质中改变了乳腺癌类器官的恶性表型
3) 基质结合EGF诱导的多药耐药性。基质结合EGF在仿生ECM中诱导了显著的多药耐药(MDR)效应。对四种常用化疗药物的敏感性测试显示,与EGF(-)组相比,EGF(+)组对阿霉素的IC50值从1.93 ± 0.10 μM增加至4.53 ± 0.52 μM,对表柔比星的IC50从0.76 ± 0.08 μM增加至2.64 ± 0.35 μM,对5-氟尿嘧啶的IC50从9.23 ± 0.94 μM增加至13.94 ± 1.39 μM。特别是对紫杉醇,EGF(+)组表现出极强的耐药性,以至于无法测定有效的IC50值。q-PCR分析显示,典型的药物外排转运蛋白ABCG2在EGF(+)组中显著上调,这与获得性MDR密切相关。此外,与DNA损伤耐受相关的H1-2基因表达下调,使乳腺癌类器官对DNA损伤诱导剂更加耐受,这与对阿霉素、表柔比星和紫杉醇增强的耐药性一致。
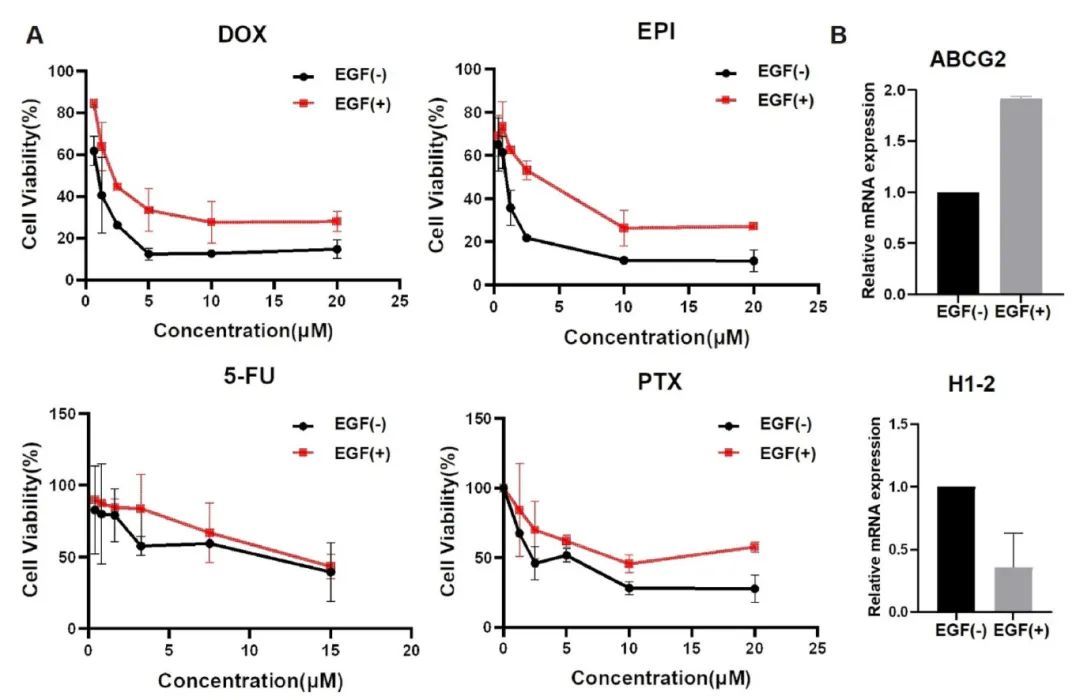
图3 基质结合表皮生长因子在仿生细胞外基质中诱导乳腺癌类器官产生多药耐药性(MDR)
4) 转录组学分析揭示的分子机制。转录组学分析揭示了基质结合EGF诱导恶性表型的分子机制。与EGF(-)组相比,EGF(+)组中291个基因上调,331个基因下调。KEGG分析显示细胞因子-细胞因子受体相互作用和ECM-受体相互作用是前两大富集功能。GSEA分析表明这两个通路中的相关基因主要聚集在上端,显示出普遍的上调趋势。在细胞因子-细胞因子受体相互作用中,IL33、生长分化因子15(GDF-15)和IL-18在EGF(+)组中显著上调,ELISA验证证实了这些促肿瘤细胞因子蛋白浓度的相应增加。在ECM-受体相互作用中,编码基质成分(如纤连蛋白FN1)和识别受体(如整合素家族)的基因表达在EGF(+)组中显著增加。PI3K-AKT信号通路在所有信号通路中富集了最多的差异表达基因,Western blot分析证实了激活信号分子(p-STAT6、p-ERK1/2、p-PI3K、p-AKT、p-mTOR)在EGF(+)组中的显著高表达。
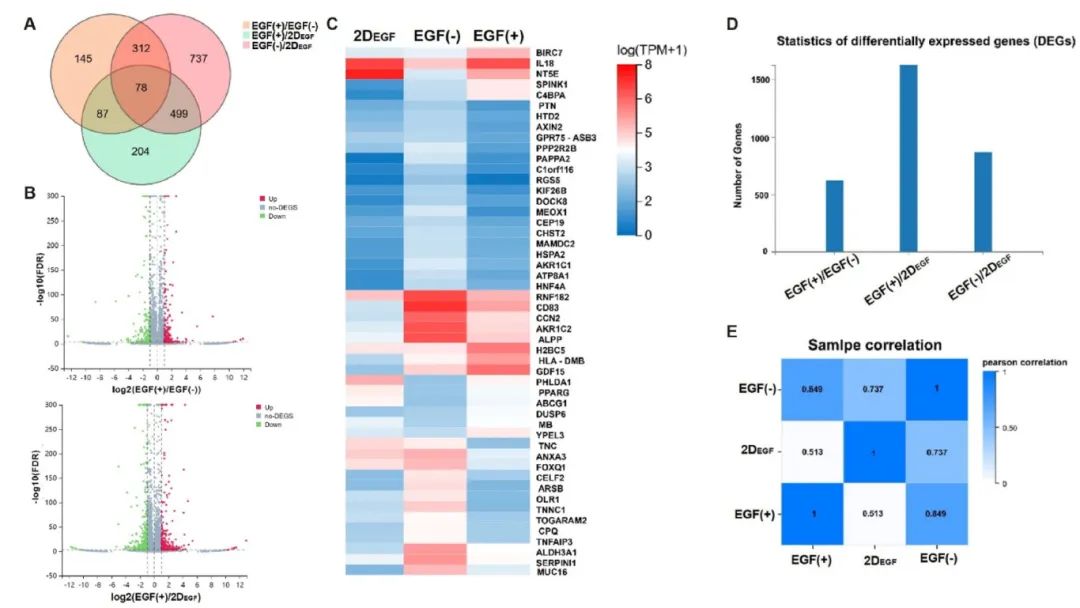
图4 全基因组转录组变化
5) 代谢组学分析发现的生物标志物。代谢组学分析为基质结合EGF诱导恶性表型提供了代谢层面的证据。主成分分析显示两组间代谢物谱存在明显分离,火山图识别出83个差异代谢物,包括53个显著上调(如L-天冬氨酸)和30个显著下调(如烟酰胺)的代谢物。层次聚类分析表明代谢通路和辅因子生物合成是受基质结合EGF影响的主要通路。L-天冬氨酸被发现是这两个通路中的差异调节代谢物之一,在EGF(+)组中显著增强表达。相关性分析显示所选差异表达基因与L-天冬氨酸和4-甲基-5-噻唑乙醇呈正相关,与泛酸和烟酰胺呈负相关。谷草转氨酶2(GOT2)是负责将草酰乙酸转化为L-天冬氨酸的线粒体氨基转移酶,基质结合EGF显著增强了线粒体中GOT2浓度,与细胞内L-天冬氨酸增加一致,表明L-天冬氨酸可能是连接癌症代谢与生长因子生物活性、ECM相互作用和信号通路的潜在生物标志物。
本研究建立了一个创新的体外3D乳腺癌类器官模型,通过海藻酸冷凝胶仿生ECM实现基质结合EGF的控制呈递,为癌症进展研究提供了新的范式。该模型成功模拟了肿瘤-基质微环境中的复杂相互作用,克服了传统2D培养和动物模型的局限性,为癌症生物学研究和药物筛选提供了更加真实可靠的平台。揭示了基质结合EGF通过激活PI3K-AKT信号通路,促进细胞因子-细胞因子受体相互作用和ECM-受体相互作用,最终重编程乳腺癌能量代谢的完整分子机制。这一发现为理解肿瘤微环境中生长因子与ECM协同作用促进癌症进展提供了重要理论基础,有助于开发靶向肿瘤微环境的新型治疗策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:揭示自闭症患者脑类器官中GABA能神经元分化缺陷研究
下一篇:揭示 HAMA-SBMA水凝胶递送软骨类器官促进软骨再生研究