常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-08-26 17:45:04 细胞资源库平台 访问量:421
体外皮肤模型是研究皮肤生物学和疾病的重要工具,但原代细胞存在批次差异、永生化细胞功能异常等问题。诱导多能干细胞(iPSC)衍生的细胞可提供稳定且功能接近天然的细胞来源,但其在构建完整皮肤模型中的应用仍需优化。在此背景下,来自英国杜伦大学团队在《Cells》(2025, 14:1044)发表研究,首次证实 iPSC 衍生的成纤维细胞(iDFs)可构建与原代成纤维细胞相似的真皮等效物,该真皮结构能支持表皮分化,形成具有完整层次的全层皮肤模型,其标志物表达和结构与天然皮肤高度一致,为个性化皮肤模型构建和疾病研究提供了可靠工具。
本研究旨在利用 iPSC 衍生的成纤维细胞构建功能稳定的真皮等效物,并验证其支持表皮形成的能力。通过将 iPSC 分化为成纤维细胞(iDFs),检测其表型与原代人真皮成纤维细胞(HDFns)的一致性;利用 3D 支架培养 iDFs 构建真皮模型,分析其细胞增殖、 extracellular 基质(ECM)沉积;随后接种原代角质形成细胞,评估全层皮肤模型的表皮分化和结构完整性。结果显示,iDFs 能形成类似 HDFns 的真皮结构,支持表皮分层分化,关键标志物(如角蛋白 10、14、兜甲蛋白)定位正确,为 iPSC 在皮肤工程中的应用提供了实验依据。
体外皮肤模型依赖于合适的细胞来源、支架和生长因子。原代细胞虽功能接近天然,但需反复分离,存在批次差异;永生化细胞虽稳定,但常因基因突变导致功能异常。iPSC 可无限增殖且能分化为功能接近原代的细胞,是理想的替代来源。
此前的 iPSC 皮肤模型存在表皮结构不完整、分化标志物表达异常等问题,部分模型缺乏天然皮肤的层次结构。本研究聚焦 iPSC 衍生的成纤维细胞,旨在构建能支持表皮正常分化的真皮等效物,解决现有模型的结构和功能缺陷,为构建更接近天然的全层皮肤模型奠定基础。
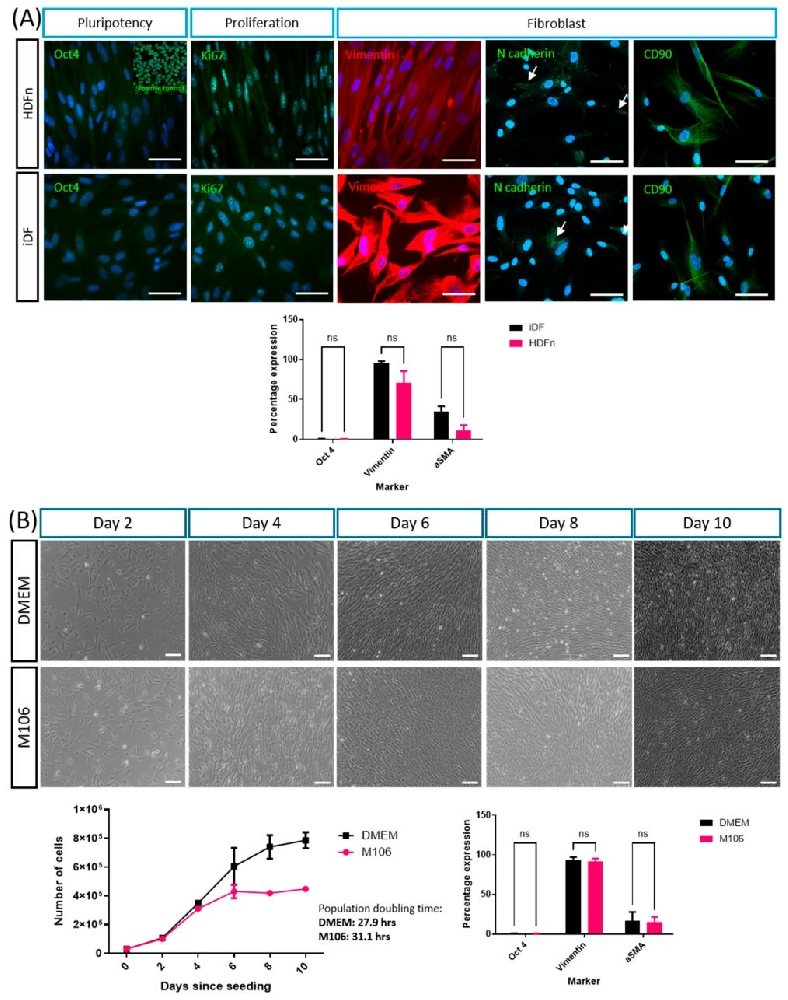
图 1:iPSC 衍生成纤维细胞(iDFs)的表型与原代细胞相似
该图验证 iDFs 的成纤维细胞特性:免疫荧光显示,iDFs 不表达多能性标志物 Oct4(排除干细胞表型),但高表达增殖标志物 Ki67 及成纤维细胞特异性标志物 vimentin、N - 钙粘蛋白、CD90,与原代 HDFns 表型一致。流式细胞术进一步证实 iDFs 不表达 Oct4,vimentin 阳性率高,α- 平滑肌肌动蛋白表达低,且在原代细胞培养基(M106)中仍维持该表型。生长曲线显示,iDFs 在 M106 中可增殖,群体倍增时间(31.1 h)略长于其推荐培养基(DMEM,27.9 h),但细胞数量随时间稳定增加,表明其适应原代细胞培养体系。
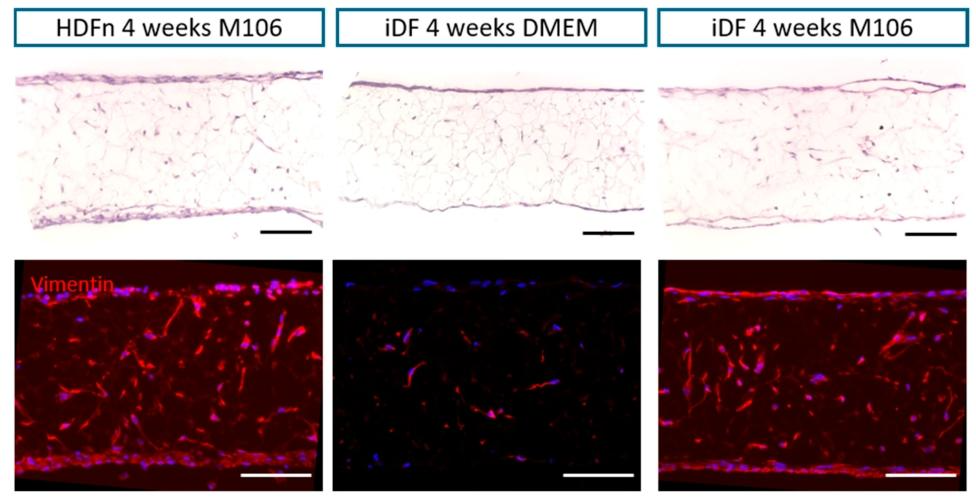
图 2:iDFs 在支架中迁移形成三维真皮结构
该图显示 iDFs 在 4 周培养期内迁移进入多孔支架,在支架上下层形成细胞层,与 HDFns 构建的真皮模型结构相似。免疫荧光显示 vimentin 阳性细胞遍布整个支架,证实细胞成功填充孔隙。两种培养基(DMEM 和 M106)均能支持真皮结构形成,为与原代模型直接对比,后续实验选用 M106 培养基。
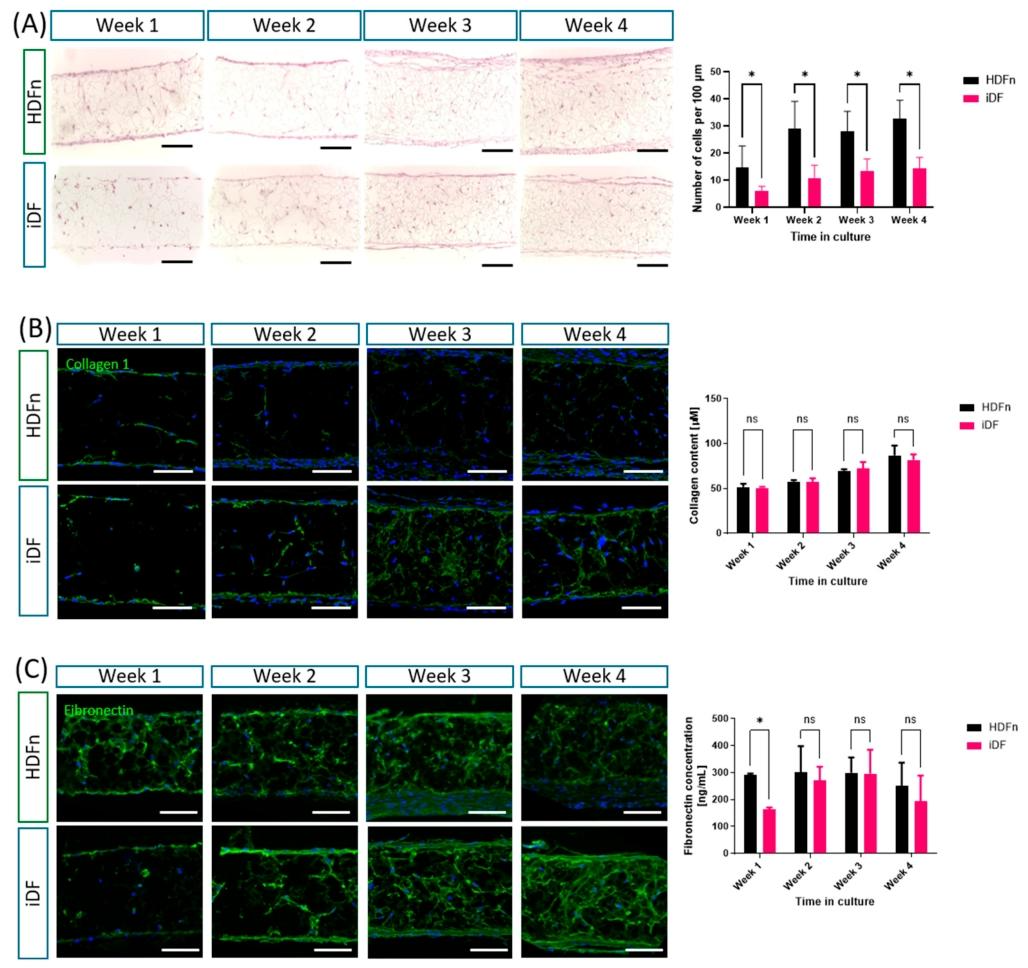
图 3:iDFs 的细胞增殖与 extracellular 基质沉积
该图对比 iDFs 与 HDFns 真皮模型的动态变化:iDFs 数量随培养时间增加,但始终约为同期 HDFns 的 1/2,支架边缘细胞层数较少。免疫荧光和定量分析显示,iDFs 模型中胶原 I 分布均匀,羟脯氨酸检测(总胶原)显示其含量与 HDFns 模型无显著差异,且随时间稳步增加。纤连蛋白通过免疫荧光和 ELISA 检测,其在 iDFs 模型中的沉积量与 HDFns 模型相近,表明尽管细胞数量较少,iDFs 仍能有效合成关键 ECM 成分。
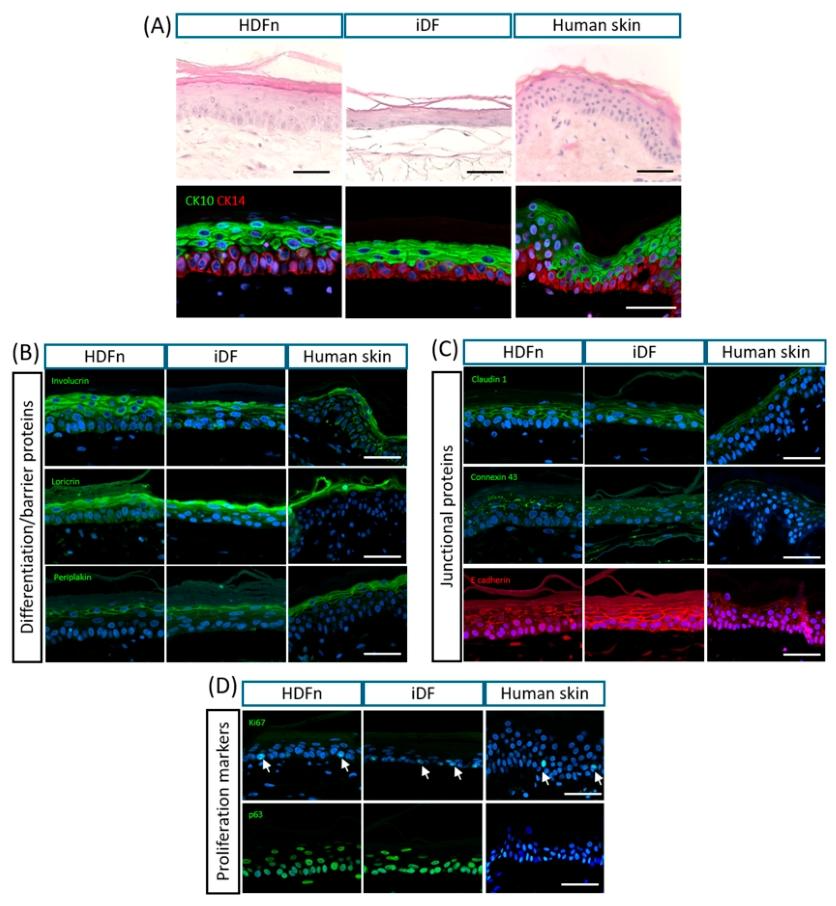
图 4:iDFs 真皮模型支持全层皮肤结构形成
该图验证 iDFs 真皮模型对表皮的支持能力:接种原代角质形成细胞后,iDFs 模型形成具有极性基底层和角质层的表皮,H&E 染色显示其结构与 HDFns 模型及天然皮肤相似(虽整体略薄)。免疫荧光显示,基底层特异性角蛋白 14 和棘层特异性角蛋白 10 定位正确,表明表皮分层分化正常;屏障蛋白(兜甲蛋白、 involucrin、periplakin)定位于上层,连接蛋白(E - 钙粘蛋白、Claudin-1、Connexin 43)表达正常,证实表皮屏障功能完整;基底层 Ki67(增殖标志物)和 p63(干细胞标志物)阳性,表明其维持增殖能力,与天然皮肤一致。
本研究首次证实 iPSC 衍生的成纤维细胞可替代原代细胞构建功能稳定的真皮等效物,解决了原代细胞批次差异和永生化细胞功能异常的问题。与此前 iPSC 皮肤模型相比,本模型优势在于:① 真皮结构依赖内源性 ECM,未使用外源性蛋白基质,更贴近天然皮肤微环境;② 表皮分层清晰,屏障蛋白和连接蛋白定位准确,克服了部分模型表皮结构紊乱的缺陷。
局限性包括:ECM 成分分析可进一步通过蛋白质组学深化;模型仅包含成纤维细胞和角质形成细胞,未来可加入黑素细胞、免疫细胞等,甚至构建含皮肤附属器的复杂模型。此外,使用原代角质形成细胞限制了模型的全 iPSC 来源,下一步可尝试 iPSC 衍生角质形成细胞,实现完全个性化皮肤模型。
iPSC 衍生的成纤维细胞(iDFs)表型与原代人真皮成纤维细胞一致,可在 3D 支架中形成具有内源性 ECM 的真皮等效物,其胶原 I 和纤连蛋白沉积量与原代模型相近。该真皮结构能支持原代角质形成细胞分化,形成分层完整、标志物定位正确的全层皮肤模型,结构与功能接近天然皮肤。本研究为利用 iPSC 构建个性化皮肤模型、研究皮肤疾病及筛选药物提供了可靠方法。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:HA 与 SP 协同发力!这款复合凝胶促进口腔组织愈合,1:0.5 比例表现最优
下一篇:牛肠道研究新工具!永生化回肠上皮细胞系建立,功能与原代细胞一致