常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-08-25 12:39:52 细胞资源库平台 访问量:258
类器官技术是一个吸引众多研究者关注的新兴领域。"类器官"是"器官"与"-oid"的组合词,指干细胞衍生的三维组织,能够重现体内发育过程和组织特异性功能。类器官通常源自多能干细胞(包括诱导多能干细胞和胚胎干细胞)或组织干细胞。2008年首次报道的人类三维脑组织被认为是"神经类器官"的开创性工作。神经类器官提供了活体人类神经组织,为研究人类发育、神经科学、神经和精神疾病以及进化提供了机会。
神经类器官可以说是发育生物学过程在培养皿中的"剪切和粘贴"。因此,理解神经类器官的背景需要发育知识,但目前的类器官研究更多将类器官作为工具来研究特定目标。这使得类器官研究更加方法论化,对于大多数新进入该领域的研究者来说,类器官方法的改进或精细化仍然困难。神经类器官的历史悠久,其主要工作由Sasai和同事完成。在早期阶段,实现了从多能干细胞的二维神经细胞诱导,包括中脑多巴胺能神经元和视网膜色素上皮。随后在2005年,Sasai和同事首次报道了三维脑组织的诱导。
从二维到三维的转换充满了偶然性。在分析二维神经诱导机制的过程中,他们发现了几个候选因子。在尝试用这些因子诱导神经元的过程中,他们寻求不诱导神经元的阴性对照条件。由于贴壁的二维神经诱导方法需要饲养细胞和血清,Sasai和同事采用了严格的阴性对照:在没有饲养细胞和血清的情况下悬浮培养小鼠胚胎干细胞。意外的是,分离的小鼠胚胎干细胞形成了具有大脑皮层特征的自组织聚集体。
近期,发布在European journal of cell biology期刊,题为Self-organization and applications of neural organoids的研究首先回顾神经类器官研究如何从发育生物学中萌芽的简史,继而重点介绍神经类器官生成过程中区域与结构自组织等引人入胜的特性。作为该领域的开拓者,该综述还以海马类器官为例,阐释如何通过方法论创新培育新型区域特异性类器官。在结构自组织方面,以展示皮层板层结构的脑类器官为例进行说明。通过呈现相关科学发现与前沿认知,该综述旨在为致力于开发新型神经类器官的研究者提供方法论指引。
1) 海马类器官的区域化自组织生成
海马是长期记忆形成的中心,负责学习等长期任务和记住姓名等短期任务。特异性区域化可以通过神经发育相关信息实现。由于大脑皮层位于前脑的最前部,大脑类器官的诱导过程从诱导组织的前化开始。大脑类器官诱导的前18天涉及TGF-β抑制剂活性(增强神经诱导)和WNT抑制剂活性(抑制后化)。因此,该过程的早期阶段主要指定为区域性前脑诱导。
在小鼠大脑中,脉络丛的背内侧部分产生BMPs和Wnt蛋白作为背化因子,位于脉络丛旁边的皮层边缘表达Wnt蛋白,诱导内侧苍白球(未来海马)的病变。基于这些信息,研究者采用了两步策略:1.强烈背化而不导致细胞死亡以创建脉络丛;2.在强烈条件下适当调节背化以创建海马区域。研究发现,当从第18-27天添加背化因子时,即使去除这些因子,类器官仍形成脉络丛。然而,当因子仅添加3-6天(第18-21天或18-24天)时,类器官显示出光滑的神经上皮和小的脉络丛区域。
2) 大脑类器官的层形成自组织
大脑类器官的层形成相关的自组织是神经类器官研究的另一个有趣方面。皮层神经上皮细胞在大脑发育过程中表现出独特的细胞分裂模式。它们首先通过对称分裂进行自我更新,然后转化为称为放射状胶质的神经祖细胞。放射状胶质具有在软脑膜表面的顶端突起,通过不对称细胞分裂产生有丝分裂后神经元,产生一个祖细胞和一个神经元。不同类型的皮层神经元按顺序产生,沿着放射状胶质的顶端突起迁移,然后以由内向外的方式定居在皮层板的适当层板中。
使用SFEBq方法,大脑类器官可以重现皮层发生的早期步骤。在人类多能干细胞中,大脑类器官在第18-20天开始表达Foxg1(约占总细胞的75%)。大多数Foxg1+神经上皮细胞表达Pax6,获得放射状胶质的身份。Reelin+ Cajal-Retzius细胞(第I层神经元)在第30天左右产生,随后产生Tbr1+/Ctip2+深层神经元(第V和VI层神经元),以及第50天后Satb2+上层神经元(第II-IV层神经元)的分化。这一过程反映了体内顺序神经元生成。
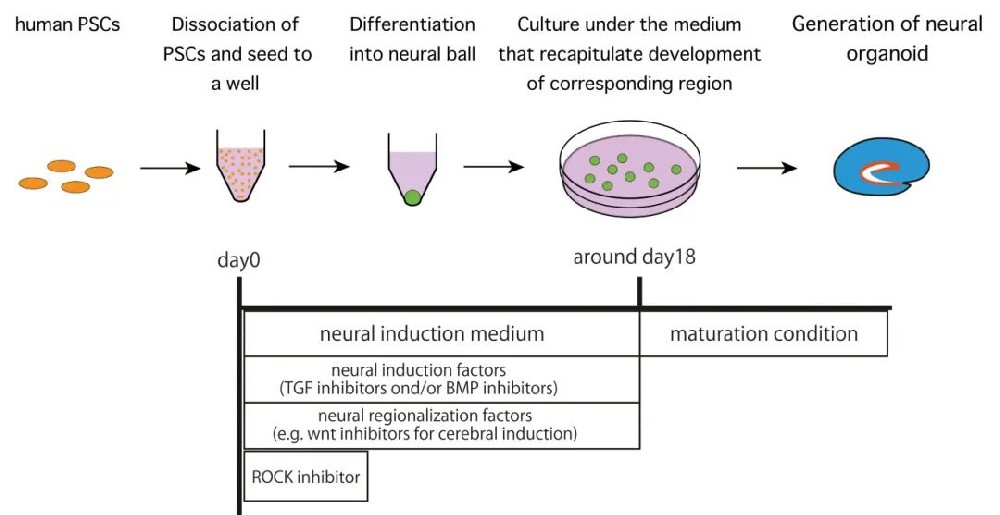
图1 快速聚集的胚状体样聚集体(SFEBq)无血清漂浮培养生成神经类器官
3) 皮层类器官的区域化和物种特异性祖细胞
大脑类器官还重现了其结构内的头尾轴形成。在早期发育过程中,COUP-TF1在大脑皮层中以尾高到吻低的梯度表达,而Sp8则以相反方向表达。FGF8被广泛认为是通过调节这些转录因子的表达来进行皮层区域化的关键参与者。有趣的是,大脑类器官的神经上皮也显示出Coup-TF1的梯度表达和SP8的反向表达。外源性FGF8处理导致SP8的广泛表达,以牺牲Coup-TF1表达为代价。
三维皮层组织的诱导允许检查人类外侧放射状胶质(oRG)样细胞。皮层发生的基本机制在哺乳动物皮层中是保守的,但灵长类皮层与啮齿动物皮层相比表现出不同的特征。最显著的组织学差异是脑室下区(SVZ)的厚度。灵长类(特别是人类)皮层具有高度扩展的SVZ,分为内侧和外侧SVZ。在人类大脑类器官中,70天后VZ外出现大量Pax6+/Sox2+/Tbr2-祖细胞。这些细胞具有基底突起但没有顶端突起,类似于体内oRG细胞。
4) 长期培养和结构复杂性
一般来说,大脑类器官的长期培养会导致聚集体中心部分的氧气和营养物质匮乏,阻碍结构稳定性,并在大约50天的培养后导致细胞死亡。为了克服这一限制,Sasai和同事使用40%氧气和营养补充的培养基,而Knoblich和同事使用旋转烧瓶培养。这两项早期研究表明,大脑类器官可以生长数月,允许诱导相当于人类发育第二个三月期的皮层组织。
在第70天,人类大脑类器官中的皮层层增加厚度并开始显示形态学分层结构。层标记表达模式揭示了复杂的层分离。在顶端侧,Pax6+/Sox2+ VZ在内侧形成,而Tbr2+中间祖细胞形成与VZ相邻的SVZ。最表面的层是边缘区(MZ),含有Reelin+ Cajal-Retzius细胞。在MZ下方,皮层神经元形成皮层板。在第30-50天,皮层板主要由Tbr1+和Ctip2+早生/深层神经元组成,但从第50-100天,它也含有几个Satb2+/Brn2+晚生/表层神经元。
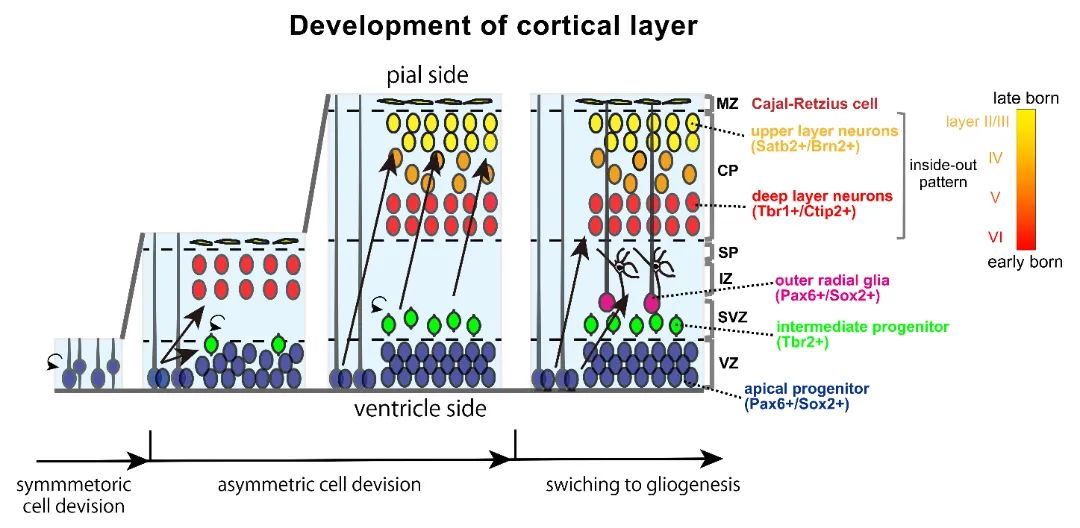
图2 皮质层的发育
总之,神经类器官技术的发展为人类神经科学研究开辟了新的道路。这种技术提供了前所未有的机会来研究人类特异性的大脑发育过程,特别是那些在动物模型中难以复现的特征。类器官模型在神经退行性疾病和神经精神疾病建模方面具有巨大潜力,这些疾病往往缺乏有效的治疗选择。此外,该技术在药物筛选研究中也显示出强大的应用前景。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:表面增强拉曼光谱技术监测人脑类器官中阿尔茨海默病生物标志物及APOE-tau轴的动态变化
下一篇:皮肤组织工程新突破!SA 修饰纤维蛋白水凝胶更稳定,轻松构建 3D 皮肤模型