常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-08-11 09:00:50 细胞资源库平台 访问量:403
人类多能干细胞(hPSCs)具有分化为多种细胞类型的能力,包括心肌细胞、肝细胞和各种血管细胞。虽然hPSCs可用于创建类器官,但同时分化器官关键细胞类型与新生血管系统仍是一个重大挑战。血管化类器官的创建对于避免中心坏死、实现更大规模的器官生长以及提高移植类器官的存活率至关重要。
由于伦理限制和获取早期发育阶段人类胚胎的技术困难,我们对人类器官血管化最早阶段的了解非常有限。模式生物虽然为器官血管化的最早阶段提供了见解,但人类特异性信息仍然缺乏。hPSCs已被证明可以模拟发育的关键方面,包括原条形成、原肠胚形成、胚层形成和特定器官细胞类型的创建。几何微图案化技术使这些发育过程的可重复和可扩展建模成为可能。
目前虽然已有研究探索了类器官血管化的多种方法,但同时分化器官关键细胞类型与具有强大分支、分层组织和管腔形成的新生血管系统尚未完全实现。这突出了类器官研究的一个主要瓶颈。因此,开发能够模拟人类发育最早阶段(对应于体内人类发育的前3周,Carnegie阶段9和10)的心脏和肝脏血管化的体外模型具有重要意义。
斯坦福大学医学院吴庆明(Joseph C. Wu)教授团队在 Science 上发表了一篇题为Gastruloids enable modeling of the earliest stages of human cardiac and hepatic vascularization的研究论文,该研究建立了第一个能够模拟人类心脏和肝脏血管化最早阶段的体外模型系统,为理解器官血管化的分子机制提供了重要工具。该模型的创建填补了人类早期发育研究的重要空白,特别是在伦理限制下无法获得早期人类胚胎的情况下。
1,微图案化技术建立空间组织的原肠胚样结构和心血管祖细胞系统:研究团队使用几何微图案化技术成功建立了可重复且可扩展的空间组织胚层形成系统。通过hESC-RUES-GLR报告细胞系,他们观察到微图案化的hPSCs能够产生组织化的胚层,在4μM CHIR诱导下,中央BRA+中胚层区域被SOX17+内胚层环包围,而SOX2+外胚层缺失。使用hESC-NKX2-5-eGFP细胞系验证了心血管祖细胞的组织化形成。单个NKX2-5-eGFP微图案在10天分化后产生了组织化的环形eGFP+心血管祖细胞,进而发育为搏动的心肌细胞。这一系统为筛选心血管类器官(cVO)形成条件提供了基础。
2,三重报告细胞系的创建及血管化条件的优化筛选:为了便于筛选各种分化条件,研究团队创建了hESC三重报告细胞系(hESC-3R),包含TNNT2启动子驱动的GFP识别心肌细胞、CDH5启动子驱动的mOrange识别内皮细胞,以及TAGLN启动子驱动的CFP识别平滑肌细胞。通过筛选34种不同的分化条件,研究发现条件32产生了最多的心肌细胞、内皮细胞和平滑肌细胞。该条件包含特定的小分子和生长因子组合:CHIR(5μM)、FGF2、IWR、VEGF、SB431542、血管生成素-1和-2、PDGF-BB以及TGF-β1,这些因子在特定时间点添加以促进血管形成、血管生成和血管成熟。
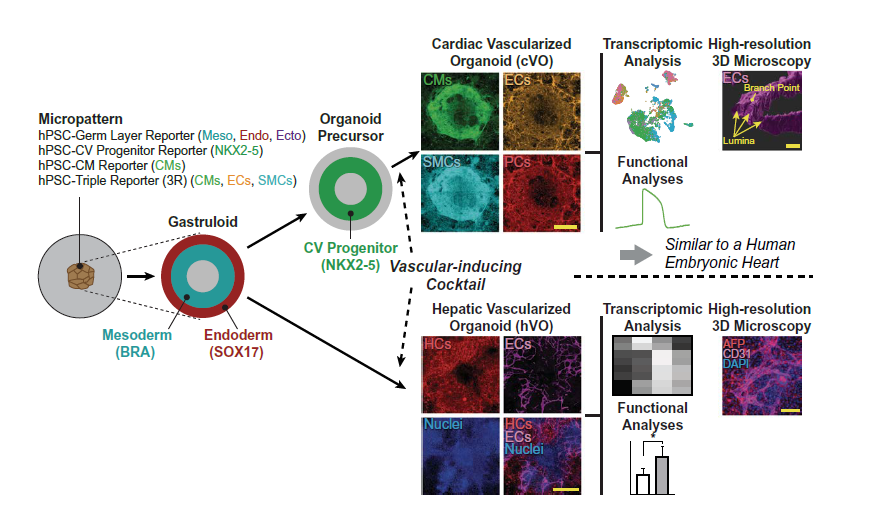
图1 对四个hPSC报告细胞系进行微图案化处理,可促使原肠胚样结构、心血管前体细胞以及 cVO的形成
3,心脏血管化类器官的细胞组成及功能特征分析:单细胞RNA测序分析显示,cVOs包含多种心肌、血管、心内膜、心外膜和神经元细胞类型,与6.5周后受孕(PCW)人类胚胎心脏具有相似的整体细胞组成。bulk RNA测序和加权基因共表达网络分析(WGCNA)表明,血管化基因在cVOs中表达最高,在第16天达到峰值。cVOs表现出分支的内皮细胞与心肌细胞和平滑肌细胞密切结合,形成了直径4-40μm的血管分支网络,具有管腔形成和功能性血管特征。功能分析显示,cVOs的搏动频率较对照组慢,但具有更长的电、钙和收缩持续时间,同时一氧化氮分泌显著增加。
4,NOTCH和BMP信号通路在血管化中的关键作用:为了探索血管化的分子机制,研究团队检验了NOTCH和BMP信号通路的作用。使用NOTCH通路拮抗剂DAPT处理显示,NOTCH通路抑制以剂量非依赖性方式减少了内皮细胞形成,同时也显著减少了心肌细胞形成。BMP通路拮抗剂Dorsomorphin的处理结果显示,BMP抑制对内皮细胞的负面影响比对心肌细胞更为明显,表明这两个通路在血管化过程中具有不同的调节作用。scRNA-seq数据显示,NOTCH-DLL-JAG受体-配体对在心肌细胞、内皮细胞和平滑肌细胞之间的相互作用在6.5-PCW人类心脏中比cVO中更为活跃,提示NOTCH通路活性随血管化和成熟增加而增强。
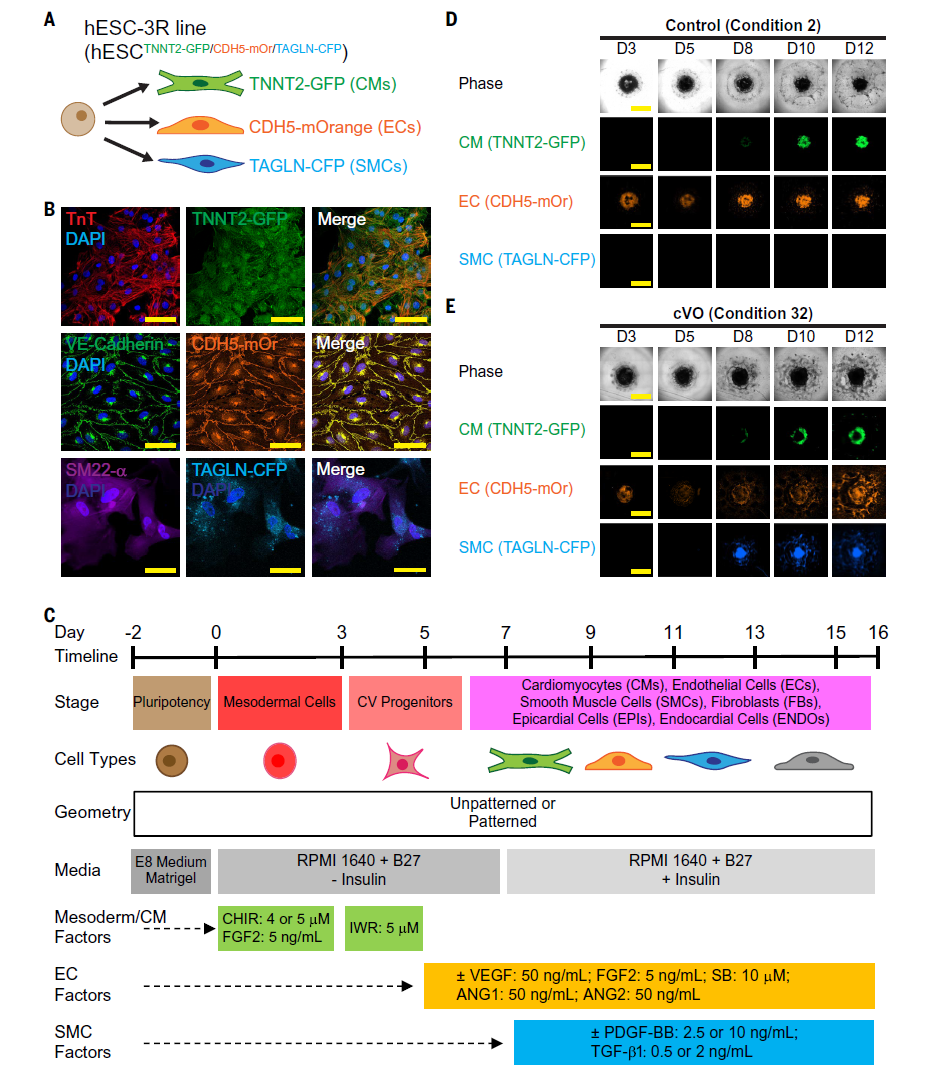
图 2 三重报告细胞系的构建可用于筛选诱导 cVO 形成的分化条件
5,肝脏血管化类器官的成功创建及血管特征:研究团队将相同的血管诱导策略应用于肝脏系统,成功创建了肝脏血管化类器官(hVOs)。通过诱导中内胚层,然后共分化血管祖细胞和肝母细胞池来产生内皮细胞、平滑肌细胞和肝细胞。bulk RNA-seq分析显示,hVO-D3组(第3天开始添加血管化因子)的肝细胞(SERPINA1和HGF)、胆管细胞(HNF1B)、内皮细胞(CDH5)和平滑肌细胞(TAGLN)基因表达最为上调。hVOs包含具有肝窦内皮细胞(LSEC)表型的血管系统,表现为THBD和LYVE标记物与CD31+/CDH5-mOrange+内皮细胞共定位。值得注意的是,hVO血管系统的平均分支长度、直径和体积均显著大于cVO血管系统。
6,药物致畸性测试的概念验证研究:为了展示该系统在药物安全性评估中的潜在应用,研究团队测试了芬太尼对血管化的影响。芬太尼是一种强效阿片激动剂,可能在妊娠期被滥用。与DAPT或多索吗啡不同,芬太尼在10nM浓度下显著增加了内皮细胞形成,这与芬太尼激活多种促血管生成信号通路的已知作用一致。这一结果证明了该体外模型在预测新药和现有药物致畸风险方面的潜在价值,特别是在人类妊娠前几周这一发育"黑箱"期间。
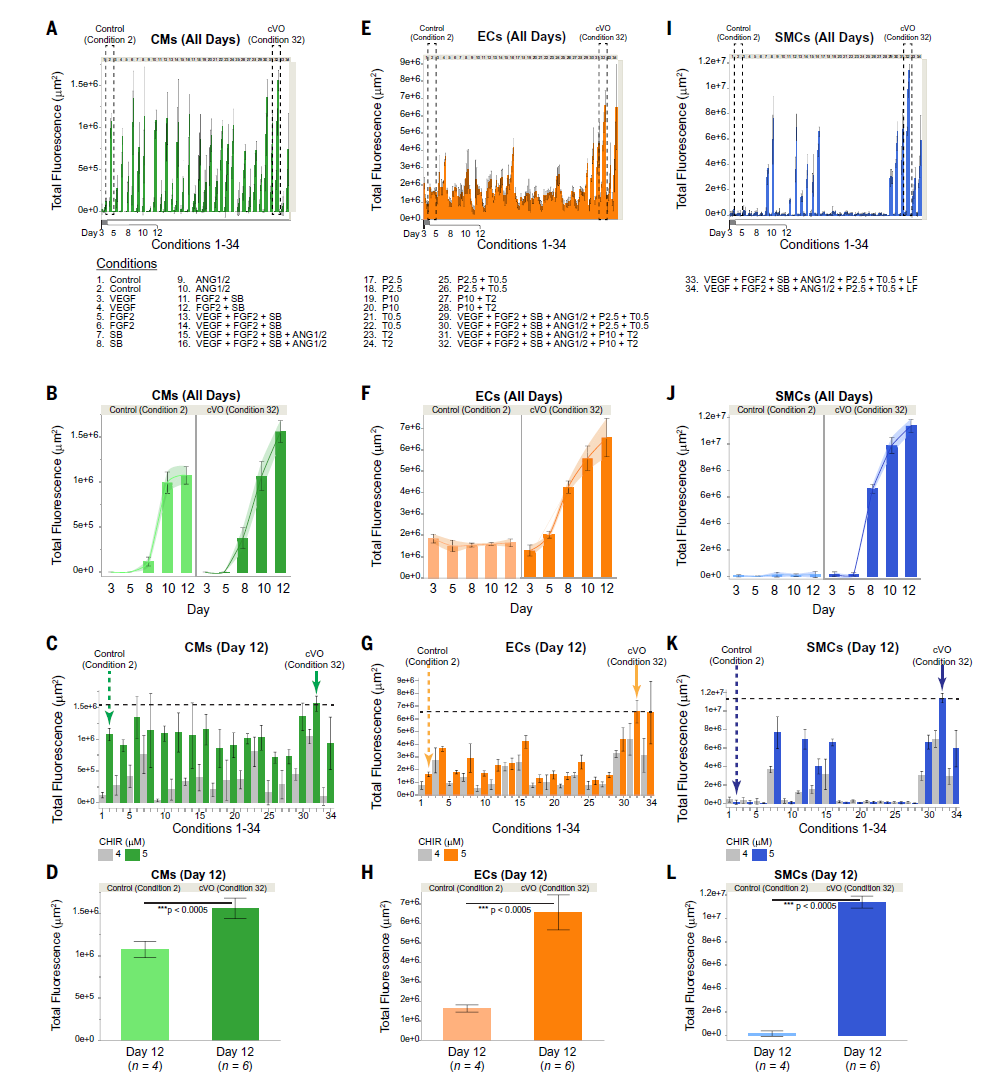
图 3 筛选确定了一种可同时产生心肌细胞、内皮细胞和平滑肌细胞以形成 cVOs 的分化条件
该研究发现的保守性发育程序表明,相同的血管诱导因子组合可用于不同器官系统的血管化,这为开发其他血管化类器官提供了基础。该模型在再生医学、疾病建模和药物筛选方面具有广泛应用前景。特别是在药物致畸性评估方面,该系统能够预测新药和现有药物在人类妊娠早期的潜在风险,为药物安全性评估提供了新的平台。此外,该研究为心脏疾病建模提供了新的工具,可用于研究先天性心脏病、心力衰竭等疾病的发病机制。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:心脏糖原自噬研究新突破:从抗体验证到通量检测的完整工具包
下一篇:从患者 iPSC 衍生视网膜类器官中无设备分离感光细胞