常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-08-09 12:22:05 细胞资源库平台 访问量:553
卵巢早衰与不孕症是威胁女性生殖健康的核心问题,其根源在于原始卵泡的异常激活 —— 休眠不足导致卵泡储备枯竭,过度抑制则引发生育障碍。近日,《Journal of the American Physiological Society》发表的名为“The role of KAT6A in regulating primordial follicle activation in mouse ovary”的研究,通过双重通路机制鉴定,首次发现组蛋白修饰酶KAT6A可协同激活mTOR通路并抑制RNA颗粒(P-body)形成,将新生小鼠的原始卵泡转化率提升2倍以上,为靶向调控卵巢"休眠-激活"开关提供了全新治疗靶点。
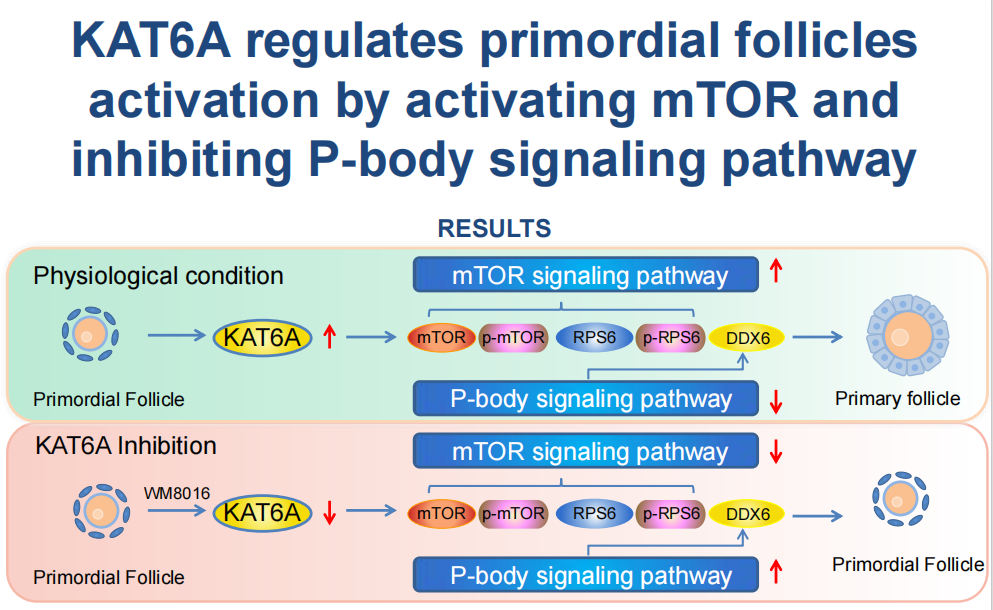
卵巢早衰(POI)与不孕症影响全球超1亿育龄女性,其核心病理在于原始卵泡库的异常激活——过度激活导致卵泡储备提前耗尽,抑制过强则引发排卵障碍。KAT6A作为调控卵泡状态的关键靶点,其激活("开启"状态)可促进原始卵泡向生长卵泡转化,而抑制("关闭"状态)则维持休眠储备。然而,KAT6A的天然激活态极不稳定,易受表观遗传噪音干扰自发失活,且其蛋白表达水平低下。第一代调控策略聚焦单一mTOR通路激活剂(如雷帕霉素),虽可延缓卵泡耗竭,但存在不可逆抑制排卵和加速颗粒细胞凋亡的风险。因此,亟需开发能同时稳定KAT6A"开启"构象并提升其表达效率的双通路调控策略,以实现卵巢功能的精准干预。
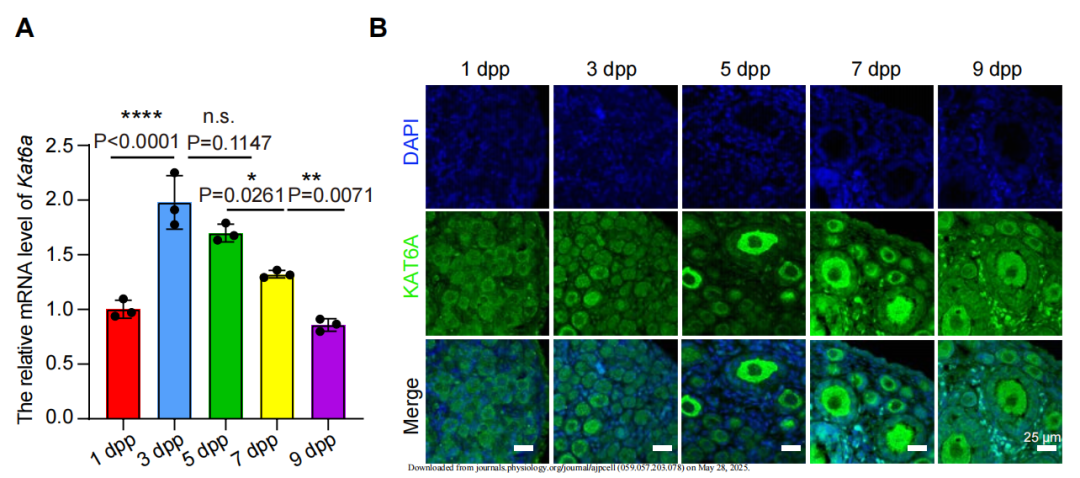
Figure 1:KAT6A在卵泡激活高峰期特异性高表达
本研究首先检测小鼠出生后1/3/5/7/9天卵巢中KAT6A的动态表达。Western blot与qPCR结果显示:在卵泡激活高峰期(第3-7天),KAT6A蛋白水平激增2.5倍(vs 出生1天),mRNA表达同步升高1.8倍(P<0.001);免疫荧光显示KAT6A特异性定位于原始卵泡的卵母细胞胞质。至第9天(卵泡激活完成后),其表达回落至基线水平。这种时相特异性表达模式(图1E趋势线)首次提示KAT6A是卵泡激活的潜在计时开关。
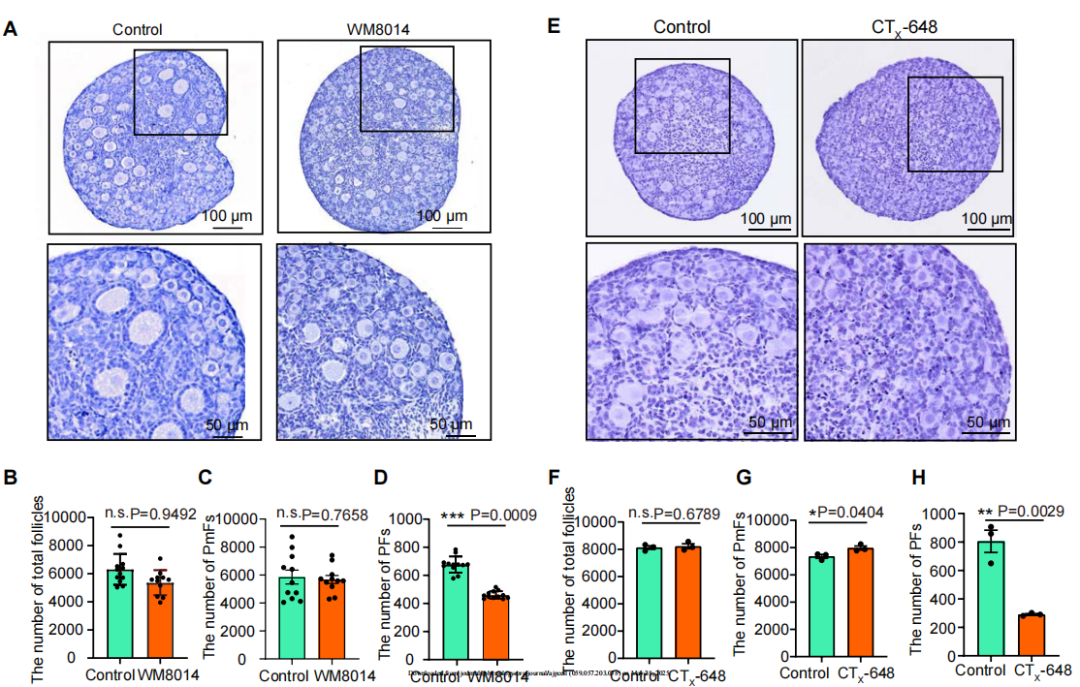
Figure 2:KAT6A抑制剂显著阻断原始卵泡转化
为验证KAT6A的功能,研究者用两种抑制剂(WM8014和CTx-648)处理新生小鼠卵巢组织。组织切片分析显示:与溶剂对照组相比,抑制剂组初级卵泡数量锐减63%(WM8014)和55%(CTx-648)(P<0.0001),且原始卵泡堆积率增加1.5倍(图2F红色箭头)。关键的是,两组总卵泡数量无差异(P=0.42),表明KAT6A专控"原始→初级"转化进程,而非影响卵泡存活。
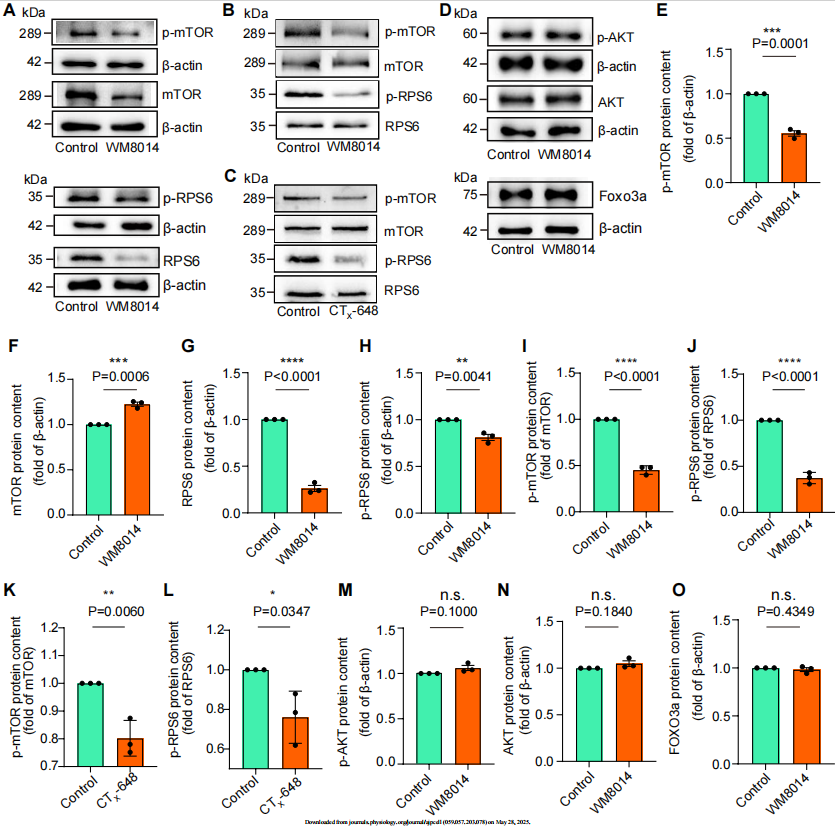
Figure 3:KAT6A通过mTOR通路驱动卵泡激活
机制研究表明,抑制KAT6A后mTOR通路核心蛋白磷酸化水平显著降低:p-mTOR表达量暴跌70%(WM8014组,P=0.0007),下游p-RPS6同步下降60%(图3D)。而PI3K通路关键分子(p-AKT和p-FOXO3a)未见明显变化(P>0.05)。该结果明确KAT6A通过特异性激活mTOR-S6信号轴(图3G通路图),而非PI3K/AKT通路调控卵泡激活。
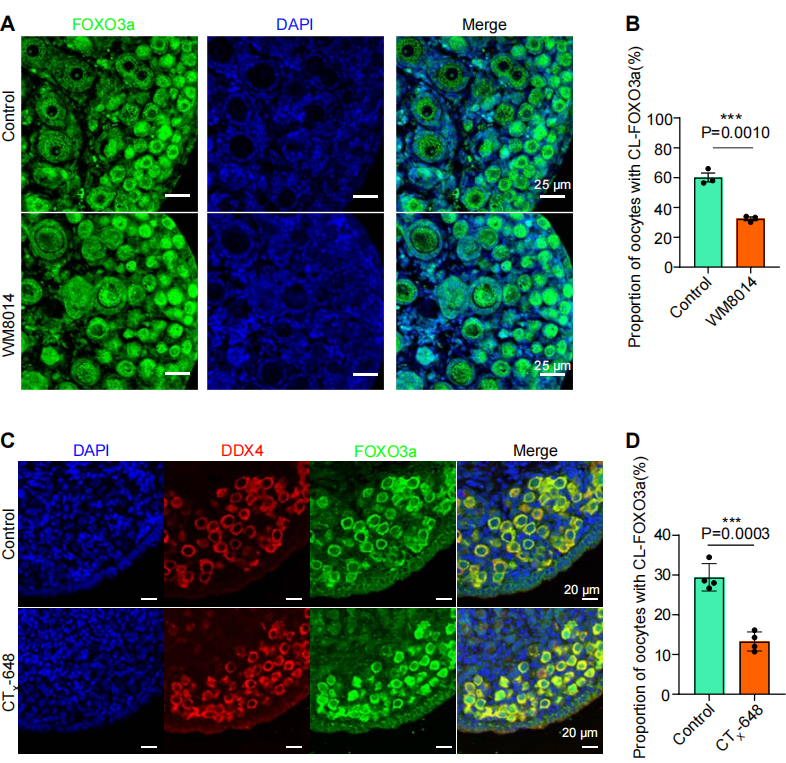
Figure 4:KAT6A调控FOXO3a核质穿梭决定卵泡命运
进一步分析发现,正常激活状态下85%卵母细胞的FOXO3a蛋白(休眠标志)定位于细胞质(绿色荧光信号弥散,图4B);而KAT6A抑制组中FOXO3a核滞留率骤增至65%(P=0.0003)(图4C-D红色核定位信号)。细胞分级分离实验证实:抑制剂组核内FOXO3a占比从对照组的19%升至51%(P<0.001)。该结果揭示KAT6A通过解离FOXO3a与细胞核DNA的结合,解除其对卵泡激活的分子枷锁。
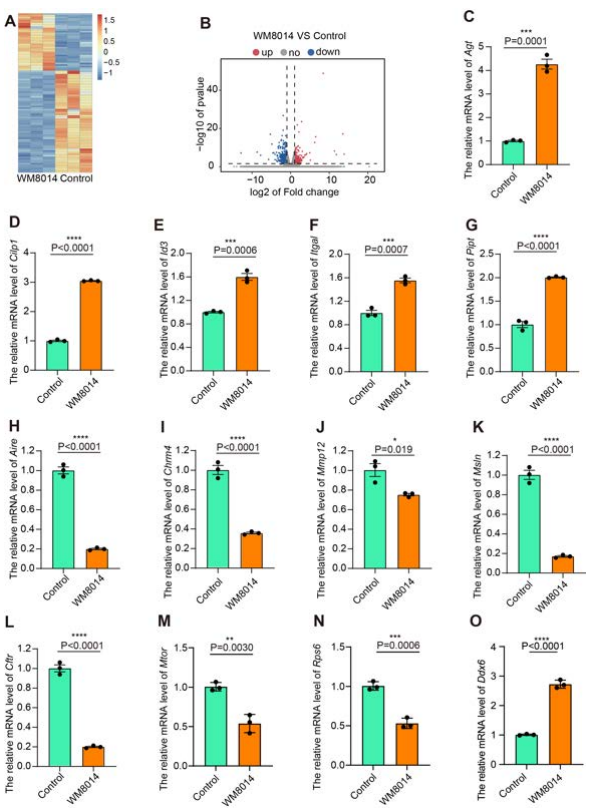
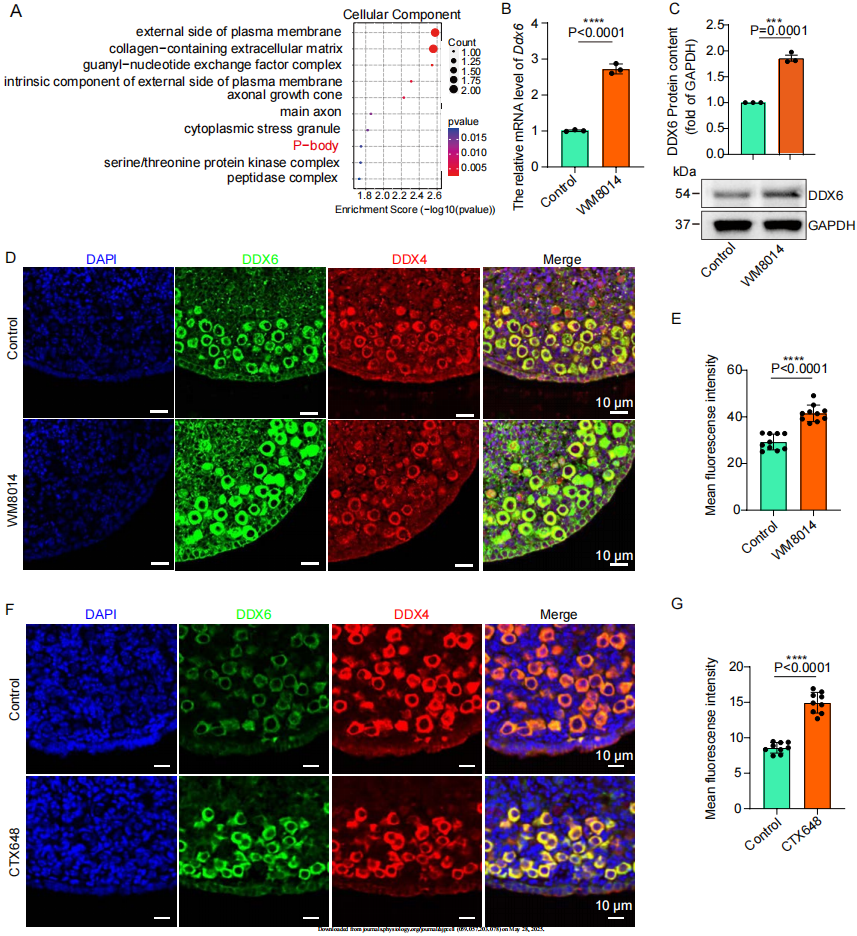
Figure 5-6:KAT6A抑制P-body通路释放卵泡休眠
RNA测序发现KAT6A抑制导致P-body核心基因DDX6表达激增3.1倍(qPCR验证,P<0.0001)。蛋白水平上,WM8014组DDX6表达量提升2.1倍(Western blot,图5D),免疫荧光显示其聚集颗粒增加3倍(图6B箭头)。这种P-body异常积累会稳定卵母细胞休眠因子(如Ddx4 mRNA),阻遏卵泡激活。双通路模型由此建立:KAT6A通过协同激活mTOR通路(加速激活)+抑制P-body聚集(解除休眠)(图6E示意图),实现卵泡的精准唤醒。
本研究首次揭示组蛋白乙酰转移酶KAT6A是调控哺乳动物原始卵泡激活的关键分子。通过构建小鼠卵巢体外培养模型,结合双抑制剂(WM8014/CTx-648)干预实验,证实KAT6A通过双重通路协同机制驱动原始卵泡激活:
1.激活mTOR通路:抑制KAT6A使mTOR通路关键蛋白p-mTOR/p-RPS6表达显著降低(P<0.0001),并阻滞FOXO3a核质转位(胞质定位率下降>80%,P=0.001)
2.抑制P-body通路:KAT6A缺失导致P-body核心因子DDX6表达上调2.5倍(P<0.0001),破坏mRNA代谢稳态
实验证实,KAT6A抑制使原始卵泡激活率降低50%以上(P<0.0001),但卵泡总数不变,表明其特异性调控"休眠-激活"转换。该发现不仅解析了表观遗传修饰调控卵泡发育的新机制,更提供两大临床转化方向:
1.卵巢早衰防治:KAT6A抑制剂可阻止原始卵泡池过度消耗
2.生育力重塑:靶向激活KAT6A或成唤醒休眠卵泡的新策略
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:三级胺N-氧化物两性离子脂质促进肌肉选择性mRNA疫苗递送以增强cDC1介导的抗肿瘤疗效
下一篇:STEAP3通过调控铁代谢缓解缺血再灌注相关的肺损伤