常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-07-01 08:58:31 细胞资源库平台 访问量:348
同源异体小鼠肿瘤模型是免疫肿瘤学(I/O)研究中不可或缺的临床前模型,但它们对免疫检查点抑制剂(ICIs)的反应有限,这可能是由于它们的固有低免疫原性。为了解决这一问题,研究人员通过将鸡卵清蛋白(OVA)这一高度免疫原性的蛋白质表达到同源异体肿瘤细胞中,开发了新的免疫原性同源异体模型。这些模型,如DC2.4-OVA和B16-OVA,显示出比它们的亲本细胞系更慢的肿瘤生长速度,这可能是由于免疫介导的排斥反应。更重要的是,这些OVA表达的模型对ICIs,特别是抗PD-1治疗,表现出更高的敏感性,这表明它们在增强T细胞介导的免疫反应方面具有潜力。此外,通过过继T细胞转移实验,研究人员验证了这些模型中存在肿瘤特异性记忆T细胞。这些结果表明,OVA工具细胞不仅增强了对ICIs的反应,而且为临床前免疫治疗评估提供了新的、具有更高免疫原性的同源异体模型,这对于I/O研究具有重要的意义。
英文标题:A scaffold vaccine to promote tumor antigen cross-presentation via sustained toll-like receptor-2 (TLR2) activation
中文标题:通过持续激活 Toll 样受体 2(TLR2)促进肿瘤抗原交叉呈递的支架疫苗
发表期刊:《Bioactive Materials》
影响因子:20.3
作者单位:
1. State Key Laboratory of Quality Research in Chinese Medicine, Institute of Chinese Medical Sciences, University of Macau, Taipa, Macau SAR, China
2. State Key Laboratory of Pharmaceutical Biotechnology, School of Life Sciences, Nanjing University, Nanjing, 210093, China
3. Department of Chemistry, CICECO – Aveiro Institute of Materials, University of Aveiro, Campus Universitário de Santiago, 3810-193, Aveiro, Portugal
作者信息:
Daping Xie, Congwei Han, Chonghao Chen
癌症疫苗虽在肿瘤治疗中潜力巨大,但其临床应用受限于细胞毒性 T 淋巴细胞(CD8+ T 细胞)激活不足。肿瘤抗原需通过主要组织相容性复合体 I 类(MHC-I)呈递给 CD8+ T 细胞(即交叉呈递),而抗原进入抗原呈递细胞(APCs)后常被溶酶体降解,难以实现 MHC-I 呈递。研究表明,细胞内活性氧(ROS)可抑制溶酶体蛋白酶并促进抗原逃逸至胞质,进而增强交叉呈递。然而,现有 ROS 诱导方法存在选择性差、需额外佐剂、ROS 动力学难以调控等挑战。本研究设计三维(3D)可注射支架疫苗,通过持续激活 TLR2 诱导最佳 ROS 动力学,促进抗原交叉呈递,以触发强效抗肿瘤免疫响应。
研究人员首先合成乙酰葡甘露聚糖(acGM)作为 TLR2 激动剂,通过双乳化法将模型抗原卵清蛋白(OVA)或肿瘤特异性抗原(TSA)包裹于 acGM 中,构建 OVA@acGM 或 TSA@acGM 纳米颗粒。随后,对透明质酸(HA)进行疏水修饰(如接入己基、十四烷基或脱氧胆酸基团),通过点击化学与八臂聚乙二醇二苯并环辛炔(PEG-8DBCO)交联,形成负载 acGM 和粒细胞 - 巨噬细胞集落刺激因子(GM-CSF)的 3D 多孔支架疫苗。通过动态光散射、扫描电镜等表征纳米颗粒及支架的理化性质,利用流式细胞术检测树突状细胞(DCs)活化、ROS 生成及 T 细胞增殖,结合免疫荧光染色和 ELISA 评估抗原呈递效率。在 B16-OVA 荷瘤小鼠、肺转移模型及 ApcMin/+ 转基因结直肠癌模型中,通过监测肿瘤生长、转移灶数量及免疫细胞浸润评估疫苗疗效。
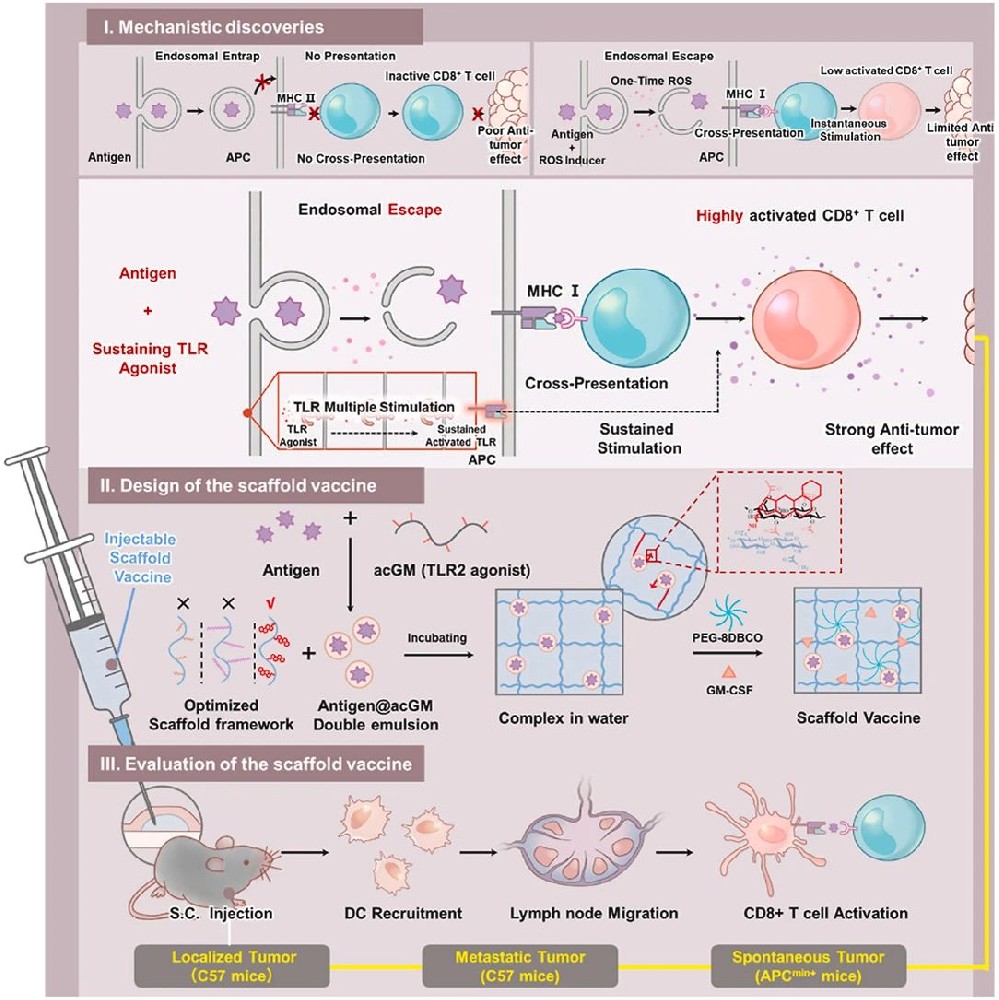
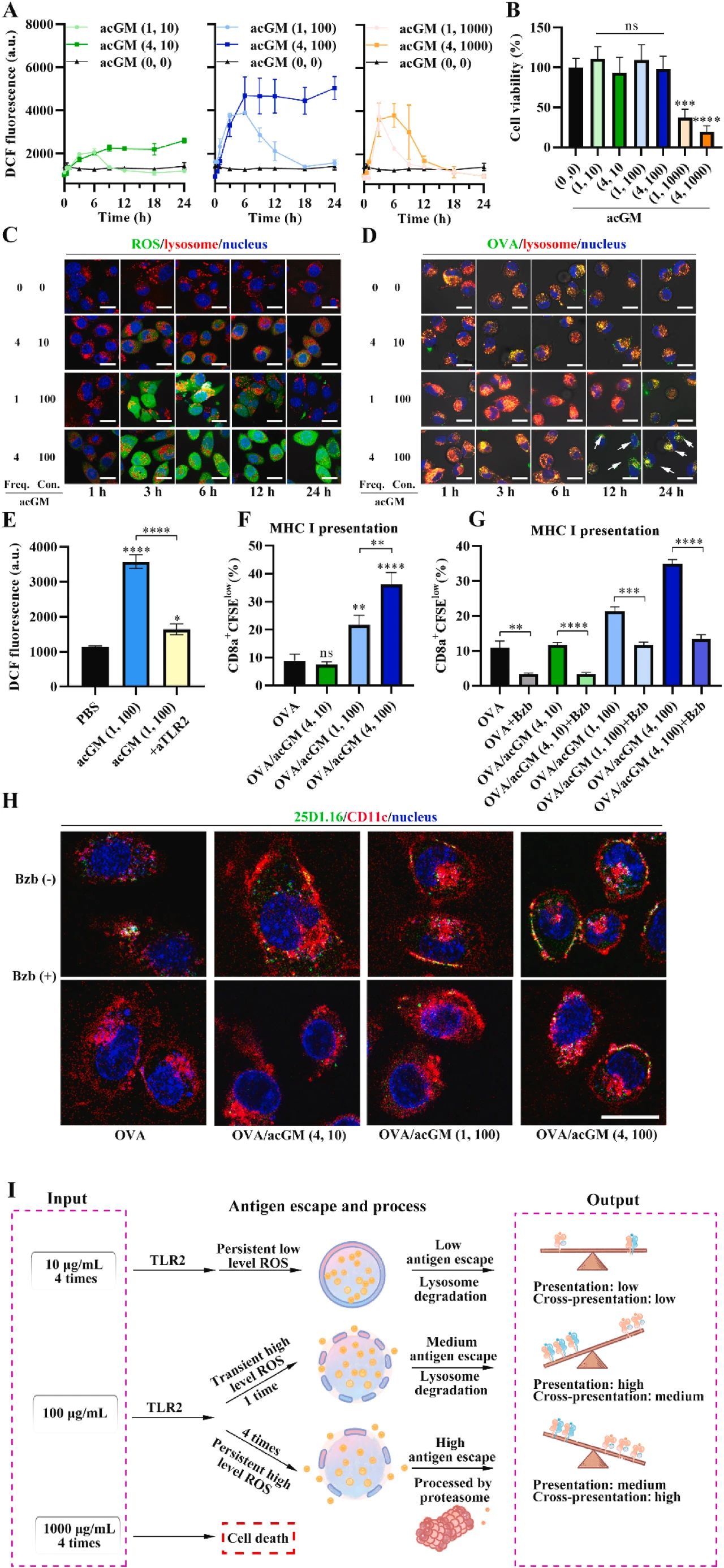
图1:细胞内 ROS 动力学对抗原呈递模式的影响
图 1 显示不同浓度和频率的 acGM 处理对骨髓来源 DCs(BMDCs)中 ROS 生成、溶酶体破坏及抗原逃逸的影响。结果表明,4 次 / 24 h、100 μg/mL acGM 处理可诱导持续高水平 ROS,显著破坏溶酶体并促进 OVA 从溶酶体逃逸,进而增强 MHC-I 介导的 CD8+ T 细胞增殖,而单次高浓度 acGM 处理因细胞毒性导致 ROS 动力学失衡,证实持续 TLR2 激活对最佳交叉呈递的必要性。
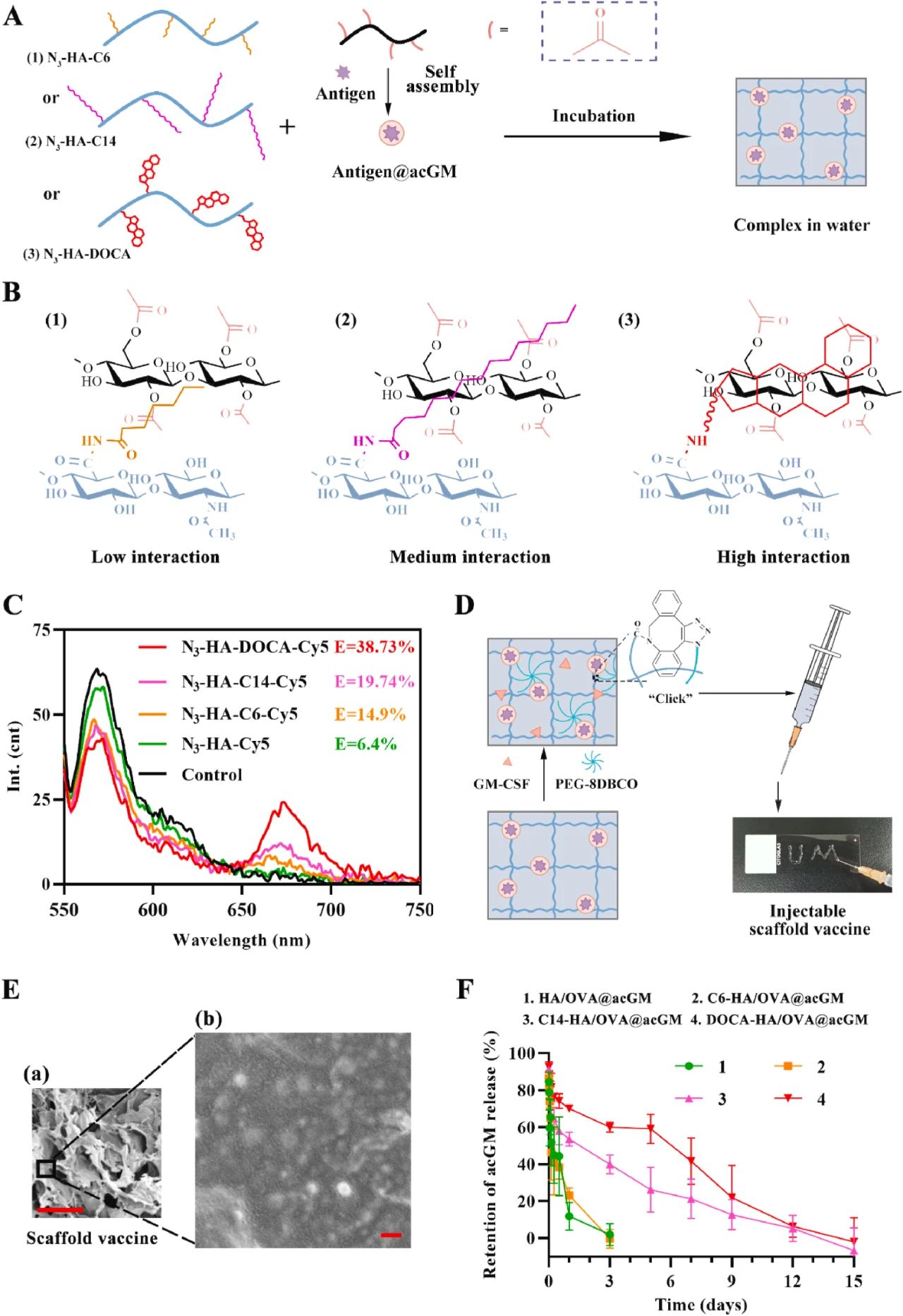
图2:可注射 3D 支架疫苗的设计与 acGM “保留 - 释放” 特性
图 2 展示了 HA 疏水修饰(接入 C6、C14 或 DOCA 基团)及支架制备过程。疏水相互作用使 DOCA-HA 支架显著延长 acGM 释放(6 天后仍保留 > 50%),而未修饰 HA 支架无法有效保留 acGM。荧光共振能量转移(FRET)实验证实 DOCA-HA 与 acGM 的最强相互作用,扫描电镜显示支架的多孔结构及 acGM 均匀分布,为局部持续激活 DCs 提供基础。

图3:支架疫苗在体内促进 DC 成熟及 ROS 生成
图 3 显示 DOCA-HA/OVA@acGM 支架在皮下注射后,募集的 CD11c+ DCs 数量在第 3 天达到峰值,且 CD86 + 成熟 DCs 比例在第 7 天仍维持较高水平,而无保留能力的 HA/OVA@acGM 组 DC 成熟迅速下降。同时,DOCA-HA 组中 ROS+ DCs 比例在注射后 14 天显著高于对照组,且引流淋巴结中 CD8+ T 细胞比例显著增加,证实支架疫苗通过持续 TLR2 激活促进 DC 成熟及系统性 T 细胞活化。
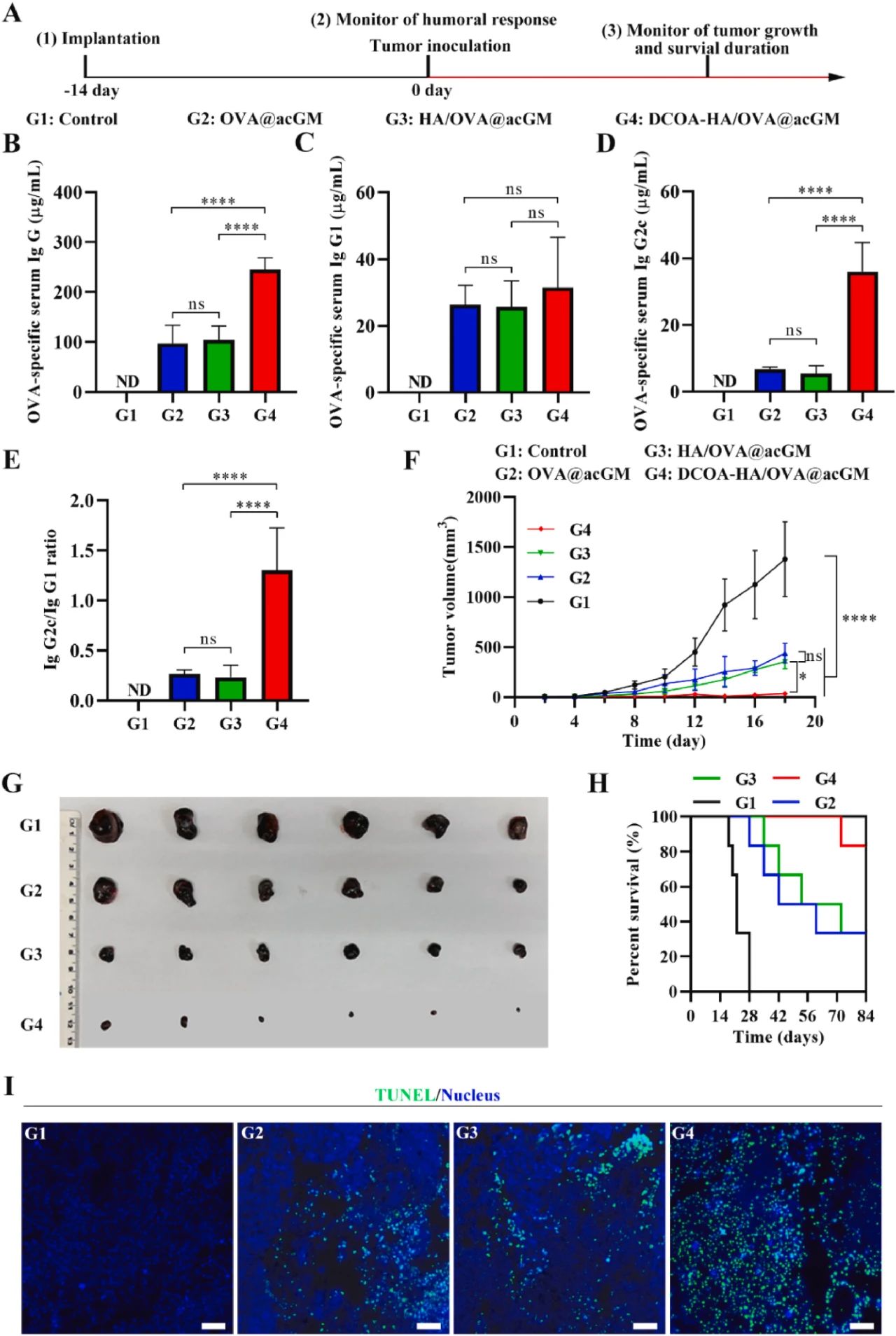
图4:OVA 负载支架疫苗抑制局部肿瘤生长
图 4 显示 DOCA-HA/OVA@acGM 支架疫苗在 B16-OVA 荷瘤小鼠中诱导最强的体液免疫(IgG2c/IgG1 比值升高)和细胞免疫响应,肿瘤体积较对照组减少约 80%,生存时间延长。肿瘤组织中 CD8+ T 细胞浸润及增殖(Ki67+)显著增加,TUNEL 染色显示肿瘤细胞凋亡率升高,表明支架疫苗通过交叉呈递激活强效抗肿瘤免疫。
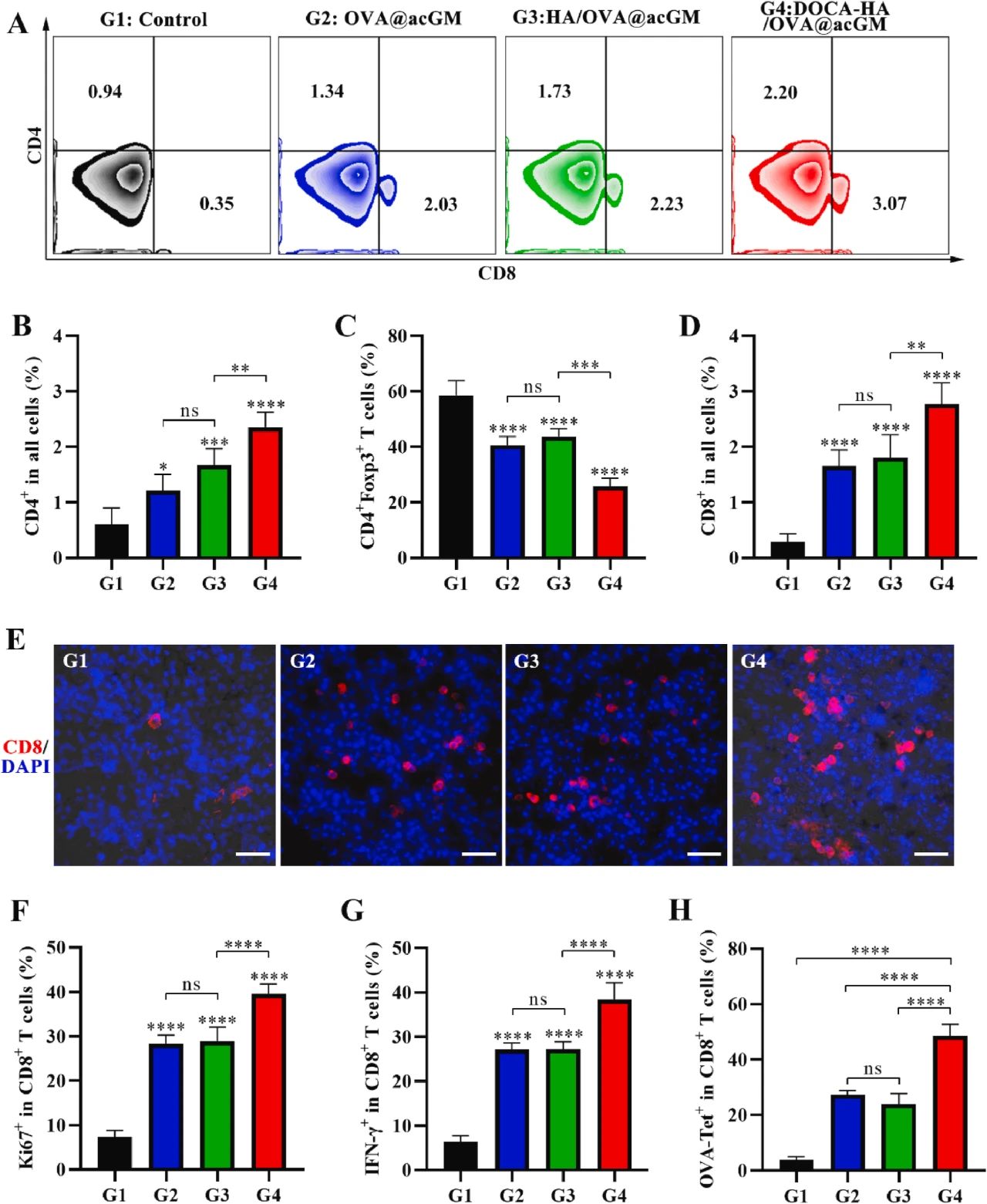
图5:支架疫苗对肺转移的抑制及免疫记忆效应
图 5 表明 DOCA-HA/OVA@acGM 组肺转移灶数量较对照组减少约 70%,脾脏中效应记忆 T 细胞(CD8+ CD44+ CD62L-)比例及 OVA 特异性 IFN-γ 分泌显著增加,体外细胞毒性实验显示该组脾细胞对靶细胞的裂解效率最高,证实支架疫苗可诱导持久的免疫记忆,有效预防肿瘤转移。
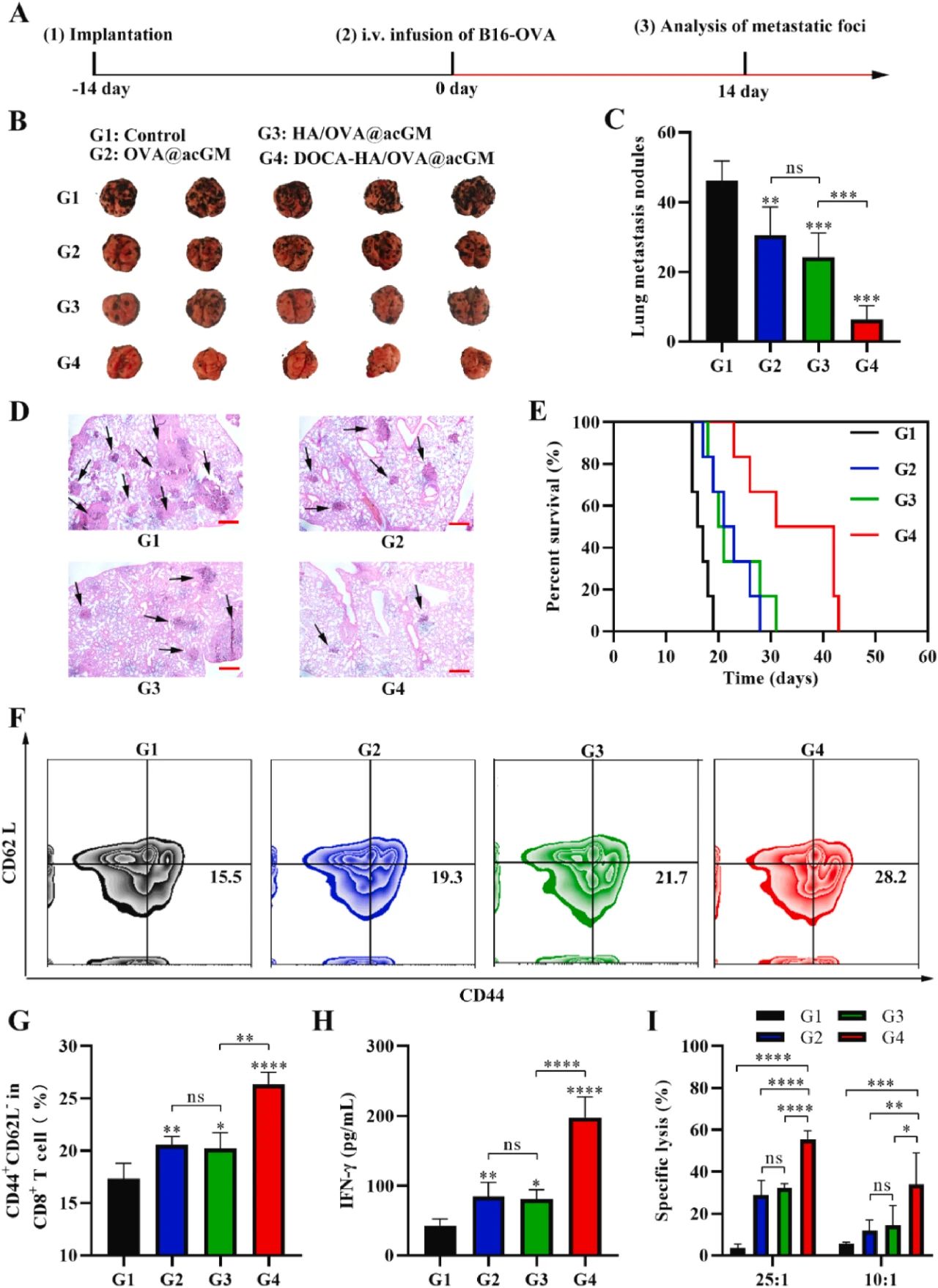
图6:TSA 负载支架疫苗对自发性结直肠癌的疗效
图 6 显示 DOCA-HA/TSA@acGM 支架疫苗在 ApcMin/+ 小鼠中显著减少结肠肿瘤数量及大小,肿瘤组织中 CD8+ T 细胞浸润及 Ki67 + 增殖细胞比例增加,IFN-γ 和颗粒酶 B 表达升高,TUNEL 染色显示肿瘤细胞凋亡增加,表明该疫苗对自发性肿瘤具有广谱抗肿瘤活性。
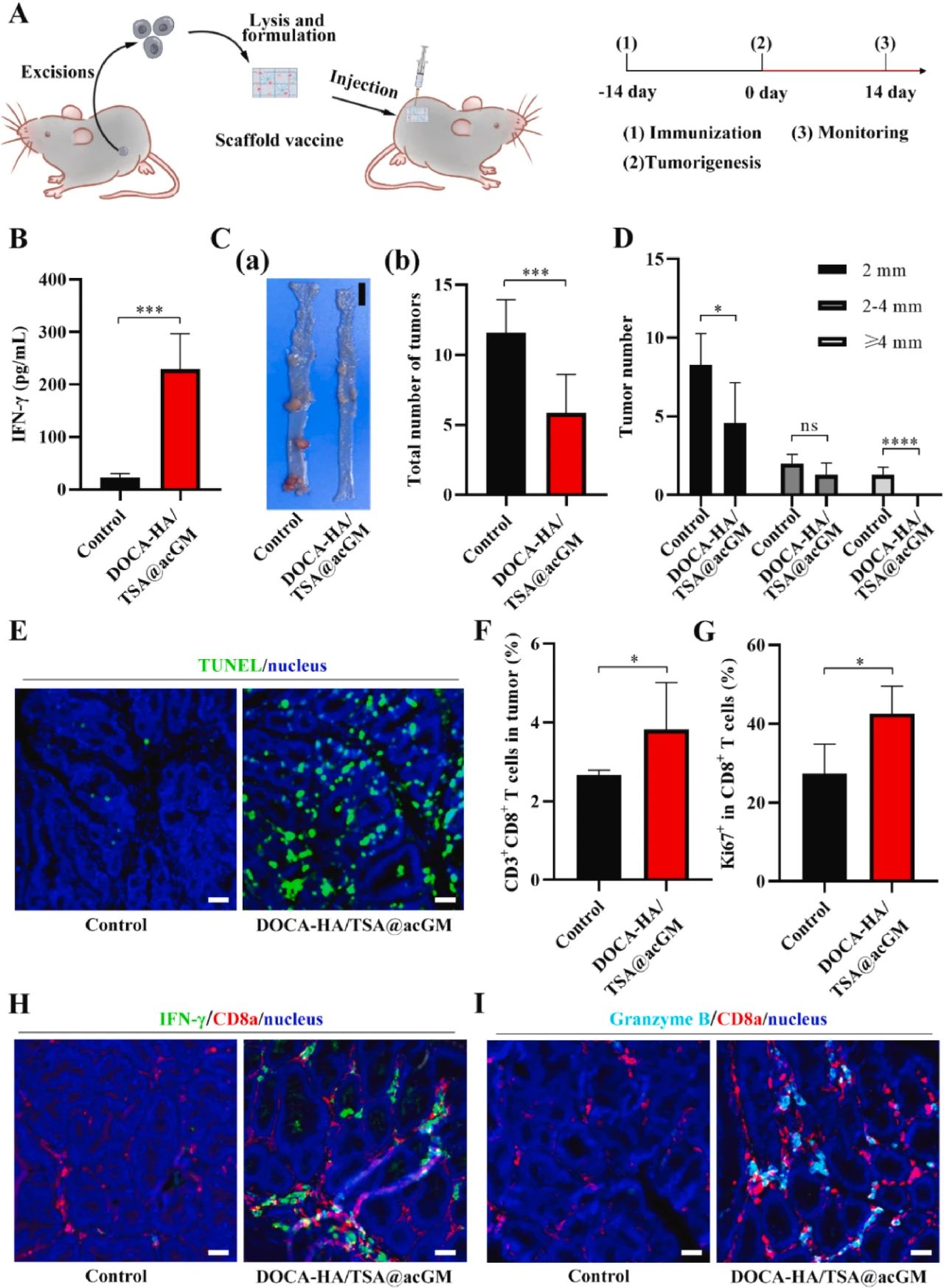
图7:TSA 负载支架疫苗在转基因 ApcMin/+ 小鼠中对自发性结直肠癌的强效抗肿瘤响应
该图展示了 DOCA-HA/TSA@acGM 支架疫苗在 ApcMin/+ 转基因小鼠(易自发形成肠道腺瘤)中的抗肿瘤效果。实验中,研究人员将肿瘤裂解物制备成 TSA@acGM 并载入 DOCA-HA 支架,皮下免疫小鼠后,通过流式细胞术、肿瘤计数、TUNEL 染色及免疫荧光等方法检测发现,该疫苗可诱导脾 CD8+ T 细胞分泌的 IFN-γ 水平较对照组提升 9.63 倍,显著减少结肠肿瘤数量(约 50%)及直径≥4 mm 的肿瘤比例,同时促进肿瘤细胞凋亡并增加肿瘤内 CD8+ T 细胞浸润及 Ki67 + 增殖细胞、IFN-γ+ 和颗粒酶 B + 细胞的表达。这表明 TSA 负载的 DOCA-HA 支架疫苗能通过持续激活 TLR2 增强肿瘤抗原交叉呈递,有效抑制自发性结直肠癌进展,为个性化肿瘤免疫治疗提供了新策略。
该支架疫苗通过疏水相互作用实现 acGM 的 “保留 - 释放”,在皮下注射后持续激活募集的 DCs 表面 TLR2,诱导最佳 ROS 动力学,促进抗原从溶酶体逃逸并通过 MHC-I 呈递给 CD8+ T 细胞。在野生型小鼠中,负载 OVA 的支架疫苗显著抑制 B16-OVA 肿瘤生长及肺转移,诱导产生记忆性 CD8+ T 细胞;在 ApcMin/+ 小鼠中,负载 TSA 的支架疫苗可减少自发性结直肠肿瘤数量,增强肿瘤浸润 CD8+ T 细胞的增殖及细胞毒性因子(如 IFN-γ、颗粒酶 B)分泌。该疫苗无需额外佐剂或外部刺激,通过调控 TLR2 激活的 ROS 动力学实现高效抗原交叉呈递,为下一代个性化癌症疫苗提供了新策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:荧光 “导航仪” 精准切除胶质母细胞瘤,小鼠模型验证生存期延长 25%
下一篇:宿主 - 病毒基因组联合分析揭开乙肝病毒逃逸人体防御的双重策略