常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-05-15 09:03:29 细胞资源库平台 访问量:223
乙肝病毒(HBV)感染是全球主要公共卫生问题之一,有超过2.5亿人慢性感染HBV。而其中有超三分之一的人口集中在我国,人数接近1亿人。NTCP工具细胞,特别是外源表达NTCP的肝癌细胞系如HepG2-NTCP和Huh7-NTCP,因其易操作、短周期、重现性佳的特点,在乙肝病毒(HBV)研究中扮演着至关重要的角色。这些细胞模型能够有效模拟HBV的感染过程,为研究HBV的生命周期、宿主限制因子、病毒复制以及药物筛选提供了一个强大而便捷的体外平台。它们不仅有助于揭示HBV感染的分子机制,如DDX3作为宿主限制因子阻碍cccDNA转录,GPC5作为附着因子在感染入胞过程中的作用,还能通过直接与NTCP相互作用或下调NTCP表达来筛选和验证抗病毒药物的活性,例如环孢菌素A及其衍生物、雷帕霉素及其衍生物等。此外,这些工具细胞还促进了对HBV宿主特异性分子的发现,为发展支持HBV感染的小动物模型提供了可能,这对于乙肝相关研究和药物开发具有重大意义。
英文标题:Identification of amino acids restricting HBV receptor function in porcine NTCP
中文标题:鉴定猪NTCP中限制HBV受体功能的氨基酸
发表期刊:《npj Viruses》
影响因子:6.8
作者单位:
1.Institute of Virology, Technical University of Munich/Helmholtz Munich
2.German Center for Infection Research (DZIF), Munich partner site
3.Oregon National Primate Research Center, Oregon Health & Science University
作者信息:Samuel D. Jeske, Jochen M. Wettengel, Florian Gegenfurtner
乙型肝炎病毒(HBV)感染全球约2.54亿人,每年导致110万死亡,但目前仍缺乏根治疗法。HBV的天然宿主仅限于人类和类人猿,现有动物模型(如免疫缺陷小鼠或黑猩猩)因伦理或生理差异受限,无法满足免疫疗法研究需求。HBV通过钠牛磺胆酸共转运蛋白(NTCP)进入肝细胞,但猪NTCP(pNTCP)无法介导HBV结合。本研究旨在鉴定pNTCP中限制HBV感染的氨基酸位点,通过人源化改造构建功能性受体,为开发免疫健全的转基因猪模型奠定基础,助力新型疗法评估。
1. 肝细胞分离与感染:通过胶原酶灌注法分离原代猪肝细胞(PPH),接种HBV后检测HBeAg,验证感染能力。
2. NTCP克隆与突变:克隆pNTCP基因,逐步替换人源序列(157-167位氨基酸),构建嵌合体phNTCP。
3. 荧光结合实验:使用荧光标记的PreS1肽段(Myrcludex B)检测NTCP与HBV的结合能力。
4. 稳定细胞系构建:利用PiggyBac转座子系统生成稳定表达hNTCP、pNTCP及嵌合体phNTCP的HepG2细胞系。
5. 感染效率评估:通过HBeAg分泌、Southern blot检测cccDNA及定量PCR分析病毒复制。
6.毒性测试:评估高剂量嵌合体NTCP对小鼠体重、血液生化指标及器官组织的影响。
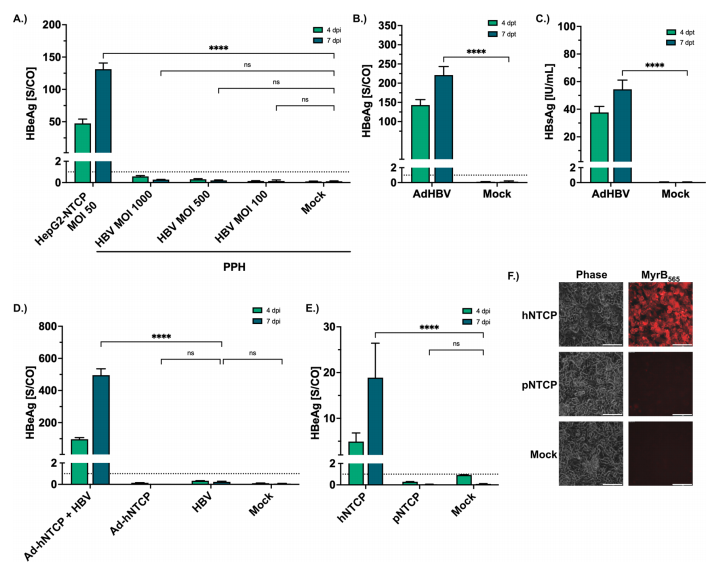
图1:人源NTCP突破猪肝细胞的HBV感染屏障
通过腺病毒载体在猪肝细胞中表达hNTCP后,HBV感染效率显著提升(图1D),HBeAg分泌量接近人肝癌细胞HepG2(图1A)。未转导hNTCP的天然猪肝细胞无法检测到HBeAg(图1A),且荧光标记的Myrcludex B结合实验显示pNTCP无法介导HBV结合(图1F)。此结果证实pNTCP缺乏HBV受体功能,而hNTCP的表达可完全解除这一限制,为后续人源化改造提供依据。
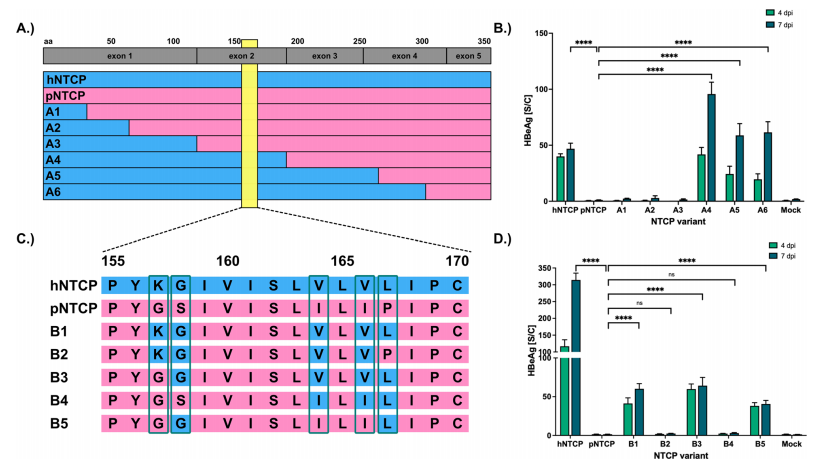
图2:157-167位氨基酸决定HBV受体功能
通过逐步替换pNTCP序列(图2A),发现人源化外显子2(含157-167位氨基酸)的嵌合体phNTCP可支持HBV感染(图2B)。进一步单点突变筛选(图2C)锁定S158G和P167L为关键位点(图2D),其突变使HBeAg分泌量接近hNTCP水平。荧光结合实验(图S3)证实这两个突变显著提升Myrcludex B结合能力,表明其直接参与HBV与受体的相互作用。
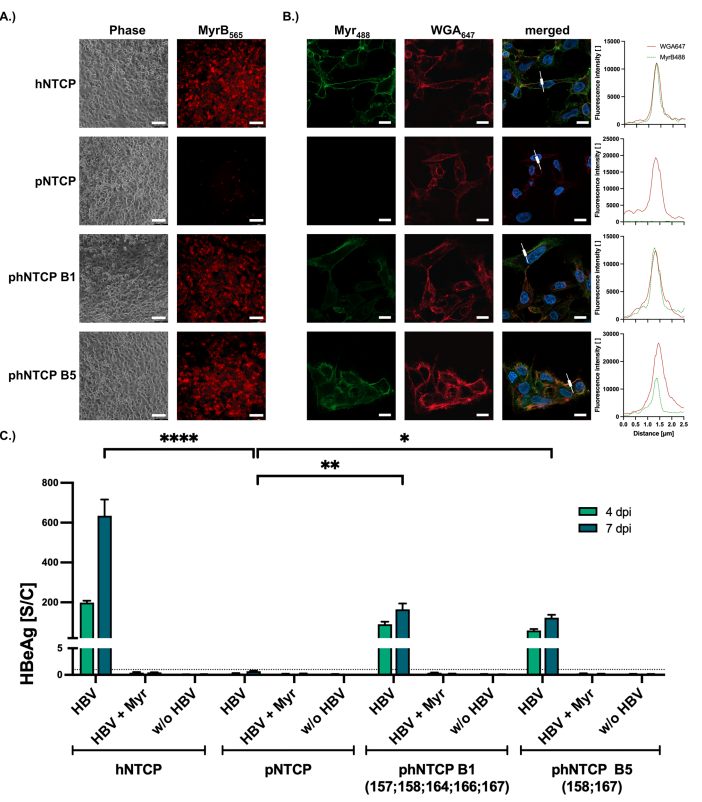
图3:稳定表达phNTCP的肝细胞实现HBV持续感染
构建稳定表达phNTCP(157-167)及双突变体(S158G/P167L)的HepG2细胞系,荧光显微镜显示Myrcludex B结合位于细胞膜(图3B),证实受体正确定位。HBV感染后,HBeAg分泌量虽低于hNTCP组,但显著高于未突变pNTCP(图3C)。Southern blot检测到cccDNA(图4C),证明phNTCP可支持完整病毒复制周期,为转基因动物模型提供直接证据。
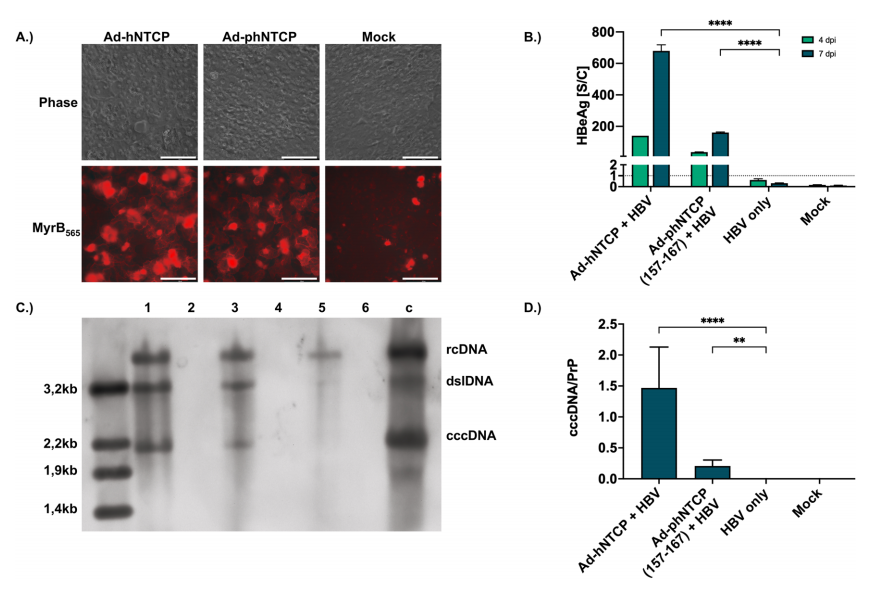
图4:嵌合体NTCP实现猪肝细胞HBV感染与cccDNA形成
腺病毒转导phNTCP(157-167)至原代猪肝细胞后,Myrcludex B结合显著(图4A),HBeAg分泌及cccDNA检测(图4B-D)证实感染成功。尽管病毒载量低于人源NTCP组,但明确检测到rcDNA和cccDNA(图4C),表明猪肝细胞可支持HBV复制。此结果为构建转基因猪模型提供了关键实验依据,未来通过优化突变组合或提升受体表达量可进一步增强感染效率。
1. 关键氨基酸鉴定:pNTCP的S158G和P167L突变是HBV结合与感染的关键限制位点,人源化后显著提升受体功能。
2. 感染模型突破:表达嵌合体phNTCP(157-167)的猪肝细胞成功支持HBV完整生命周期(包括cccDNA形成),病毒载量达1×10⁷基因组/毫升。
3. 安全性验证:高剂量phNTCP连续注射未引发小鼠器官损伤,仅短暂性血脂升高,生物相容性良好。
4. 应用前景:通过CRISPR技术构建转基因猪,可开发首个免疫健全的HBV感染模型,助力cccDNA靶向药物和免疫疗法评估。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:告别针头!可溶微针贴片3分钟释放纳米疫苗,免疫力飙升不输打针
下一篇:无毒高亮!新型荧光素配方让活体脑部追踪“看得更久、更清楚”