常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-05-07 09:00:00 细胞资源库平台 访问量:253
荧光素酶报告基因系统是一种基于荧光素酶催化底物氧化反应产生生物发光的检测技术,广泛应用于细胞生物学研究。其中,萤火虫荧光素酶(firefly luciferase, Fluc)因其高灵敏度、宽线性检测范围(约7~8个数量级)以及较短的半衰期(在哺乳动物细胞中约为3小时,在植物细胞中约为3.5小时)而成为最常用的报告基因。其发光信号强度在酶浓度为10⁻¹⁶ mol/L至10⁻⁸ mol/L的范围内与酶活性呈线性关系,并且在理想条件下可检测到低至10⁻²⁰ mol/L的荧光素酶活性。此外,荧光素酶报告基因系统具有非放射性、检测快速、灵敏度高(比氯霉素乙酰转移酶CAT高100倍)等优点,特别适用于高通量筛选和活细胞检测。通过将荧光素酶报告基因载体转染至宿主细胞后,可利用荧光素酶检测系统灵敏且便捷地监测基因表达水平,已成为细胞生物学研究中的重要工具。
英文标题:Assessment of α-Fetoprotein Targeted HSV1-tk Expression in Hepatocellular Carcinoma with In Vivo Imaging
中文标题:甲胎蛋白靶向HSV1-tk在肝细胞癌中的体内成像评估及治疗效应研究
发表期刊:《Cancer Biother. Radiopharm》
影响因子:2.4
作者单位:
1.Korea Institute of Radiological and Medical Sciences
2.Dankook University
作者信息:
Ju Hui Park, Kwang II Kim, Kyo Chul Lee
肝细胞癌(HCC)的早期诊断和治疗仍面临挑战,甲胎蛋白(AFP)作为HCC的血清标志物,在胎儿期后表达沉默,但在肝癌中重新激活。研究利用AFP特异性增强子/启动子驱动单纯疱疹病毒胸苷激酶(HSV1-tk)基因表达,结合放射性核素成像技术(如18F-FHBG PET)和代谢成像(18F-FDG PET),旨在实现AFP阳性肝癌的靶向基因治疗和实时疗效监测,提升治疗特异性并减少对正常组织的毒性。
本研究通过构建受AFP增强子/启动子调控的HSV1-tk重组腺病毒(AdAFP-TK),验证其体外和体内的靶向表达及治疗效果。首先,通过分子克隆技术将HSV1-tk基因插入AFP调控序列下游,构建AdAFP-TK,并在293细胞中扩增和纯化。体外实验中,采用RT-PCR和125I标记的IVDU(5-碘乙烯基-2'-脱氧尿苷)摄取实验,评估AFP阳性肝癌细胞(HuH-7、HepG2)与阴性细胞(HT-29、SK-Hep-1)中HSV1-tk的表达特异性;通过MTT法检测不同浓度GCV(0-100 μM)对感染AdAFP-TK的细胞存活率影响。动物模型中,Balb/c-nu/nu小鼠皮下接种HuH-7或HepG2肿瘤后,瘤内注射AdAFP-TK与AdAFP-fLuc(荧光素酶基因)混合液,利用生物发光成像(BLI)和18F-FHBG PET分别监测荧光素酶和HSV1-tk的靶向表达。治疗组小鼠接受GCV(50 mg/kg)连续5天腹腔注射,通过肿瘤体积测量和18F-FDG PET动态评估代谢变化以验证疗效。
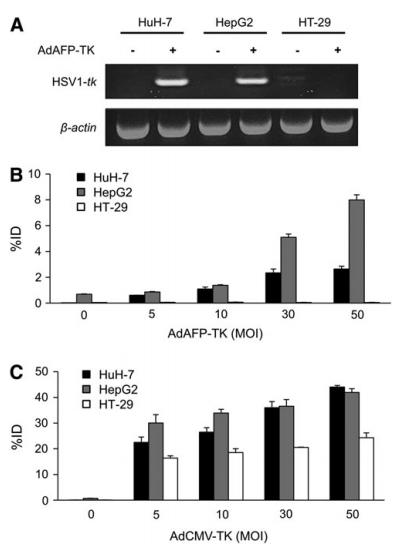
图1:体外验证AFP靶向HSV1-tk表达
通过RT-PCR和放射性核苷类似物摄取实验,明确AdAFP-TK的靶向性。RT-PCR结果显示,仅在AFP阳性细胞(HuH-7、HepG2)中检测到HSV1-tk mRNA,而AFP阴性细胞(HT-29、SK-Hep-1)无表达。125I-IVDU摄取实验进一步显示,AdAFP-TK感染的HuH-7和HepG2细胞在MOI=50时,放射性摄取分别达53倍和161倍于阴性对照组(HT-29),且与病毒剂量呈正相关。这一结果证实了AFP增强子/启动子对HSV1-tk表达的严格调控,为后续体内靶向性奠定基础。
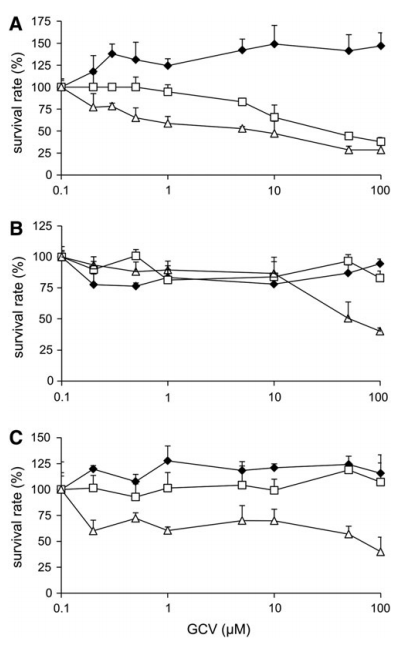
图2:GCV介导的细胞毒性分析
MTT实验表明,AdAFP-TK联合GCV对AFP阳性细胞具有选择性杀伤作用。在GCV浓度为100 μM时,HuH-7细胞存活率降至20%以下(MOI=10),而AFP阴性细胞(HT-29、SK-Hep-1)存活率仍高于80%。相比之下,CMV启动子驱动的AdCMV-TK对所有细胞均表现出广谱毒性,与AFP调控组的靶向性形成鲜明对比。该实验验证了AFP靶向系统的安全性,避免对正常组织的脱靶效应。
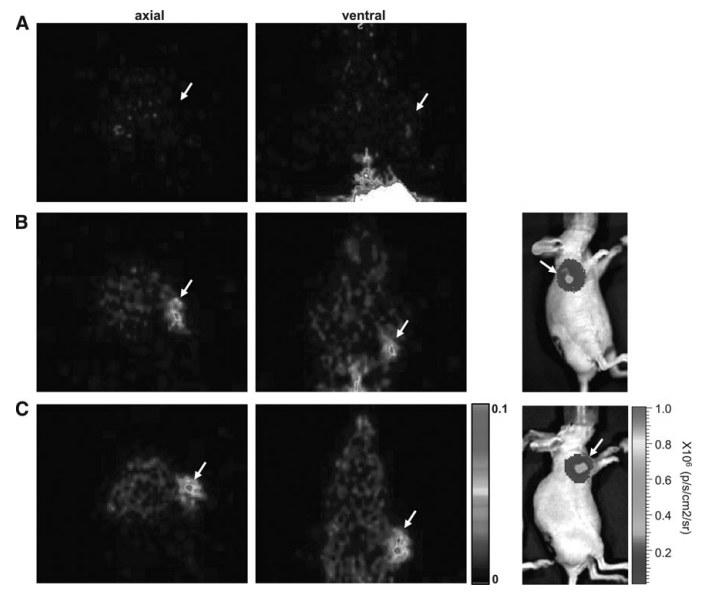
图3:体内AFP靶向基因表达的分子成像
混合注射AdAFP-TK和AdAFP-fLuc后,BLI和18F-FHBG PET同步显示AFP阳性肿瘤的基因表达。BLI显示荧光信号集中于HuH-7和HepG2瘤体,而18F-FHBG PET定量分析表明,注射病毒的肿瘤放射性摄取显著高于肌肉(SUVmax达5.27),未注射病毒组仅1.16。这一多模态成像策略不仅验证了AFP调控系统的靶向效率,还证明了HSV1-tk作为治疗-成像双功能基因的潜力。
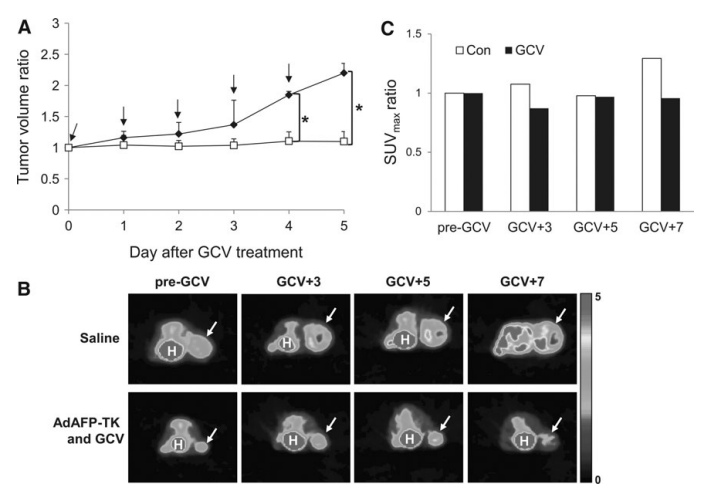
图4:GCV治疗的体内疗效评估
GCV治疗后,AdAFP-TK组的HuH-7肿瘤体积增长显著抑制(第7天体积较对照组减少50%),而18F-FDG PET显示治疗组SUVmax逐渐下降,对照组持续上升。代谢变化早于形态学改变,表明18F-FDG PET可早期反映治疗响应。该结果凸显了分子影像在疗效动态监测中的优势,为临床转化提供了重要依据。
AdAFP-TK在AFP阳性肝癌细胞(HuH-7、HepG2)中特异性激活HSV1-tk表达,体外实验显示GCV(100 μM)可显著抑制AFP阳性细胞存活率(p<0.05),而阴性细胞未受影响。体内分子成像证实,AFP调控的荧光素酶和HSV1-tk表达分别通过BLI和18F-FHBG PET可视化,肿瘤/肌肉放射性比值达3.46-5.27。GCV治疗显著抑制肿瘤生长(第4天起差异显著,p<0.05),18F-FDG PET显示治疗组代谢活性持续下降,对照组则升高。该研究首次实现AFP靶向基因治疗与多模态成像(BLI/PET)的同步验证,为肝癌的精准治疗和疗效实时监测提供了新策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:3 小时出结果!新型 NanoLuc 报告菌株解锁酵母双杂交定量检测新姿势
下一篇:SOX4通过EBF2介导的产热基因程序促进小鼠棕色脂肪的发育和维持