常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-04-24 09:00:00 细胞资源库平台 访问量:343
乙肝病毒(HBV)感染是全球主要公共卫生问题之一,有超过2.5亿人慢性感染HBV。而其中有超三分之一的人口集中在我国,人数接近1亿人。NTCP工具细胞,特别是外源表达NTCP的肝癌细胞系如HepG2-NTCP和Huh7-NTCP,因其易操作、短周期、重现性佳的特点,在乙肝病毒(HBV)研究中扮演着至关重要的角色。这些细胞模型能够有效模拟HBV的感染过程,为研究HBV的生命周期、宿主限制因子、病毒复制以及药物筛选提供了一个强大而便捷的体外平台。它们不仅有助于揭示HBV感染的分子机制,如DDX3作为宿主限制因子阻碍cccDNA转录,GPC5作为附着因子在感染入胞过程中的作用,还能通过直接与NTCP相互作用或下调NTCP表达来筛选和验证抗病毒药物的活性,例如环孢菌素A及其衍生物、雷帕霉素及其衍生物等。此外,这些工具细胞还促进了对HBV宿主特异性分子的发现,为发展支持HBV感染的小动物模型提供了可能,这对于乙肝相关研究和药物开发具有重大意义。
英文标题:A Multivalent mRNA Therapeutic Vaccine Exhibits Breakthroughs in Immune Tolerance and Virological Suppression of HBV by Stably Presenting the Pre-S Antigen on the Cell Membrane
中文标题:基于细胞膜稳定呈递Pre-S抗原的多价mRNA治疗性疫苗在HBV免疫耐受突破和病毒抑制中展现突破性效果
发表期刊:《Pharmaceutics》
影响因子:4.9
作者单位:
1.School of Life Science and Technology, China Pharmaceutical University, Nanjing 211198, China
2.Jiangsu Cell Tech Medical Research Institute Co., Ltd., Nanjing 211100, China
作者信息:Shang Liu, Jie Wang, Yunxuan L
慢性乙型肝炎(CHB)的免疫耐受主要由高水平的乙肝表面抗原(HBsAg)介导,导致B细胞和T细胞功能耗竭。现有治疗手段(如干扰素和核苷类似物)仅对少数患者有效。Pre-S抗原是HBV感染肝细胞的关键靶点,但其线性肽疫苗因缺乏结构表位效果有限。本研究通过设计多价mRNA疫苗(编码L、M、S三种HBV表面抗原蛋白),旨在稳定表达Pre-S抗原于细胞膜,激活特异性抗体和T细胞反应,打破免疫耐受并实现功能性治愈。
本研究通过多步骤验证mRNA疫苗的疗效与机制:首先,构建编码HBV L、M、S蛋白的mRNA,采用脂质纳米颗粒(LNP)封装,并通过体外转染293T细胞验证抗原表达(流式细胞术和Western blot)。其次,利用稳定转染的HEK293F细胞系(LS-4C6、LS-4G2)分析L蛋白在细胞膜上的定位及膜筏结构形成(透射电镜)。动物实验方面,分别在HBV转基因(Tg)小鼠、pAAV HBV1.2(质粒诱导)和rAAV8 HBV1.3(腺相关病毒载体)模型中评估疫苗效果,检测血清HBsAg、HBsAb、HBeAg及HBV DNA水平;通过ELISA分析抗体亲和力,流式细胞术检测抗原依赖性T细胞IFN-γ分泌。最后,通过急性毒性实验(肝肾功能、器官病理学)验证疫苗安全性。
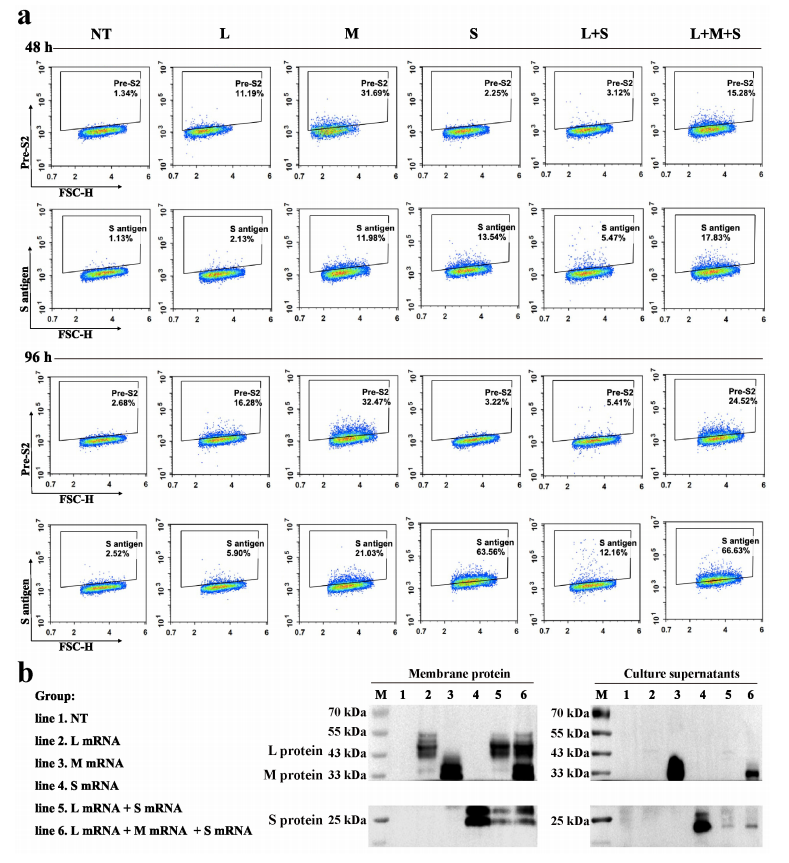
图1:L蛋白与S/M蛋白共表达增强Pre-S抗原的细胞膜定位
通过流式细胞术和Western blot分析发现,L蛋白单独表达时易被降解,而与S或M蛋白共转染时,L蛋白在293T细胞膜上的表达显著增强(流式显示Pre-S阳性细胞比例提升至50%以上)。透射电镜(TEM)进一步显示,L+S共表达细胞表面形成密集的膜筏结构,促进B细胞受体(BCR)识别。此结果为疫苗设计提供了关键依据:S蛋白不仅辅助L蛋白稳定表达,还通过膜筏增强抗原呈递效率。
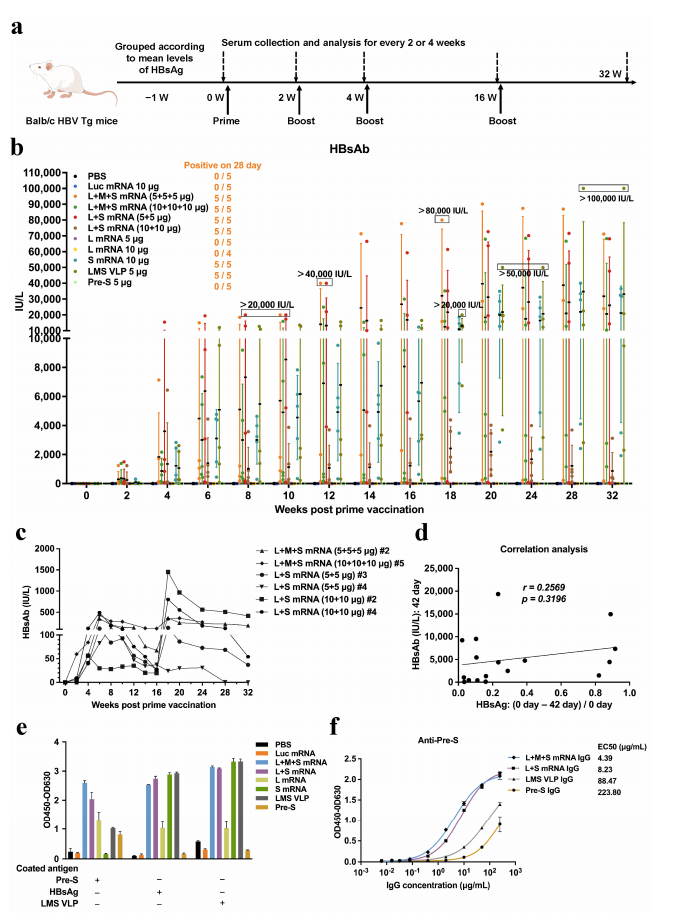
图2:LMS mRNA疫苗在HBV Tg小鼠中打破HBsAg介导的免疫耐受
在HBV Tg小鼠(血清HBsAg>500 IU/mL)中,LMS mRNA免疫组在2周后即检测到HBsAb,4次免疫后抗体水平超40,000 IU/L,且可持续至32周。ELISA显示,疫苗诱导的IgG对结构Pre-S抗原(LMS VLP)的亲和力(EC50=3.2 nM)显著高于线性肽疫苗(无结合),证实疫苗成功激活针对天然构象表位的抗体,突破高HBsAg环境下的免疫耗竭。
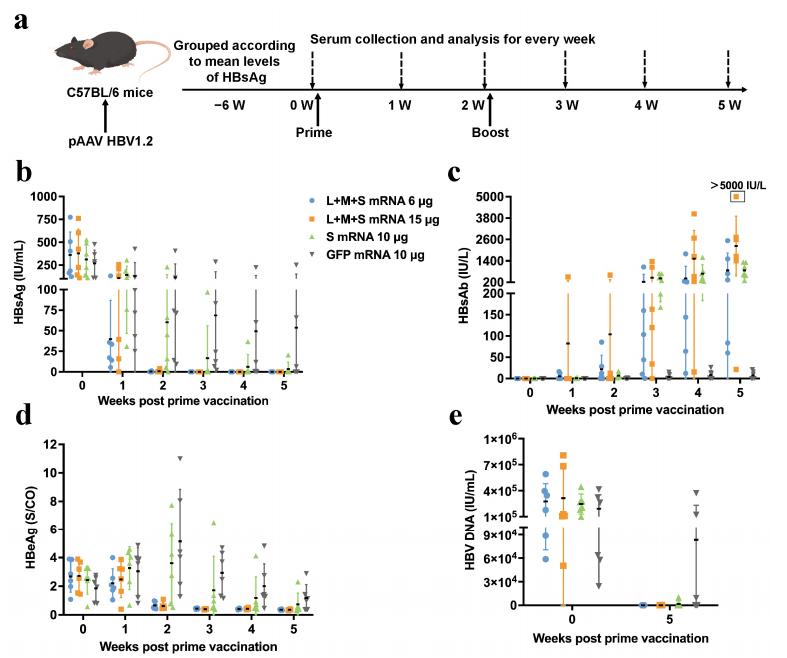
图3:LMS mRNA疫苗在pAAV HBV1.2模型中诱导血清抗原清除
在pAAV HBV1.2小鼠(短期HBV表达模型)中,低剂量LMS mRNA(6μg)免疫2次后,血清HBsAg和HBeAg在3周内转阴,5周时HBV DNA降至检测限以下(<10 IU/mL)。相比之下,S mRNA组需更高剂量(10μg)且效果延迟,表明LMS疫苗通过Pre-S靶向作用快速抑制病毒复制。
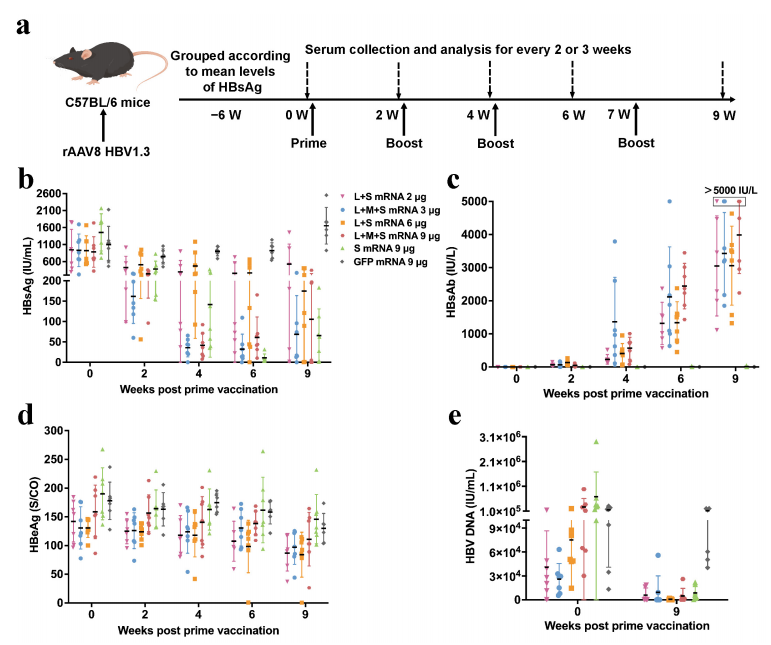
图4:LMS mRNA疫苗在rAAV8 HBV1.3模型中实现病毒抑制与T细胞激活
在rAAV8 HBV1.3小鼠(高病毒载量模型)中,9μg LMS mRNA免疫4次后,血清HBsAg下降>90%,60%小鼠HBeAg转阴,HBV DNA降低2-3个数量级。流式分析显示,疫苗组CD3+ T细胞经抗原刺激后IFN-γ分泌比例达12.5%(对照组<1%),证实疫苗激活了Pre-S依赖性T细胞应答,协同抗体清除病毒。
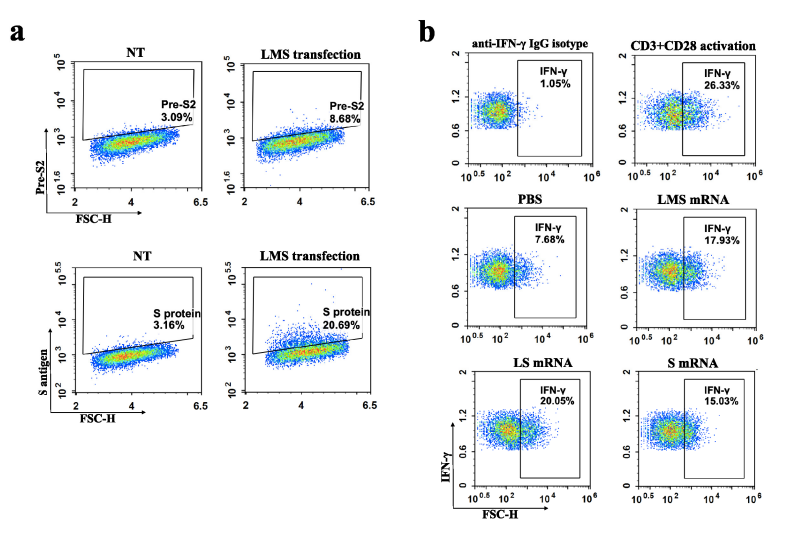
图5:LMS mRNA疫苗激活抗原依赖性T细胞反应的机制验证
通过体外共培养实验,将免疫后小鼠的T细胞与表达LMS抗原的BALB/3T3细胞共孵育,疫苗组T细胞IFN-γ阳性率显著升高(LMS组15.3% vs PBS组0.8%),且依赖Pre-S抗原呈递(未转染细胞无激活)。此结果明确了疫苗通过膜抗原-MHC-I途径激活细胞免疫的核心机制。
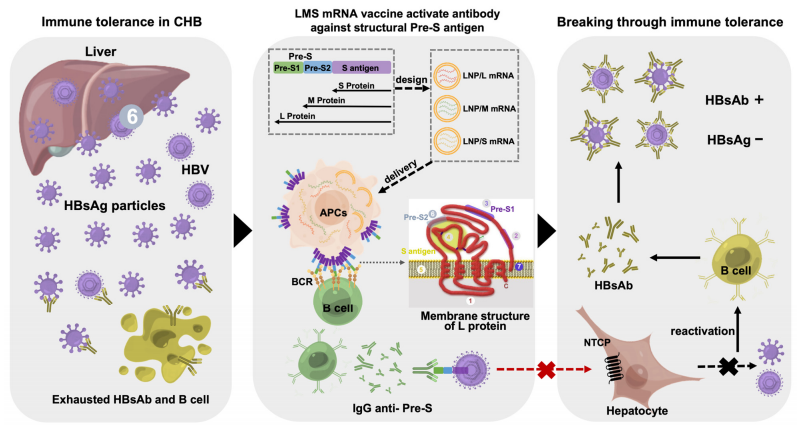
图6:LMS mRNA疫苗治疗慢性乙型肝炎的机制示意图
图示疫苗作用流程:LNP递送mRNA至细胞,表达L/M/S蛋白并锚定于膜表面,形成Pre-S抗原簇;B细胞通过BCR识别膜筏结构产生HBsAb,阻断HBV感染肝细胞;同时,抗原经APC加工后激活CD8+ T细胞,分泌IFN-γ直接清除感染细胞。双途径协同实现HBsAg血清学转换和病毒清除。
本研究证实,LMS多价mRNA疫苗通过S蛋白辅助稳定表达Pre-S抗原于细胞膜,形成膜筏结构,有效激活B细胞产生高滴度HBsAb,突破HBsAg介导的免疫耐受。在HBV Tg小鼠中,疫苗诱导的抗体对结构Pre-S抗原(LMS VLP)具有高亲和力,显著优于线性肽疫苗;在pAAV和rAAV模型中,疫苗清除血清HBsAg和HBV DNA,并激活抗原特异性T细胞分泌IFN-γ。此外,急性毒性实验显示疫苗安全,无显著器官损伤。该疫苗通过协同体液与细胞免疫,为慢性乙型肝炎的功能性治愈提供了新策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:双剑合璧!中国团队突破性癌症疗法:DNA疫苗+基因PD-1抗体,小鼠生存率超60%!