常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-03-13 14:23:59 细胞资源库平台 访问量:380
乙肝病毒(HBV)感染是全球主要公共卫生问题之一,有超过2.5亿人慢性感染HBV。而其中有超三分之一的人口集中在我国,人数接近1亿人。NTCP工具细胞,特别是外源表达NTCP的肝癌细胞系如HepG2-NTCP和Huh7-NTCP,因其易操作、短周期、重现性佳的特点,在乙肝病毒(HBV)研究中扮演着至关重要的角色。这些细胞模型能够有效模拟HBV的感染过程,为研究HBV的生命周期、宿主限制因子、病毒复制以及药物筛选提供了一个强大而便捷的体外平台。它们不仅有助于揭示HBV感染的分子机制,如DDX3作为宿主限制因子阻碍cccDNA转录,GPC5作为附着因子在感染入胞过程中的作用,还能通过直接与NTCP相互作用或下调NTCP表达来筛选和验证抗病毒药物的活性,例如环孢菌素A及其衍生物、雷帕霉素及其衍生物等。此外,这些工具细胞还促进了对HBV宿主特异性分子的发现,为发展支持HBV感染的小动物模型提供了可能,这对于乙肝相关研究和药物开发具有重大意义。
英文标题:Discovery of pentacyclic triterpene conjugates as HBV polymerase/NTCP dual-targeting inhibitors with potent anti-HBV activities
中文标题:五环三萜缀合物作为HBV聚合酶/NTCP双靶点抑制剂的发现及其抗乙肝病毒活性研究
发表期刊:《Bioorganic Chemistry》
影响因子:5.1
作者单位(前三个):
1. School of Traditional Chinese Medicine, Southern Medical University, Guangzhou 510515, China
2. School of Pharmacy, Xiamen Medical College, Xiamen 361023, China
3. School of Pharmacy, Xiamen Medical College, Xiamen 361023, China
作者信息(前三个):
Yixin Chen, Meitao Duan, Jianling Xu
乙肝病毒(HBV)感染是导致肝硬化和肝癌的主要因素,现有药物(如核苷类似物)仅能抑制病毒复制但难以清除表面抗原(HBsAg)。为实现临床功能性治愈,需同时抑制病毒DNA复制和清除HBsAg。研究基于五环三萜类化合物(PTs)对宿主细胞钠牛磺胆酸共转运多肽(NTCP)的高亲和力,以及核苷类似物齐多夫定(AZT)对HBV聚合酶(Pol)的抑制作用,设计双靶点抑制剂。通过分子杂交策略合成五环三萜-AZT缀合物,旨在同时阻断病毒进入宿主细胞和抑制病毒复制,为乙肝治疗提供新型候选药物。
研究通过点击化学反应将五环三萜类化合物(如甘草次酸、齐墩果酸、熊果酸和桦木酸)与核苷类似物齐多夫定(AZT)缀合,合成了20种新型缀合物。首先,对五环三萜的羟基或羧基进行炔丙基化修饰,再与AZT的叠氮基团通过铜催化点击反应连接。随后,通过MTT法评估缀合物对HepG2.2.15细胞的毒性(CC50),并利用ELISA检测其对HBsAg和HBeAg分泌的抑制效果(IC50)。进一步通过荧光定量PCR(Q-PCR)分析缀合物对HBV DNA复制的抑制作用。为阐明作用机制,采用分子对接模拟缀合物与HBV聚合酶(Pol)及NTCP的结合模式,并通过表面等离子共振(SPR)实验验证其与HBV Pol C区肽段及NTCP表位的结合亲和力。
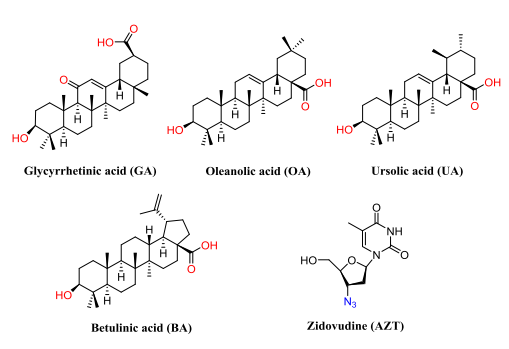
图1:五环三萜-AZT缀合物的合成路线示意图
该图展示了20种五环三萜(PTs)与齐多夫定(AZT)缀合物的合成路径。首先,通过炔丙基化反应对五环三萜(如甘草次酸、齐墩果酸等)的羟基或羧基进行修饰,生成炔丙基化中间体(化合物1-20)。随后,利用铜催化的点击化学反应(CuAAC),将中间体与AZT的叠氮基团连接,形成1,2,3-三唑环结构,最终得到目标缀合物(化合物21-40)。合成过程中通过硅胶柱层析纯化,并通过核磁共振(NMR)和高分辨质谱(HRMS)验证结构。该路线设计简洁高效,为后续生物活性评价提供了多样化的化合物库。
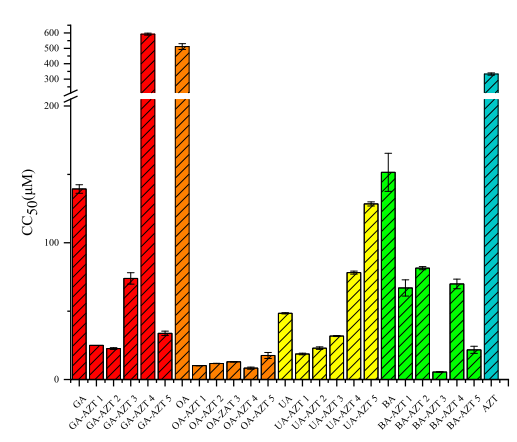
图2:缀合物的细胞毒性(CC50)对比分析
此图通过MTT法评估了缀合物对HepG2.2.15细胞的毒性。结果显示,大部分缀合物的CC50值介于5.52 μM(BA-AZT3)至592.03 μM(GA-AZT4)之间,其中GA系列缀合物毒性最低(平均CC50=136.4 μM),OA系列毒性最高(平均CC50=12.16 μM)。BA-AZT1的CC50为66.94 μM,显著优于母体化合物BA(151.5 μM)和AZT(333.28 μM)。数据表明,缀合化策略在降低部分化合物毒性的同时,保留了活性基团的功能性。
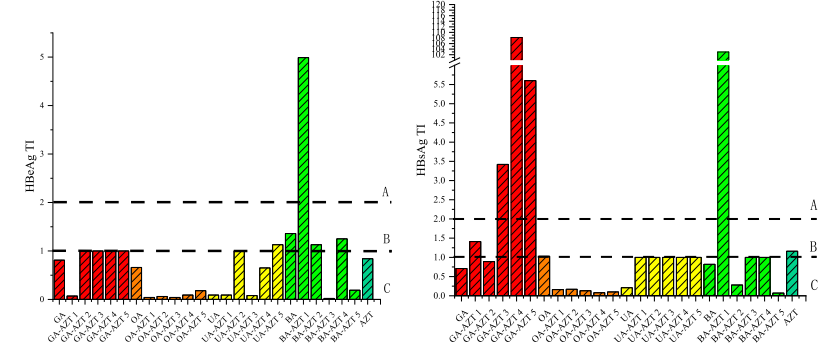
图3:缀合物对HBsAg和HBeAg分泌的抑制作用
通过ELISA检测缀合物对HBsAg和HBeAg的抑制效果。BA-AZT1表现最为突出,其抑制HBsAg的IC50为0.65 μM(TI=102.98),较BA和AZT分别提高284倍和442倍;对HBeAg的IC50为13.42 μM(TI=4.99)。GA-AZT4的HBsAg抑制活性(IC50=5.44 μM)也显著优于母体GA(IC50=199.04 μM)。图中数据进一步显示,C-28/C-30位羧基及C3羟基乙酰化修饰可增强抗原抑制活性,而酯键与酰胺键对活性影响无显著差异。
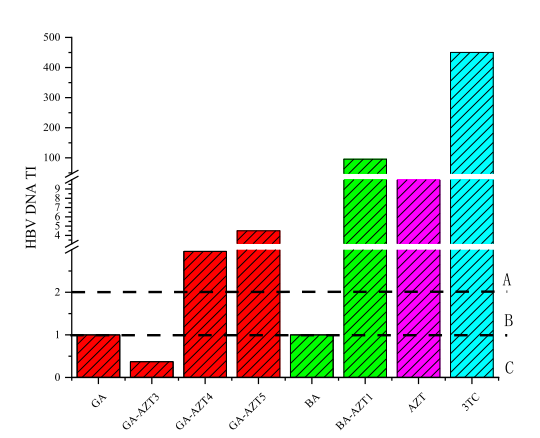
图4:缀合物对HBV DNA复制的抑制作用
基于Q-PCR的HBV DNA定量分析表明,BA-AZT1对病毒DNA复制的抑制活性最强(IC50=0.70 μM,TI=95.62),较AZT(IC50=7.29 μM)提高10.4倍,与阳性药拉米夫定(3TC,IC50=0.84 μM)相当。GA-AZT5的IC50为7.51 μM,而母体GA和OA无显著抑制效果(IC50>100 μM)。图中数据验证了缀合物通过靶向HBV Pol抑制病毒复制的双重机制,同时突显BA-AZT1的高效性和低毒性。
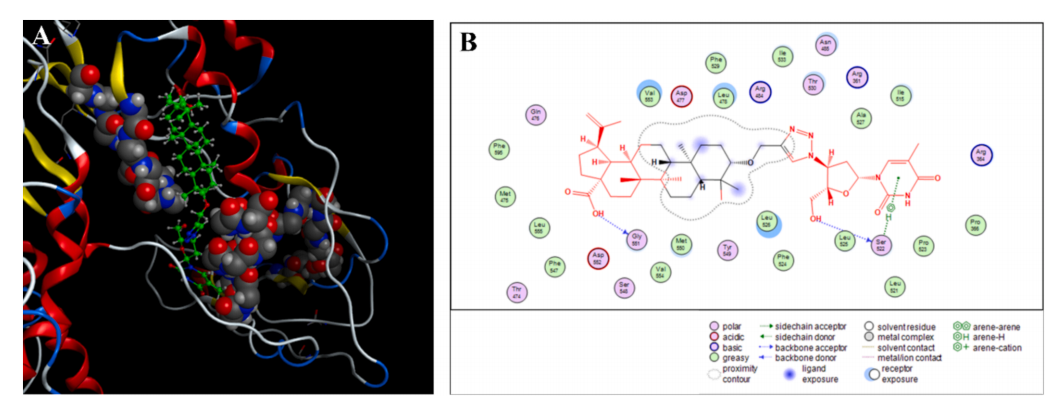
图5:BA-AZT1与HBV Pol的分子对接模型
分子对接模拟显示,BA-AZT1的AZT部分嵌入HBV Pol逆转录区(RT区)的B区(505-528位氨基酸),与515 Ile、520 Pro等残基形成疏水作用,其C5羟基与522 Ser形成氢键。BA部分则与C区(546-556位)的547 Phe、553 Val等残基通过疏水链结合,且C28羧基与551 Gly形成氢键。该模型揭示了BA-AZT1通过协同作用同时靶向Pol的B/C区,增强结合稳定性,解释了其强效抑制DNA复制的分子基础。
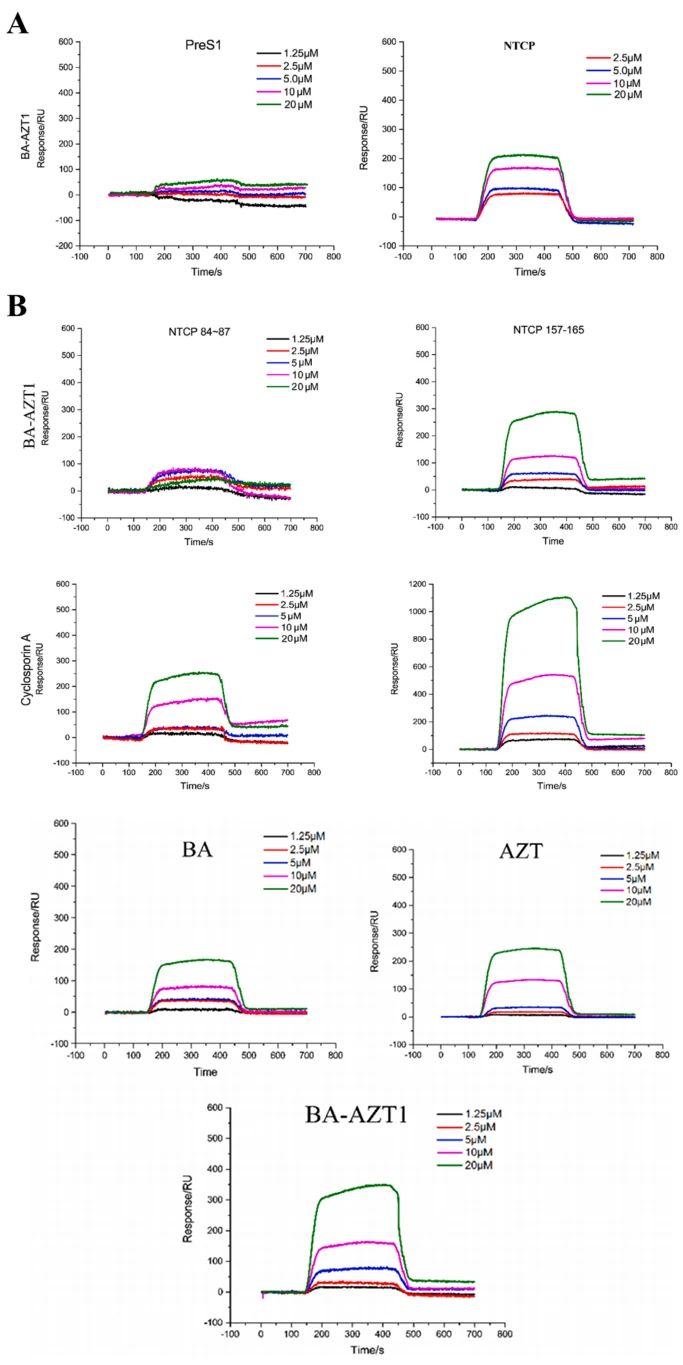
图6:SPR分析BA-AZT1与靶点的结合亲和力
表面等离子共振(SPR)实验显示,BA-AZT1与HBV Pol C区肽段的结合亲和力(KD=19.55 μM)显著高于母体BA(KD=53.21 μM)和AZT(KD=31.82 μM)。此外,BA-AZT1选择性结合NTCP的157-165表位(KD=38.79 μM),而对病毒PreS1蛋白无显著结合。数据证实其通过阻断NTCP介导的病毒入侵和抑制Pol功能的双靶点机制发挥抗HBV作用。
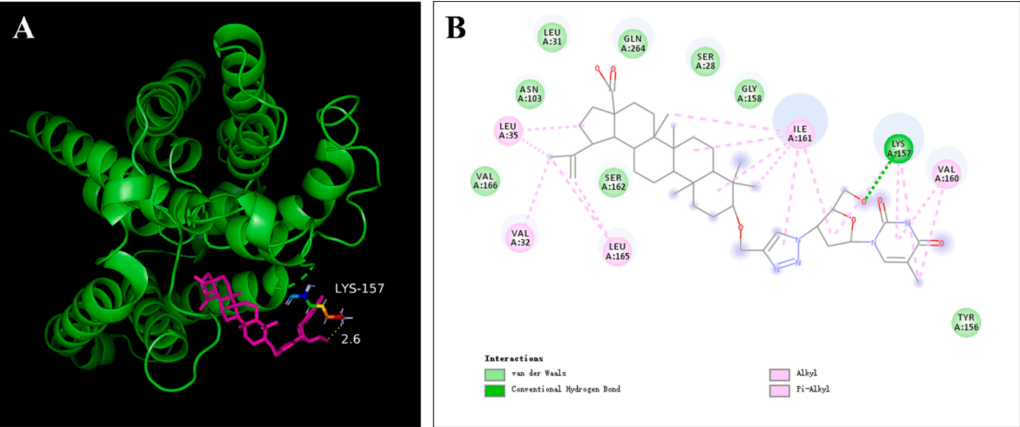
图7:BA-AZT1与NTCP 157-165表位的相互作用模式
分子对接表明,BA-AZT1的平面五环骨架插入NTCP的157-165表位界面。AZT部分与157 Lys形成氢键及π-烷基作用,BA部分与161 Ile、165 Leu等残基通过疏水作用结合,同时与156 Tyr、162 Ser等形成范德华力。该相互作用模拟解释了BA-AZT1通过竞争性占据NTCP病毒结合位点,阻断HBV进入宿主细胞的分子机制,为其抑制HBsAg分泌提供了结构依据。
研究发现,缀合物BA-AZT1表现出显著的双靶点抑制活性:其抑制HBsAg分泌的IC50为0.65 μM,治疗指数(TI)达102.98,活性较母体化合物BA和AZT分别提高284倍和442倍;同时,抑制HBV DNA复制的IC50为0.70 μM,活性为AZT的10.4倍,治疗指数(95.62)显著优于对照药物。机制研究表明,BA-AZT1的AZT部分靶向HBV Pol的B区,抑制DNA复制,而五环三萜骨架插入NTCP的157-165表位,阻断病毒进入宿主细胞。分子对接和SPR实验证实,BA-AZT1通过氢键、疏水作用及范德华力与靶点强效结合。该研究为开发兼具抗病毒复制和清除表面抗原功能的双靶点抗HBV药物提供了新思路。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:基于明亮生物发光的BRET传感器蛋白用于检测细胞内半胱天冬酶活性