常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-05-10 17:00:00 细胞资源库平台 访问量:7
在生物医学研究和药物开发领域,生物发光成像技术因其高信噪比而被广泛应用于细胞测定和动物成像研究。然而,传统的荧光素酶种类有限,限制了同时成像多个分子和细胞事件的能力。为了突破这一限制,科学家们开发了一种新型的ATP非依赖性荧光素酶——NanoLuc(NL),它源自深海虾Oplophorus gracilirostris,并经过工程改造以增强蛋白质稳定性。NanoLuc作为一种小型(19 kDa)、高亮度的荧光素酶,其亮度是传统萤火虫或海肾荧光素酶的100倍,并且使用furimazine作为底物产生明亮的辉光型发光。NanoLuc的意义在于其为双报告基因生物发光分子成像提供了新的可能。它不仅可以在活体小鼠的表层和深层组织中成像,而且其生物发光随时间的变化可以用来定量肿瘤生长,甚至在少量血清中也能检测到分泌的NL。此外,NanoLuc与萤火虫荧光素酶的结合使用,为在完整细胞和活体小鼠中定量TGF-β信号传导的两个关键步骤提供了一种新型双荧光素酶成像策略,从而在正常生理、疾病和药物开发中扩展了信号转导的成像能力。NanoLuc的作用不仅体现在其高灵敏度和高稳定性上,它还具有更小的尺寸,这使得在标记细胞和蛋白质时对样本的侵入性更小,有助于保持细胞或组织的天然状态。NanoLuc的快速反应、低背景发光和多样灵活等特点,使其在生物学和医学研究中具有广泛的应用前景。因此,NanoLuc作为一种新的报告基因,不仅增强了我们对生物过程的理解和疾病机理的研究,而且在开发潜在治疗方法和疗法方面发挥了重要作用。
英文标题:The Fatty Acid Transporter CD36 Mediates Uptake, Biodistribution, and Cardioprotection by Small Extracellular Vesicles From HEK293 Cells
中文标题:CD36 介导 HEK293 来源小细胞外囊泡的摄取、体内分布与心脏保护作用
发表期刊:《Journal of Extracellular Vesicles》
影响因子:14.5
作者单位:
The Hatter Cardiovascular Institute, University College London, London, UK
作者信息:
第一作者:Li Shen
通讯作者:Zhi-Liang Lu
小细胞外囊泡(sEVs)是介导细胞间信息交流的纳米级生物活性分子载体,在心肌梗死(MI)模型中已被证实具有显著的心脏保护效应,但其被心肌细胞、内皮细胞摄取的具体分子机制,以及静脉注射后的体内分布规律尚未完全阐明;脂肪酸转运蛋白 CD36 是广泛表达于心肌细胞、血管内皮细胞与巨噬细胞表面的脂质结合型清道夫受体,可特异性识别 sEVs 膜上的磷脂酰丝氨酸(PS)等脂质成分,基于 sEVs 与氧化型低密度脂蛋白(oxLDL)的结构相似性,本研究提出科学假设:CD36 是介导 HEK293 来源 sEVs 细胞摄取、体内器官分布的关键分子,并进一步探究 CD36 在 sEVs 减轻心肌缺血再灌注(I/R)损伤中的核心作用,明确无再生特性的 HEK293 细胞来源 sEVs 是否具备心肌保护治疗潜力。
本研究通过CD63 - 纳米荧光素酶(Nluc) 融合质粒转染 HEK293 细胞,构建可被高灵敏示踪的标记 sEVs;采用切向流过滤(TFF)联合尺寸排阻色谱(SEC)纯化 sEVs,通过纳米颗粒跟踪分析(NTA)测定 sEVs 粒径与浓度、DELFIA 免疫检测鉴定 sEVs 特异性标志物(CD9、CD63、CD81)、BCA 蛋白 assay 评估 sEVs 纯度;体外实验选用人冠脉微血管内皮细胞(HCMEC)、人冠脉动脉内皮细胞(HCAEC)、人脐静脉内皮细胞(HUVEC)及原代成年大鼠心肌细胞,使用 CD36 不可逆抑制剂 SSO、网格蛋白介导内吞(CME)抑制剂氯丙嗪进行干预,通过荧光素酶活性检测与激光共聚焦成像评估 sEVs 细胞摄取效率;体内实验构建 C57BL/6 小鼠心肌 I/R 损伤模型(左前降支结扎 40min,再灌注 2h),在再灌注起始阶段经颈静脉注射 HEK293-sEVs,通过全身生理盐水灌注排除血管残留干扰,检测 sEVs 在心、肺、肝、脾、肾、脑等器官的分布水平,采用 TTC + 伊文思蓝双染色法测定心肌梗死面积与风险区面积;实验数据以均值 ± 标准误(mean±SEM)表示,采用单因素 ANOVA 联合 Tukey 事后检验进行统计学分析,P<0.05为差异具有统计学意义。
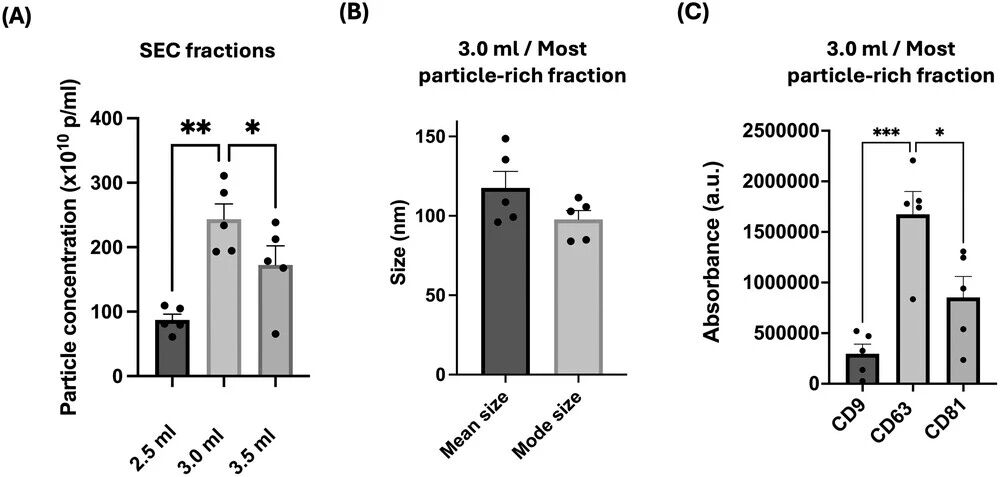
图 1:HEK293-sEVs 分离纯化后理化与生化表征完全符合功能实验要求
研究采用切向流过滤联合尺寸排阻色谱对 HEK293 细胞上清中的 sEVs 进行纯化,收集不同洗脱体积的组分后通过纳米颗粒跟踪分析(NTA)检测颗粒浓度与粒径分布,结果显示3.0mL 洗脱组分为 sEVs 高度富集组分,颗粒浓度高达 (2.4±0.2)×10¹² particles/mL,粒径分布峰值约为 108nm,模式粒径为 97nm±43nm,符合小细胞外囊泡(直径 < 200nm)的标准特征;同时通过 DELFIA 免疫检测发现,该组分高表达 sEVs 经典特异性标志物 CD9、CD63、CD81,其中 CD63 的表达水平最为显著;BCA 蛋白定量结合颗粒 / 蛋白比计算证实,该组分 sEVs 纯度达到 “高水平” 标准,无明显蛋白杂质污染,可直接用于后续体外摄取与体内功能实验,为研究结果的可靠性提供了基础保障。
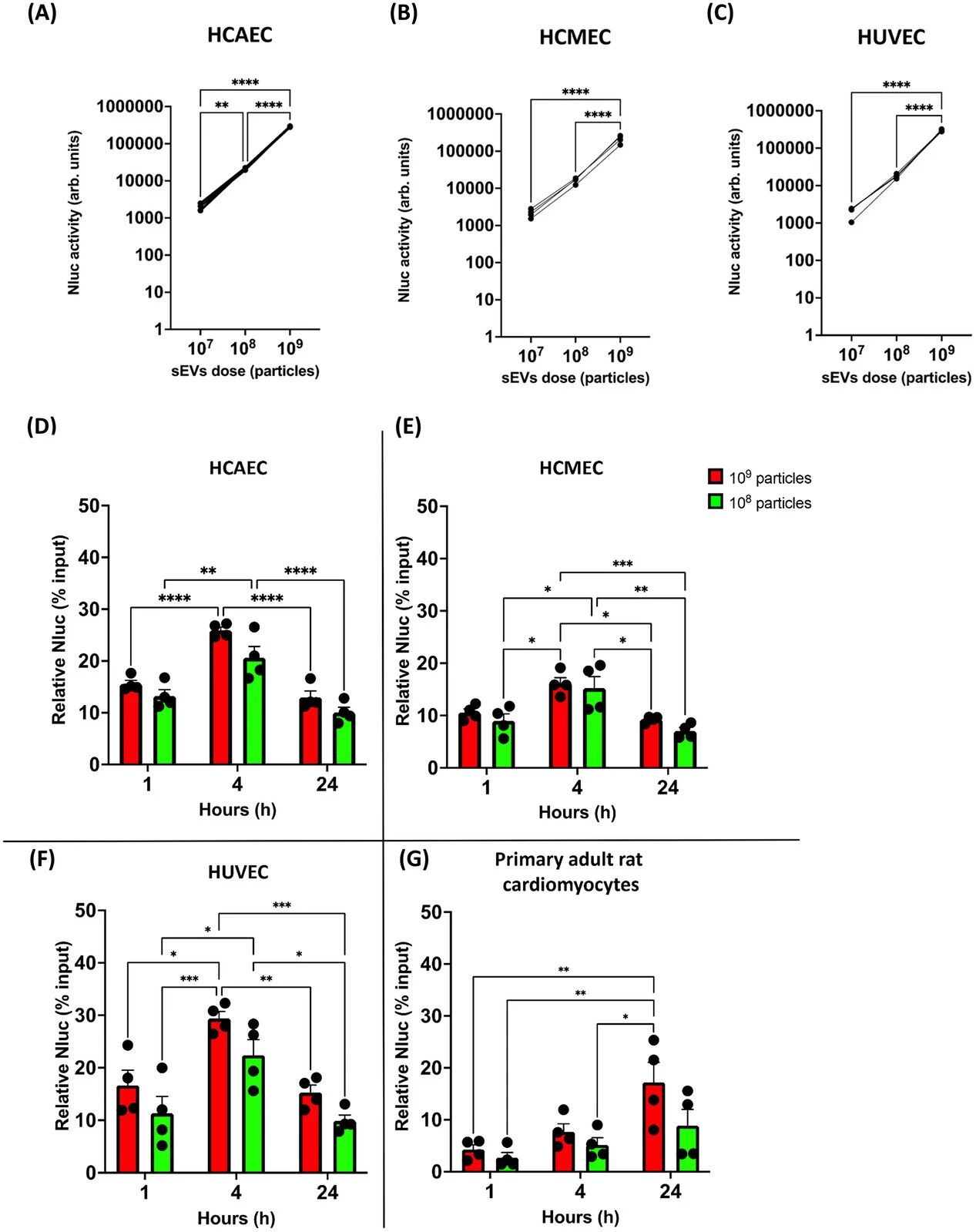
图 2:心脏来源内皮细胞对 HEK293-sEVs 的摄取效率远高于原代心肌细胞
研究将不同剂量(10⁷、10⁸、10⁹个)的 HEK293-sEVs 分别与人冠脉内皮细胞(HCAEC、HCMEC)、人脐静脉内皮细胞(HUVEC)及原代成年大鼠心肌细胞共孵育,设置 1h、4h、24h 三个时间节点检测细胞内纳米荧光素酶活性,评估 sEVs 摄取效率。结果显示,三种内皮细胞均呈现明显的剂量依赖性摄取,且在共孵育 1h 时即可快速摄取大量 sEVs,4h 达到摄取峰值,24h 因胞内降解导致摄取量有所下降;与之形成鲜明对比的是,原代大鼠心肌细胞在 1h 时 sEVs 摄取量极低,仅为内皮细胞的 4.3% 左右,直至 24h 才达到较高摄取水平,呈现显著的时间依赖性摄取特征。该结果直接证实,心脏内皮细胞是 HEK293-sEVs 的主要快速摄取细胞,而心肌细胞对 sEVs 的摄取速度慢、效率低。
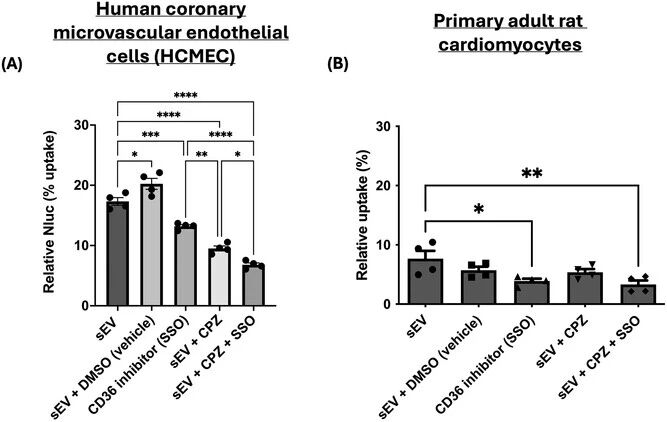
图 3:CD36 是介导 HEK293-sEVs 被心脏细胞摄取的关键受体,且在内皮细胞中与网格蛋白内吞通路协同作用
为明确 CD36 在 sEVs 摄取中的作用,研究采用 CD36 特异性不可逆抑制剂 SSO 预处理细胞,同时以氯丙嗪抑制网格蛋白介导内吞(CME)作为阳性对照,检测 HCMEC 与原代大鼠心肌细胞对 sEVs 的摄取变化。结果显示,SSO 抑制 CD36 后,人冠脉微血管内皮细胞(HCMEC)对 sEVs 的摄取量显著降低 25±6%,原代大鼠心肌细胞摄取量降低 49±20%;在 HCMEC 中,单独抑制 CME 通路可使 sEVs 摄取降低 45±5%,同时抑制 CD36 与 CME 通路可产生协同效应,使摄取量降低 60±3%;而在原代心肌细胞中,抑制 CME 通路对 sEVs 摄取无明显影响。该结果证实,CD36 独立介导 sEVs 被心肌细胞摄取,在心脏内皮细胞中则与 CME 通路共同、协同调控 sEVs 的内吞过程。
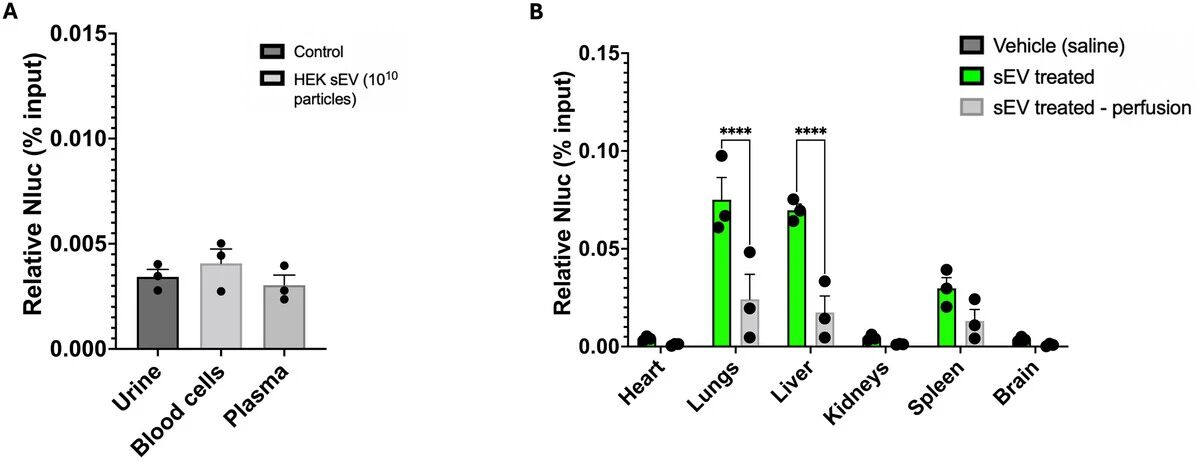
图 4:全身生理盐水灌注可排除血管内残留干扰,准确反映 HEK293-sEVs 在体内器官的真实摄取水平
为精准评估 sEVs 的体内分布,研究在小鼠静脉注射 HEK293-sEVs 1h 后,对部分小鼠进行全身生理盐水灌注处理,清除器官血管内残留的 sEVs,对比灌注与未灌注组小鼠器官及体液的荧光素酶活性。结果显示,静脉注射 sEVs 1h 后,超过 99% 的 sEVs 从血液循环中被清除,主要分布于肺、肝、脾三大器官,其中肺部信号最强;未灌注组小鼠肺、肝器官的荧光信号显著高于灌注组,提示未进行灌注处理会因血管内 sEVs 残留大幅高估组织细胞的真实摄取量;而尿液、血细胞、血浆等体液中的 sEVs 信号均低于 0.005%,几乎可忽略不计。该结果明确了全身灌注是 sEVs 体内分布检测的必要步骤,保证了分布数据的准确性。
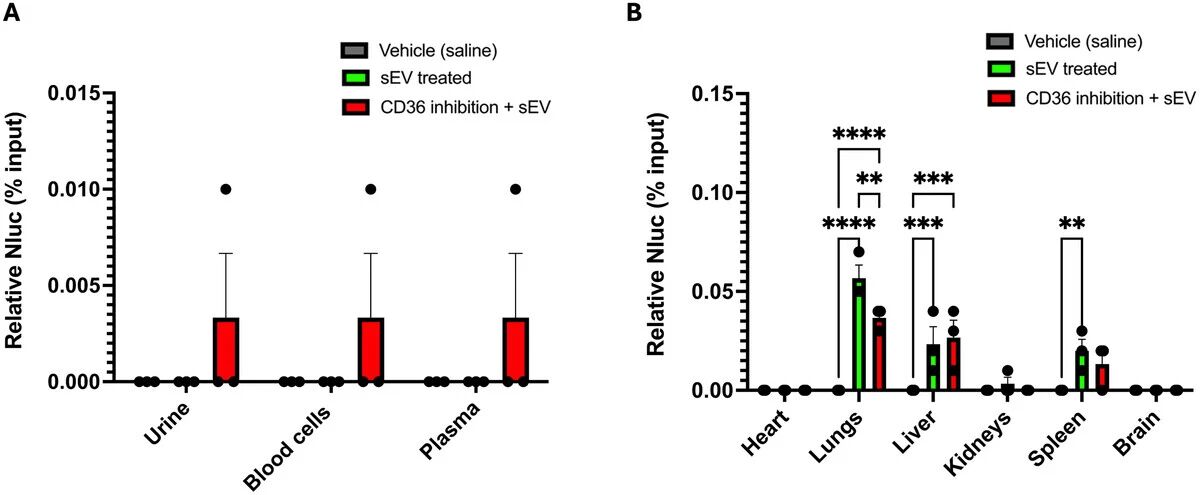
图 5:CD36 抑制可显著降低 HEK293-sEVs 在小鼠肺部的体内富集水平
研究通过腹腔注射 SSO 预先抑制小鼠体内 CD36 功能,1h 后再静脉注射 HEK293-sEVs,检测 sEVs 在各器官与体液中的分布变化。结果显示,CD36 被抑制后,sEVs 在小鼠肺部的摄取量较单纯 sEVs 处理组显著降低,差异具有统计学意义;而在肝、脾、肾、心、脑等其他器官,以及尿液、血细胞、血浆等体液中,sEVs 的分布水平无明显变化。该结果直接证明,CD36 分子特异性调控 HEK293-sEVs 在肺部的靶向富集,是影响 sEVs 体内器官分布的关键分子。
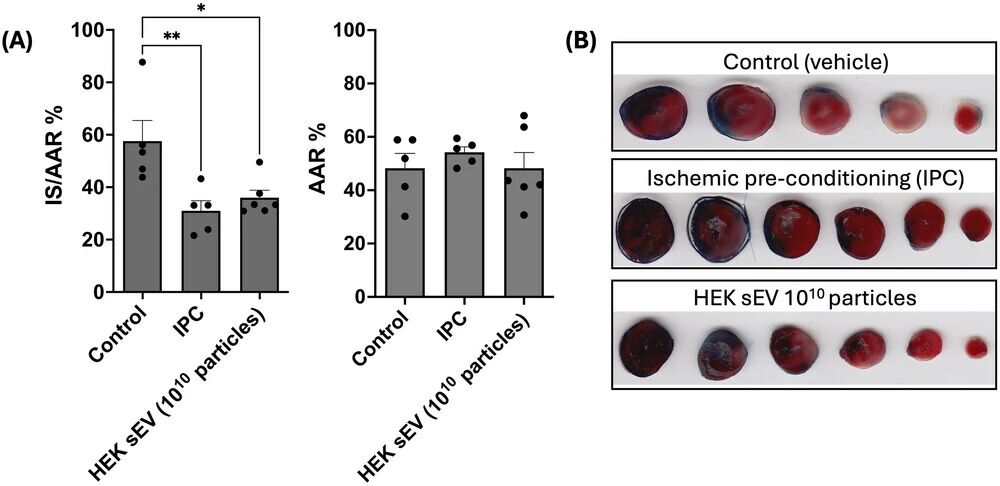
图 6:HEK293-sEVs 在小鼠心肌缺血再灌注损伤模型中发挥显著的心脏保护作用
研究构建小鼠心肌 I/R 损伤模型,在再灌注起始阶段经颈静脉注射 10¹⁰个 HEK293-sEVs,再灌注 2h 后通过 TTC + 伊文思蓝双染色法测定心肌梗死面积。结果显示,与生理盐水对照组相比,HEK293-sEVs 处理组小鼠的心肌梗死面积从 58%±8% 显著降至 36%±3%,保护效果显著(P<0.05);同时设置缺血预处理(IPC)阳性对照组,其心肌保护效果与 HEK293-sEVs 处理组相当,且各组小鼠心肌风险区(AAR)面积无显著差异,排除了手术操作差异对结果的干扰。该结果首次证实,无再生、免疫调节特性的 HEK293 细胞来源 sEVs,仍具备显著的心肌缺血再灌注损伤保护能力。
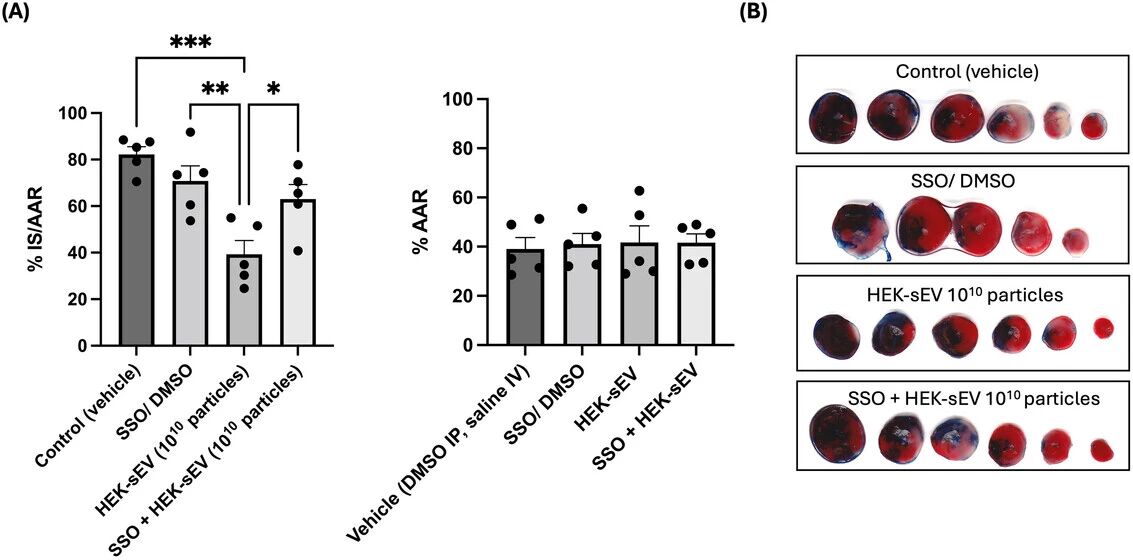
图 7:CD36 功能完整是 HEK293-sEVs 发挥心脏保护作用的必需条件
为验证 CD36 是否为 sEVs 心脏保护的核心分子,研究在小鼠造模前 1h 腹腔注射 SSO 抑制 CD36,再于再灌注起始给予 HEK293-sEVs,检测心肌梗死面积变化。结果显示,单独使用 SSO 抑制剂对小鼠心肌梗死面积无明显影响,与对照组无统计学差异;而 SSO 联合 HEK293-sEVs 处理组,sEVs 缩小心肌梗死面积的保护效应完全消失,梗死面积从单纯 sEVs 组的 39%±6% 回升至 63%±6%。该结果明确证实,CD36 的功能完整是 HEK293-sEVs 发挥心肌保护作用的必需前提,阻断 CD36 可完全消除 sEVs 的心脏保护效应。
本研究首次证实脂肪酸转运蛋白 CD36是介导 HEK293 来源小细胞外囊泡(sEVs)被心脏细胞摄取、调控体内器官分布的关键分子,心脏内皮细胞对 sEVs 的快速摄取高度依赖 CD36 通路,心肌细胞则通过 CD36 独立介导 sEVs 内吞;静脉注射 HEK293-sEVs 可显著减轻小鼠心肌缺血再灌注损伤,有效缩小心肌梗死面积,且该心脏保护作用完全依赖 CD36 的正常功能,抑制 CD36 后保护效应彻底消失;同时研究突破传统认知,证实无再生、免疫调节特性的普通细胞系(HEK293)来源 sEVs 仍具备心肌梗死治疗潜力。该研究明确了 CD36 在 sEVs 心脏保护中的核心机制,为小细胞外囊泡靶向心脏递送、急性心肌梗死的无细胞治疗提供了全新的分子靶点与研发方向。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:核酸研究新工具:HAMMER 精准检测 APOBEC3A mRNA 编辑活性