常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-05-08 17:00:00 细胞资源库平台 访问量:8
在癌症免疫治疗中,肿瘤浸润 Treg 细胞是导致免疫逃逸的关键 “帮凶”,其高表达 PD-L1 和 CD47 等免疫检查点分子,既抑制效应 T 细胞活性,又通过 “别吃我” 信号逃避巨噬细胞吞噬。CD47 阻断在血液肿瘤中已显疗效,但实体瘤中面临抗原沉陷效应和肿瘤选择性不足的难题;而系统性抑制免疫检查点常伴随严重的脱靶毒性。因此,开发兼具肿瘤特异性和双靶点抑制功能的治疗工具,成为突破实体瘤治疗瓶颈的关键。
来自香港浸会大学中医药学院表型组学研究中心、整合生物信息学与转化科学研究所、粤港澳大湾区适配体转化医学与药物研发国际研究平台,以及英国伯明翰大学医学院的团队在《Molecular Biomedicine》上发表题为Targeting tumor‑infiltrating regulatory T cells: combining CD47 and PD‑L1 inhibition via a novel aptamer‑siRNA chimera的文章,研发了一种新型 PD-L1 适配体 - CD47 siRNA 嵌合体,通过双靶向抑制 PD-L1 和 CD47 信号,选择性耗尽肿瘤浸润调节性 T 细胞(Treg),在小鼠肝癌模型中显著抑制肿瘤生长并延长生存期,为实体瘤免疫治疗提供了非抗体类新策略。
1.PD-L1 适配体 - CD47 siRNA 嵌合体的设计与合成:采用内部 C3 间隔子将团队前期开发的 PD-L1 特异性适配体与 CD47 siRNA 偶联,构建 Cy5 标记的双功能嵌合体,通过酶联寡核苷酸 assay(ELONA)验证其与 PD-L1 蛋白的结合亲和力。
2.体外细胞实验验证靶向性与功能:分离小鼠肝癌模型中的肿瘤浸润 Treg 细胞,通过流式细胞术、共聚焦显微镜检测嵌合体的结合特异性、细胞摄取效率及内吞途径;采用 qPCR 和 Western blot 验证 CD47 沉默效果,Transwell 实验评估 Treg 细胞迁移能力。
3.体内动物实验评估抑瘤效果:构建 C57BL/6J 小鼠皮下 Hepa1-6 肝癌模型,从接种后第 7 天起每 3 天静脉注射嵌合体(2mg/kg),持续至第 29 天,监测肿瘤生长曲线、重量及小鼠生存期;通过 H&E 染色、Ki67 和 TUNEL 染色分析肿瘤增殖与凋亡。
4.免疫微环境与机制分析:采用流式细胞术检测肿瘤组织中 Treg、CD8⁺T 细胞、巨噬细胞等免疫细胞的数量与功能;通过 Seahorse 分析仪检测糖酵解速率(ECAR)和氧消耗速率(OCR),结合 Western blot 分析代谢相关信号通路(pERK1/2、pRac1 等)。
5.安全性与代谢组学评估:检测小鼠红细胞计数、肝肾功能指标(AST、ALT、BUN 等)评估生物安全性;通过液相色谱 - 质谱联用(LC-MS)分析血清氨基酸代谢谱,探究嵌合体对代谢通路的调控作用。
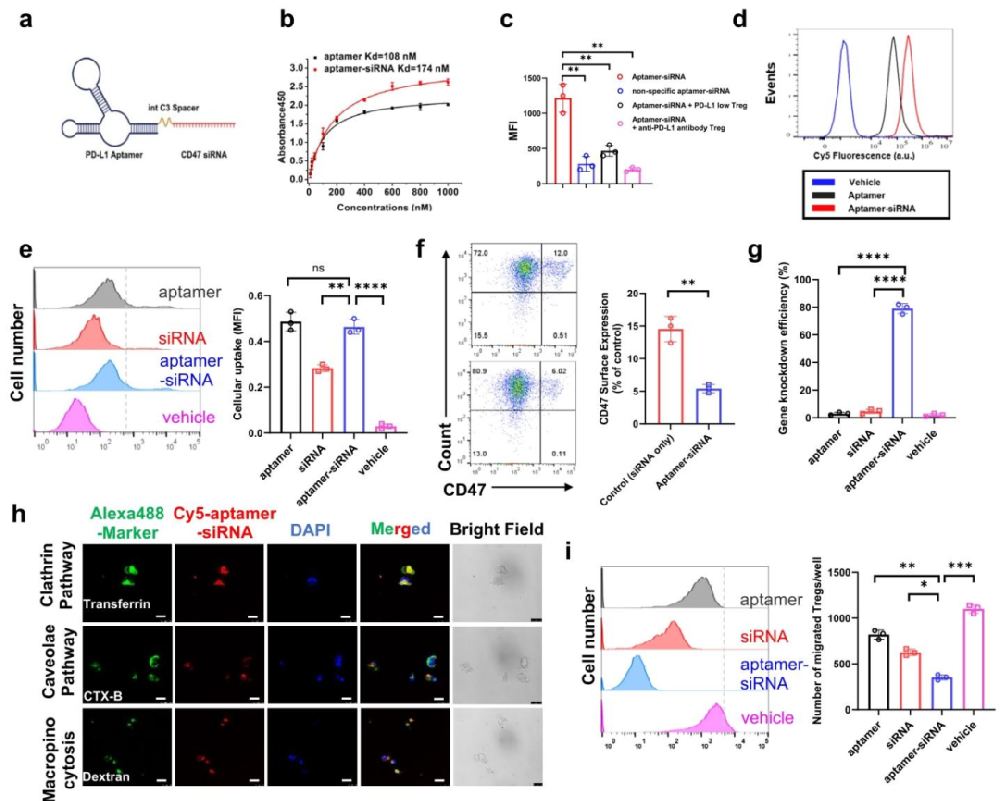
图1:嵌合体的合成表征与靶向细胞结合功能
该 PD-L1 适配体 - CD47 siRNA 嵌合体通过 C3 间隔子成功偶联,与 PD-L1 蛋白的结合亲和力维持在纳摩尔水平(Kd=174nM),虽略低于单独适配体但能避免脱靶结合。流式细胞术和共聚焦结果显示,嵌合体可特异性结合 PD-L1 高表达的肿瘤浸润 Treg 细胞,对 PD-L1 低表达细胞及经抗 PD-L1 抗体封闭的细胞结合能力极弱;其细胞摄取效率与游离适配体相当,显著高于游离 siRNA,且主要通过网格蛋白介导的内吞途径进入细胞。qPCR 和流式验证表明,嵌合体可高效沉默 Treg 细胞的 CD47 表达,同时显著抑制 Treg 细胞向 IP10(肝肿瘤微环境关键趋化因子)的迁移。
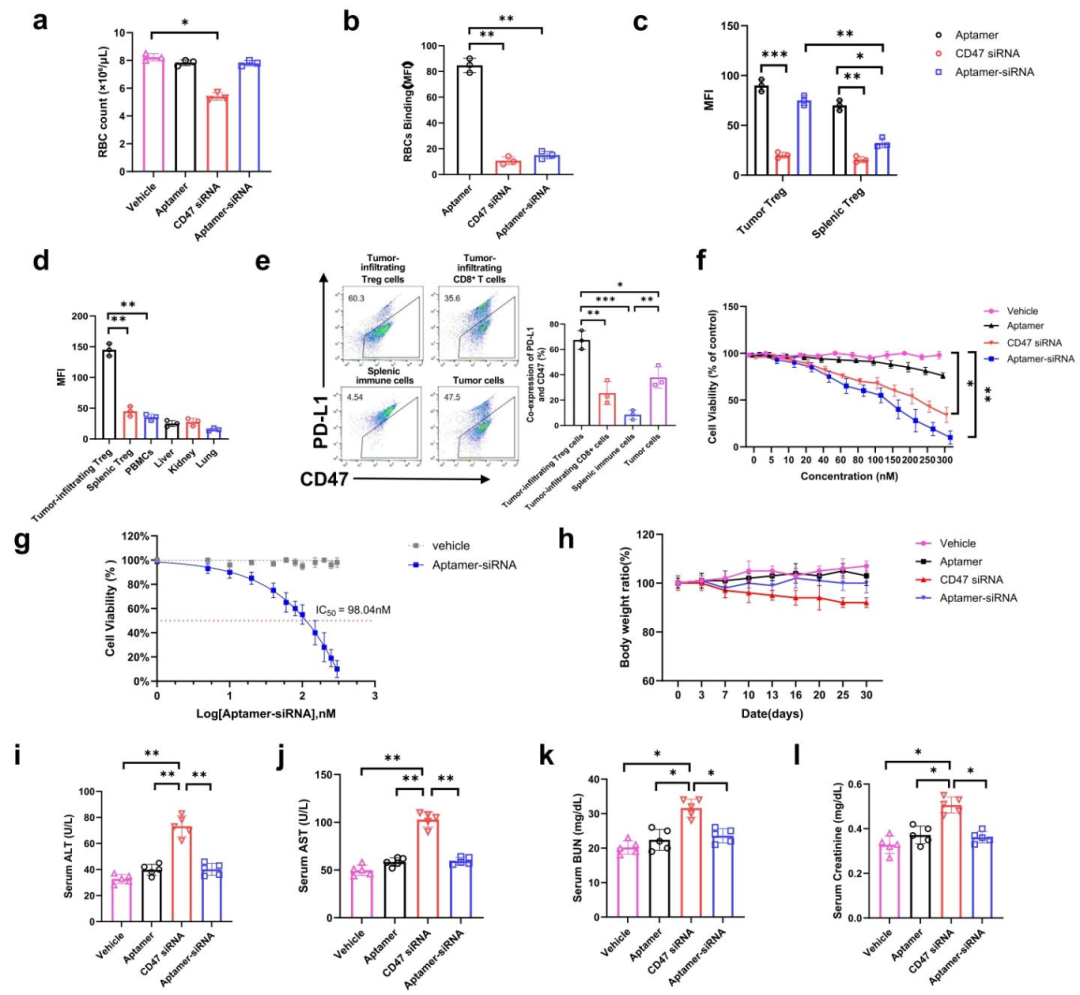
图2:嵌合体的肿瘤靶向特异性与体内安全性
体内生物分布分析显示,嵌合体在肿瘤浸润 Treg 细胞中富集程度显著高于脾脏 Treg 细胞和外周血单个核细胞(PBMC),且对肝、肾、肺等主要器官无明显蓄积。安全性评估表明,嵌合体处理组小鼠的红细胞计数与对照组无差异,而单独 siRNA 组出现轻微下降;肝肾功能指标(AST、ALT、BUN、肌酐)均在正常范围,且小鼠体重稳定,无明显系统毒性。MTT 实验显示嵌合体对肿瘤浸润 Treg 细胞的半数抑制浓度(IC50)为 98.04nM,具备强效靶向杀伤能力。
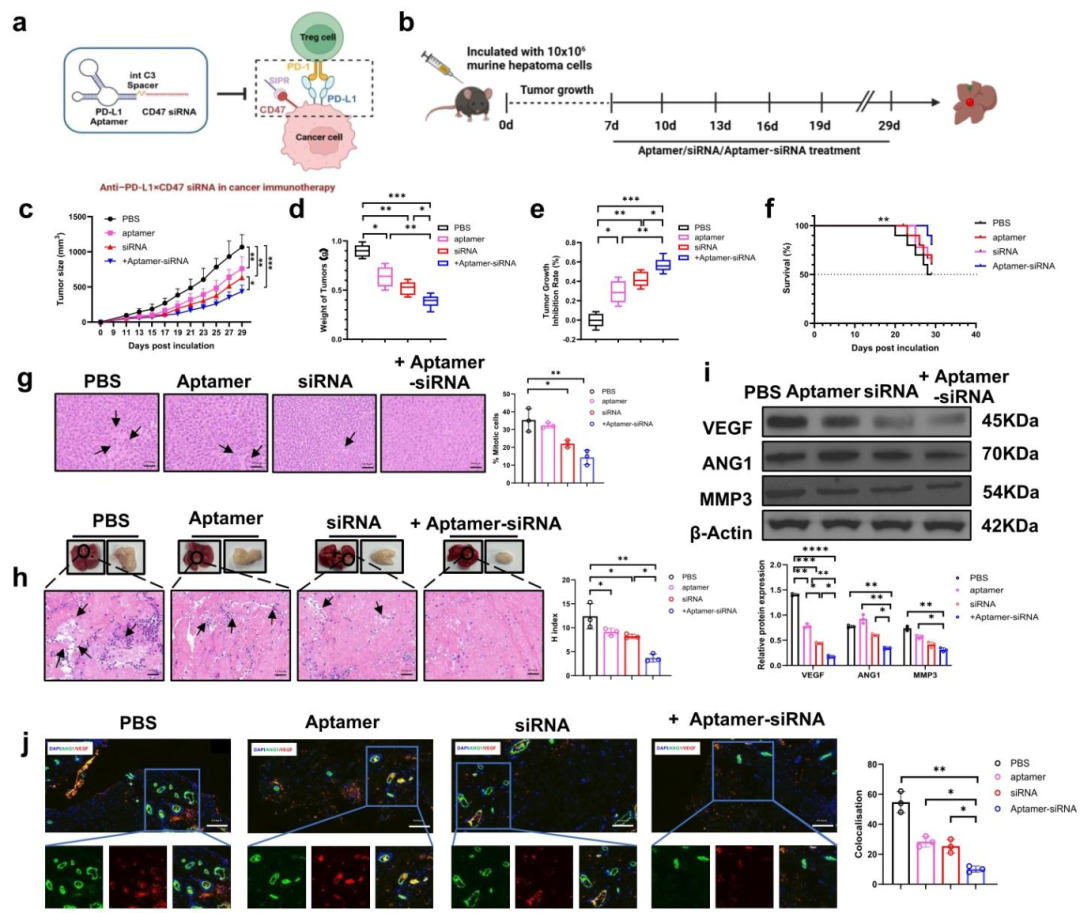
图3:嵌合体显著抑制肝癌生长并阻断血管生成
在小鼠肝癌模型中,嵌合体治疗组的肿瘤体积和重量显著小于 PBS 组、单独适配体组及单独 siRNA 组,肿瘤抑制率大幅提升;Kaplan-Meier 生存分析显示,嵌合体处理组小鼠生存期显著延长。组织学分析表明,嵌合体可减少肿瘤组织中 Ki67 阳性增殖细胞数量,增加 TUNEL 阳性凋亡细胞比例;Western blot 和免疫荧光结果显示,肿瘤组织中 VEGF、MMP-3、ANG-1 等血管生成关键分子的表达显著降低,且 VEGF 与 ANG-1 的共定位明显减少,表明血管生成过程受到有效抑制。
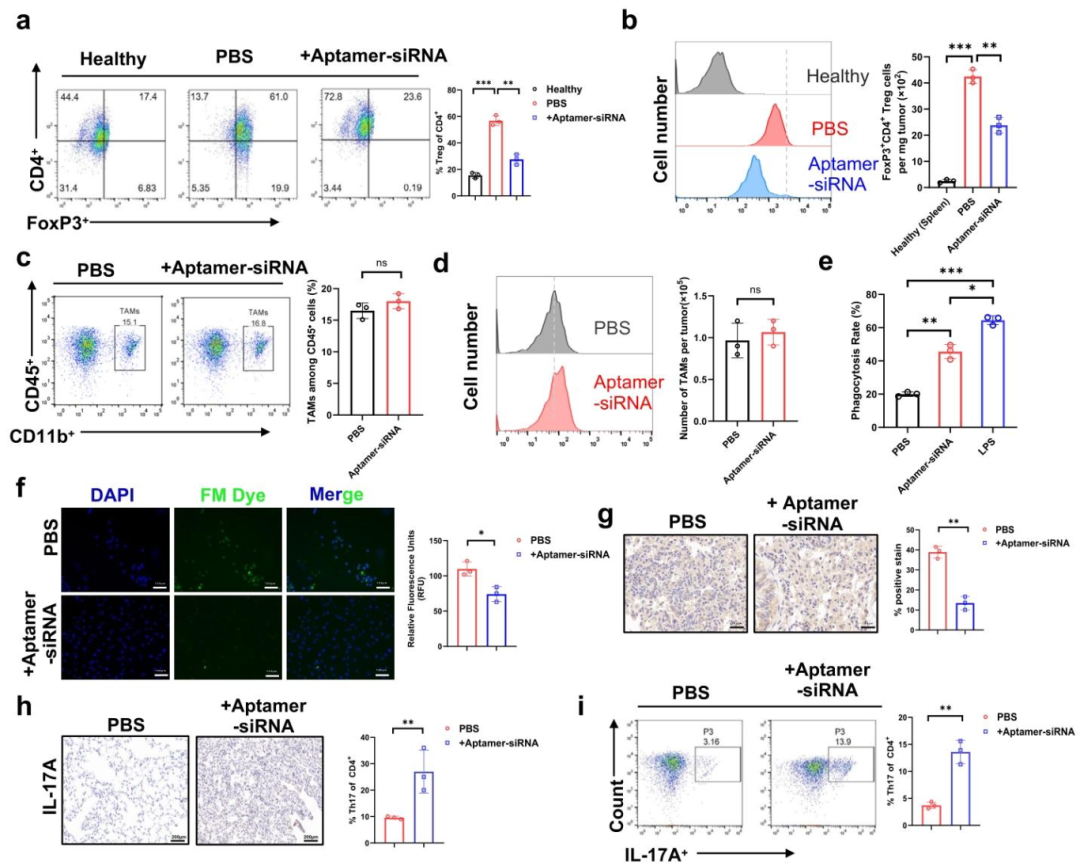
图4:嵌合体选择性耗尽 Treg 细胞并增强抗肿瘤免疫浸润
流式细胞术分析显示,嵌合体治疗后肿瘤组织中 FoxP3⁺CD4⁺Treg 细胞的频率和绝对数量显著减少,但总 CD4⁺T 细胞数量无明显变化,且 Th17 细胞(IL-17A⁺CD4⁺)比例代偿性增加。肿瘤相关巨噬细胞(TAM)的数量和极化状态(CD80⁺M1/CD206⁺M2)无明显改变,但巨噬细胞的吞噬活性显著增强;同时,肿瘤浸润 CD8⁺T 细胞的数量显著增加,且 IFN-γ、颗粒酶 B、CD69 等效应分子和激活标志物的表达上调,提示效应 T 细胞功能增强。免疫组化和荧光染色进一步验证了 Treg 细胞浸润减少和 Th17 细胞浸润增加的表型。
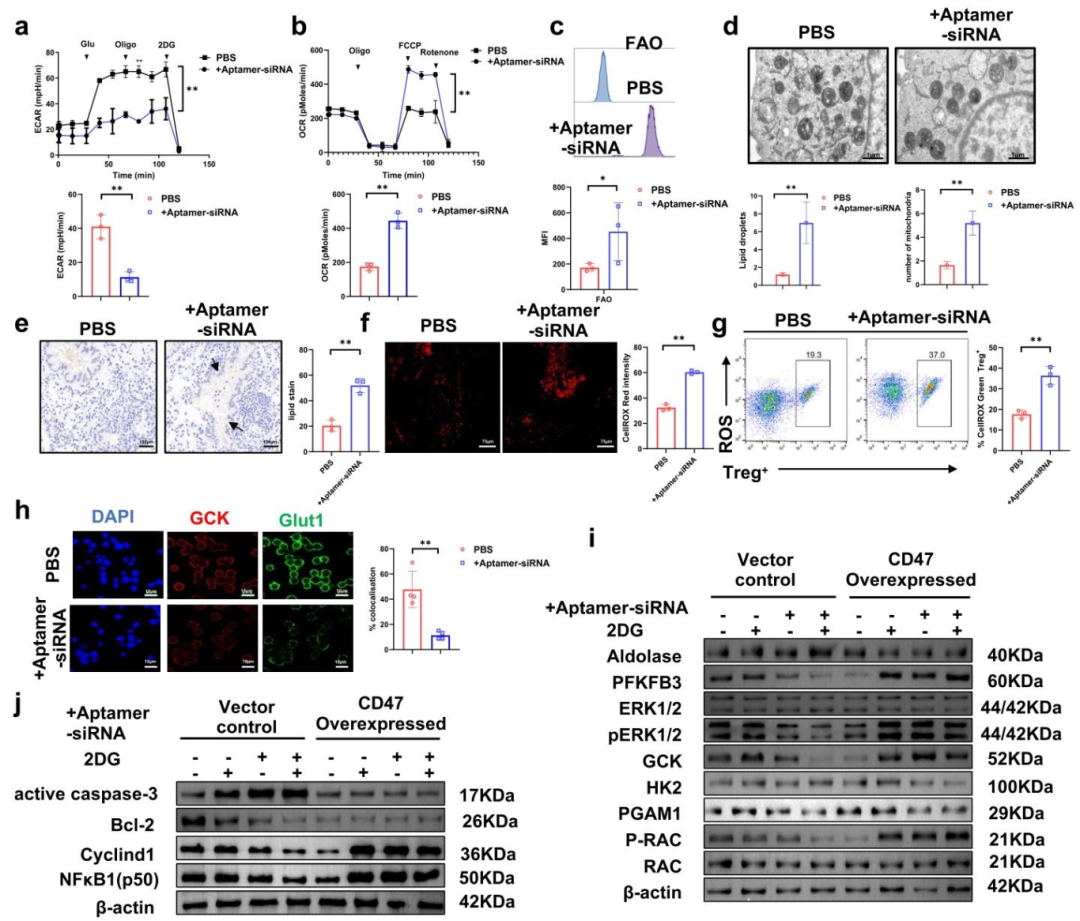
图5:嵌合体诱导 Treg 细胞代谢重编程与凋亡
Seahorse 分析显示,嵌合体处理后 Treg 细胞的糖酵解速率(ECAR)显著降低,线粒体呼吸速率(OCR)和脂肪酸氧化(FAO)活性升高,伴随细胞内脂质滴积累和线粒体活性氧(ROS)水平增加。共聚焦和 Western blot 结果表明,Treg 细胞中葡萄糖转运蛋白 Glut1 和葡萄糖激酶(GCK)的表达下调,糖酵解相关蛋白(PFKFB3、p-ERK1/2、p-Rac1)表达降低;同时,Cyclin D1、Bcl-2、NF-κB 等存活相关分子表达减少,活性 caspase-3 表达增加,提示 Treg 细胞发生凋亡。CD47 过表达可逆转上述代谢和凋亡表型,证实 CD47 沉默是关键调控因素。
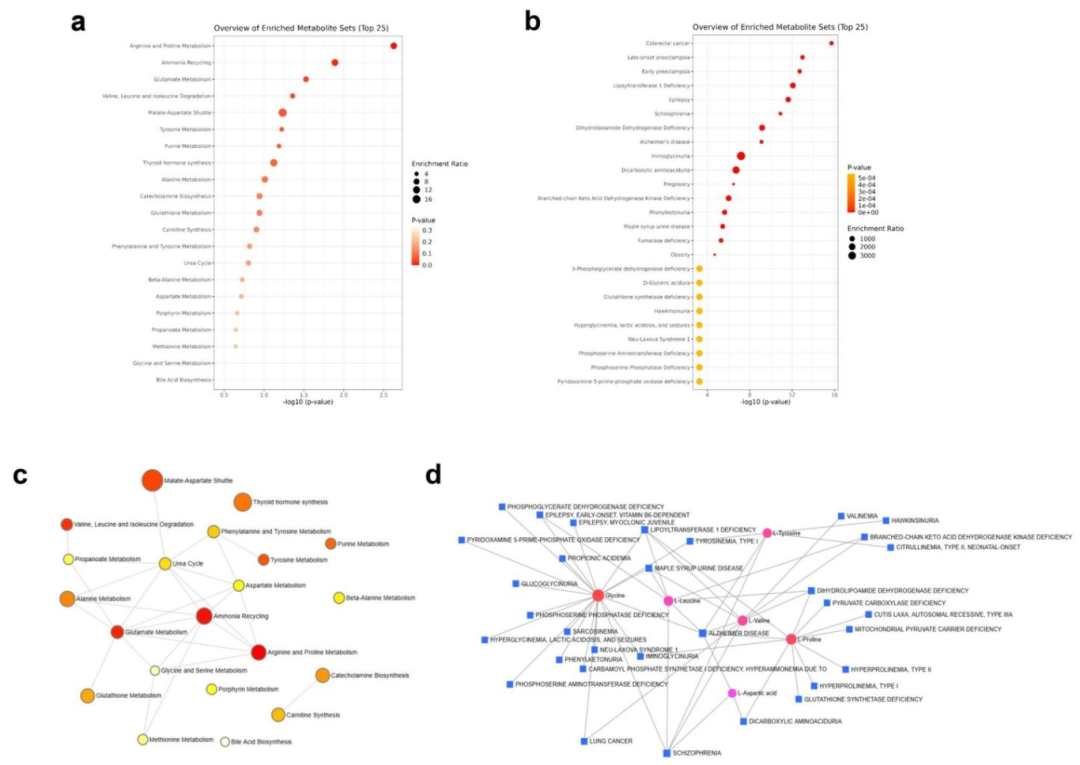
图6:嵌合体调控脯氨酸代谢通路影响肿瘤免疫微环境
代谢组学分析显示,嵌合体治疗后小鼠血清中天门冬氨酸、甘氨酸、亮氨酸、脯氨酸等氨基酸水平显著改变。KEGG 通路富集分析表明,精氨酸 - 脯氨酸代谢、缬氨酸 - 亮氨酸 - 异亮氨酸降解等通路被显著调控;疾病特征富集分析显示,这些代谢变化与脂质转移酶 1 缺乏症、二氢硫辛酰胺脱氢酶缺乏症等代谢疾病相关,其中脯氨酸作为核心代谢物,其水平降低可能通过重塑肿瘤微环境的免疫抑制表型,促进抗肿瘤免疫应答。
该研究针对实体瘤免疫治疗中 CD47 阻断的局限性和系统性免疫检查点抑制的脱靶毒性,设计了一种新型 PD-L1 适配体 - CD47 siRNA 嵌合体,通过 PD-L1 介导的靶向递送实现对肿瘤浸润 Treg 细胞的精准识别,同时发挥 PD-L1 抑制和 CD47 沉默的协同作用,既破坏 Treg 细胞的免疫抑制功能,又通过代谢重编程(抑制糖酵解、增强脂肪酸氧化)和凋亡诱导耗尽 Treg 细胞,进而解除对 CD8⁺T 细胞和巨噬细胞的抑制,重塑抗肿瘤免疫微环境。在小鼠肝癌模型中,该嵌合体展现出显著的抑瘤效果和良好的生物安全性,为实体瘤免疫治疗提供了一种非抗体类、肿瘤特异性的新策略;但研究仍存在单一肿瘤模型的局限性,未来需在更多实体瘤模型中验证,并深入解析代谢重编程的上游调控机制,推动该 RNA 疗法向临床转化。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:体视学定量分析肿瘤浸润免疫细胞:转移性黑色素瘤免疫治疗的预测新工具
下一篇:表木兰脂素 A 通过抑制 p38/NF-κB 及 AP-1 信号通路减少 PMA 诱导的 THP-1 细胞 IL-6 生成