常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-05-01 09:00:00 细胞资源库平台 访问量:23
在生物医学研究和药物开发领域,生物发光成像技术因其高信噪比而被广泛应用于细胞测定和动物成像研究。然而,传统的荧光素酶种类有限,限制了同时成像多个分子和细胞事件的能力。为了突破这一限制,科学家们开发了一种新型的ATP非依赖性荧光素酶——NanoLuc(NL),它源自深海虾Oplophorus gracilirostris,并经过工程改造以增强蛋白质稳定性。NanoLuc作为一种小型(19 kDa)、高亮度的荧光素酶,其亮度是传统萤火虫或海肾荧光素酶的100倍,并且使用furimazine作为底物产生明亮的辉光型发光。NanoLuc的意义在于其为双报告基因生物发光分子成像提供了新的可能。它不仅可以在活体小鼠的表层和深层组织中成像,而且其生物发光随时间的变化可以用来定量肿瘤生长,甚至在少量血清中也能检测到分泌的NL。此外,NanoLuc与萤火虫荧光素酶的结合使用,为在完整细胞和活体小鼠中定量TGF-β信号传导的两个关键步骤提供了一种新型双荧光素酶成像策略,从而在正常生理、疾病和药物开发中扩展了信号转导的成像能力。NanoLuc的作用不仅体现在其高灵敏度和高稳定性上,它还具有更小的尺寸,这使得在标记细胞和蛋白质时对样本的侵入性更小,有助于保持细胞或组织的天然状态。NanoLuc的快速反应、低背景发光和多样灵活等特点,使其在生物学和医学研究中具有广泛的应用前景。因此,NanoLuc作为一种新的报告基因,不仅增强了我们对生物过程的理解和疾病机理的研究,而且在开发潜在治疗方法和疗法方面发挥了重要作用。
英文标题:Development of a novel NanoBRET high-throughput drug screening assay for human GnRH receptor using sulfo-cyanine 5 fluorophore
中文标题:基于磺化花青素 5 荧光团构建人促性腺激素释放激素受体的新型纳米生物发光共振能量转移高通量药物筛选方法
发表期刊:《Journal of Pharmaceutical Analysis》
影响因子:8.9
作者单位:
1.Department of Biosciences and Bioinformatics, and Suzhou Municipal Key Lab of Cancer Biology and Chronic Disease, School of Science, Xi'an Jiaotong-Liverpool University, Suzhou, Jiangsu, 215123, China
2.Department of Biochemistry, Cell and Systems Biology, Institute of Systems, Molecular and Integrative Biology, University of Liverpool, Liverpool, L69 7BE, United Kingdom
作者信息:
第一作者:Li Shen
通讯作者:Zhi-Liang Lu
G 蛋白偶联受体(GPCRs)是人体细胞膜表面最大的受体超家族,介导细胞感知外界信号并启动下游级联反应,是目前临床超过 30% 药物的作用靶点,在生殖疾病、肿瘤、内分泌紊乱等疾病治疗中占据核心地位;传统 GPCR 配体结合研究以放射性配体结合法为金标准,但该方法存在放射性安全隐患、废弃物处理困难、操作繁琐、无法适配高通量药物筛选(HTS)的致命缺陷,而表面等离子共振、受体色谱等无标记技术存在膜蛋白固定困难、非特异性结合高、检测环境脱离生理状态的问题;纳米生物发光共振能量转移(NanoBRET)技术以高亮度、小分子量的 NanoLuc 为供体,无需外部激发光,可在活细胞生理状态下实现配体 - 受体结合的实时、均相检测,成为 GPCR 药物筛选的理想技术;促性腺激素释放激素受体(GnRHR)属于 A 类 GPCR,主要偶联 Gq/11 蛋白,调控人体生殖内分泌功能,是治疗性早熟、子宫内膜异位症、前列腺癌、乳腺癌等激素依赖性疾病的关键靶点,然而人源 GnRHR(hGnRHR)存在天然细胞膜表达量极低、第二胞外环赖氨酸 191(K191)导致受体膜定位效率差的问题,同时现有 NanoBRET 体系常用的 BODIPY、TAMRA 等荧光团存在非特异性结合高、水溶性差、与 NanoLuc 能量转移效率不足的缺陷,严重限制了 hGnRHR 靶向药物的高通量筛选与药理学研究;基于此,本研究以磺化花青素 5(sCy5)为新型荧光团,理性设计并合成高亲和力、低非特异性结合的 GnRH 荧光配体,同时通过 N 端融合 IL-6 分泌信号肽 - NanoLuc 并敲除 K191 位点改造 hGnRHR,构建兼具高灵敏度、高特异性、低背景、活细胞兼容的 NanoBRET 配体结合体系,最终建立可用于 hGnRHR 靶向小分子与肽类药物的高通量筛选平台,为 GnRHR 信号选择性药物研发提供全新技术工具。
本研究首先采用分子克隆技术构建系列重组质粒,将 hGnRHR cDNA 亚克隆至含 NanoLuc 的 pNLF1-N.CMV hygro 与含 IL-6 分泌信号肽的 pNLF1-secN.CMV hygro 载体,通过重叠延伸 PCR 分别构建 K191E 点突变与 K191 缺失(K191Δ)的突变体质粒,并在 secNluc 与 hGnRHR 之间插入 GGGS 柔性连接肽以保证受体正确折叠;选用 HEK293、COS-7、SCL60(稳定表达大鼠 GnRHR 的 HEK293 细胞)为实验细胞,在含 10% 胎牛血清、2mM L - 谷氨酰胺、双抗的 DMEM 培养基中,37℃、5% CO₂条件下培养,通过 Fugene HD 转染试剂进行瞬时转染,电转法构建稳定表达 N-secNluc-hGnRHR 与 N-secNluc-hGnRHR-K191Δ 的 HEK293 细胞株,经潮霉素 B 筛选与有限稀释法获得单克隆高表达细胞株;通过化学合成将天然 GnRH I 第 6 位甘氨酸替换为 D - 赖氨酸,将 sCy5-NHS 或 BODIPY630/650-NHS 与 D - 赖氨酸的 ε- 氨基共价偶联,制备 sCy5-D-Lys⁶-GnRH 与 BODIPY630/650-D-Lys⁶-GnRH 两种荧光配体,经 HPLC 纯化与质谱验证纯度 > 97%;在 SCL60 细胞中进行荧光配体饱和结合与竞争抑制实验,4℃孵育 4 小时后洗涤去除未结合配体,检测 640nm 激发、680nm 发射的荧光强度;通过 Western blot 检测 p-ERK1/2 磷酸化水平,评估荧光配体的受体激动活性,以 β-actin 为内参,Odyssey 红外成像系统定量;利用共聚焦显微镜观察 sCy5-D-Lys⁶-GnRH 与改造受体的细胞膜共定位,结合细胞膜标志物 mTFP-H-Ras 验证受体定位;在瞬时 / 稳定表达改造受体的细胞中开展 NanoBRET 检测,加入 Nano-Glo 底物后同步检测 460nm(供体)与 610nm(受体)发射光,计算 Raw BRET 与校正 BRET 比值,开展饱和结合、竞争抑制、实时结合动力学实验;采用 GraphPad Prism 7.0 软件进行数据拟合,计算 K_D、IC₅₀、K_I、k_on、k_off 等动力学参数,通过 Z’因子评估高通量筛选适用性,所有实验均独立重复 3 次以上,数据以均值 ± 标准差表示,P<0.05 为差异具有统计学意义。
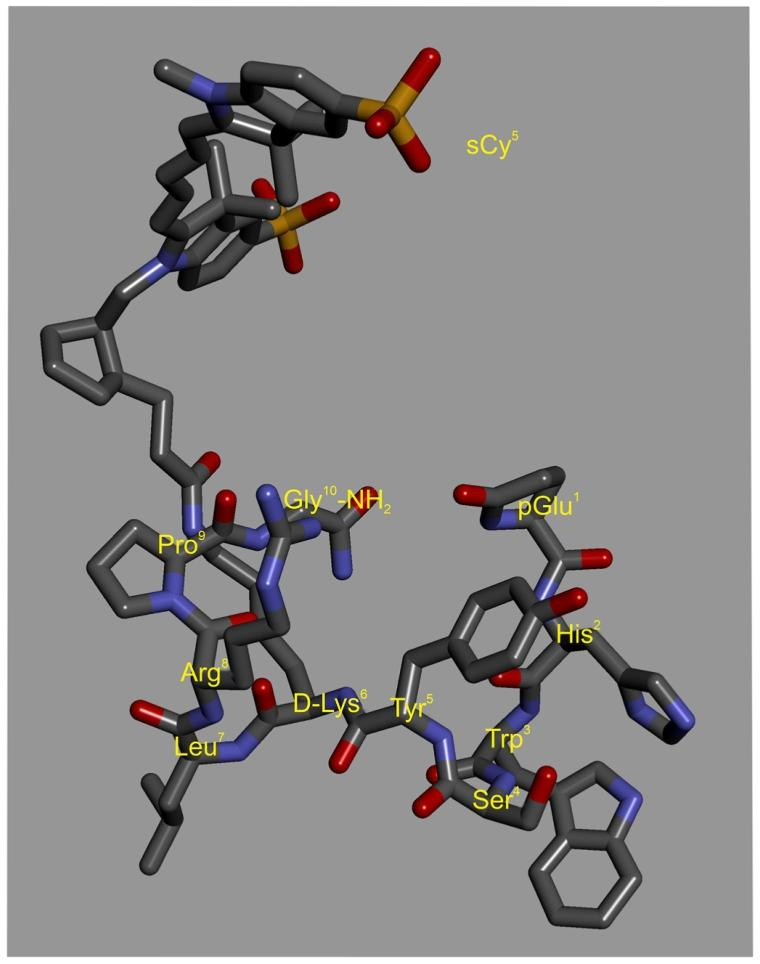
图 1 sCy5-D-Lys⁶-GnRH 的分子结构与设计原理
该图展示了新型荧光 GnRH 类似物 sCy5-D-Lys⁶-GnRH 的理性设计思路与分子结构,天然 GnRH I 为十肽,核心活性构象为围绕第 6 位甘氨酸的 βII’转角,该构象是配体结合受体的关键;研究将第 6 位甘氨酸替换为 D - 赖氨酸,将 sCy5 通过酰胺键共价连接在 D - 赖氨酸的 ε- 氨基上,该修饰方式可稳定肽链的 βII’转角构象,保留配体 N 端 pGlu¹-His²-Trp³-Ser⁴与 C 端 Pro⁹-Gly¹⁰-NH₂的受体结合关键位点,同时使 sCy5-D-Lys⁶基团向受体结合口袋外侧延伸,完全避免荧光团对配体 - 受体结合的空间位阻干扰,既保证了荧光配体的高受体亲和力与特异性激动活性,又使 sCy5 与膜上 N-secNluc-hGnRHR-K191Δ 的 NanoLuc 供体处于最优 BRET 能量转移距离,为高效能量传递奠定结构基础。
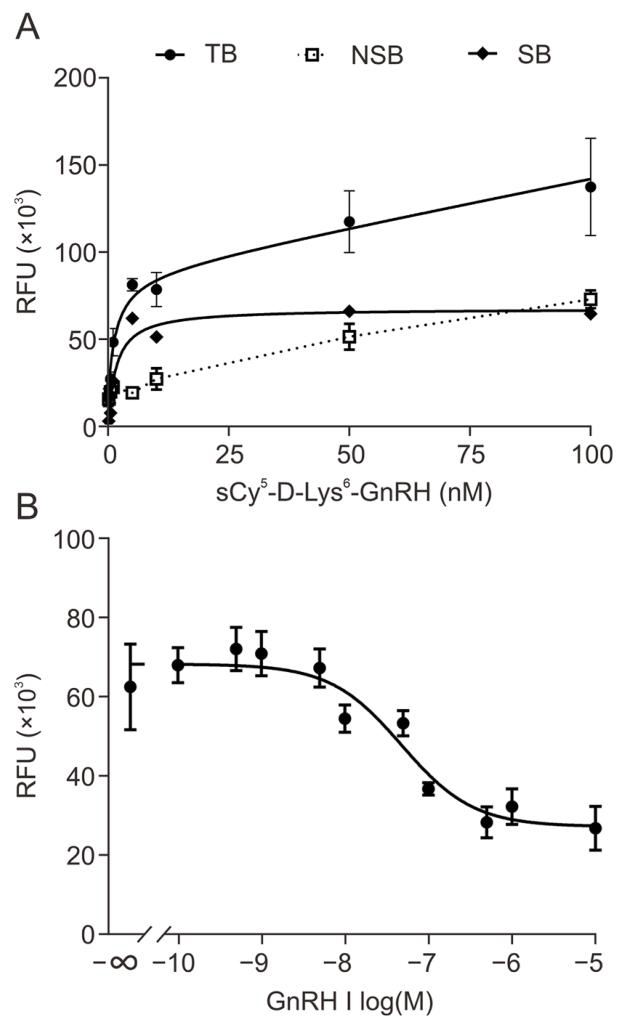
图 2 sCy5-D-Lys⁶-GnRH 在 SCL60 细胞中的受体结合特性验证
图 A 为 sCy5-D-Lys⁶-GnRH 在稳定表达大鼠 GnRHR 的 SCL60 细胞中的饱和结合曲线,实验设置总结合组与 100 倍过量未标记 GnRH I 竞争的非特异性结合组,经单位点结合模型拟合得到解离常数 K_D=2.7±0.91 nM,表明该荧光配体与 GnRHR 具有纳摩尔级高亲和力,特异性结合占比极高,非特异性结合水平极低;图 B 为竞争抑制结合曲线,以 10nM sCy5-D-Lys⁶-GnRH 为示踪配体,梯度浓度未标记 GnRH I 可竞争性抑制荧光配体结合,计算得 IC₅₀=14±0.85 nM,经 Cheng-Prusoff 方程换算 K_I=9.5±2.8 nM,该数值与天然 GnRH I 的受体亲和力高度匹配,证实 sCy5-D-Lys⁶-GnRH 与天然配体共享 GnRHR 的正构结合位点,结合特异性优异,完全满足 NanoBRET 示踪配体的核心要求。
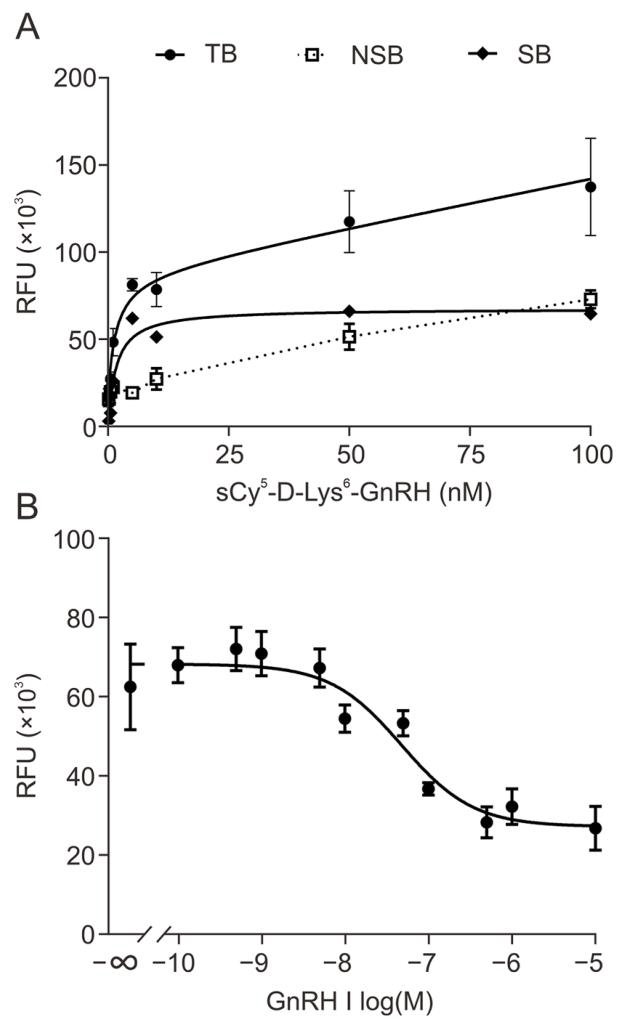
图 3 sCy5-D-Lys⁶-GnRH 对 GnRHR 的激动活性与信号特异性验证
图 A 为时间依赖性 p-ERK1/2 磷酸化检测结果,10nM sCy5-D-Lys⁶-GnRH 与天然 GnRH I 均在刺激 5 分钟后诱导 p-ERK1/2 达到峰值,荧光配体组峰值倍数为 17±6.7,天然配体组为 18±3.3,60 分钟后信号均显著衰减,二者信号动力学曲线完全重合,证明荧光配体可精准模拟天然配体的受体激活时序;图 B 为剂量依赖性 p-ERK1/2 曲线,sCy5-D-Lys⁶-GnRH 的 EC₅₀=0.44±0.27 nM,天然 GnRH I 的 EC₅₀=2.1±0.95 nM,荧光配体激动活性略高于天然配体,归因于 D-Lys⁶-sCy5 修饰对 βII’转角构象的稳定作用;图 C 为特异性验证实验,GnRHR 特异性拮抗剂 Cetrorelix 可完全阻断两种配体诱导的 p-ERK1/2 激活,无关 sCy5 标记的 kisspeptin-10(sCy5-KP10)无法激活受体,证实 sCy5-D-Lys⁶-GnRH 的激动效应完全由 GnRHR 介导,无脱靶激活,功能特异性极强。
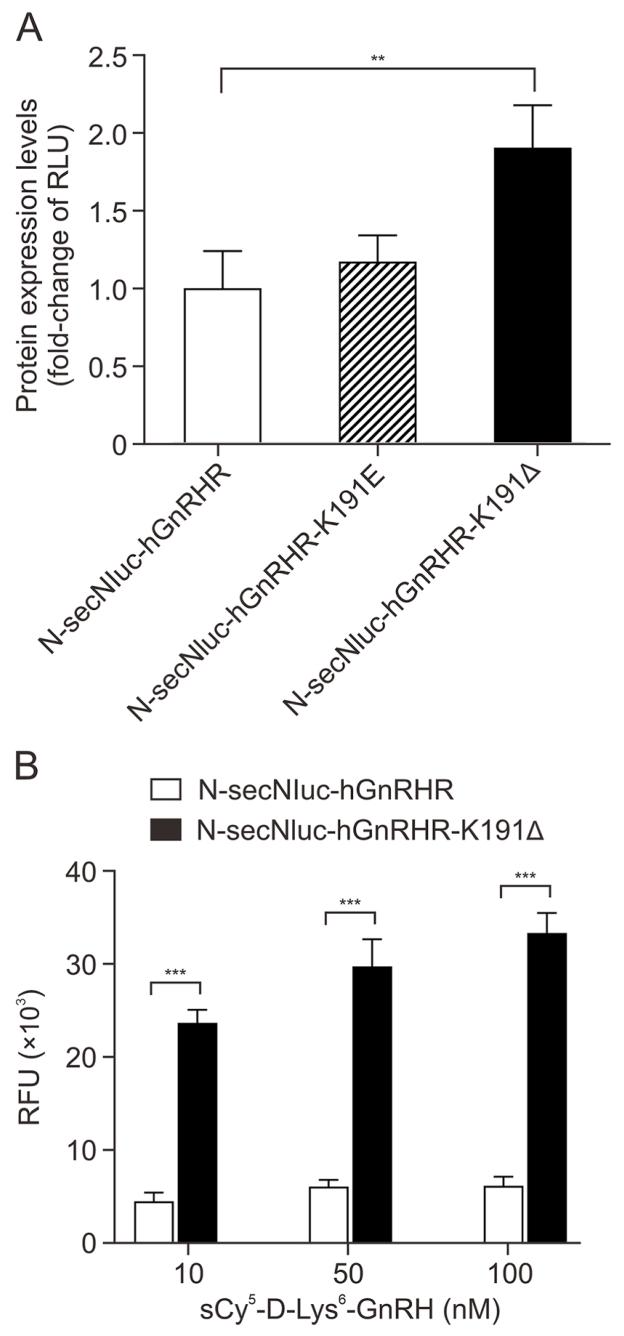
图 4 N-secNluc-hGnRHR 及其突变体的全细胞与细胞膜表达水平
图 A 为全细胞 NanoLuc 发光强度检测结果,瞬时转染的 HEK293 细胞中,N-secNluc-hGnRHR-K191Δ 的发光值较野生型 N-secNluc-hGnRHR 显著提升 1.91 倍(P<0.01),K191E 突变体仅轻微提升,表明 K191 缺失可显著提高融合受体的总蛋白表达量;图 B 为细胞膜受体表达水平检测,在 COS-7 细胞中用 10、50、100nM sCy5-D-Lys⁶-GnRH 结合细胞膜定位的受体,N-secNluc-hGnRHR-K191Δ 的细胞膜荧光信号较野生型提升 4.5-5 倍(P<0.001),证实 K191 缺失不仅提升总表达量,更关键的是大幅增强受体的细胞膜转运、插入与滞留效率,解决了 hGnRHR 天然膜表达量极低的核心难题,为高强度 NanoBRET 信号提供保障。
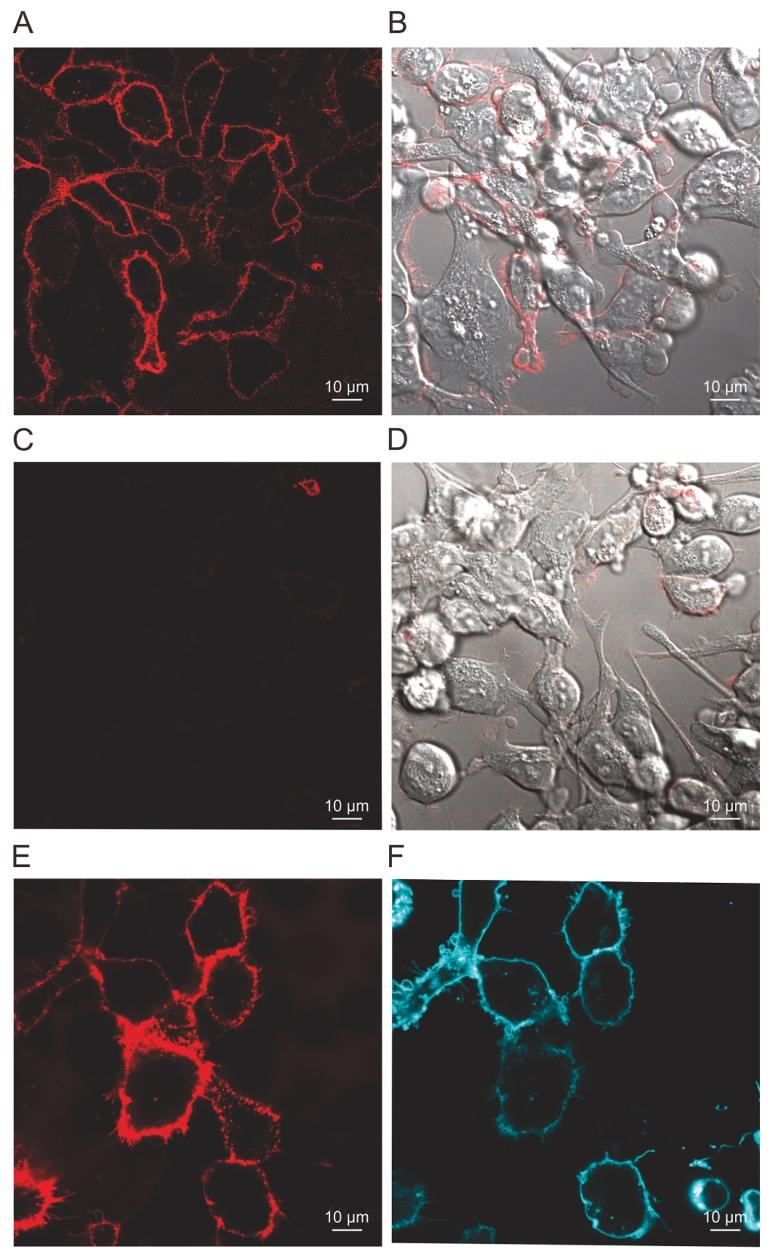
图 5 共聚焦显微镜验证 sCy5-D-Lys⁶-GnRH 与改造受体的细胞膜特异性结合
图 A、B 显示稳定表达 N-secNluc-hGnRHR-K191Δ 的 HEK293 细胞与 10nM sCy5-D-Lys⁶-GnRH 孵育后,细胞膜呈现均匀、明亮的红色荧光,胞内无明显荧光聚集,证明改造受体完全定位于细胞膜;图 C、D 显示加入 100 倍过量未标记 GnRH I 后,细胞膜荧光信号完全消失,证实荧光结合具有高度特异性;图 E、F 通过细胞膜标志物 mTFP-H-Ras 共定位,红色荧光(sCy5 配体)与蓝绿色荧光(细胞膜标志物)完全重合,进一步确认配体仅结合细胞膜上的改造受体,无胞内非特异性结合,受体定位与配体结合均符合 NanoBRET 检测要求。
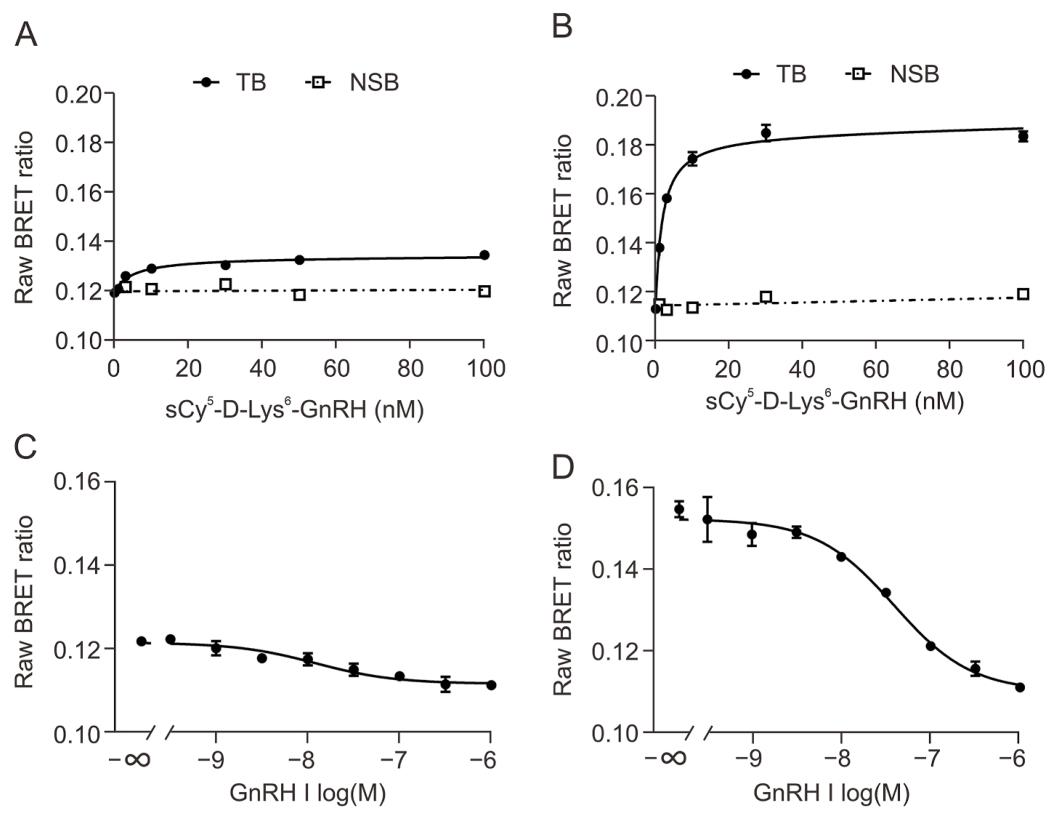
图 6 瞬时表达细胞中 NanoBRET 饱和结合与竞争抑制实验
图 A、C 为野生型 N-secNluc-hGnRHR 的 NanoBRET 结果,饱和结合 K_D=7.8±8.2 nM,特异性 BRET 信号极弱,竞争抑制曲线信噪比差;图 B、D 为 N-secNluc-hGnRHR-K191Δ 的 NanoBRET 结果,饱和结合 K_D=5.2±3.1 nM,与荧光结合法结果高度一致,特异性 BRET 信号较野生型提升 5 倍,非特异性结合维持极低水平;竞争抑制实验中 GnRH I 的 IC₅₀=28±0.91 nM,K_I=9.6±3.1 nM,与天然受体亲和力无差异,证实 K191 缺失仅提升受体膜表达量,不改变配体结合特性,大幅提高 NanoBRET 检测灵敏度与信噪比。
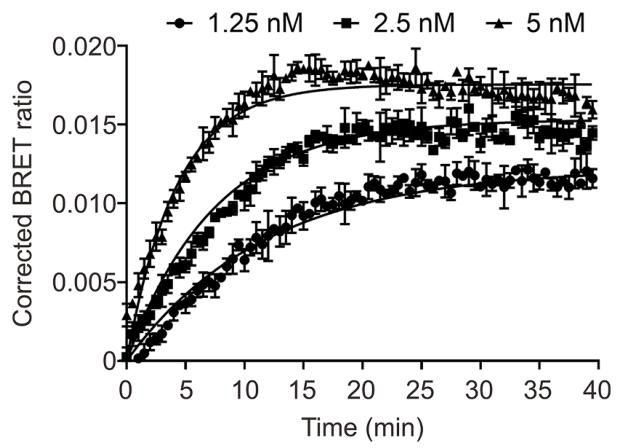
图 7 稳定表达 N-secNluc-hGnRHR-K191Δ 细胞的配体实时结合动力学
在 37℃生理温度下,对稳定细胞株开展实时 NanoBRET 结合检测,设置 1.25、2.5、5nM 三个浓度的 sCy5-D-Lys⁶-GnRH,连续监测 40 分钟的 BRET 信号变化;经双浓度结合动力学模型拟合,得到结合速率常数 k_on=3.0±0.74×10⁷ M⁻¹・min⁻¹,解离速率常数 k_off=0.03±0.01 min⁻¹,由 k_off/k_on 计算得 K_D=1.0±0.19 nM,与饱和结合实验的 K_D 值完全吻合;该结果表明 GnRH 配体与受体的结合为一步直接结合机制,无受体构象重排的多步结合过程,同时证实本 NanoBRET 体系可在生理温度下实时、精准检测配体结合动力学,优于传统 4℃低温结合实验。
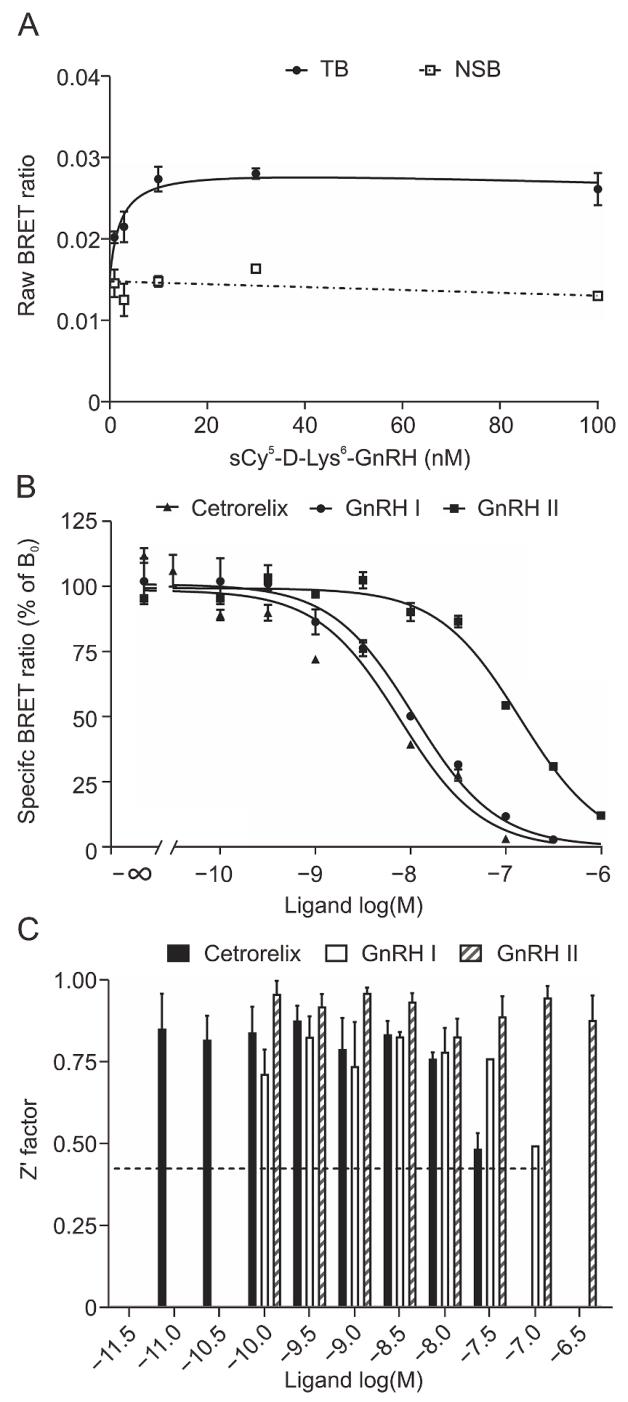
图 8 稳定细胞株 NanoBRET 体系的高通量筛选适用性验证
图 A 为稳定细胞株的饱和结合曲线,K_D=1.7±0.39 nM,非特异性结合信号极低,特异性结合曲线拟合度极高;图 B 为竞争抑制曲线,GnRH 拮抗剂 Cetrorelix、天然配体 GnRH I、GnRH II 均呈现典型的 S 型抑制曲线,亲和力差异与文献报道完全一致;图 C 为 Z’因子计算结果,在有效竞争浓度范围内 Z’因子均≥0.5,满足高通量筛选 “高稳健性、低变异性” 的核心标准,证实该体系无需洗涤、无需分离游离配体,均相检测模式完全适配 96/384 孔板高通量药物筛选。
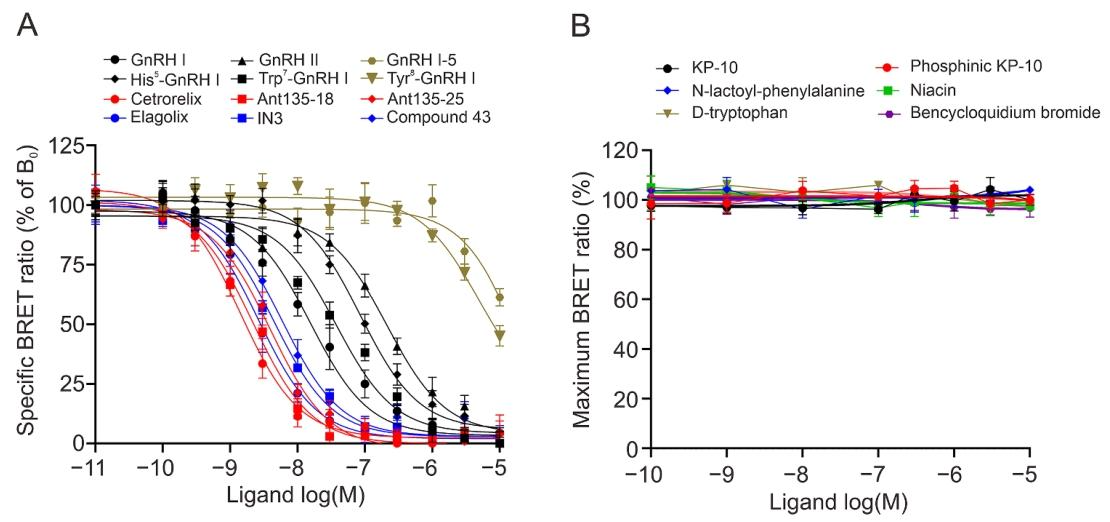
图 9 小规模化合物库验证 NanoBRET 筛选体系的特异性与广谱适用性
图 A 为 GnRH 系列配体的竞争抑制结果,GnRH I、GnRH II、单氨基酸替换类似物 His⁵-GnRH I、Trp⁷-GnRH I 的 K_I 值在 2.07±0.32~30.26±3.98 nM 之间,Tyr⁸-GnRH I、GnRH 1-5 亲和力显著降低,肽类拮抗剂 Cetrorelix、Ant135-18、Ant135-25 与非肽类拮抗剂 Elagolix、IN3、Compound 43 均表现出高亲和力,K_I 值低于 GnRH I;图 B 为无关化合物检测结果,kisspeptin-10、N - 乳酰苯丙氨酸、烟酸等 GnRHR 非配体化合物无任何抑制作用,证实该筛选体系可精准区分特异性配体与非特异性化合物,无假阳性,特异性与灵敏度均达到高通量筛选要求。
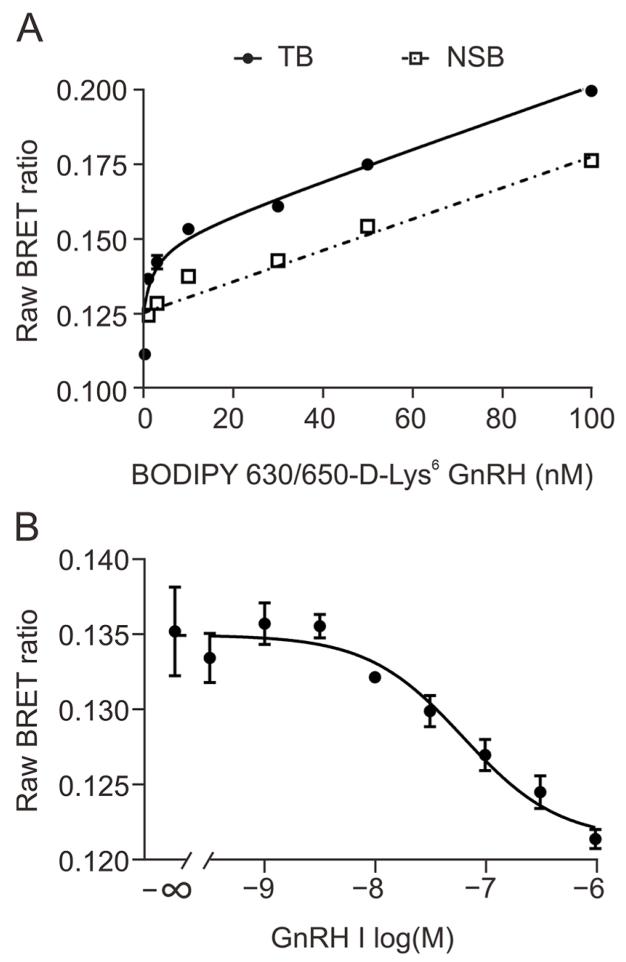
图 10 BODIPY630/650-D-Lys⁶-GnRH 与 sCy5-D-Lys⁶-GnRH 的 NanoBRET 性能对比
图 A 为 BODIPY 荧光配体的饱和结合曲线,K_D=1.5±0.66 nM,但非特异性结合信号极高,特异性结合占比极低,信噪比差;图 B 为竞争抑制曲线,GnRH I 的 K_I=7.6±1.4 nM,是 sCy5 体系的 5.8 倍,曲线拟合度差,数据变异大;对比结果证实,sCy5 因携带磺酸根负电荷、水溶性极高,可通过电荷排斥降低细胞膜磷脂的非特异性吸附,而 BODIPY 为中性疏水荧光团,易嵌入细胞膜导致高非特异性结合,明确 sCy5 是 hGnRHR NanoBRET 体系的最优荧光团,性能显著优于传统 BODIPY 荧光团。
本研究针对人促性腺激素释放激素受体天然细胞膜表达量低、传统配体检测方法存在放射性风险、现有 NanoBRET 荧光配体非特异性结合高的核心痛点,完成了配体与受体的双重优化改造:理性设计并合成了基于磺化花青素 5 的新型荧光配体 sCy5-D-Lys⁶-GnRH,该配体保留天然 GnRH 的 βII’转角活性构象,具备纳摩尔级高亲和力、特异性激动活性与极低非特异性结合,同时 sCy5 与 NanoLuc 的能量转移效率优异;通过 N 端融合 IL-6 分泌信号肽 - NanoLuc 并敲除第二胞外环 K191 位点,构建了 N-secNluc-hGnRHR-K191Δ 改造受体,在不改变配体结合亲和力与特异性的前提下,使受体细胞膜表达量提升 4.5-5 倍,NanoBRET 特异性信号提升 5 倍;基于此构建的活细胞 NanoBRET 配体结合体系,无需洗涤、无需分离游离配体,均相检测模式下 Z’因子≥0.5,完全满足高通量药物筛选要求,可精准检测配体饱和结合、竞争抑制、实时动力学参数,同时能高效区分 GnRHR 特异性配体与无关化合物;对比实验证实 sCy5 荧光团的非特异性结合远低于传统 BODIPY 荧光团,是 GPCR NanoBRET 筛选的优选荧光团;该体系不仅为 hGnRHR 的配体药理学研究、信号选择性药物筛选提供了无放射性、高灵敏、高稳健性的全新技术平台,其 “荧光配体理性设计 + 受体膜表达优化” 的策略也可推广至其他低表达 GPCR 的 NanoBRET 高通量筛选方法构建,为 GPCR 靶向创新药物研发提供了可复制的通用技术方案。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:Eomesodermin+CD4+T 细胞:治愈性免疫治疗的关键 “双功能” 细胞
下一篇:rs713586风险变异通过ZFP42-TET1介导的DNA甲基化调控ADCY3而非DNAJC27,导致肥胖