常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-30 17:00:00 细胞资源库平台 访问量:60
1 型调节性 T 细胞(Tr1)是一类不表达 FoxP3 但可分泌 IL-10 的 CD4+T 细胞,在慢性感染、自身免疫病及器官移植中承担免疫耐受维持的核心功能。Eomes 作为关键转录因子,已被证实可促进 Tr1 细胞分化并减轻异基因骨髓移植(BMT)后的移植物抗宿主病(GVHD),但 Eomes 在 Tr1 细胞分化的具体阶段、以及细胞治疗后 Tr1 细胞兼具的调节与杀伤功能的调控机制,长期存在空白。
此外,嵌合抗原受体 T 细胞(CAR-T)疗法虽为癌症治疗带来革命,但 CD4+CAR-T 细胞的功能异质性(促炎毒性与抗肿瘤活性的平衡)是制约疗效的关键。明确 Eomes 对 CD4+T 细胞(包括 Tr1 及 CAR-T)功能的调控作用,是填补免疫治疗靶点空白、实现 “疗效提升 + 毒性降低” 双重目标的核心科学问题。
这篇发表在《Immunity》上的文章,首次揭示了 Eomes 驱动 CD4+T 细胞向 Tr1 细胞分化的完整轨迹(从 Eomes+IL-10 - 前体到 Eomes+IL-10 + 成熟 Tr1),证实 Eomes+CD4+T 细胞兼具免疫调节与细胞毒性的 “双功能” 特性:一方面可通过分泌 IL-10 抑制过度炎症、减轻细胞因子释放综合征(CRS),另一方面可通过穿孔素 / 颗粒酶及 Fas/FasL 通路介导抗肿瘤杀伤;在 CAR-T 治疗中,Eomes+CD4+CAR-T 细胞可维持长期持久性并控制肿瘤复发,且在长期缓解的淋巴瘤患者体内稳定存在(占 CD4+CAR-T 细胞的 40%-80%)。该发现为优化免疫治疗方案提供了全新细胞与分子靶点。
本研究采用 “临床问题 - 小鼠模型 - 机制验证 - 临床样本回溯” 的闭环设计,核心实验流程分为 4 步,覆盖表型分析、功能验证与临床转化:
1.实验模型构建与样本采集:构建 Eomes 条件性敲除(Cd4cre+xEomesfl/fl)、IL-10/IFNγ 双报告(HULK)等基因修饰小鼠模型,建立异基因 BMT 及 CD19 靶向 CAR-T 治疗的白血病小鼠模型;同时收集 13 例接受 CD19 CAR-T 治疗的 B 细胞淋巴瘤患者的外周血样本,用于临床表型验证。
2.细胞表型与转录组分析:通过流式细胞术(含 FlowSOM 高维分析)、单细胞 / 批量 RNA 测序(scRNA-seq/bulk RNA-seq)、伪时间轨迹分析,解析 Eomes+CD4+T 细胞的分化阶段、分子标记(TIGIThiDNAM-1lo)及核心通路;利用逆转录病毒过表达 Eomes,验证其对细胞功能的直接调控作用。
3.体外功能验证:分离不同分化阶段的 Eomes+CD4+T 细胞,开展体外抑制实验(检测对效应 T 细胞增殖的抑制能力)、细胞毒实验(检测对白血病细胞的杀伤活性),明确其免疫调节与抗肿瘤功能的物质基础(IL-10、穿孔素 / 颗粒酶)。
4.体内功能验证:在 BMT 模型中评估 Eomes+CD4+T 细胞的移植物抗白血病(GVL)效应与抗炎作用;在 CAR-T 治疗模型中验证 Eomes 对 CAR-T 细胞毒性、持久性及 CRS 的调控;通过竞争性移植实验明确 Fas/FasL 通路的协同杀伤作用。
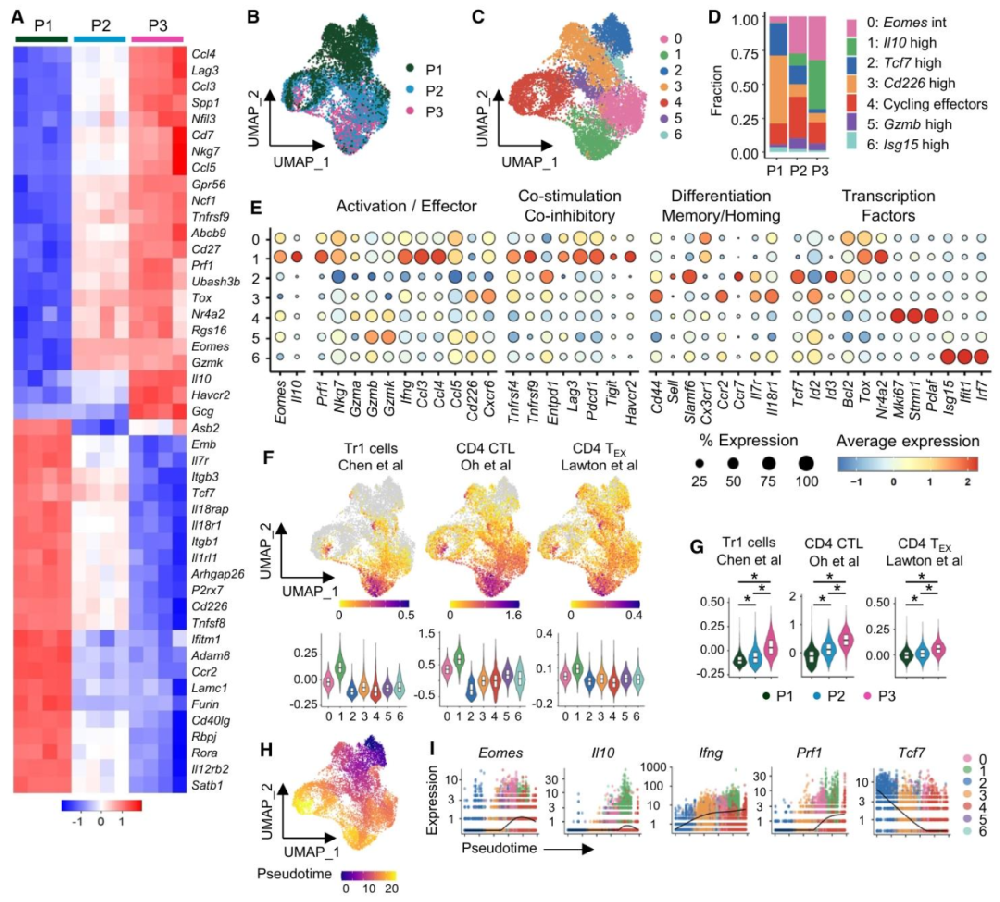
图1:Eomes+CD4+T 细胞兼具调节、细胞毒与耗竭样转录特征
该结果通过批量及单细胞 RNA 测序解析了 BMT 后供体 CD4+T 细胞的转录组图谱。研究将 CD4+T 细胞分为 Eomes-IL-10-(P1)、Eomes+IL-10-(P2)、Eomes+IL-10+(P3)三群,发现 Eomes + 亚群(P2、P3)随分化进程逐步上调效应分子(Prf1、Gzmk)、耗竭相关基因(Tox、Lag3)及调节性细胞因子(Il10),同时下调祖细胞标记(Tcf7、Il7r);伪时间分析证实分化轨迹为 P1→P2→P3,且 Eomes 与 Il10 表达随分化逐步升高,而 Tcf7 表达持续降低。基因集富集分析(GSEA)进一步显示,P3 亚群显著富集 Tr1 细胞、CD4 细胞毒性 T 淋巴细胞(CTL)及耗竭 T 细胞通路,证实 Eomes+CD4+T 细胞的 “双功能” 转录基础。
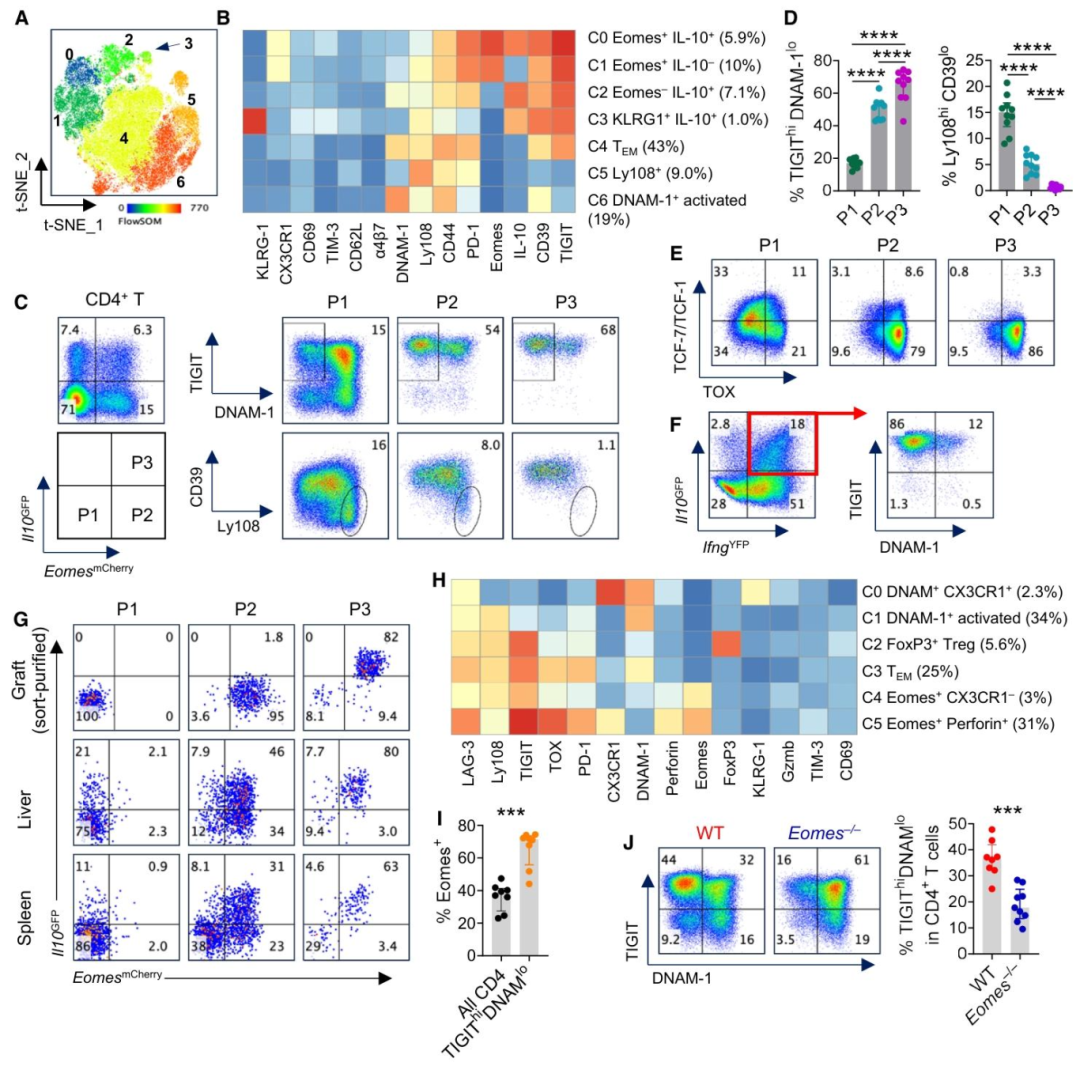
图2:Eomes 驱动 Tr1 分化并可通过 TIGIT/DNAM-1 表型识别
该结果通过流式高维分析验证了转录组发现的表型特征。FlowSOM 聚类显示,Eomes+CD4+T 细胞高表达 TIGIT、PD-1、CD39 等共抑制分子,低表达活化受体 DNAM-1,呈现 TIGIThiDNAM-1lo 表型;Eomes 条件性敲除后,该表型细胞比例显著降低,且无法从 Eomes+IL-10 - 前体分化为 Eomes+IL-10 + 成熟 Tr1;在 HULK 报告小鼠中,IFNγ+IL-10 + 的功能性 Tr1 细胞均局限于 TIGIThi 亚群,且该亚群对 CD19 + 靶细胞的杀伤能力显著高于 TIGITlo 亚群,证实 TIGIT/DNAM-1 可作为 Eomes + 功能 Tr1 细胞的特异性标记。
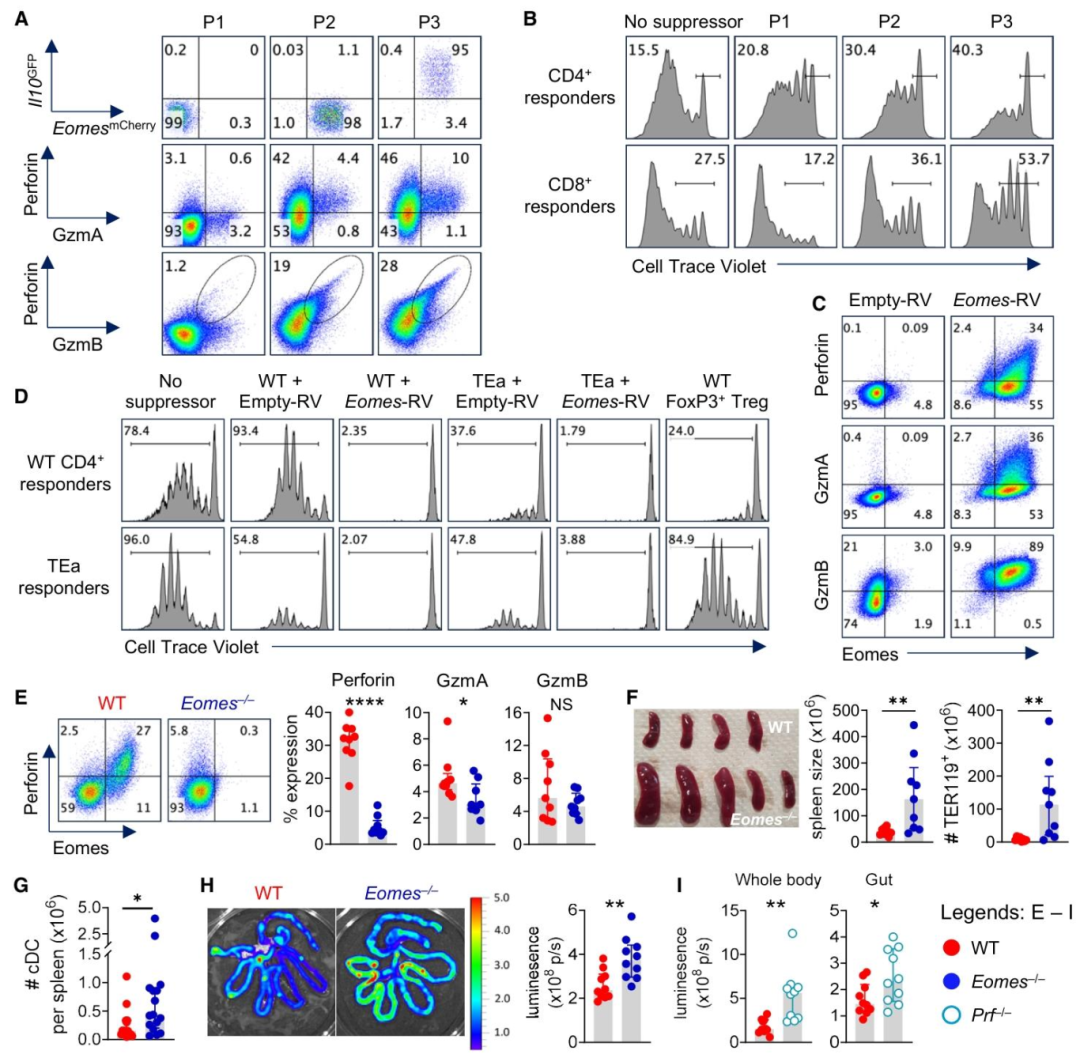
图3:Eomes+CD4+T 细胞可独立于 IL-10 发挥抑制作用并清除抗原提呈细胞
该结果明确了 Eomes+CD4+T 细胞免疫调节功能的物质基础。体外实验显示,Eomes+IL-10 - 前体(P2)虽不分泌 IL-10,但因高表达穿孔素 / 颗粒酶,对效应 T 细胞的抑制能力介于 P1 与 P3 之间;过表达 Eomes 可显著增强 CD4+T 细胞的细胞毒分子表达及抑制活性,且抑制效果优于 FoxP3+Treg;体内实验中,Eomes 敲除的 CD4+T 细胞因穿孔素表达不足,无法清除 CD11c + 树突状细胞,导致小鼠出现噬血细胞性淋巴组织细胞增生症(HLH)样脾肿大及红细胞异常聚集,证实 Eomes 通过调控穿孔素介导抗原提呈细胞清除,维持免疫稳态。
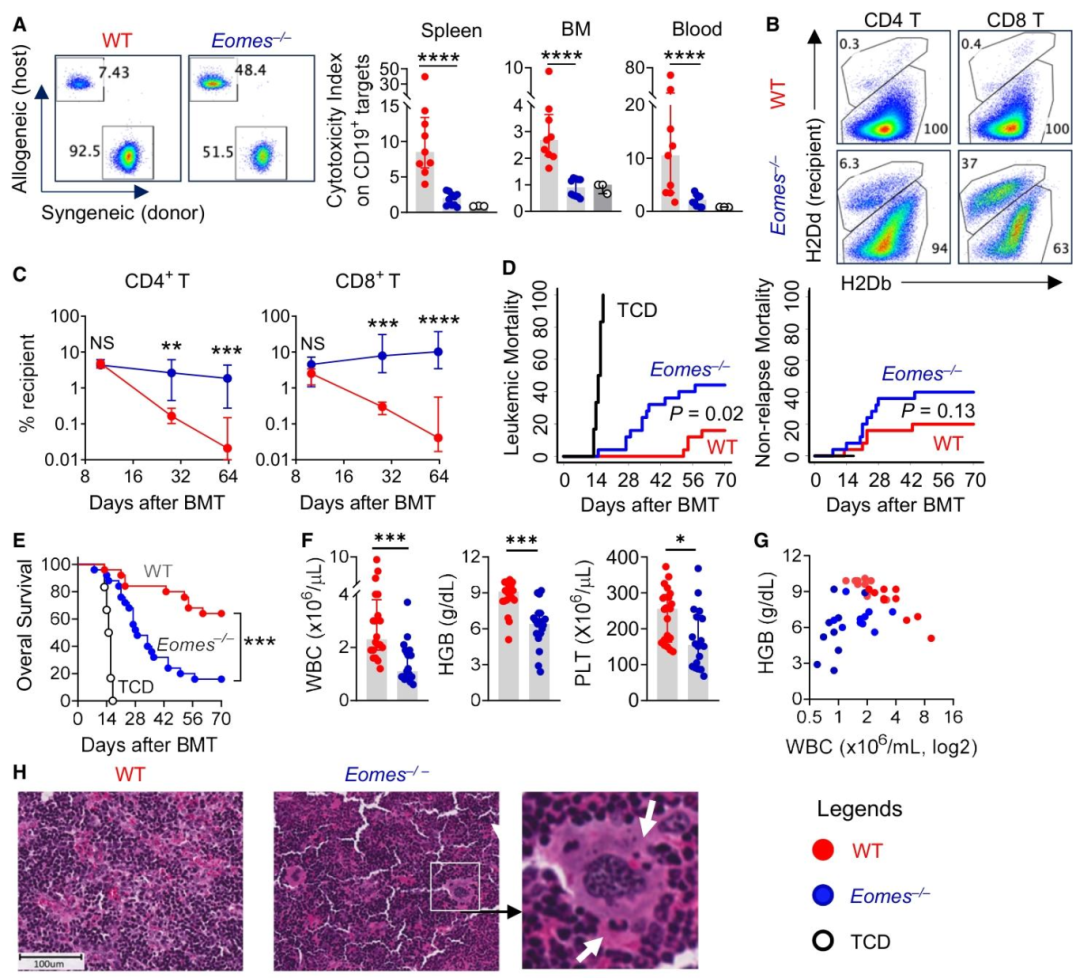
图4:Eomes+CD4+T 细胞介导 GVL 效应并限制过度炎症
该结果在 BMT 模型中验证了 Eomes+CD4+T 细胞的体内双重功能。体内杀伤实验显示,Eomes 敲除的 CD4+T 细胞对宿主 CD19+B 细胞的杀伤能力显著降低,导致 T 细胞嵌合率异常、白血病复发率升高,小鼠生存率显著下降;同时,Eomes 缺失会引发严重的全血细胞减少、脾组织细胞增生,表现为 HLH 样炎症表型,证实 Eomes+CD4+T 细胞是 BMT 后介导 GVL 效应、防止过度炎症的核心细胞群。
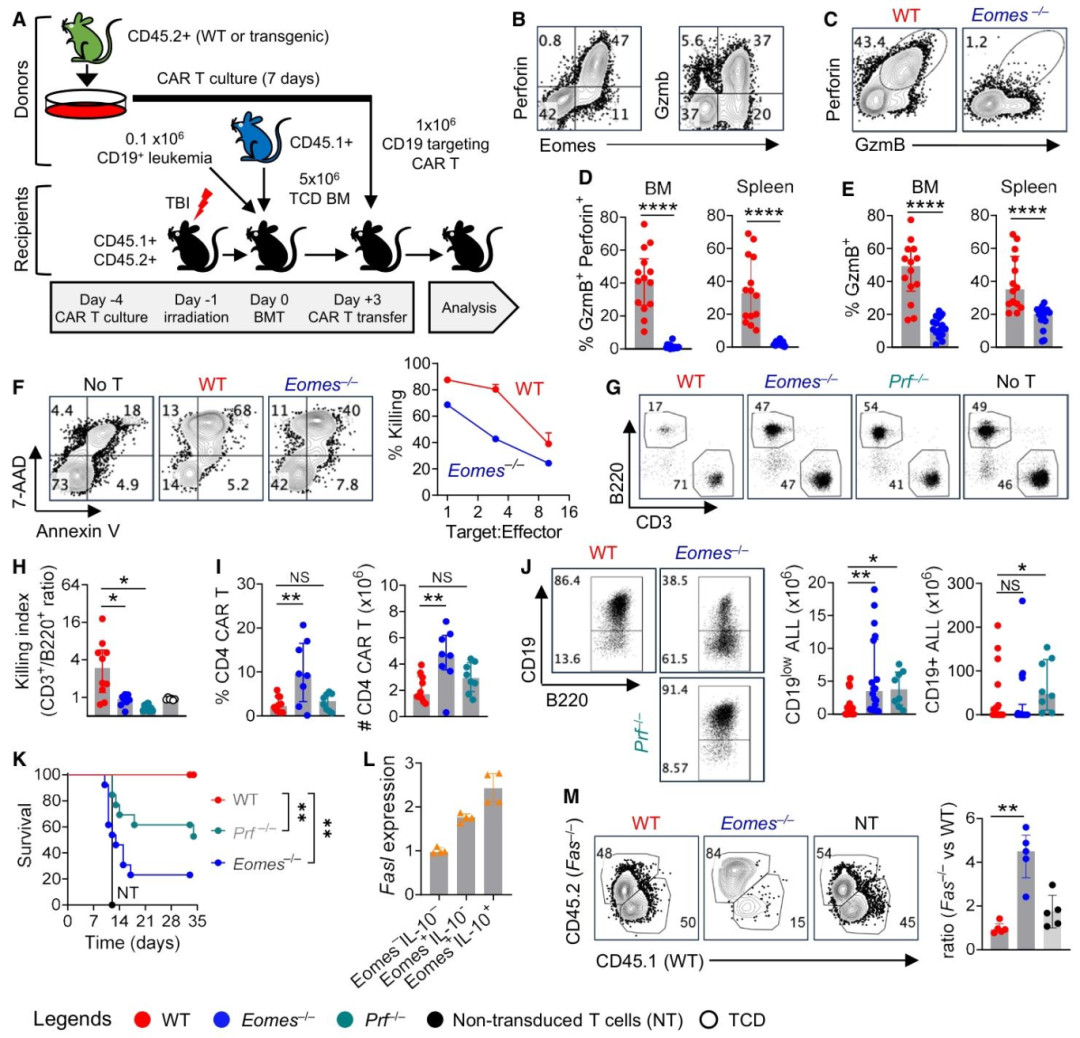
图5:Eomes 调控 CD4+CAR-T 细胞的细胞毒功能与肿瘤控制
该结果明确了 Eomes 在 CAR-T 治疗中的关键作用。在 CD19 靶向 CAR-T 治疗模型中,Eomes+CD4+CAR-T 细胞高表达穿孔素 / 颗粒酶 B,而 Eomes 敲除后,双阳性细胞比例近乎消失,CAR-T 细胞对白血病细胞的体外 / 体内杀伤能力显著减弱;进一步实验证实,Eomes 还可通过增强 Fas/FasL 通路协同杀伤靶细胞,且 Eomes 或穿孔素敲除的 CAR-T 细胞会导致 CD19 低表达白血病细胞逃逸,小鼠生存期显著缩短,证实 Eomes 是 CD4+CAR-T 细胞抗肿瘤功能的核心调控因子。
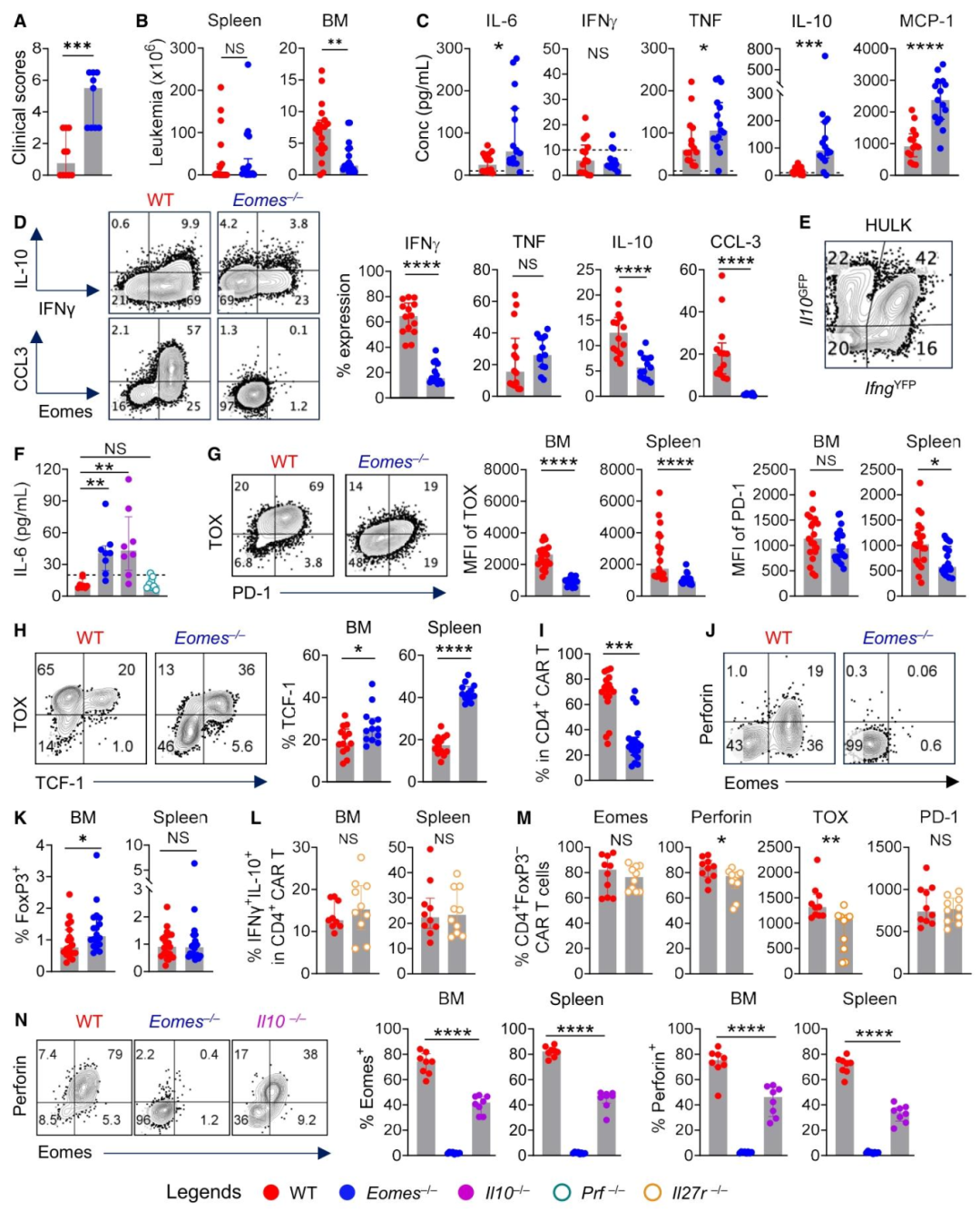
图6:Eomes+CD4+CAR-T 细胞呈 Tr1 样表型并控制 CRS
该结果揭示了 Eomes+CD4+CAR-T 细胞的抗炎作用及机制。Eomes 敲除的 CD4+CAR-T 细胞输注小鼠后,会出现更严重的临床症状及更高水平的 CRS 相关细胞因子(IL-6、TNF、MCP-1);HULK 报告小鼠证实,野生型 CD4+CAR-T 细胞中多数 IFNγ+ 细胞同时分泌 IL-10,呈典型 Tr1 表型;IL-10 敲除的 CAR-T 细胞会导致血浆 IL-6 水平显著升高,而穿孔素敲除无此效应,证实 Eomes+CAR-T 细胞通过 IL-10 抑制单核细胞来源的 IL-6,从而减轻 CRS。此外,Eomes 敲除会导致 CAR-T 细胞早期过度扩增但长期持久性下降,证实其对 CAR-T 细胞命运的双向调控。
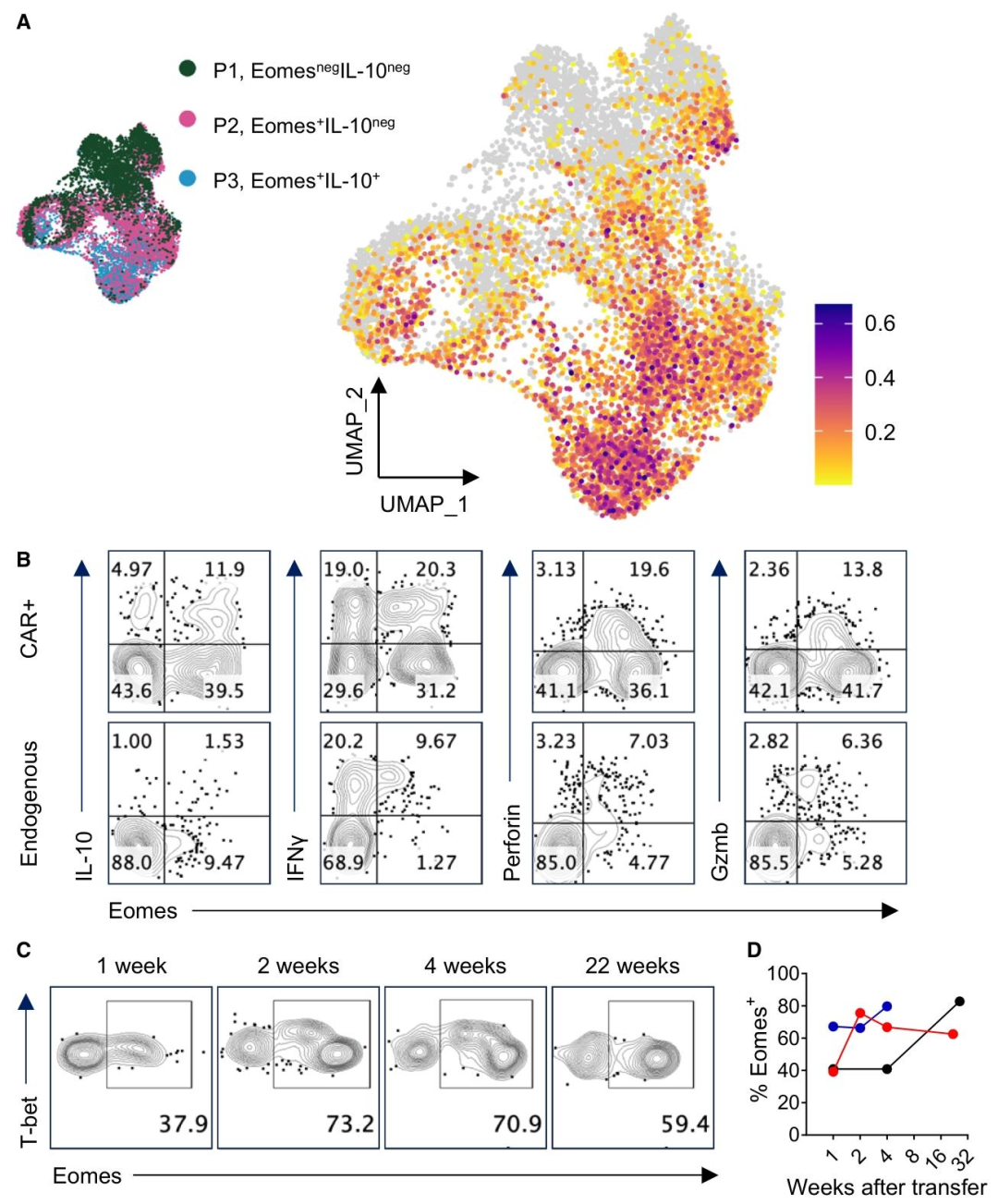
图7:Eomes+CD4+CAR-T 细胞在长期缓解患者体内稳定存在
该结果完成了从基础研究到临床样本的回溯验证。将人 CD4+CAR-T 细胞的核心基因集投射到小鼠 UMAP 图谱,发现其与小鼠 Eomes+Tr1 细胞高度富集;在接受 CD19 CAR-T 治疗的淋巴瘤患者体内,CD4+CAR-T 细胞高表达 Eomes 及 Tr1 相关标记(IL-10、IFNγ、穿孔素),且随时间推移,Eomes 表达稳定而 T-bet 表达下调,与小鼠模型表型一致;在生存期超 180 天的患者体内,Eomes+CD4+CAR-T 细胞占比维持在较高水平,证实其与长期缓解密切相关。
本研究以 Eomes 为核心切入点,系统解析了 CD4+T 细胞向 Tr1 细胞分化的完整轨迹,首次明确了 Eomes+CD4+T 细胞 “调节 - 杀伤” 的双功能特性:在分化层面,Eomes 驱动细胞从祖细胞状态逐步获得耗竭样表型、调节性细胞因子及细胞毒分子;在功能层面,其既可通过 IL-10 抑制过度炎症、缓解 CRS,又可通过穿孔素 / 颗粒酶及 Fas/FasL 通路介导抗肿瘤杀伤;在 CAR-T 治疗中,Eomes 不仅维持 CD4+CAR-T 细胞的长期持久性,还可平衡治疗疗效与毒性。该研究打破了 “调节性 T 细胞无杀伤功能” 的传统认知,阐明了 Eomes 在免疫治疗中的核心调控作用,为优化细胞治疗方案、开发靶向 Eomes 的联合疗法提供了关键理论与实验依据。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:棒状小胶质细胞如何调控 TDP-43 相关神经变性的皮层兴奋性?
下一篇:基于磺化花青素 5 荧光团构建人促性腺激素释放激素受体的新型纳米生物发光共振能量转移高通量药物筛选方法