常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-30 00:00:00 细胞资源库平台 访问量:22
肌萎缩侧索硬化(ALS)是一种致命的进行性神经变性疾病,其核心病理特征为脑和脊髓运动神经元的选择性退变,最终导致患者肌肉无力、瘫痪乃至死亡,而 TDP-43 蛋白的异常聚集是绝大多数 ALS 病例的核心病理标志。临床研究已证实,运动皮层过度兴奋是 ALS 前驱期的典型特征,该现象会诱发早期神经元毒性并加速运动神经元退变,但其背后的调控机制长期未被阐明。
小胶质细胞作为中枢神经系统的固有免疫细胞,不仅承担着维持脑内稳态的基础功能,还能敏锐感知并调控神经元活动。此前研究已发现小胶质细胞激活是 ALS 的病理标志之一,但在 TDP-43 相关神经变性中,小胶质细胞如何响应并调控运动皮层过度兴奋、是否存在特异性亚群参与该过程,尚未有明确答案。因此,探索小胶质细胞在 TDP-43 相关神经变性中对皮层兴奋性的调控机制,成为填补 ALS 早期干预靶点空白的关键科学问题。
这篇核心成员覆盖多个国际顶尖科研机构的文章Rod-shaped microglia interact with neuronal dendrites to regulate cortical excitability in TDP-43 related neurodegeneration,首次在 TDP-43 神经变性小鼠模型(rNLS8)和 ALS 患者死后脑组织中,鉴定出一种特异性小胶质细胞亚群 ——棒状小胶质细胞。研究证实,该细胞亚群依赖 TREM2/DAP12 信号通路形成,可通过与神经元树突紧密结合、吞噬兴奋性突触的方式,有效缓解运动皮层过度兴奋;若敲除 TREM2 基因抑制棒状小胶质细胞形成,会导致小鼠神经元钙超载加剧、运动功能缺损加重且生存率显著下降。这一发现明确了棒状小胶质细胞的神经保护作用,为 ALS 等 TDP-43 相关神经变性疾病的早期靶向干预提供了全新的细胞与分子靶点。
1.实验模型构建与样本采集:构建 DOX 依赖型 TDP-43 神经变性小鼠模型(rNLS8),通过撤除 DOX 饮食诱导病理表型;同时将 rNLS8 小鼠与 TREM2 敲除(KO)小鼠杂交构建验证模型;此外收集 31 例 ALS 患者及 25 例对照的死后运动皮层组织样本用于临床验证。
2.神经活动动态监测:先通过慢性植入 32 通道硅探针,记录小鼠运动皮层各层神经元的基线及疾病进展期放电频率;再利用 AAV 介导的 GCaMP6s 标记,结合在体双光子钙成像,追踪清醒小鼠运动皮层兴奋性神经元的钙瞬变信号变化。
3.转录组学与细胞分型分析:在疾病峰值期(撤除 DOX 后 3 周)采集小鼠脑组织,通过 10x Visium 空间 RNA 测序(spRNA-seq)绘制脑区转录组图谱;同时分离皮层细胞开展单细胞 RNA 测序(scRNA-seq),完成细胞亚群分型与差异基因分析。
4.细胞形态与相互作用验证:采用 IBA1 等标志物的免疫荧光染色,结合三维成像技术,观察小胶质细胞形态及与神经元结构的结合情况;通过电镜解析棒状小胶质细胞与树突的超微相互作用模式;利用配体 - 受体互作分析预测细胞间通讯机制。
5.功能与通路验证:开展转棒、悬线、旷场等行为学实验评估小鼠运动功能与生存情况;结合 TREM2 敲除模型,验证该通路对棒状小胶质细胞形成及神经元兴奋性的调控作用。
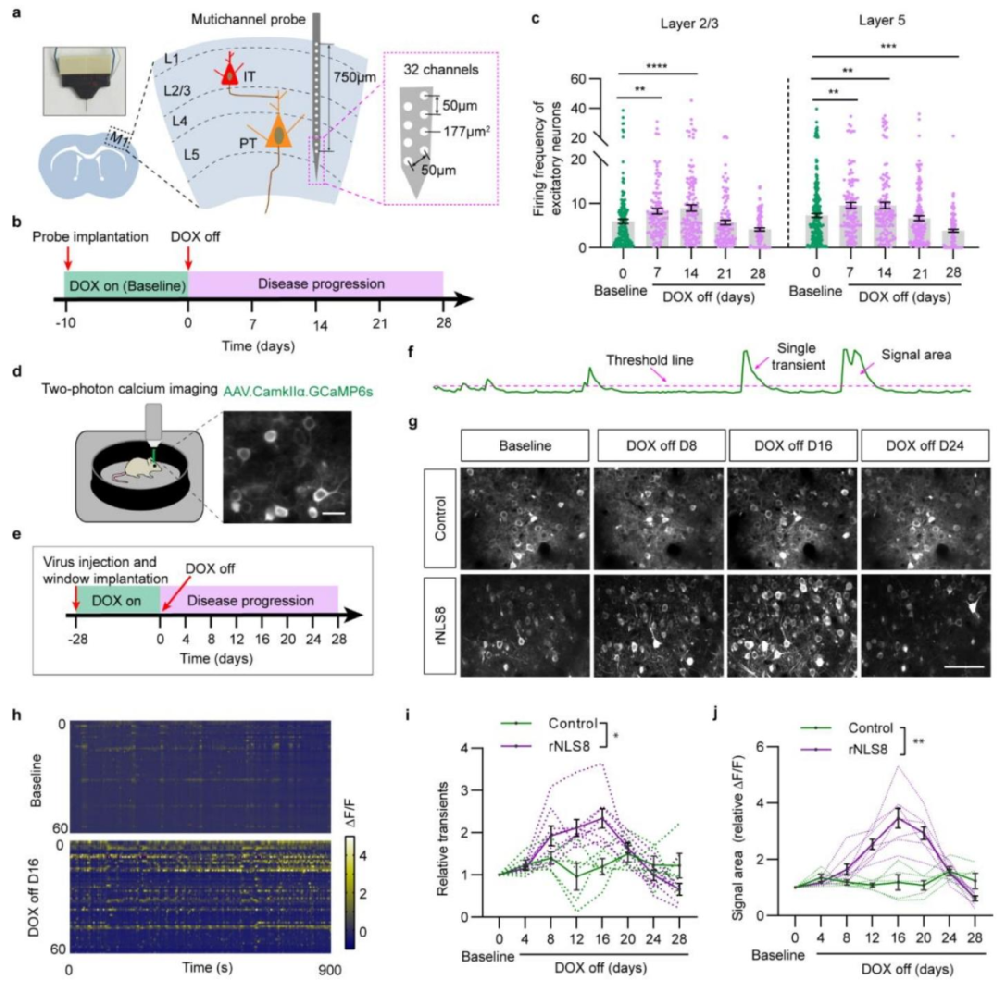
图1:rNLS8 小鼠疾病早期出现运动皮层过度兴奋
在基线状态下,rNLS8 小鼠与对照小鼠的运动皮层 2/3 层和 5 层神经元放电频率无显著差异,且抑制性神经元放电频率高于兴奋性神经元;但撤除 DOX 诱导 TDP-43 表达后,rNLS8 小鼠在 1-2 周内运动皮层 2/3 层和 5 层兴奋性神经元放电频率显著升高,钙瞬变频率及信号面积在 2-3 周达到峰值(钙信号面积较基线提升 228±49%)。进一步验证发现,该早期过度兴奋与锥体神经元自身兴奋性升高相关,而非抑制性神经元功能下降,且此阶段神经元密度无显著变化,但尼氏小体减少提示神经元已出现应激损伤。
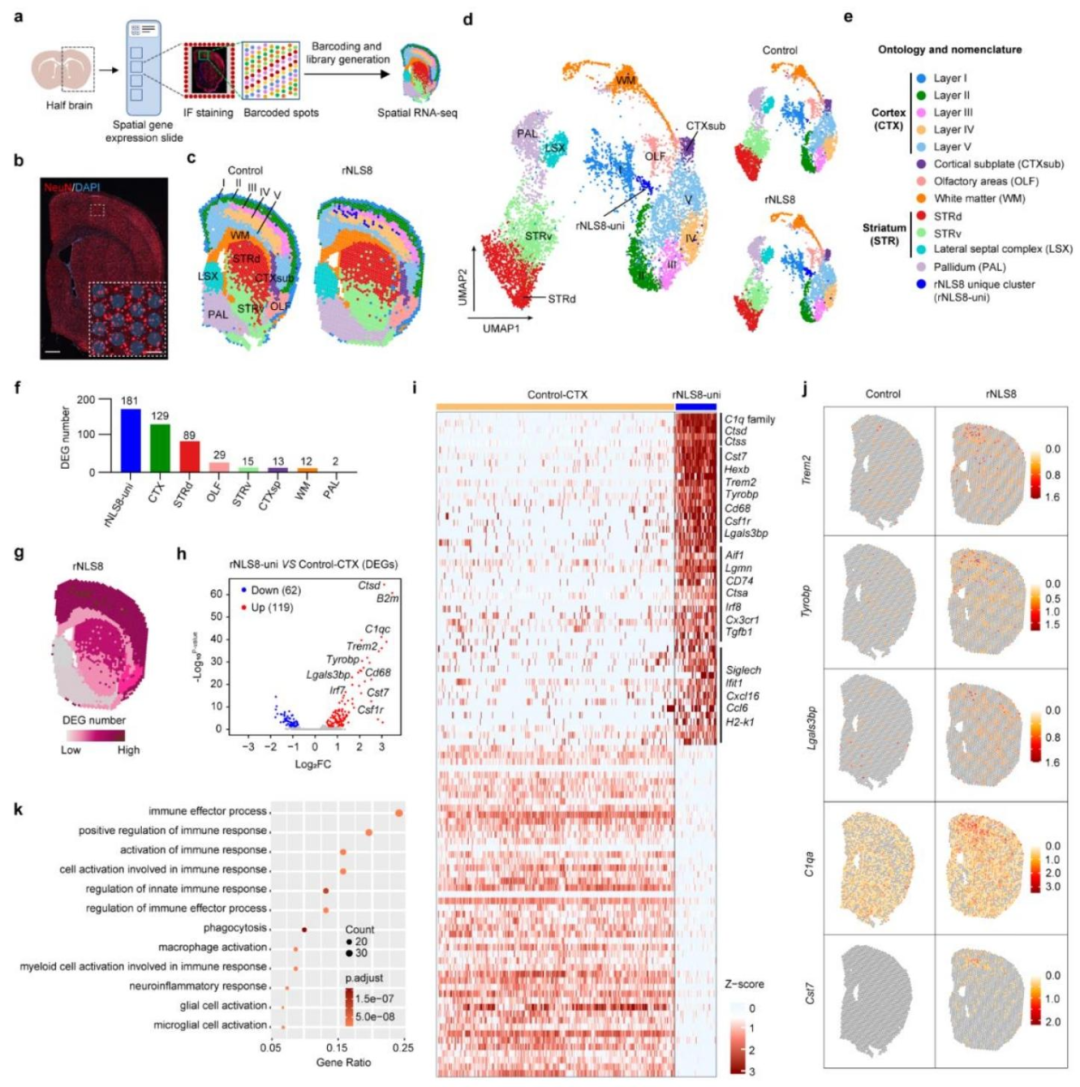
图2:空间转录组揭示皮层小胶质细胞为神经过度兴奋的主要响应细胞
对撤除 DOX 后 3 周小鼠脑组织的空间 RNA 测序显示,rNLS8 小鼠皮层出现独特的 “sp-rNLS8-unique” 转录簇,该簇与皮层(CTX)簇的差异基因(DEGs)数量最多;其中前 100 个上调基因多为小胶质细胞特异性基因(如补体 Clq 家族、Trem2、Cd68 等);GO 富集分析显示 “小胶质细胞激活”“免疫应答”“吞噬作用” 为核心富集通路,同时皮层簇还富集了 “突触传递”“突触修剪” 相关的神经元基因,提示小胶质细胞是早期神经过度兴奋的核心响应细胞,且伴随突触层面的病理重塑。
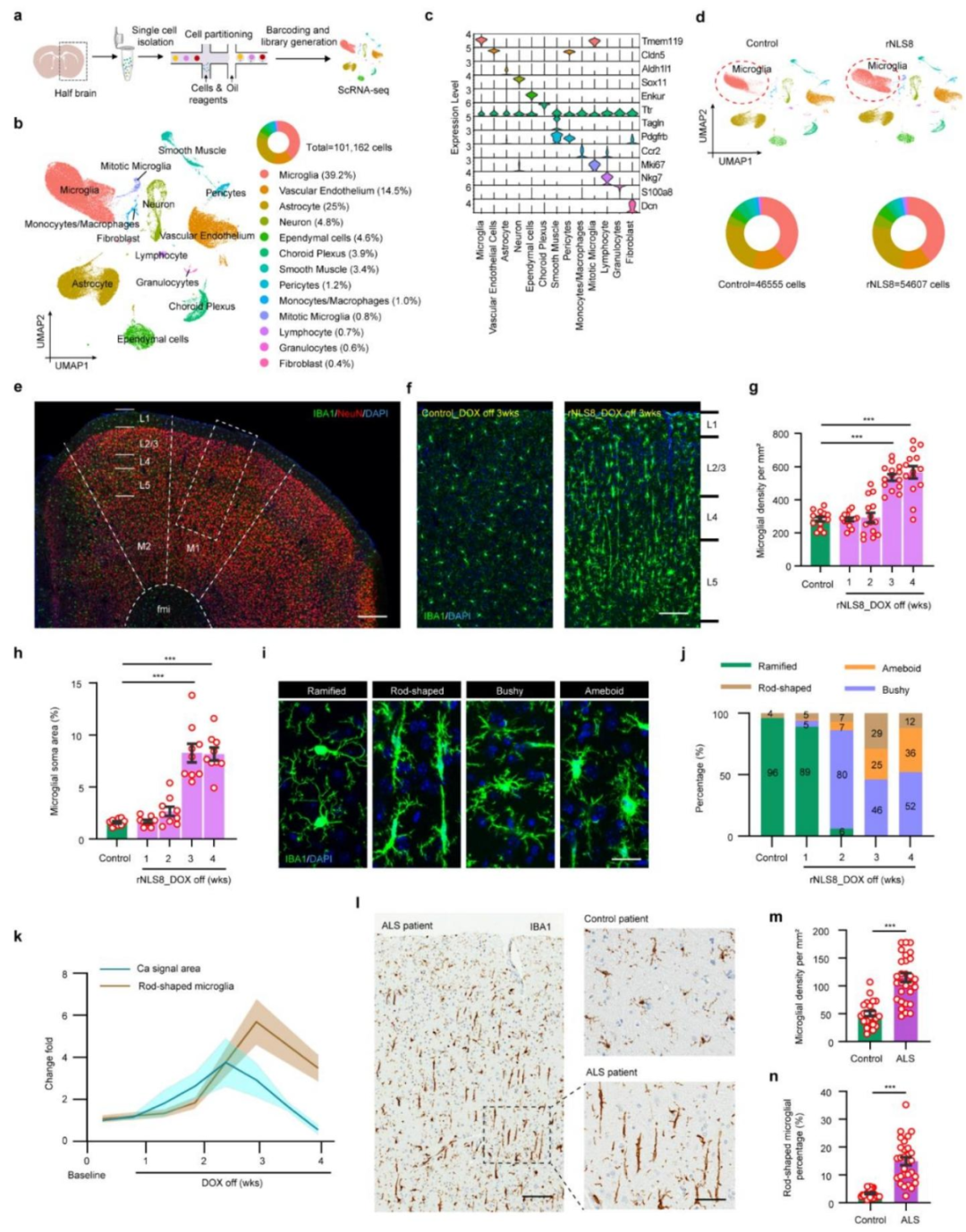
图3:rNLS8 小鼠与 ALS 患者中存在独特的棒状小胶质细胞亚群
单细胞 RNA 测序将皮层细胞分为 13 个主要类型,其中小胶质细胞占比最高;免疫荧光染色显示,rNLS8 小鼠运动皮层小胶质细胞密度与胞体面积在撤除 DOX 后 3 周达峰值,且出现阿米巴样、丛生样及棒状等特殊形态,其中棒状小胶质细胞呈细长极化形态,主要分布于 2/3 层和 4 层,其占比变化与神经元钙信号面积变化呈正相关;临床样本验证发现,ALS 患者运动皮层中棒状小胶质细胞占比及总小胶质细胞密度均显著高于对照,证实该细胞亚群的临床相关性。
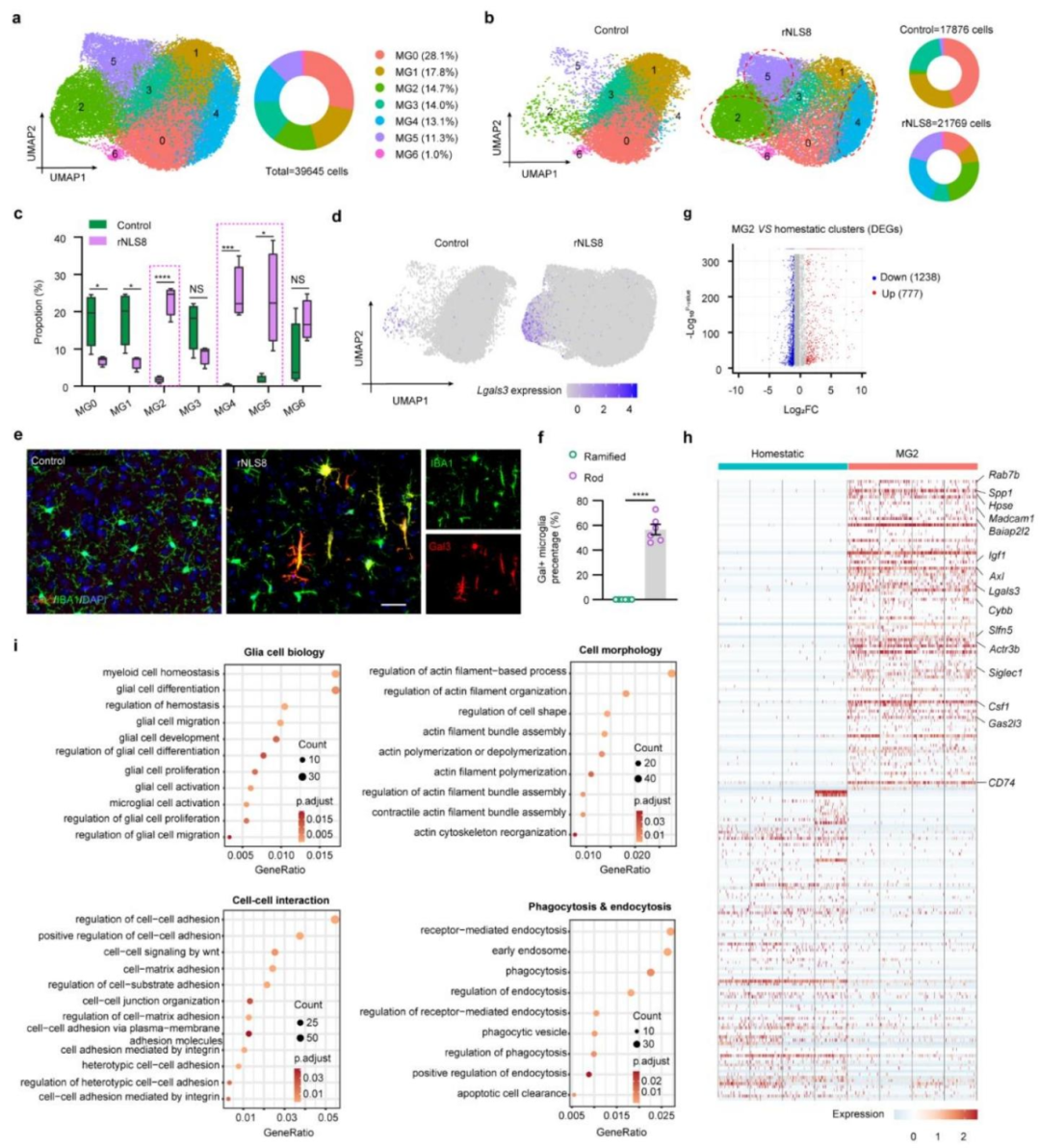
图4:棒状小胶质细胞具有独特的疾病相关转录与功能特征
将小胶质细胞进一步分为 7 个亚群,其中 rNLS8 小鼠特异性富集的 MG2 亚群为 “疾病相关小胶质细胞(DAM)”,其下调稳态标志物(P2ry12、Tmem119),上调 Apoe、Lgals3 等 DAM 标志物;免疫染色验证发现 60% 的棒状小胶质细胞特异性表达 Galectin-3(Lgals3 编码),提示其属于 MG2 亚群;MG2 亚群的差异基因富集于细胞黏附、吞噬作用、细胞形态重塑通路,提示该亚群具备与神经元相互作用及突触调控的功能基础。
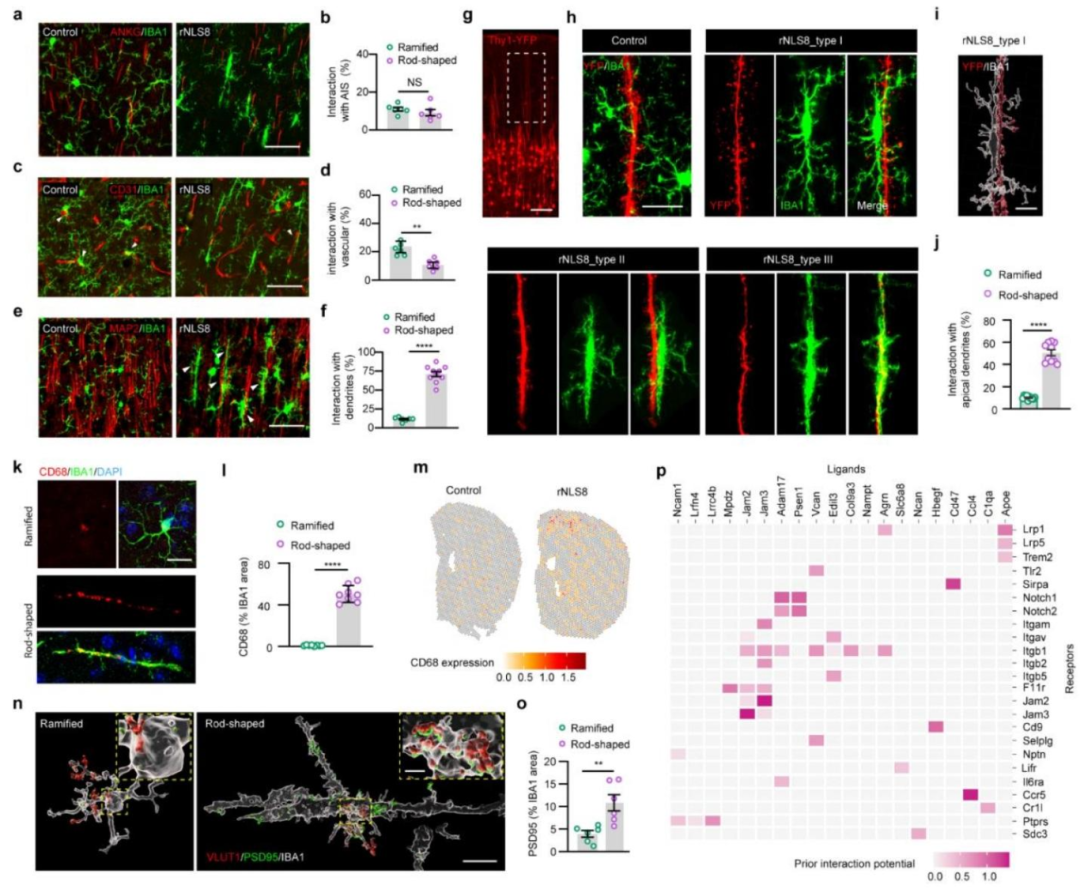
图5:棒状小胶质细胞优先与神经元树突结合并吞噬兴奋性突触
免疫荧光共标显示,约 70% 的棒状小胶质细胞与神经元树突(MAP2 标记)结合,其中近 50% 靶向 5 层锥体神经元的顶树突,且存在 “连接树突与树突棘”“包裹顶树突” 等 3 种超微作用模式;同时棒状小胶质细胞高表达吞噬标志物 CD68,且可大量吞噬兴奋性突触标志物(VGLUT1/PSD95);配体 - 受体互作分析发现,小胶质细胞高表达黏附(Notch 家族)与吞噬(Trem2)相关受体,神经元来源的 Apoe 等可作为潜在配体介导二者相互作用。
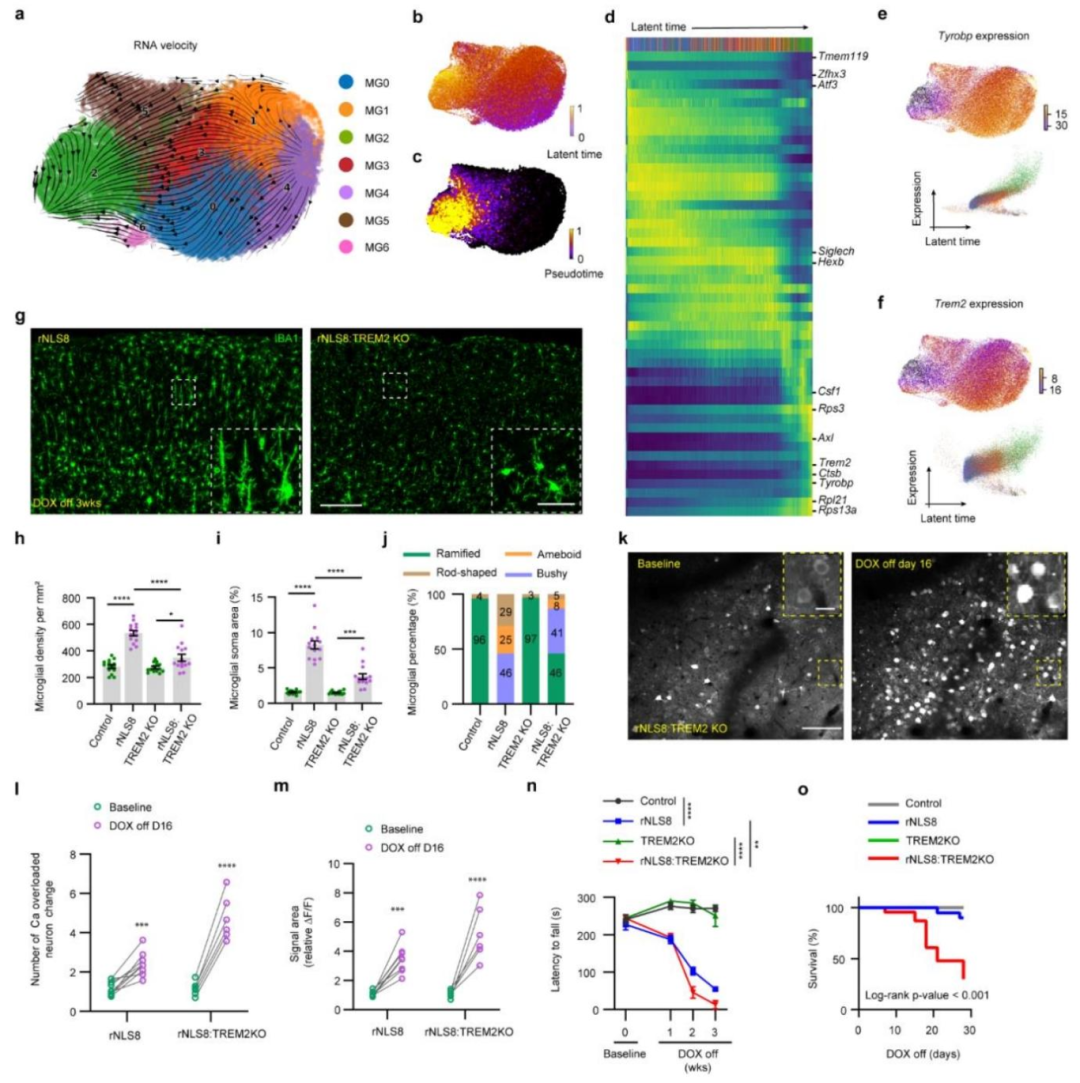
图6:TREM2/DAP12 通路调控棒状小胶质细胞形成并影响疾病表型
RNA velocity 分析显示小胶质细胞从稳态亚群逐步向 MG2(棒状小胶质细胞所属亚群)分化,且分化过程中 Tyrobp(编码 DAP12)与 Trem2 表达显著上调;TREM2 敲除后,rNLS8 小鼠运动皮层小胶质细胞密度、胞体面积及棒状细胞占比均显著降低;同时神经元钙超载现象加剧(钙信号面积提升至 412±19%),小鼠运动功能(转棒潜伏期)显著下降,生存周期缩短,证实 TREM2/DAP12 通路是棒状小胶质细胞形成的关键调控通路,且该细胞亚群可通过抑制神经元过度兴奋发挥神经保护作用。
本研究以 TDP-43 相关神经变性小鼠模型为核心,先通过电生理与钙成像明确了疾病早期运动皮层过度兴奋的特征及来源;再结合空间与单细胞转录组技术,鉴定出响应该病理状态的特异性棒状小胶质细胞亚群,并明确其疾病相关转录特征;随后通过形态学与功能实验,揭示该细胞亚群可通过靶向神经元顶树突、吞噬兴奋性突触来抑制皮层过度兴奋;最后借助 TREM2 敲除模型,验证了该通路对棒状小胶质细胞形成的调控作用及细胞亚群的神经保护功能。该研究不仅阐明了小胶质细胞调控神经环路兴奋性的新机制,还为 ALS 等 TDP-43 相关神经变性疾病的早期靶向干预提供了新的细胞与分子靶点。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:SFRP2 单克隆抗体通过重塑肿瘤相关巨噬细胞抑制三阴性乳腺癌生长与转移
下一篇:Eomesodermin+CD4+T 细胞:治愈性免疫治疗的关键 “双功能” 细胞