常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-28 17:00:00 细胞资源库平台 访问量:13
人类脑类器官 —— 这个由多能干细胞培育出的 “微型大脑”,是近年来神经科学领域的 “明星工具”:它能模拟人脑发育过程,为阿尔茨海默病、小头症等神经疾病提供理想模型,更被寄予 “修复受损大脑” 的厚望。
但脑类器官的发展始终面临 “瓶颈”:由于缺乏功能性循环系统,内部易缺氧、细胞死亡,导致神经祖细胞(NPC)耗竭,不仅限制了类器官的成熟,也让其移植到宿主脑后的整合效果大打折扣。此外,物理刺激(如超声)对脑类器官发育、移植整合的影响,以及如何修复小头症等神经发育疾病的类器官缺陷,这些关键问题一直缺乏明确答案。
来自天津大学医学工程与转化医学研究院的团队在神经科学顶刊《BRAIN》上发表题为 “Low-intensity ultrasound ameliorates brain organoid integration and rescues microcephaly deficits” 的研究,首次揭示:低强度超声(LIUS)可通过调控 YAP 信号通路,显著促进脑类器官发育、提升移植后的结构与功能整合,并成功挽救小头症模型的神经缺陷,为非侵入性治疗神经发育疾病和脑损伤提供了全新策略。
实验方法:严谨设计,多维度验证
为解答 “LIUS 如何影响脑类器官” 这一核心问题,团队从类器官制备、超声干预、动物模型、检测技术四个维度构建实验体系,确保结果可靠:
脑类器官制备:采用已验证的 protocol(参考 Xiang et al., 2019),从人多能干细胞(hPSC)诱导皮质类器官,重点观察神经祖细胞(NPC)富集的心室区(VZ)发育。
LIUS 干预参数:
体外刺激:3MHz 平面换能器(有效辐射面积 5cm²),筛选出 0.2W 为最优强度(低强度无热损伤,且促发育效果最显著);
体内刺激:1MHz 聚焦换能器(焦距 21mm),移植后 7 天开始持续刺激 1 个月,避免损伤宿主脑。
动物分组与模型:
正常类器官移植:将小鼠分为对照组(n=30)、LIUS 预处理组(n=15)、体内 LIUS 刺激组(n=15),每组含短期(2 个月)、长期(5 个月)实验及电生理记录亚组;
小头症模型:通过 CRISPR/Cas9 构建 ASPM 基因敲除(ASPM⁻/⁻)hESC,诱导小头症类器官,分组同上(n=15 / 组)。
检测技术:结合组织学染色(Ki67、NeuN、YAP 等标志物)、单细胞测序(scRNA-seq)、 bulk RNA-seq、柔性多电极阵列电生理记录(3-5 个月纵向监测)、疼痛行为学实验(von Frey 刺激),多维度验证 LIUS 的作用。
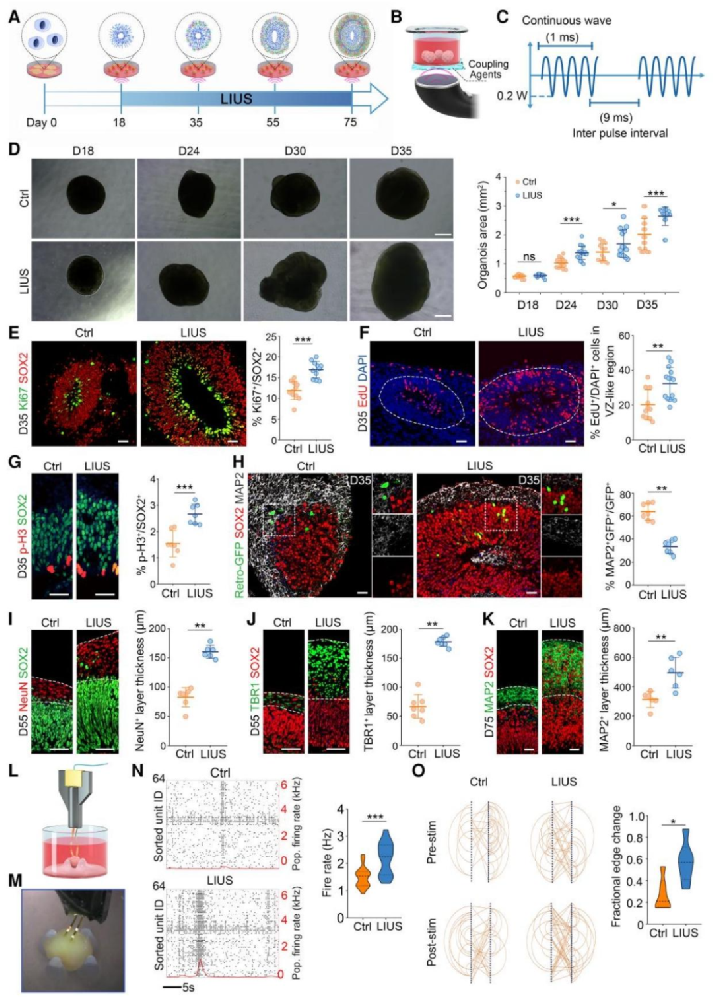
图1:低强度超声(LIUS)显著促进皮质类器官增殖与成熟
团队从类器官发育早期(Day18,神经祖细胞 NPC 富集阶段)开始用 0.2W LIUS 刺激,追踪至 Day75 发现:LIUS 组类器官面积持续大于对照组,NPC 增殖标志物(Ki67⁺、EdU⁺、p-H3⁺)阳性细胞比例更高、心室区(VZ)NPC 层更厚,同时细胞凋亡减少;发育早期 LIUS 延迟 NPC 向神经元分化(为增殖留时间),后期却显著增厚皮质板(CP)层、增加深层神经元(TBR1⁺/CTIP2⁺)数量,且突触密度(SYN⁺PSD95⁺)与电生理活性(放电率、burst 数量)均提升,高频刺激后功能连接更强,证明 LIUS 能同时促进类器官增殖与神经网络成熟。
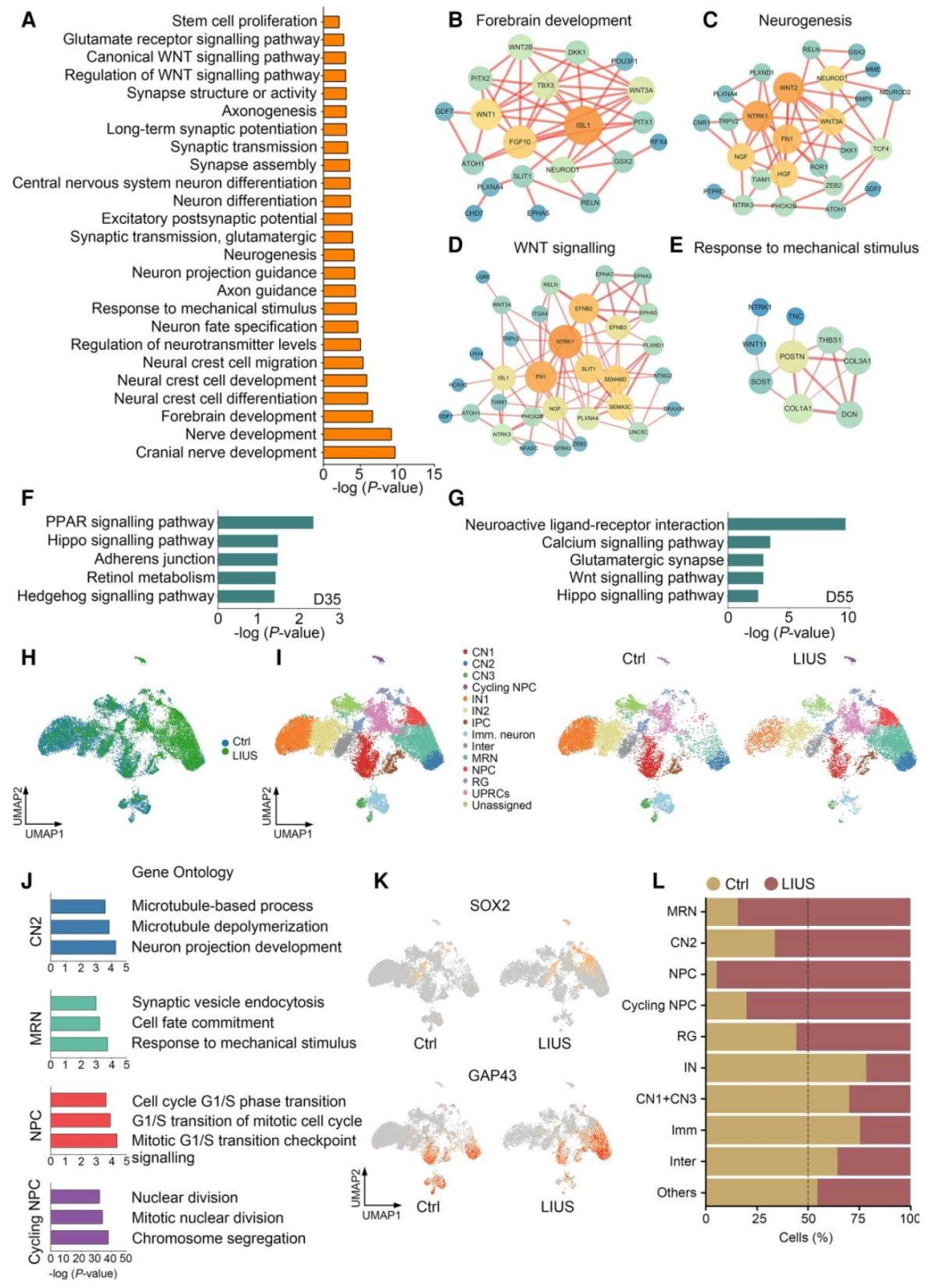
图2:LIUS 重塑神经发育相关基因表达图谱
为探究 LIUS 的分子机制,团队对 Day35/55 的类器官进行转录组分析,结果显示:Day35 时 LIUS 组有 417 个差异表达基因(DEG),Day55 时增至 2292 个,这些 DEG 显著富集于 “前脑发育”“神经发生”“WNT 信号通路”“机械刺激响应” 等神经发育核心通路;单细胞测序进一步发现,LIUS 组中 “机械刺激响应神经元(MRN)”“神经祖细胞(NPC)”“放射状胶质细胞(RGC)” 比例显著升高,从分子与细胞层面证实 LIUS 对神经发育的调控作用。
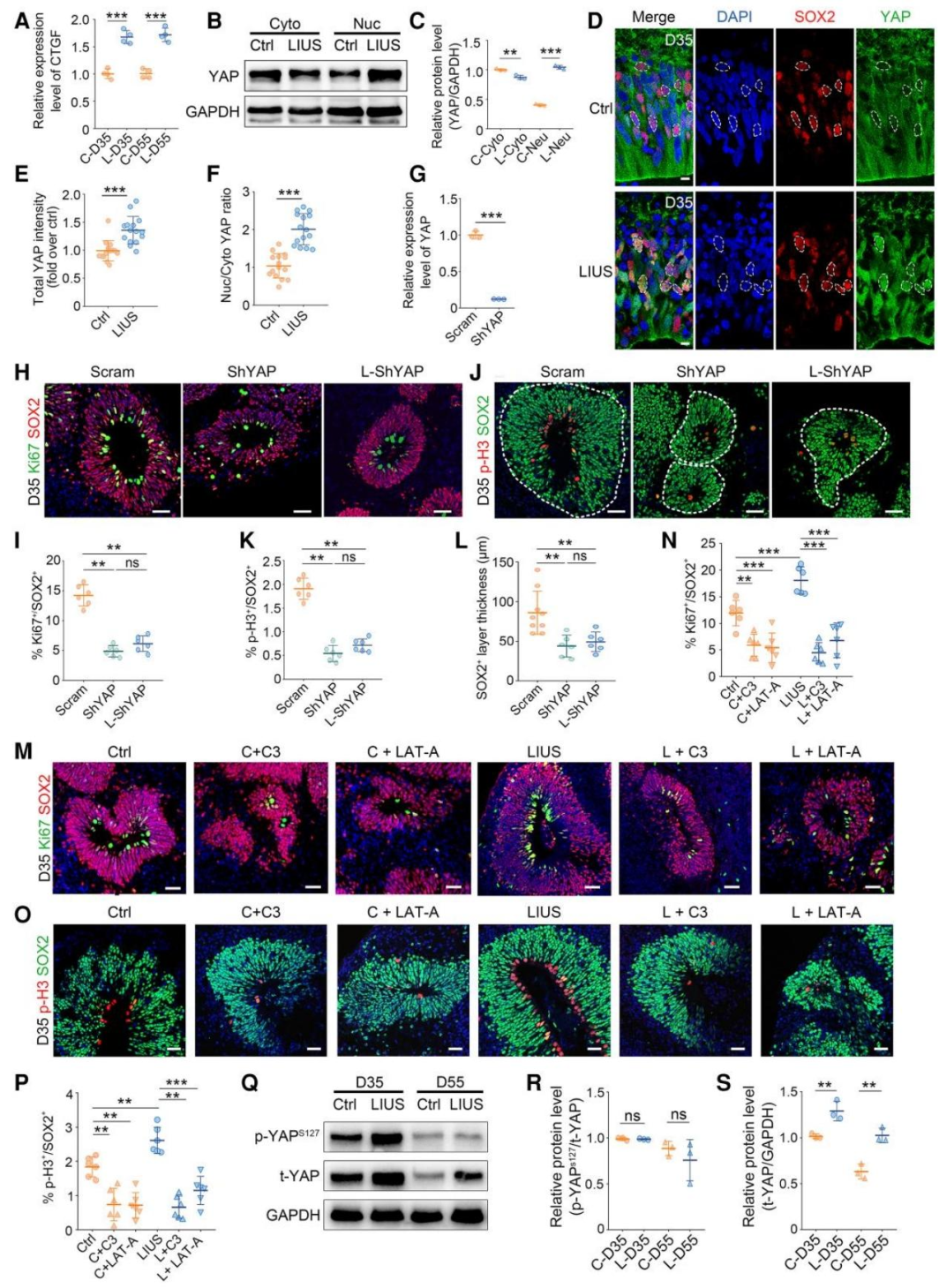
图3:YAP 是 LIUS 促增殖效应的 “关键中介”
针对机械敏感转录因子 YAP 的研究发现:LIUS 组 YAP 靶基因 CTGF 表达升高,且 YAP 蛋白更多定位于细胞核(核内 YAP↑、胞质 YAP↓),表明 YAP 被激活;通过慢病毒敲低 YAP 后,LIUS 促进 NPC 增殖的效果完全消失,而用肌动蛋白抑制剂(Lat-A)或 Rho 抑制剂(C3 转移酶)处理也会逆转 LIUS 的作用,但 YAP 磷酸化水平(Hippo 通路标志)无变化,证明 LIUS 是通过 “Rho - 肌动蛋白 - YAP” 通路而非经典 Hippo 通路促进 NPC 增殖。
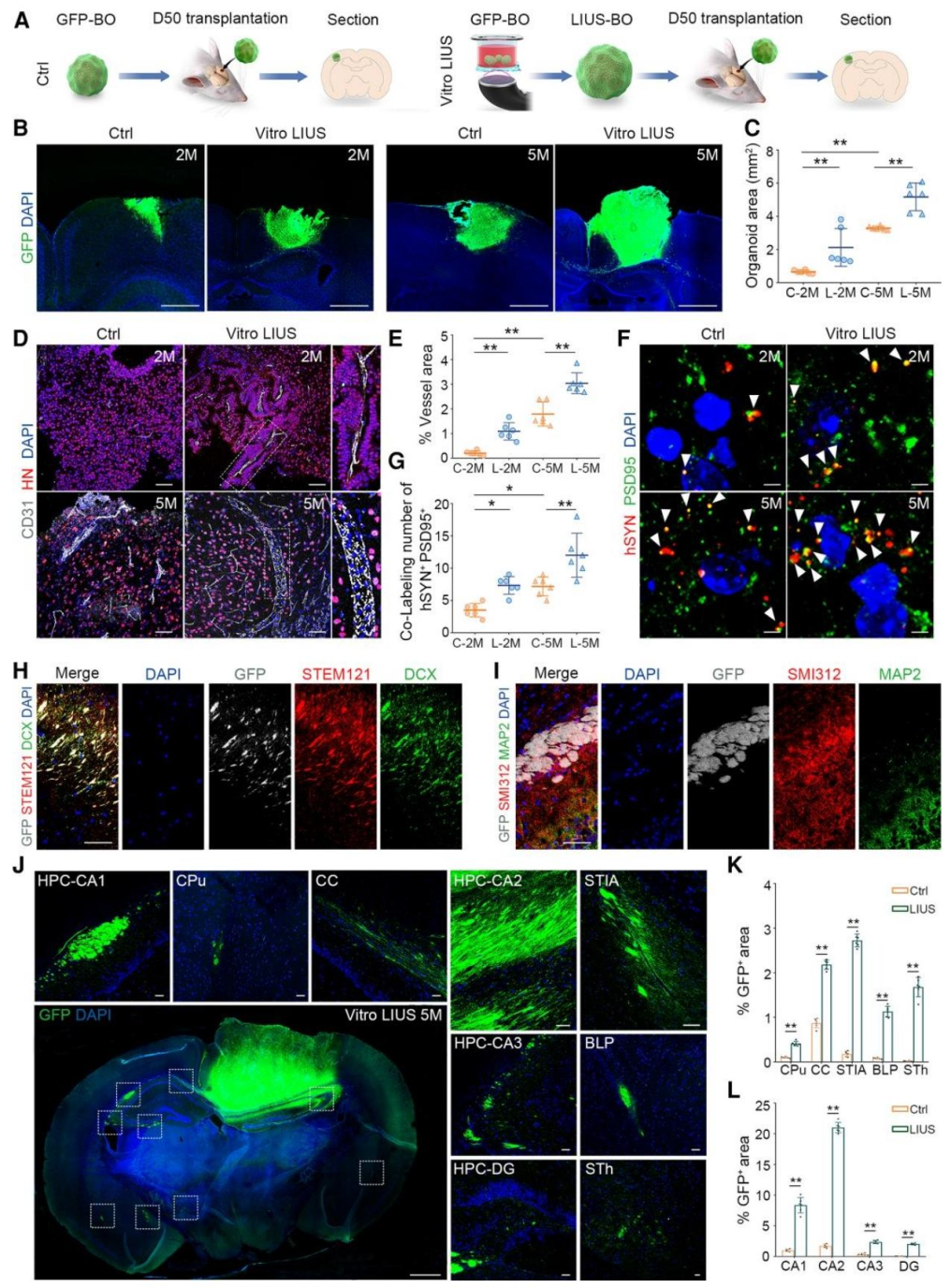
图4:LIUS 预处理让类器官移植物在宿主脑内 “活得更好、长得更熟”
将 Day50 的类器官移植到小鼠损伤躯体感觉皮层(S1 区)后观察发现:LIUS 预处理组移植物面积随时间(2-5 个月)持续大于对照组,且无畸胎瘤形成;移植物内宿主来源血管(CD31⁺HN⁻)密度更高,成熟神经元(NeuN⁺)更多、星形胶质细胞(GFAP⁺)更少;移植物与宿主脑的突触连接(hSYN⁺PSD95⁺)更密集,轴突能投射到对侧皮质、海马等更远脑区,为功能整合奠定结构基础。
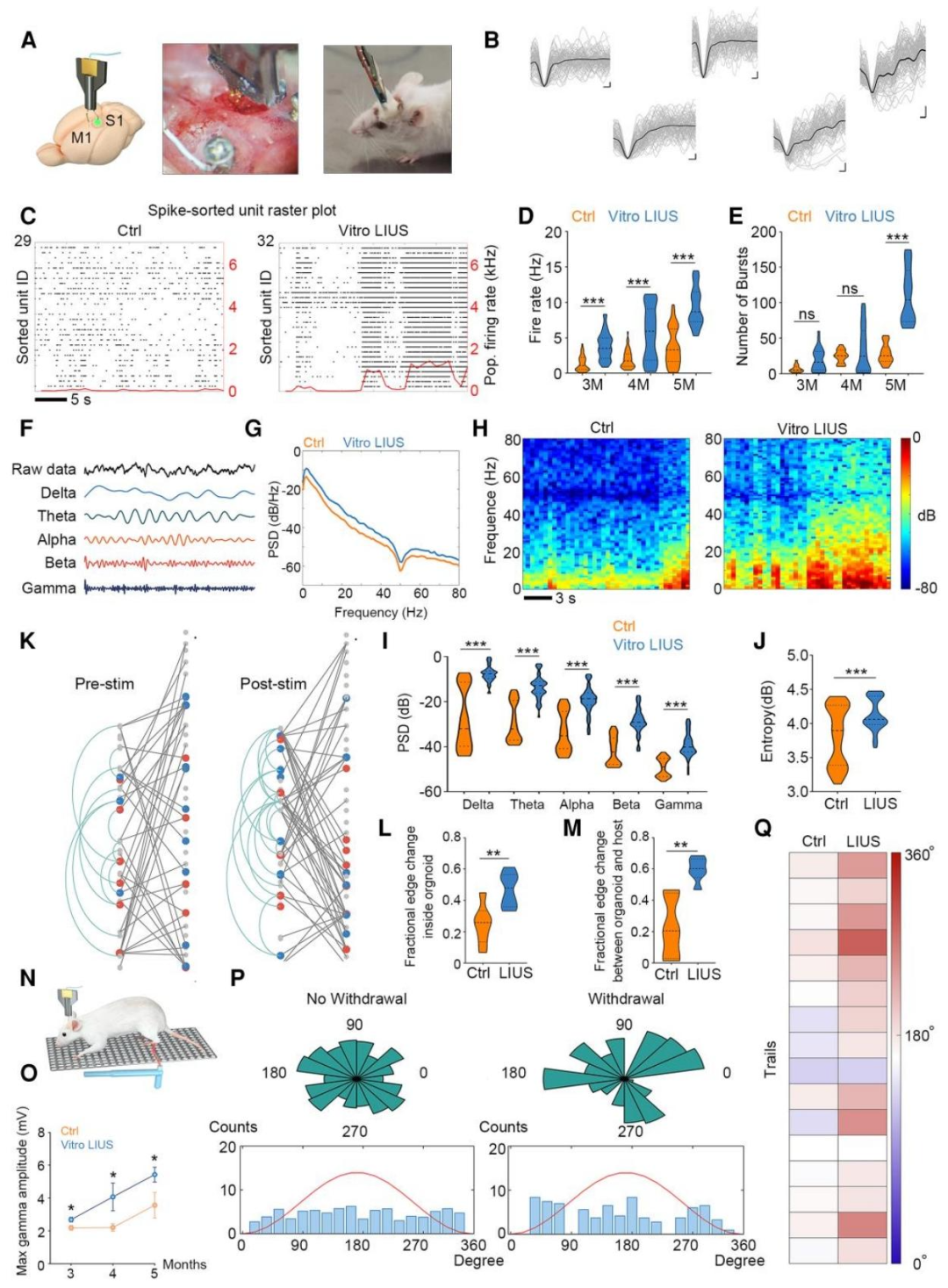
图5:LIUS 预处理让移植物与宿主脑 “功能互通”
通过柔性多电极阵列(32 个电极在移植物、32 个在宿主运动皮层)纵向记录 3-5 个月发现:LIUS 组移植物的放电率、burst 数量及全频段电活动能量均持续高于对照组;给小鼠后爪施加疼痛刺激时,LIUS 组移植物的 gamma 振荡(疼痛相关神经活动)幅度更大,神经元 spike 与 gamma 相位锁定更深,证明移植物已融入宿主疼痛感知回路,实现功能性整合。
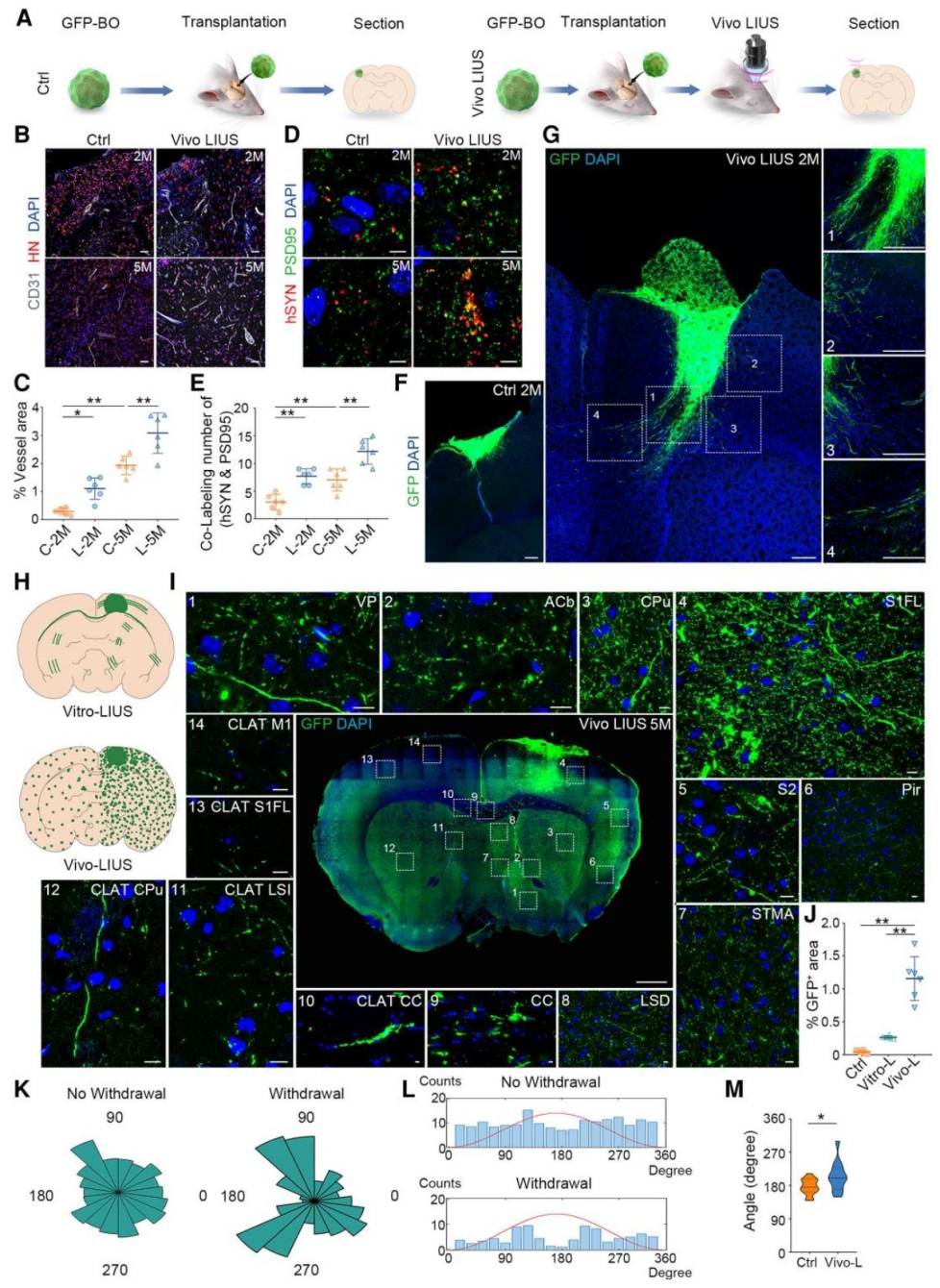
图6:体内 LIUS 刺激让移植物 “弥散投射,突破瘢痕”
不同于移植前预处理,移植后 7 天开始的体内 LIUS 刺激展现独特优势:移植物轴突能向宿主深部脑区(伏隔核、丘脑底核)投射,5 个月时移植物边界模糊(弥散投射),对侧半球投射密度显著高于对照组;同时,宿主脑内 GFAP⁺胶质细胞密度降低,移植物周围无 “胶质瘢痕”(对照组常见),解决了神经移植中轴突投射受阻的关键问题,且血管化、电生理活性与功能整合效果与体外预处理相当。
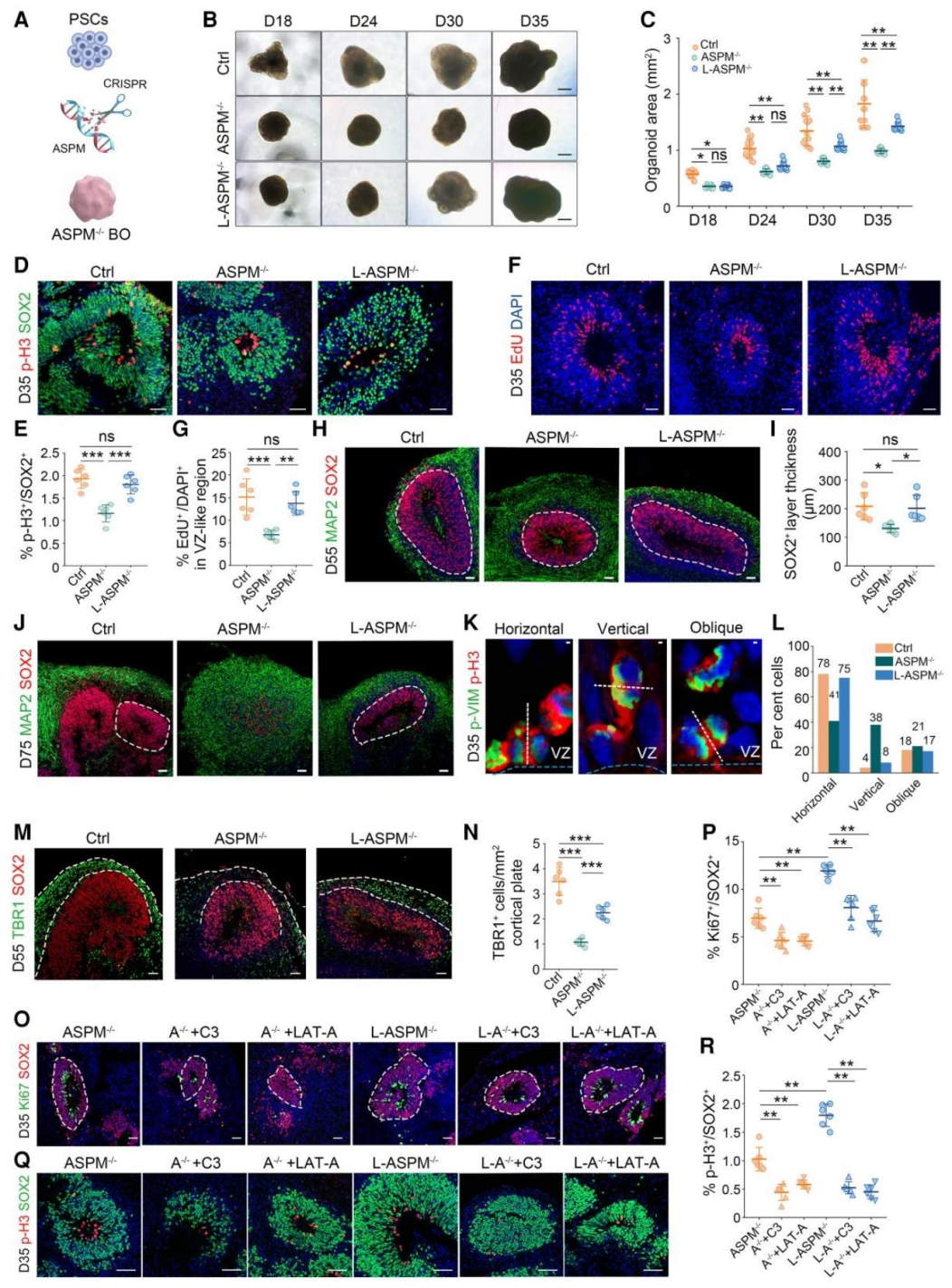
图7:LIUS “挽救” ASPM 突变体类器官的小头症缺陷
对 ASPM 基因敲除(ASPM⁻/⁻)小头症类器官的研究发现:ASPM⁻/⁻类器官显著小于对照组,无典型脑室结构,NPC 增殖减少、细胞分裂方向异常(水平分裂↓、垂直 / 倾斜分裂↑);LIUS 处理后,类器官面积恢复,脑室结构重现,NPC 增殖标志物阳性细胞比例回升,水平分裂比例正常化,神经元数量(TBR1⁺)与突触密度显著增加,且 YAP 核定位升高、Lat-A/C3 转移酶会逆转修复效果,证明 LIUS 通过 YAP 通路挽救小头症缺陷。
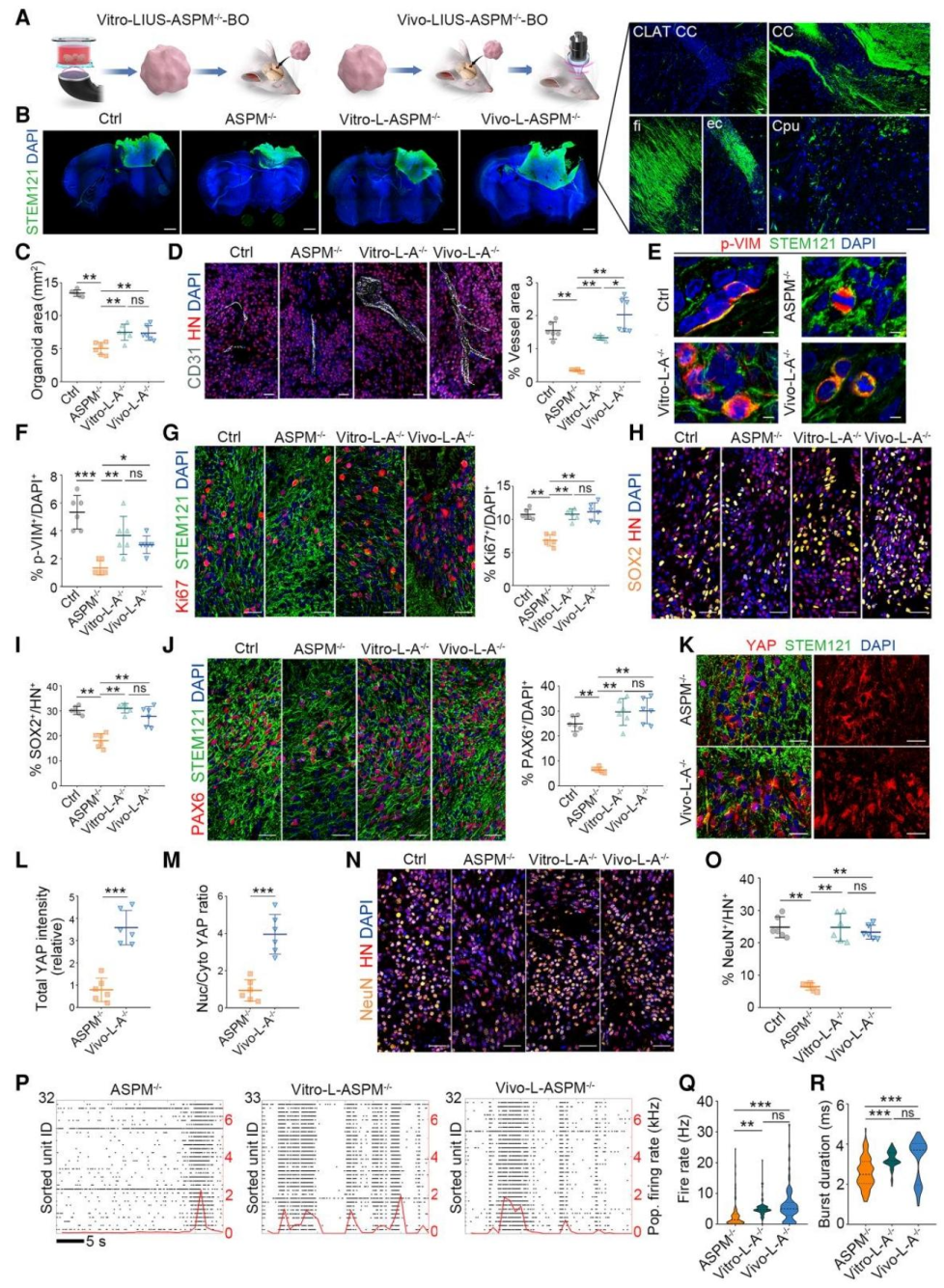
图8:LIUS 促进移植的 ASPM 突变体类器官 “在宿主脑内发育”
将 ASPM⁻/⁻类器官移植到小鼠脑后发现:未处理的 ASPM⁻/⁻移植物面积显著缩小,而体外 / 体内 LIUS 处理后面积恢复,宿主来源血管(CD31⁺)密度升高;移植物内增殖 NPC(p-VIM⁺、Ki67⁺)与成熟神经元(NeuN⁺)数量显著增加,电生理活性(放电率、burst 持续时间)接近正常类器官水平,证实 LIUS 在体内环境中同样能修复小头症类器官的神经发育缺陷。
天津大学医学工程与转化医学研究院团队在《BRAIN》发表的这项研究,通过 “体外类器官培养 - 体内移植 - 多维度检测” 的系统实验,首次证实低强度超声(LIUS)可作为调控脑类器官发育与功能的非侵入性工具,其核心机制是通过 “Rho - 肌动蛋白 - YAP” 通路激活神经祖细胞(NPC)增殖:LIUS 不仅能解决脑类器官缺氧、NPC 耗竭、成熟慢的发育瓶颈,构建更接近人脑的神经网络;还能通过移植前预处理或移植后体内刺激,促进移植物血管化、减少胶质瘢痕、增强轴突投射与宿主脑的功能整合,优化神经移植效果;更重要的是,LIUS 成功挽救了 ASPM 突变导致的小头症类器官结构与功能缺陷,为小头症等神经发育疾病及脑损伤修复提供了全新的非侵入性策略,未来随着 LIUS 参数优化与灵长类模型验证,有望进一步推动临床转化。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:胶质细胞富集型皮质类器官,解锁人类星形胶质细胞研究新范式
下一篇:基于阳离子三酰脂质的 mRNA 脂质复合物实现肿瘤细胞高效 mRNA 转染