常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-28 09:00:00 细胞资源库平台 访问量:19
星形胶质细胞是人类大脑中数量最丰富的胶质细胞,它们不仅为神经元提供结构支持与营养供给,更在突触形成、神经炎症调控、血脑屏障维持中发挥关键作用 —— 其功能异常与阿尔茨海默病、癫痫、脑损伤等多种神经系统疾病密切相关。
然而,人类星形胶质细胞的研究长期受限于两大难题:一是模型稀缺,传统皮质类器官因人类皮质胶质发生启动较晚,需培养 3 个月以上才会出现少量星形胶质细胞,且成熟周期长达 1 年,难以满足研究需求;二是功能验证难,体外培养的类器官缺乏血管网络与宿主脑微环境,无法模拟星形胶质细胞在体内的复杂形态(如血管周足)与功能(如神经炎症反应)。
来自美国索尔克生物研究所的团队在《Nature Biotechnology》发表题为 “Morphological diversification and functional maturation of human astrocytes in glia-enriched cortical organoid transplanted in mouse brain” 的研究,首次构建出胶质细胞富集型皮质类器官模型:通过诱导祖细胞 “胶质发生转换”,8-10 周内即可使星形胶质细胞占比达 25%-31%;更重要的是,将该类器官移植到小鼠脑内后,人类星形胶质细胞不仅分化出多种解剖学亚型,还能形成血管周足、响应神经炎症,为解析人类星形胶质细胞功能及相关疾病机制提供了全新平台。
实验方法:精准诱导 + 体内移植,构建功能完整的星形胶质细胞模型
团队围绕 “高效诱导星形胶质细胞分化” 与 “验证体内功能” 两大目标,设计了严谨的实验体系:
1. 胶质细胞富集型皮质类器官的构建
诱导策略:从人多能干细胞(hESC/hiPSC)形成类胚体(EB)后,在神经外胚层诱导阶段(Day1-Day14)添加血小板衍生生长因子(PDGF-AA,已知胶质发生关键因子),并使用星形胶质细胞专用培养基(AstroM)培养;Day22 后换用含 10% 胎牛血清(FBS)的分化培养基,补充 BDNF、GDNF 等神经营养因子,促进细胞成熟。
关键筛选:通过免疫染色验证神经祖细胞(SOX2⁺)、星形胶质细胞(GFAP⁺、HepaCAM⁺)与神经元(NeuN⁺)的分化效率,最终确定 8-10 周龄的类器官(星形胶质细胞占比 25%-31%)用于后续移植。
2. 类器官移植与体内验证
移植模型:将 8-10 周龄的类器官移植到免疫缺陷小鼠(NOD.Cg-Prkdcscid/2rg tm1wj/SzJ,NSG 小鼠)的 retrosplenial 皮质损伤腔中,术后饲养 2-8 个月,观察星形胶质细胞的形态分化与功能整合。
神经炎症模型:通过立体定位注射向移植后的类器官注入肿瘤坏死因子 -α(TNFα,促炎细胞因子),5 小时后通过流式分选纯化胶质细胞,结合单细胞 RNA 测序(scRNA-seq)分析反应性星形胶质细胞的转录组变化;同时在体外类器官中加入 TNFα 与 CD38 抑制剂(78c),验证 CD38 信号的作用。
检测技术
结合单细胞核 RNA 测序(snRNA-seq)、空间转录组(NanoString GeoMx DSP)、共聚焦显微镜成像、电子显微镜(EM)三维重建、行为学与分子生物学实验(qPCR、Western blot、谷氨酸摄取实验),从分子、细胞、组织层面多维度验证星形胶质细胞的分化、成熟与功能。
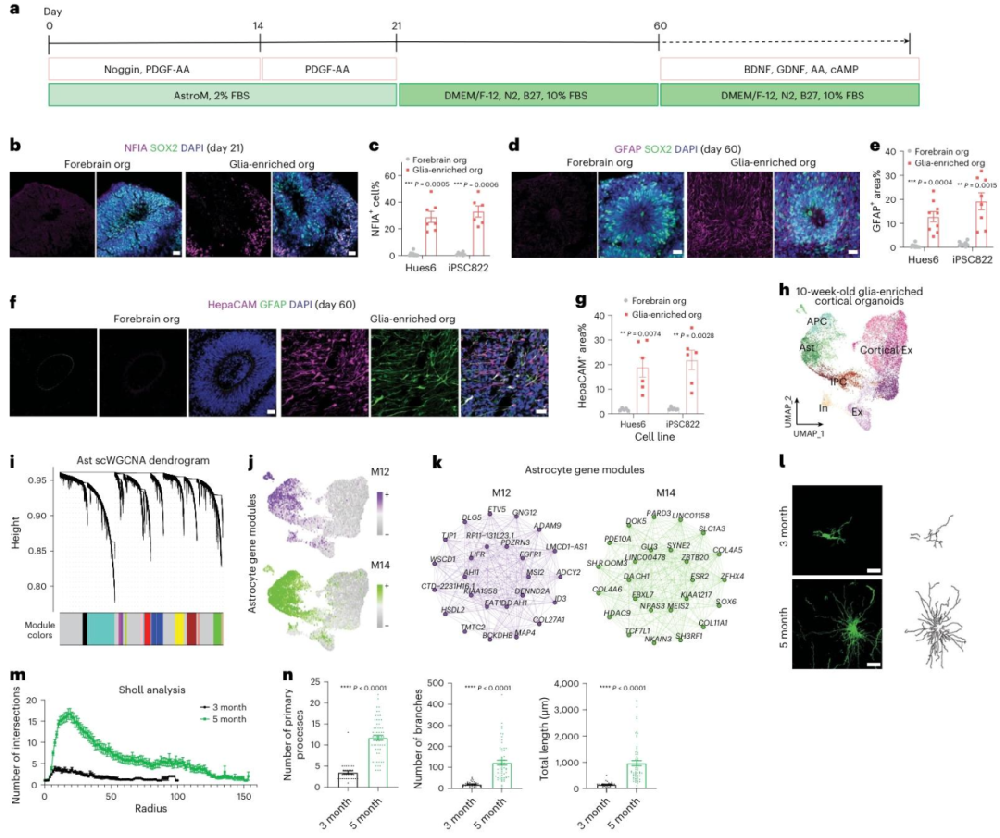
图1:胶质细胞富集型皮质类器官实现星形胶质细胞快速分化与成熟
为解决传统类器官星形胶质细胞分化慢的问题,团队采用 “PDGF-AA 诱导 + 星形胶质细胞培养基” 策略,结果显示:分化 3 周时,类器官中胶质发生关键因子 NFIA⁺细胞比例显著高于传统前脑类器官,2 个月时星形胶质细胞标志物 GFAP⁺、HepaCAM⁺区域面积是传统类器官的 3-5 倍,10% FBS 培养条件分化效率最高;snRNA-seq 鉴定出皮质兴奋性神经元、抑制性神经元及占比 25%-31% 的星形胶质细胞(含 5%-8% 增殖型胶质祖细胞),WGCNA 发现星形胶质细胞核心基因模块富集 “细胞黏附”“谷氨酸转运” 功能基因;GFAP::GFP AAV 标记显示,3 月龄星形胶质细胞已具分支结构,5 月龄时分支数量与长度显著增加,且能高效摄取谷氨酸,证实其功能成熟。
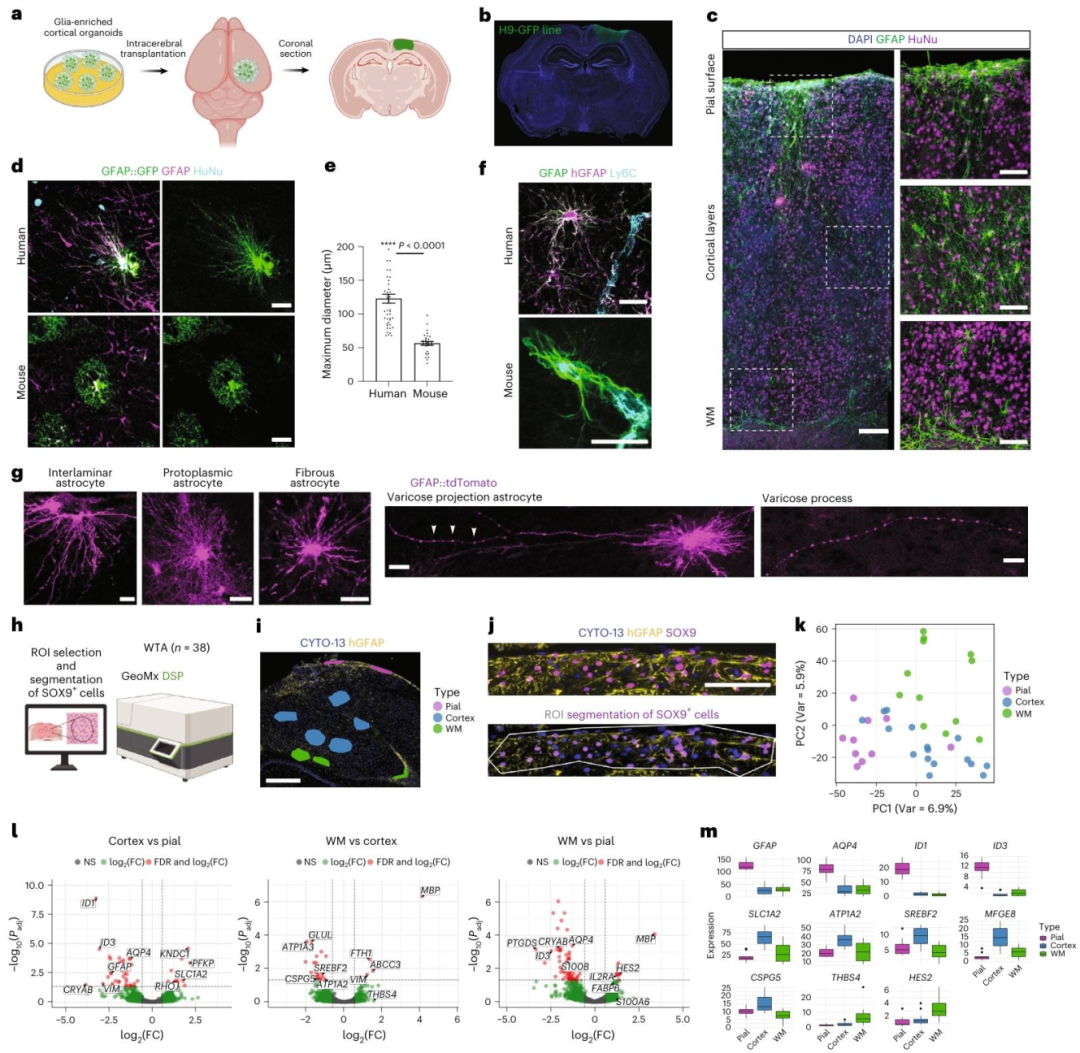
图2:移植后人类星形胶质细胞分化出多种解剖学亚型,且具有层特异性分子特征
将 8-10 周龄类器官移植到 NSG 小鼠皮质损伤腔后,6-8 个月观察发现:人类星形胶质细胞最大直径(约 150μm)显著大于小鼠(约 50μm),原浆型星形胶质细胞突起更复杂,且向血管延伸突起的方式与小鼠存在物种差异;移植后的人类星形胶质细胞分化出层间型(软脑膜下,突起贯穿皮质层)、原浆型(皮质层内,围绕突触)、纤维型(白质区,与髓鞘相关)及人类特有的曲张投射型星形胶质细胞;空间转录组(GeoMx DSP)分析显示,软脑膜区星形胶质细胞高表达 GFAP、AQP4,皮质区富集 SLC1A2(谷氨酸转运体)、ATP1A2(钠钾 ATP 酶),白质区高表达 THBS4(血栓调节蛋白)、HES2(转录因子),证实其分子功能的空间特异性。
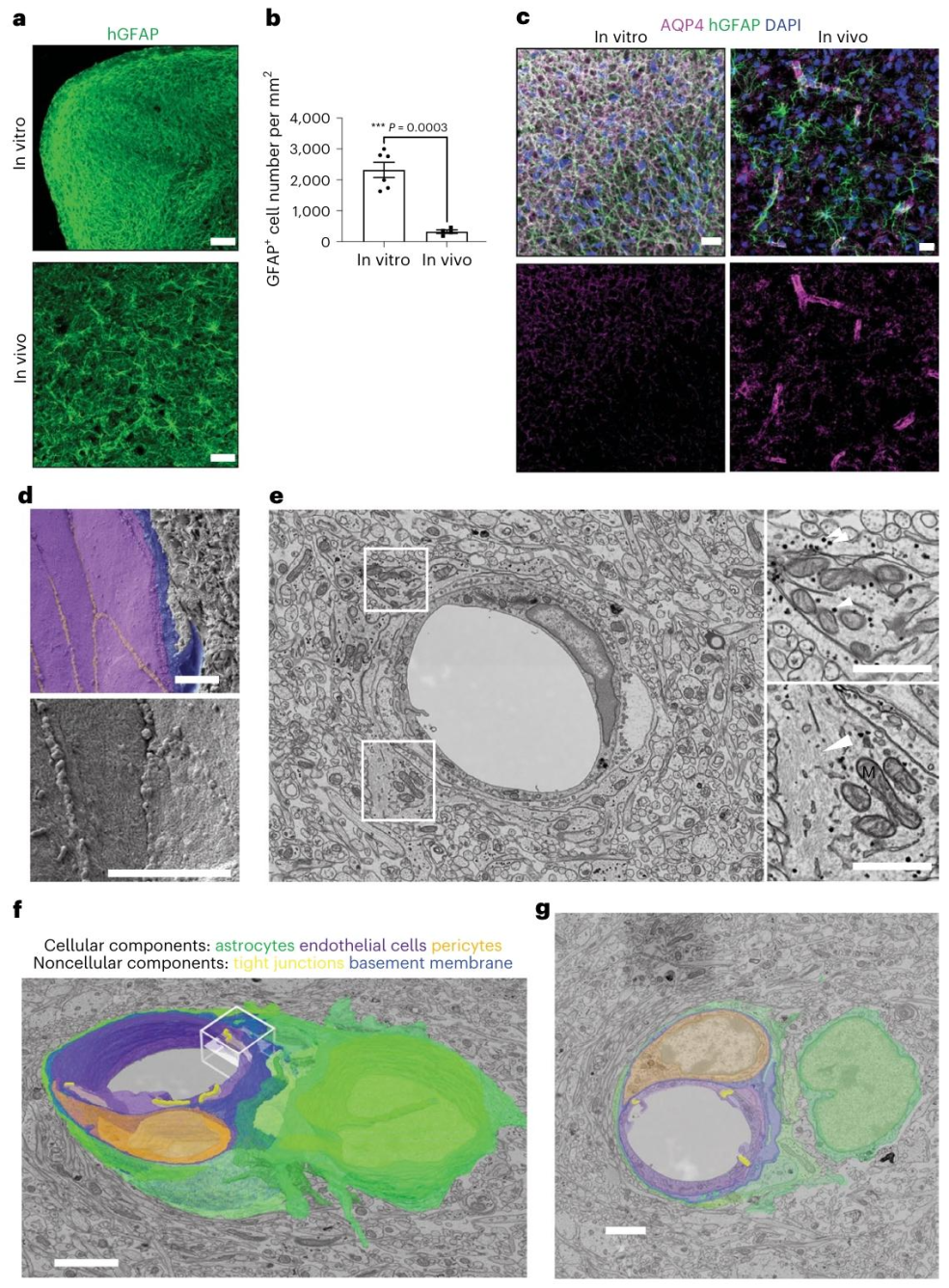
图3:人类星形胶质细胞在移植后形成血管周足,与宿主血管紧密耦合
针对星形胶质细胞血管周足这一体外无法模拟的结构,研究发现:体外类器官中星形胶质细胞 AQP4(水通道蛋白)表达分散,而移植后 AQP4 在突起末端高度富集形成血管周足,同时表达 Kir4.1(钾离子通道)、Glut1(葡萄糖转运体),与体内人类星形胶质细胞特征一致;扫描电镜观察到移植区血管内皮细胞间存在紧密连接,星形胶质细胞突起包裹血管表面形成胶质界膜,透射电镜显示星形胶质细胞胞质含糖原颗粒、胶质丝(GFAP),三维重建证实突起完全覆盖血管表面,实现与宿主血管的功能耦合。
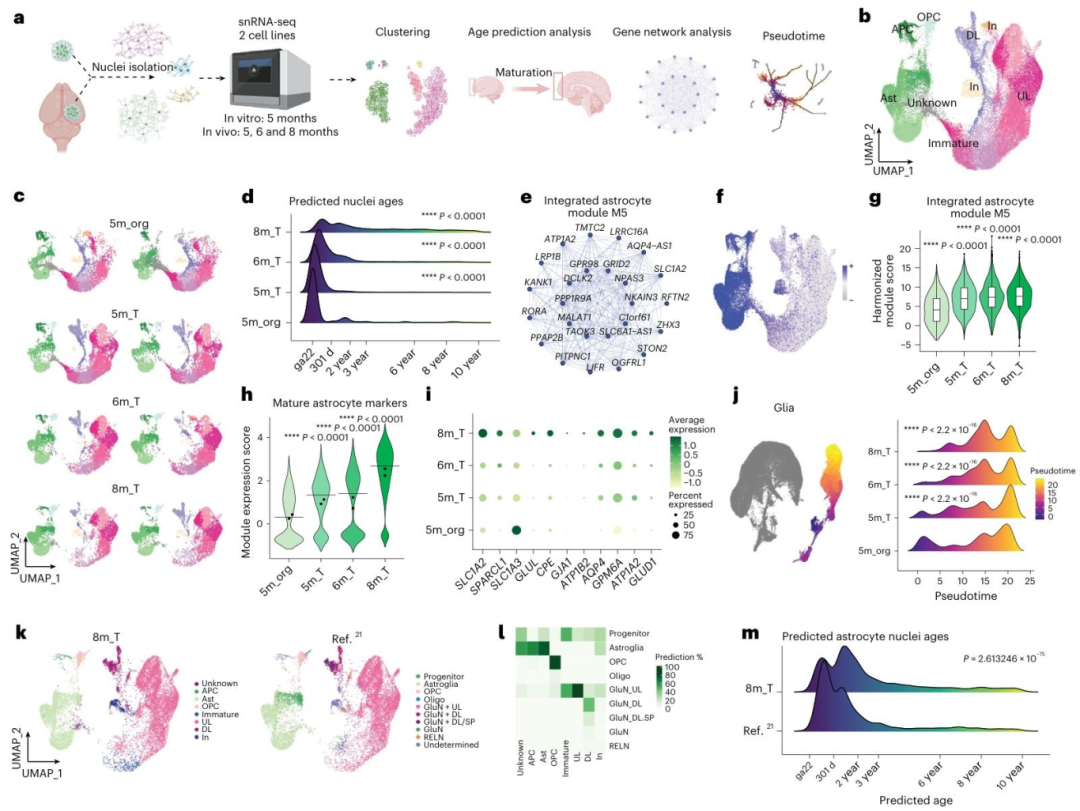
图4:移植显著促进类器官细胞成熟,星形胶质细胞达到产后阶段水平
对 5 月龄体外类器官、5/6/8 月龄移植类器官的 snRNA-seq 分析显示:5 月龄体外类器官细胞主要对应人类胎儿期脑组织,移植后细胞逐渐向产后阶段过渡,8 月龄移植类器官中 94.5% 的上层皮质神经元、75.8% 的星形胶质细胞对应人类产后 301 天以上细胞状态,显著高于传统皮质类器官(56.2% 星形胶质细胞达产后水平);移植后星形胶质细胞成熟标志物(AQP4、SLC1A2、GLUL)表达显著高于体外类器官,伪时间轨迹分析显示其从胶质祖细胞向成熟星形胶质细胞分化进程更快,且核心功能模块基因表达得分更高,与人类脑组织细胞类型组成、基因表达模式高度相似。
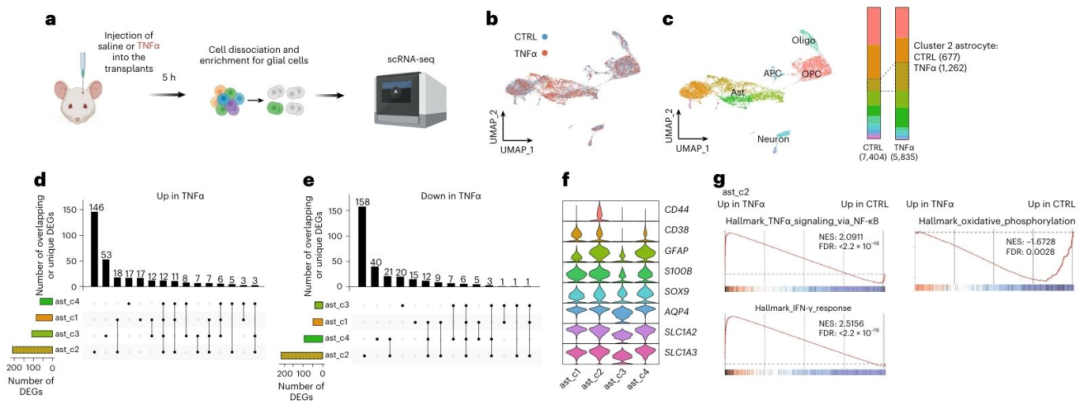
图5:神经炎症下人类星形胶质细胞表现出异质性反应
向移植类器官注射 TNFα(模拟神经炎症)后,scRNA-seq 分析发现:TNFα 处理使星形胶质细胞分为 4 个亚群,其中 Cluster 2 亚群(CD44⁺、CD38⁺、GFAP⁺)占比从 9% 升至 22%,该亚群高表达 NF-κB、IFN-γ 信号通路相关基因(如 RELA、STAT1),是主要促炎反应亚群,其他亚群炎症相关基因表达变化不显著,证实星形胶质细胞对炎症反应具有异质性;GSEA 分析显示 Cluster 2 亚群中 “氧化磷酸化”“线粒体呼吸链组装” 通路显著下调,提示炎症导致该亚群代谢应激。
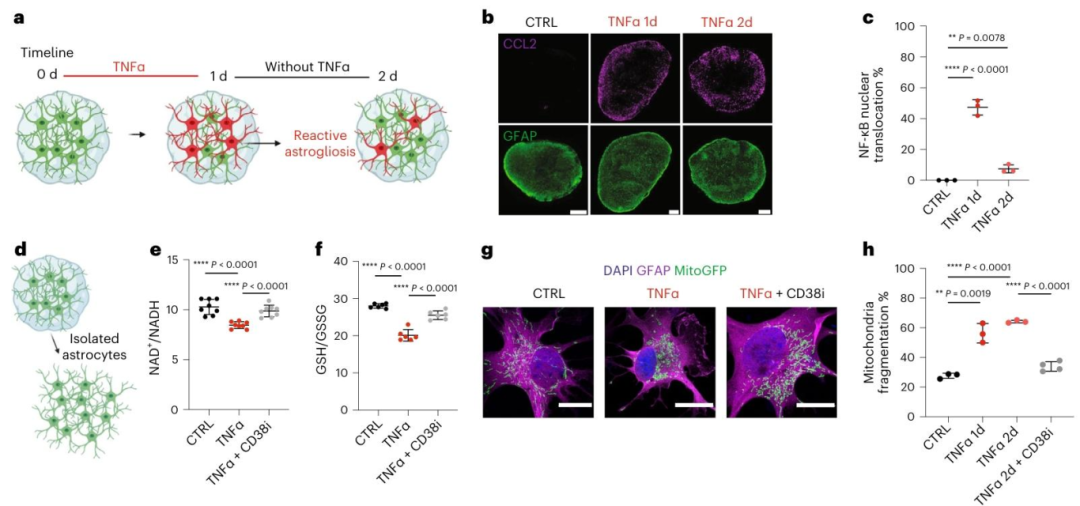
图6:CD38 信号通路介导反应性星形胶质细胞的代谢与线粒体应激
为验证炎症应激调控机制,体外实验显示:TNFα 处理 24 小时后,星形胶质细胞 NAD⁺/NADH 比值、GSH/GSSG 比值(氧化应激指标)显著降低,线粒体碎片化比例增加;TNFα 处理同时使星形胶质细胞 CD38(主要 NAD⁺降解酶)表达显著上调,加入 CD38 抑制剂(78c)后,NAD⁺/NADH 比值、GSH/GSSG 比值恢复,线粒体碎片化比例降低;免疫染色证实 TNFα 处理使星形胶质细胞 NF-κB 核转位比例升高,而 CD38 抑制剂不影响 NF-κB 激活,说明 CD38 主要调控代谢应激,而非直接抑制炎症通路。
通过 “PDGF-AA 诱导胶质发生转换 + NSG 小鼠皮质移植” 的创新策略,成功构建胶质细胞富集型皮质类器官模型,解决了人类星形胶质细胞研究中模型稀缺与功能验证难的痛点:该模型在 8-10 周内即可使星形胶质细胞占比达 25%-31%,且保留神经元等细胞多样性;移植后人类星形胶质细胞不仅分化出层间型、原浆型、纤维型及人类特有的曲张投射型等解剖学亚型,还形成血管周足结构并与宿主血管紧密耦合,同时在神经炎症刺激下表现出异质性反应;进一步研究证实 CD38 信号通路是介导反应性星形胶质细胞代谢与线粒体应激的关键靶点,为解析人类星形胶质细胞在生理与病理状态下的功能提供了理想模型,也为脑损伤、神经退行性疾病等星形胶质细胞相关疾病的机制研究与靶向治疗开发奠定了重要基础。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:一针“快进”20天:微创穿刺技术为乳腺癌类器官研究按下“加速键”
下一篇:低强度超声让脑类器官 “重生”,为脑损伤修复与小头症治疗开辟新路径