常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-16 09:00:00 细胞资源库平台 访问量:12
英文标题:Dual-mode hepatoprotective nanoplatform combines ROS scavenging and FGF21 activation for precision acute liver injury therapy
中文标题:双模式肝保护纳米平台结合ROS清除与FGF21激活用于精准急性肝损伤治疗
发表期刊:《Acta Pharmaceutica Sinica B (APSB)》
影响因子:14.6
作者单位:
厦门大学(儿童保健科、儿科学系、生命科学学院、药学院、公共卫生学院)福州大学附属省立医院中山大学肿瘤防治中心厦门大学四川研究院等
作者信息:
Xinyu Tan, Man Li, Zhibin Lan, Wenxiang Zhang, Junjie Zou, Yibo An, Jingwen Zheng, Xuwen Xiang, Jing Lin, Sheng Lin, Wenjie Ni, Lin Che, Gang Liu, Jing Chen, Zhixiang Lu
研究背景:
急性肝损伤(ALI)是一类以短期内大量肝细胞损伤、肝功能衰竭为特征的临床急症,尽管诱因多样,但氧化应激(ROS爆发)是所有ALI亚型的核心共同机制。过量ROS触发肝细胞释放炎性细胞因子(TNF-α、IL-6)和凋亡相关蛋白,形成恶性循环,最终可进展为肝硬化或肝癌。目前临床上缺乏有效的防治策略。
水飞蓟素(Silymarin)是一种经典抗氧化保肝药物,具有抗炎、抗纤维化、降脂等活性,但其水溶性极差、口服生物利用度低,严重限制临床疗效。成纤维细胞生长因子21(FGF21)是一种由肝脏分泌的内分泌因子,可对抗氧化应激和铁过载诱导的肝损伤,但天然FGF21在血浆中易降解、半衰期短。基因治疗虽可递送FGF21质粒(pFGF21),但存在递送效率低和免疫原性问题。
介孔二氧化硅纳米颗粒(MSN)具有高比表面积和良好生物相容性,但降解较慢。二硒键(Se-Se)键能低于二硫键,具有优异的活性氧响应性,可在高ROS微环境中氧化裂解并清除ROS。此外,M2型巨噬细胞膜包覆技术可赋予纳米载体炎症主动靶向能力和免疫调节功能。
研究创新点:
1.三重协同机制:平台整合了(a)外源性抗氧化(水飞蓟素+二硒键直接清除ROS)、(b)内源性免疫代谢调控(FGF21激活Nrf2/HO-1通路,诱导M2型巨噬细胞极化)、(c)脂质代谢重编程(抑制脂肪酸合成,促进氧化),实现了抗氧化-抗炎-代谢调控的多维度治疗。
2.智能响应性药物释放:利用ALI微环境中高ROS和弱酸性(pH 5.5-6.8)的特征,二硒键桥接的MSN核心在ROS触发下结构崩解,实现水飞蓟素的按需精准释放(48小时释放率92%),减少全身毒副作用。
3.仿生主动靶向:M2巨噬细胞膜包覆使纳米颗粒获得炎症趋化因子受体(如CCR2),在ALI小鼠肝脏中实现特异性蓄积(24小时仍保持高强度信号),显著优于无包覆颗粒及其他细胞膜类型。
4.治疗-预防一体化:该系统不仅可治疗已发生的肝损伤,还具备预防性保护功能,扩大了临床干预窗口。
5.首次揭示“代谢-免疫”双轴调控机制:通过蛋白质组学分析,证实M2@SAM-F21通过调控巨噬细胞代谢重编程(抑制糖酵解HK2/PKM2、激活氧化磷酸化)逆转M1/M2极化失衡,恢复肝脏免疫微环境稳态。
1. 纳米平台构建与表征
MSN合成:溶胶-凝胶法,使用CTAT模板、TEOS和BTESePD(二硒键前体)共水解缩合,得到二硒键桥接介孔二氧化硅纳米颗粒(直径≈70 nm)。
氨基功能化(AMSN):通过APTES后接枝法,将zeta电位从-22.55 mV逆转至+43.47 mV。
药物装载:
水飞蓟素:DMF溶剂中室温搅拌24小时,装载效率31.57±1.91%。
pFGF21:4°C下AMSN与质粒按不同质量比(10:1~50:1)孵育30分钟。
M2巨噬细胞膜提取:IL-4/IL-13诱导RAW264.7细胞向M2极化,通过冻融、匀浆、差速离心获得膜囊泡。
膜包覆:将Sil-AMSN/pFGF21与M2膜以2:1质量比共挤出通过400 nm聚碳酸酯膜(20次),得到M2@SAM-F21。
表征手段:TEM、DLS、元素mapping、FT-IR、XPS、BCA蛋白定量。
2. 体外实验
细胞模型:
AML-12小鼠肝细胞(正常肝细胞)
RAW264.7小鼠巨噬细胞
氧化应激诱导:10 mmol/L APAP处理4小时;酒精性肝损伤模型:200 mmol/L乙醇处理24小时。
细胞活力:CCK-8法。
ROS检测:DCFH-DA探针,流式细胞术和荧光显微镜。
凋亡检测:Annexin V-FITC/PI双染,流式细胞术。
线粒体膜电位:JC-1染色。
活/死细胞染色:Calcein-AM/PI。
细胞因子检测:ELISA(TNF-α, IL-6, IL-10)。
巨噬细胞极化:免疫荧光(CD86为M1标志,CD206为M2标志)、流式细胞术、Western blot。
脂质积累检测:Oil Red O、Nile Red、BODIPY 493/503染色。
Western blot:检测FGF21、Nrf2、HO-1、SOD2、CD36、ACOX1、HK2、PKM2等。
qRT-PCR:验证相关基因mRNA表达。
3. 体内实验
动物模型:
APAP诱导急性肝损伤(ALI):C57BL/6J小鼠腹腔注射300 mg/kg APAP。
酒精性肝损伤(EtOH-ALI):Lieber-DeCarli液体饮食法(5%乙醇液体饲料10天,终末50%乙醇灌胃5 g/kg)。
治疗方案:
APAP-ALI:造模后2小时内静脉注射5 mg/kg纳米颗粒,24小时后处死。
EtOH-ALI:灌胃后8小时开始每日静脉注射,连续7天,末次注射后9小时处死。
血清生化:ALT、AST、TC、TG(全自动生化分析仪)。
氧化应激指标:MDA、T-SOD、GSH(试剂盒)。
组织病理:H&E染色、TUNEL凋亡检测、DHE超氧阴离子染色、Oil Red O脂质染色。
免疫组化/免疫荧光:F4/80/CD86(M1)、F4/80/CD206(M2)、Nrf2、HO-1。
生物分布:ICG标记的纳米颗粒,小动物活体成像。
生物安全性:血常规、肝肾功能、组织病理、溶血实验。
蛋白质组学:对照组、ALI模型组、M2@SAM-F21治疗组肝脏样本,LC-MS/MS分析,GO/KEGG/PPI网络分析。
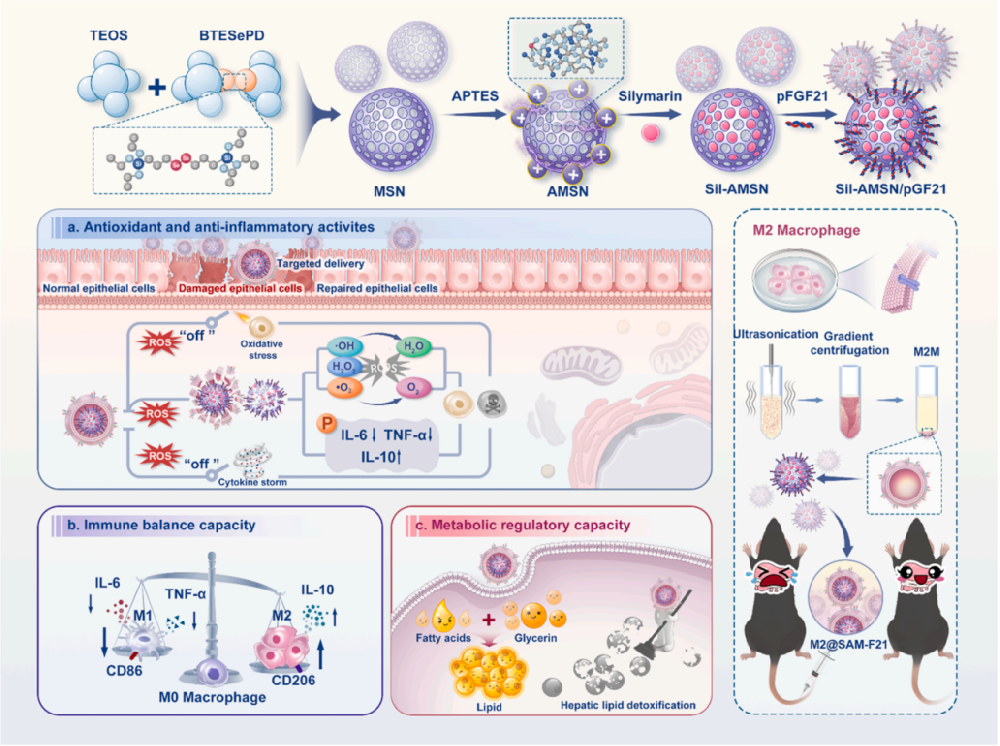
方案:M2@SAM-F21纳米治疗平台示意图。该纳米治疗平台由二硒化物桥联介孔二氧化硅核心构成,核心内共载有水飞蓟素与FGF21质粒,并外覆M2巨噬细胞膜涂层,实现炎症靶向递送与免疫逃逸功能。该集成系统通过三重协同机制发挥作用:(a) 抗氧化与抗炎活性,(b) 免疫平衡调节能力,(c) 代谢调控功能。这些协同作用共同实现了对急性肝损伤(ALI)中氧化应激风暴、炎症级联反应及脂质代谢紊乱的协同抑制。
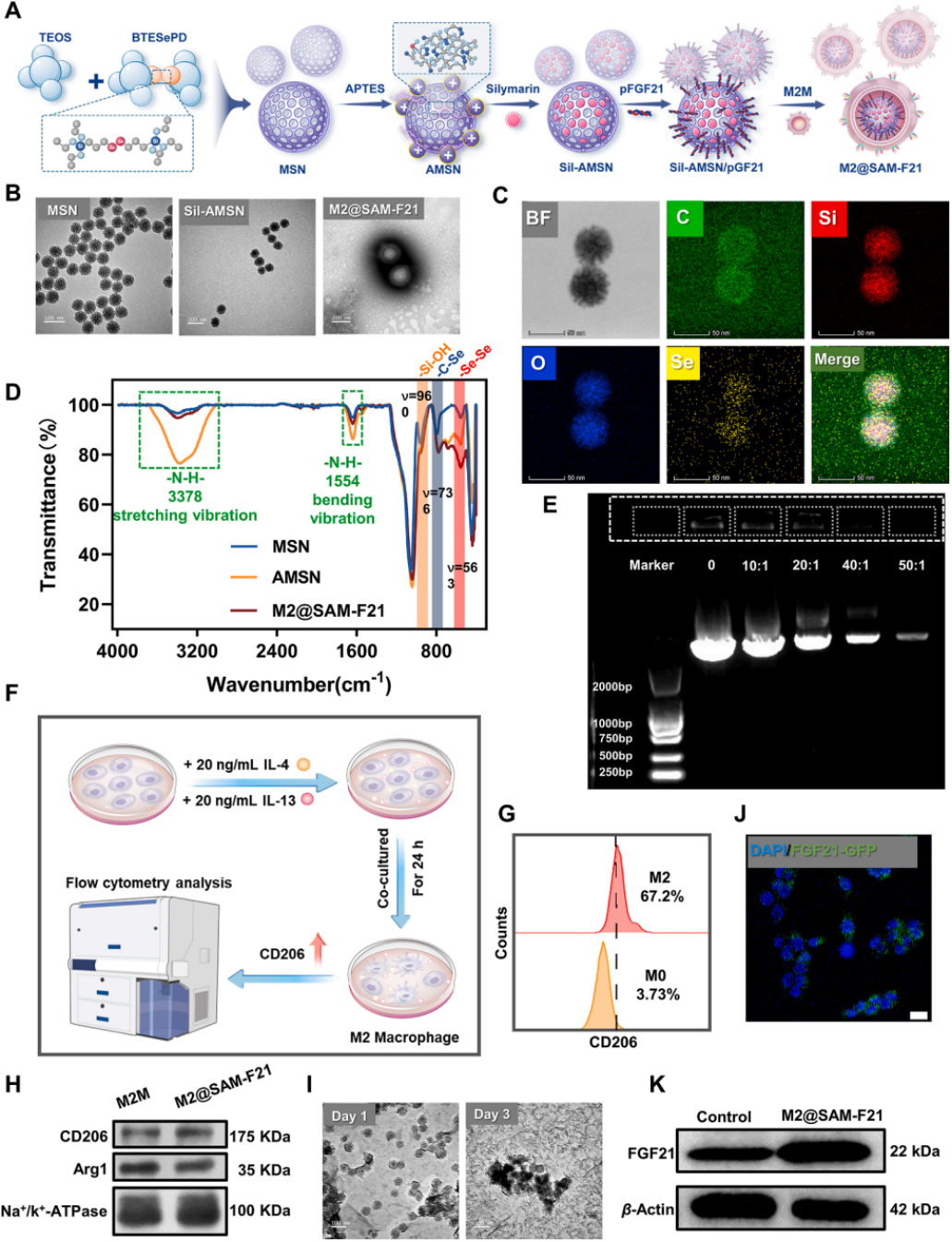
图1 | M2@SAM-F21的合成与表征
(A)M2@SAM-F21纳米颗粒制备流程示意图。
(B)MSN、Sil-AMSN和M2@SAM-F21的透射电镜(TEM)图像。
(C)元素mapping图;BF为明场,C、Si、O、Se分别表示不同元素的荧光信号,Merge为叠加图像。比例尺:50 nm。
(D)MSN、AMSN和M2@SAM-F21的傅里叶变换红外光谱(FT-IR)。
(E)AMSN与pFGF21(10 μg)按质量比0、10:1、20:1、40:1、50:1(μg/μg)形成复合物后,0.7%琼脂糖凝胶电泳图。上样孔从左至右为:分子量标记、0 μg(对照)、100、200、400、500 μg AMSN。
(F)M2巨噬细胞极化示意图。
(G)流式细胞术分析巨噬细胞从M0向M2表型的极化。
(H)M2巨噬细胞膜组和M2@SAM-F21组中M2膜标志物的Western blot分析。Na⁺/K⁺-ATPase作为上样对照。
(I)MSN在100 μmol/L H₂O₂条件下第1天和第3天的TEM图像。比例尺:100 nm。
(J)经或未经M2@SAM-F21处理的细胞免疫荧光图像。蓝色荧光(DAPI)为细胞核,绿色荧光(GFP标签)表示FGF21的表达。比例尺:20 μm。
(K)对照组和M2@SAM-F21处理组中FGF21和β-actin表达水平的Western blot分析。β-Actin作为上样对照。
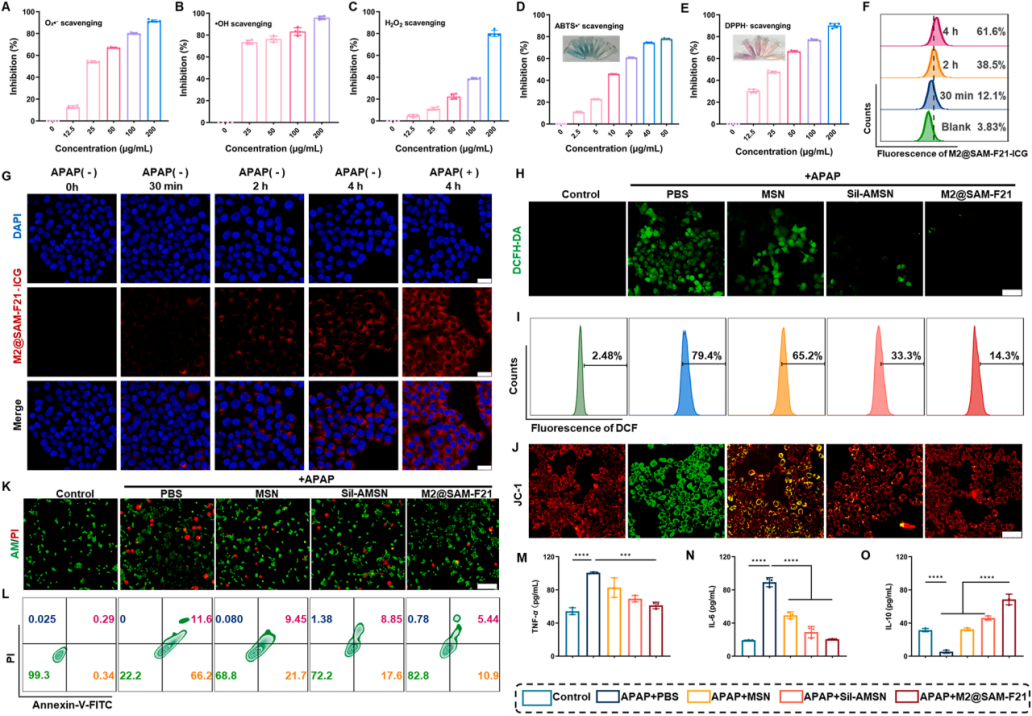
图2 | M2@SAM-F21的体外ROS清除和抗炎活性
(A-E)M2@SAM-F21对超氧阴离子(A)、羟基自由基(B)、过氧化氢(C)、ABTS⁺(D)和DPPH·(E)的清除能力。数据以均值±SD表示,来自四次(B、C)或五次(A、D、E)独立重复。
(F)流式细胞术分析不同时间点AML-12细胞中M2@SAM-F21-ICG的荧光强度。
(G)M2@SAM-F21-ICG处理后不同时间点AML-12细胞的共聚焦显微镜图像。蓝色荧光(DAPI)为细胞核,红色荧光为M2@SAM-F21-ICG。比例尺:20 μm。
(H)不同处理条件下AML-12细胞ROS染色的代表性荧光图像。绿色荧光表示细胞内ROS水平(DCFH-DA染色)。比例尺:50 μm。
(I)流式细胞术分析AML-12细胞内ROS水平。
(J)JC-1探针评估的AML-12细胞线粒体膜电位(MMP)代表性荧光图像。比例尺:50 μm。
(K)不同处理条件下AML-12细胞活性的代表性荧光图像。绿色荧光表示活细胞(Calcein-AM),红色荧光表示死细胞(PI)。比例尺:200 μm。
(L)流式细胞术显示的AML-12细胞凋亡和坏死分布。
(M-O)AML-12细胞中炎性细胞因子浓度的测定,包括TNF-α(M)、IL-6(N)和IL-10(O)。均值±SD(n=5),*P<0.001,**P<0.0001,单因素方差分析。
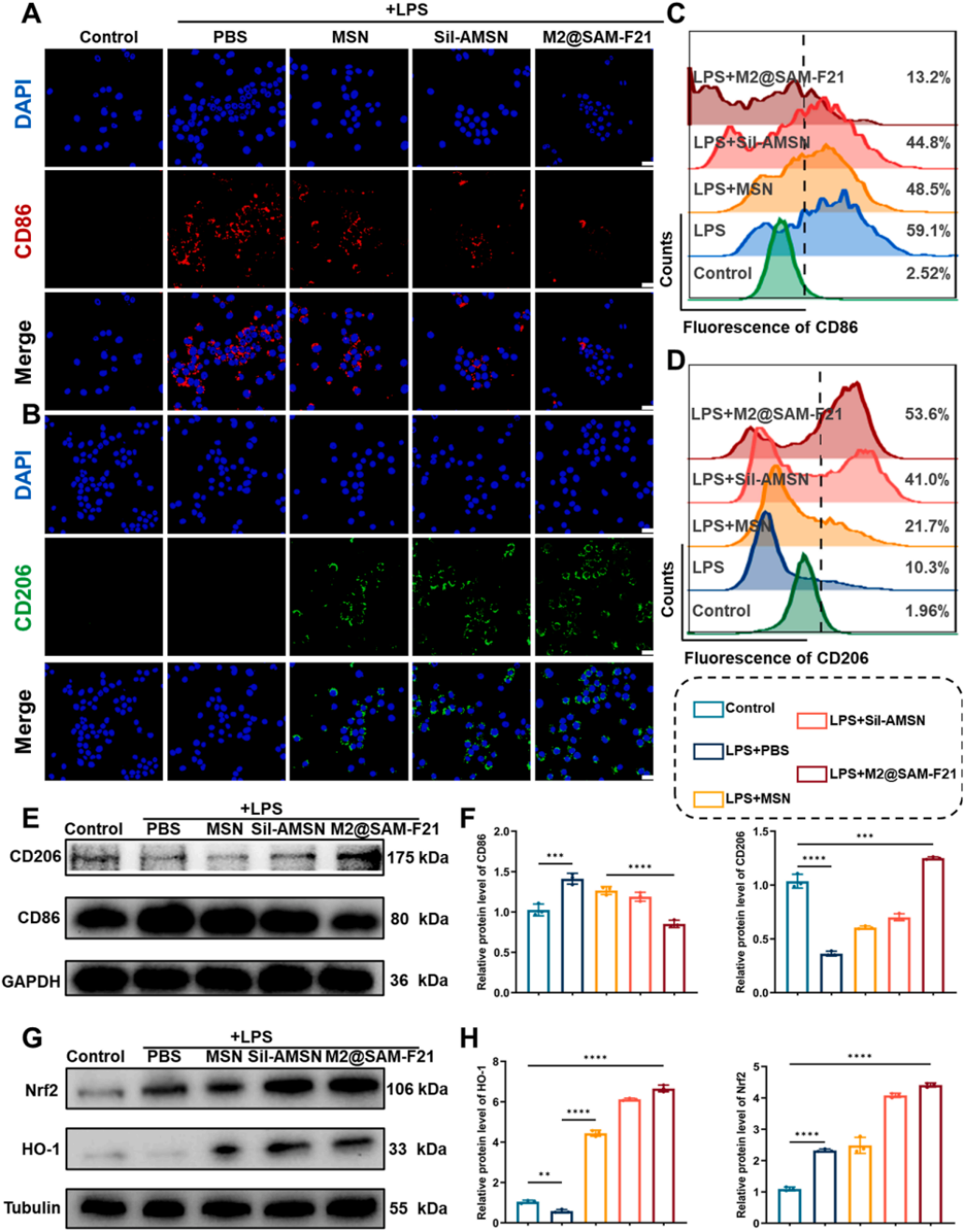
图3 | M2@SAM-F21的免疫平衡能力
(A)LPS刺激的RAW264.7巨噬细胞免疫荧光分析;细胞核用DAPI染色(蓝色),M1极化标志物CD86为红色。比例尺:20 μm。
(B)LPS刺激的RAW264.7巨噬细胞免疫荧光分析;细胞核用DAPI染色(蓝色),M2极化标志物CD206为绿色。比例尺:20 μm。
(C)流式细胞术分析RAW264.7细胞内CD86水平。
(D)流式细胞术分析RAW264.7细胞内CD206水平。
(E)不同组中CD206和CD86水平的Western blot分析。
(F)CD86(左)和CD206(右)相对蛋白水平的定量分析。
(G)不同组中Nrf2和HO-1表达水平的Western blot分析。
(H)Nrf2(左)和HO-1(右)相对蛋白水平的定量分析。均值±SD(n=3),P<0.01,P<0.001,***P<0.0001,ns表示无显著性,单因素方差分析。
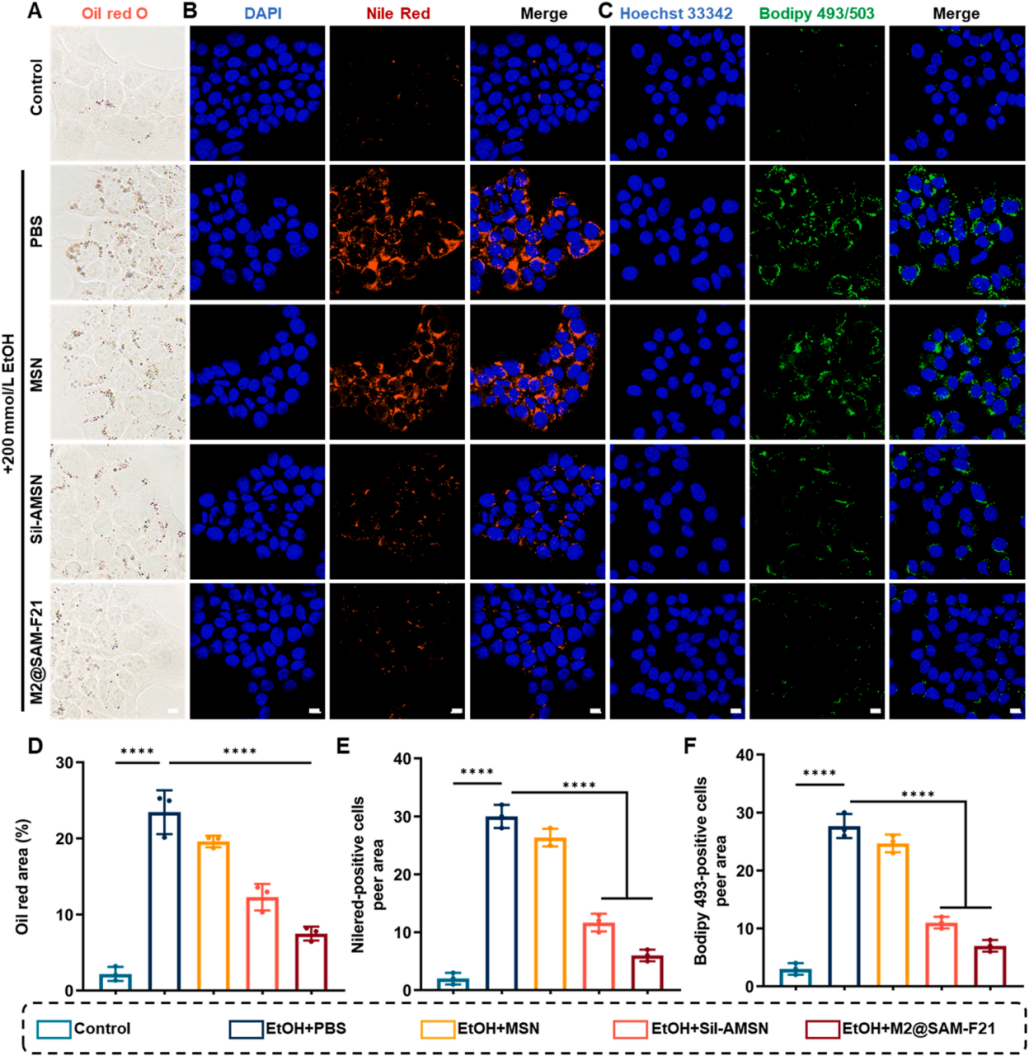
图4 | M2@SAM-F21的代谢调节能力。
(A)不同药物联合200 mmol/L EtOH处理后细胞的油红O染色图像。图像显示细胞内脂质积累。比例尺:100 μm。
(B)200 mmol/L EtOH刺激细胞的免疫荧光图像,DAPI(蓝色,细胞核)和Nile Red(红色,脂滴)染色。比例尺:10 μm。
(C)200 mmol/L EtOH刺激细胞的免疫荧光图像,Hoechst 33342(蓝色,细胞核)和BODIPY 493/503(绿色,脂滴)染色。比例尺:10 μm。
(D-F)各组中油红O染色面积(D)、Nile Red阳性细胞(E)和BODIPY 493阳性细胞(F)的相对面积统计图。均值±SD(n=3),****P<0.0001,单因素方差分析。
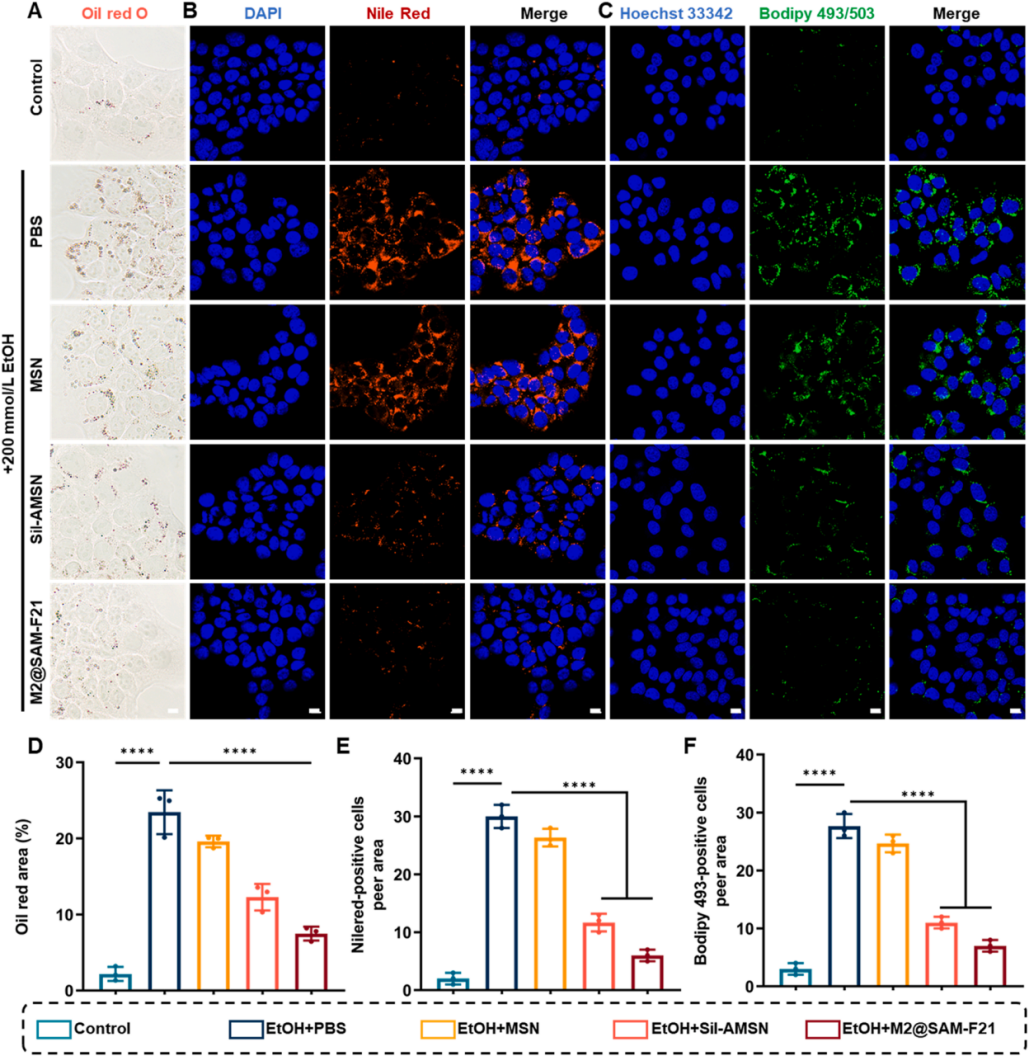
图5 | M2@SAM-F21的体内生物安全性与靶向性评估
(A)静脉注射后第14天,M2@SAM-F21对主要器官(心脏、肝脏、脾脏、肺和肾脏)的体内毒性评估。比例尺:50 μm。
(B、C)正常小鼠(对照组)和静脉注射M2@SAM-F21后第1天(B)和第14天(C)小鼠的肝功能指标(ALT、AST)和肾功能参数(CRE、BUN)血清水平。均值±SD,n=5。
(D)尾静脉注射ICG、Sil-AMSN-ICG或M2@SAM-F21-ICG后不同时间点(30分钟、2小时、6小时、12小时和24小时)小鼠的体内荧光成像。显示肝脏区域的荧光强度。
(E)主要器官(H:心脏,Li:肝脏,S:脾脏,Lu:肺,K:肾脏,B:肠道)离体荧光成像的代表性图像。
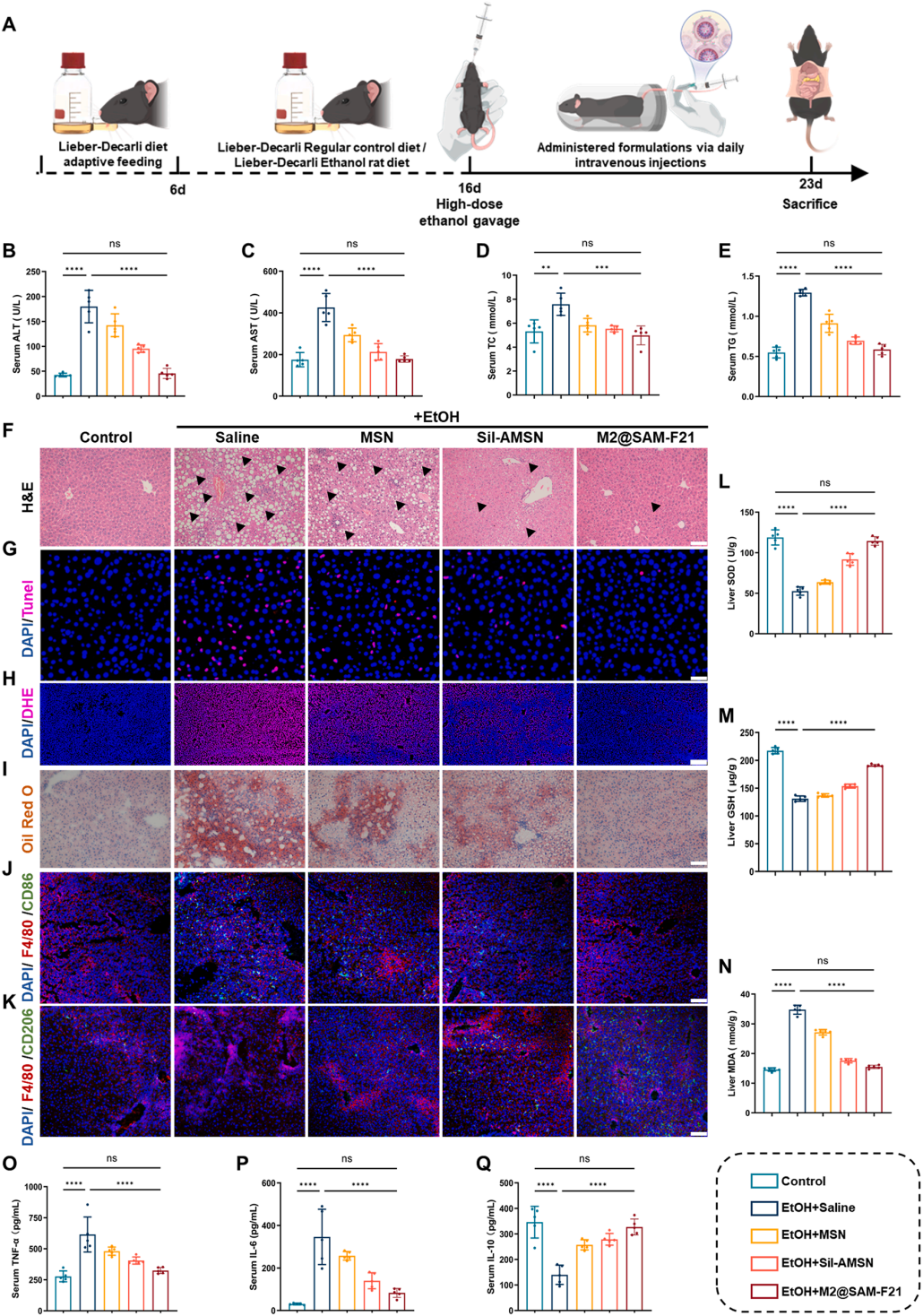
图6 | M2@SAM-F21对酒精性肝损伤(EtOH-ALI)的体内治疗效果
(A)Lieber-DeCarli饮食诱导的酒精性肝损伤小鼠模型实验时间线示意图。时间线分为四个阶段:适应性喂养、对照/乙醇饮食、正常饮食与治疗、处死。
(B-E)实验期间各组小鼠血清ALT(B)、AST(C)、TC(D)和TG(E)水平。
(F-K)各组小鼠肝脏组织代表性H&E染色(F)、TUNEL检测(G)、DHE染色(H)、油红O染色(I)以及免疫荧光染色(F4/80/CD86(J)和F4/80/CD206(K))图像。细胞核用DAPI染色(蓝色),巨噬细胞标志物(F4/80,绿色)与CD86(红色)或CD206(红色)共染。
(L-N)各组小鼠肝脏组织中MDA(L)、SOD(M)和GSH(N)水平。
(O-Q)各组小鼠血清中TNF-α(O)、IL-6(P)和IL-10(Q)水平。均值±SD(n=5),P<0.05,P<0.01,P<0.001,****P<0.0001,单因素方差分析。
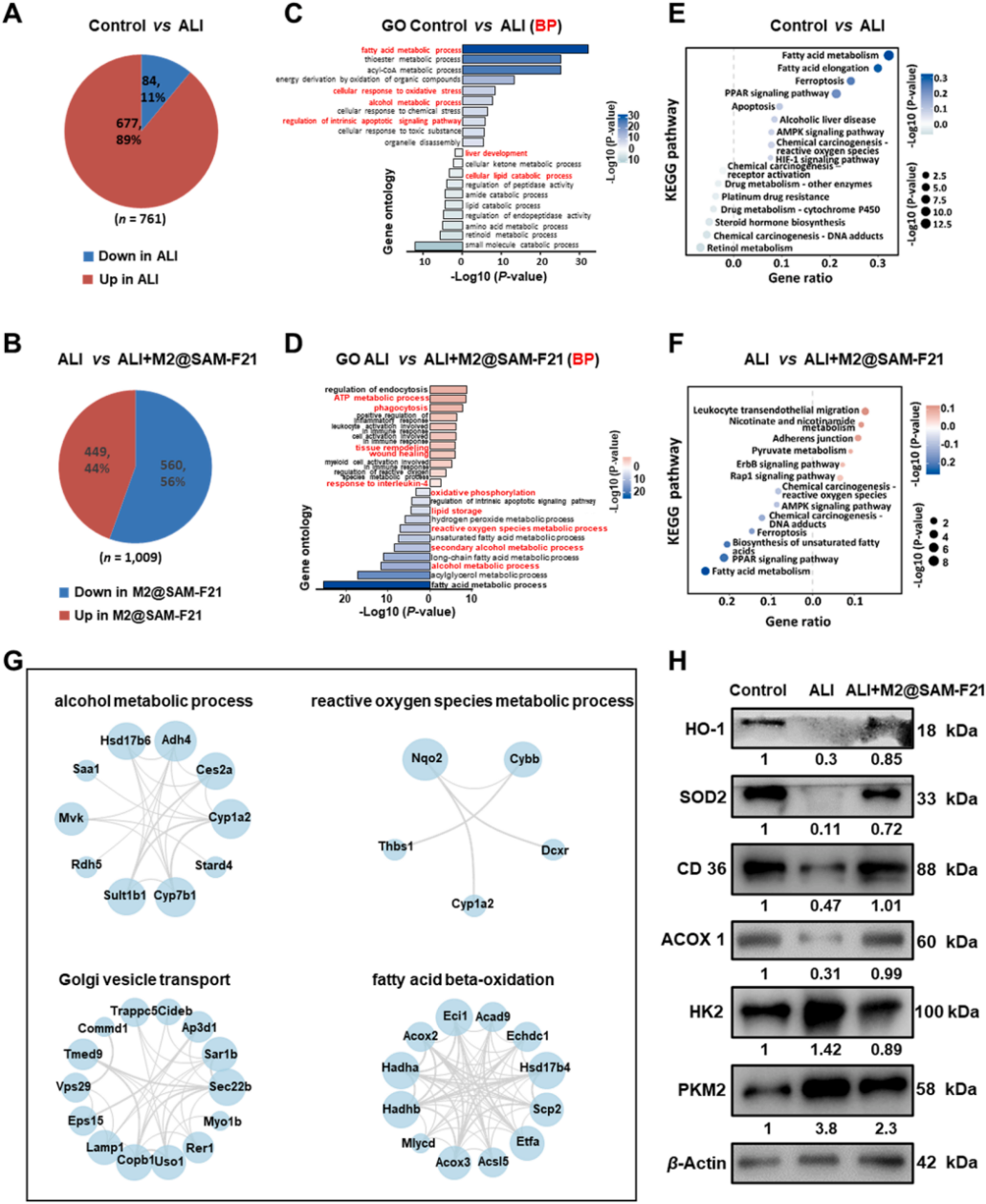
图7 | 基于蛋白质组学的M2@SAM-F21治疗机制研究
(A)ALI组差异表达蛋白分布的饼图。
(B)M2@SAM-F21治疗后差异表达蛋白分布的饼图。
(C)对照组-ALI组比较中上调和下调蛋白的GO-BP分析。
(D)ALI组-M2@SAM-F21组比较中上调和下调蛋白的GO-BP分析。
(E)对照组-ALI组比较中差异表达蛋白的KEGG通路分析。
(F)ALI组-M2@SAM-F21组比较中差异表达蛋白的KEGG通路分析。
(G)对照组、ALI组和M2@SAM-F21治疗组中差异表达基因的蛋白质-蛋白质相互作用(PPI)网络分析。节点代表蛋白质,边代表相互作用。网络聚焦于酒精代谢、活性氧代谢和脂肪酸β-氧化等过程。
(H)不同组中HO-1、SOD2、CD36、ACOX1、HK2、PKM2和β-actin表达水平的Western blot分析。β-Actin作为上样对照。右侧标示蛋白质分子量。
1.成功构建仿生纳米平台:M2@SAM-F21具有均匀粒径(~70 nm)、高药物装载效率(水飞蓟素31.6%)、ROS/pH双响应释放特性(48小时ROS组释放92%),以及M2膜介导的炎症主动靶向能力。
2.体外多维度保护效应:
高效清除多种ROS(O₂⁻、·OH、H₂O₂、ABTS⁺、DPPH·),恢复线粒体膜电位,显著降低APAP诱导的肝细胞凋亡(Annexin V/PI)。
抑制TNF-α和IL-6,升高IL-10,发挥抗炎作用。
诱导巨噬细胞从M1向M2表型极化(CD86↓,CD206↑),激活Nrf2/HO-1抗氧化通路。
在酒精性肝细胞模型中显著减少脂滴积累(油红O、Nile Red、BODIPY验证)。
3.体内卓越治疗效果:
在EtOH-ALI和APAP-ALI两种模型中,M2@SAM-F21显著降低血清ALT、AST、TC、TG水平,恢复至接近正常范围。
组织病理显示肝细胞空泡化、脂肪变性和凋亡(TUNEL)显著减轻,超氧阴离子(DHE)水平下降。
恢复肝脏GSH和SOD活性,降低MDA含量。
逆转酒精诱导的M1/M2失衡(F4/80⁺CD86⁺ M1减少,F4/80⁺CD206⁺ M2增加)。
生物分布显示M2@SAM-F21在肝脏特异性蓄积长达24小时,优于游离ICG和无膜颗粒。
蛋白质组学揭示机制:M2@SAM-F21通过抑制脂肪酸代谢、ROS代谢、凋亡通路(PPAR信号、铁死亡、HIF-1信号),同时激活免疫相关通路(白细胞跨内皮迁移、烟酸/烟酰胺代谢),并调控糖酵解关键酶(HK2、PKM2)的表达,实现“代谢-免疫”双轴重编程。
4.优异生物安全性:高剂量静脉注射后未见主要器官病理损伤,肝肾功能、血常规指标正常,溶血率<5%,符合ISO 10993-5标准。
文献意义:
本研究首次构建了一种集仿生主动靶向、ROS响应释放、基因-药物共递送于一体的M2巨噬细胞膜包覆二硒键桥接介孔二氧化硅纳米平台(M2@SAM-F21),用于急性肝损伤的精准治疗。该平台突破了传统水飞蓟素口服生物利用度低和FGF21半衰期短的瓶颈,实现了“外源性抗氧化-内源性免疫代谢调控”的双模式协同治疗。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:基于 NanoLuc 筛选鉴定鞣花酸为天然 GPR35 激动剂用于溃疡性结肠炎治疗
下一篇:人视网膜类器官模型揭示 MYCN 扩增视网膜母细胞瘤的发育易感窗口与治疗脆弱性