常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-14 09:00:00 细胞资源库平台 访问量:11
原代肝细胞是肝脏生理、病理及药物研发的核心工具,但传统分离依赖 1976 年 Seglen 建立的两步胶原酶灌注法,存在诸多痛点:门静脉插管技术要求高、胶原酶批次差异导致重复性差、在体灌注易污染、动物伦理审批严格。
德国米尔滕尼生物公司与亚琛工业大学合作团队在《Biomedicines》上发表题为Isolation of Hepatocytes from Liver Tissue by a Novel, Semi-Automated Perfusion Technology的研究,开发 gentleMACS 半自动灌注系统:以切除的肝叶为原料,无需插管,通过标准化酶解和机械解离,实现肝细胞快速、高纯度、高活力分离,符合动物实验 3R 原则(替代、减少、优化),解决传统方法的核心缺陷。
1. 核心实验材料
动物模型:不同品系小鼠(CD1、BALB/c、C57BL/6),5-12 周龄,雌雄均有。
关键试剂:Liver Perfusion Kit(含酶 D/R/A、缓冲液 P 等标准化试剂)、肝细胞培养基(含 10% FBS、谷氨酰胺、青链霉素)。
核心设备:gentleMACS Octo Dissociator 加热版、gentleMACS Perfuser(灌注装置,含 Lid/Clamp/Grid/Base 组件)、gentleMACS C 管(解离用)、MACS SmartStrainer(100μm,过滤)。
检测工具:流式细胞仪、荧光显微镜、Western blot 系统、RT-PCR 仪、台盼蓝染色试剂盒。
2. 关键实验技术(半自动分离流程)
(1)装置与试剂准备
灌注装置组装:将 Perfusion Sleeves 安装到加热版解离仪,Perfuser Base-Lid 固定到仪器,预热至 37℃。
试剂配制:用试剂盒制备预消化缓冲液(无钙)、平衡缓冲液、酶消化混合液(酶 D/R/A + 平衡缓冲液),均预热至 37℃。
(2)肝叶处理与固定
小鼠处死后,快速分离肝叶(优先左外侧叶),PBS 冲洗后置于 Perfuser 的 Grid 中央,用 Clamp 固定。
将 Grid - 肝叶 - Clamp 组件与 Lid 连接,拧紧固定到 Base,装置的 4 根针头自动刺入肝组织。
(3)自动化灌注与酶解
运行预设程序(37C_m_LIPK_1):依次完成预灌注(无钙缓冲液,洗去血液)、平衡灌注、酶消化灌注(10min),程序自动暂停以更换缓冲液 / 酶液。
灌注过程中,肝组织颜色从红色(含血)变为苍白(洗去血液),酶解后质地变软。
(4)肝细胞解离与纯化
酶解后,将肝叶转移至含酶消化液的 C 管,运行解离程序(LIPK_HR_1)5min,轻柔释放肝细胞。
细胞悬液经 100μm SmartStrainer 过滤,30×g 低温离心 5min,收集沉淀(肝细胞),弃上清(含非实质细胞)。
(5)鉴定与功能验证
纯度 / 活力:台盼蓝排斥法检测活力,流式细胞仪验证纯度;
表型鉴定:免疫荧光 / Western blot 检测肝细胞标志物(CK8、ZO-1、HNF4α);
功能验证:RT-PCR 检测白蛋白(Alb)、HNF4α mRNA 表达,Western blot 检测 LCN2 分泌,IL-1β 刺激实验验证细胞敏感性。
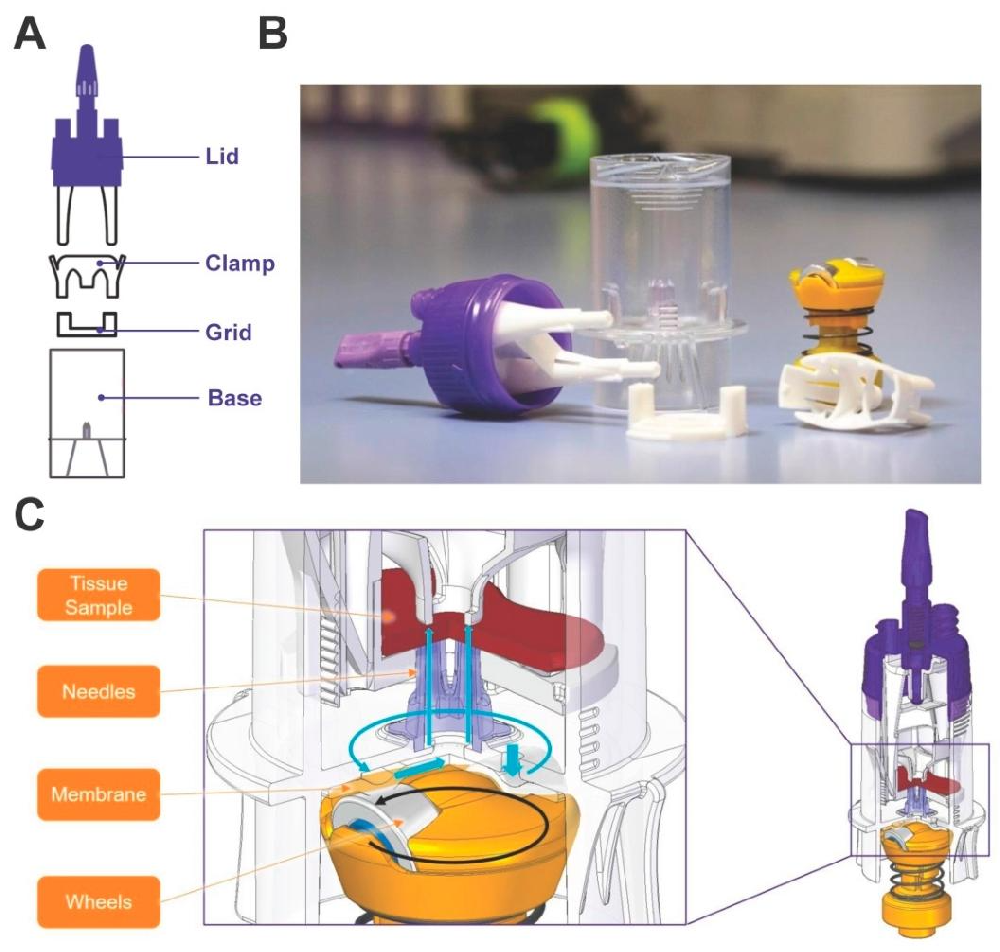
图1:gentleMACS 灌注装置结构
该图展示核心装置组成:(A-C)装置拆解为 Lid、Clamp、Grid、Base 四部分,Base 含内置蠕动泵和针头阵列,可精准输送液体;Lid 顶部的 Adjuster 可调节针头刺入深度,适配不同大小肝组织。结果表明,装置设计无需手动插管,简化操作流程。

图2:肝细胞分离完整操作流程
该图呈现分步操作:(A)装置组件;(B-C)肝叶固定到 Grid;(D-E)组件组装固定;(F)预设程序步骤;(G-H)手动更换缓冲液;(J-O)肝叶转移至 C 管解离;(P-Q)过滤离心获得肝细胞沉淀。结果显示,全程可在 3h 内完成,支持最多 8 个样本并行处理。
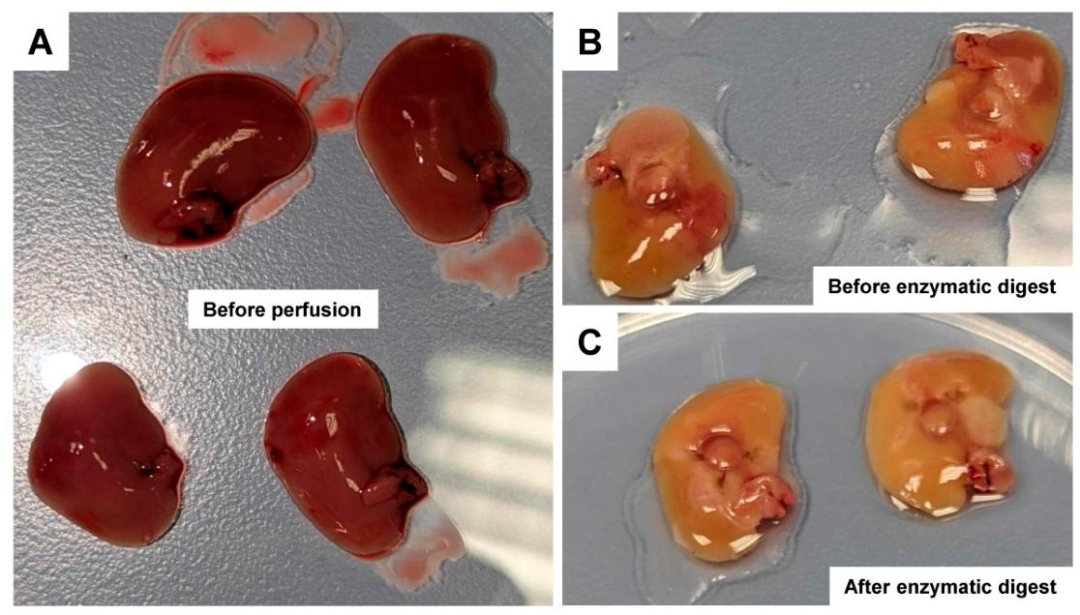
图3:肝组织灌注过程中的颜色变化
该图直观反映灌注效果:(A)灌注前肝叶呈红色(含血);(B)预灌注后变为苍白(血液洗净);(C)酶解后质地变软、颜色均匀。结果证实,灌注和酶解过程充分,组织解离完全。

图4:肝细胞形态学特征
该图显示培养后肝细胞形态:(2-24h)肝细胞贴壁生长,24h 后呈现典型的六边形扁平形态(100×/200×),符合原代肝细胞的形态学标志。结果表明,分离的肝细胞保留正常贴壁和形态分化能力。
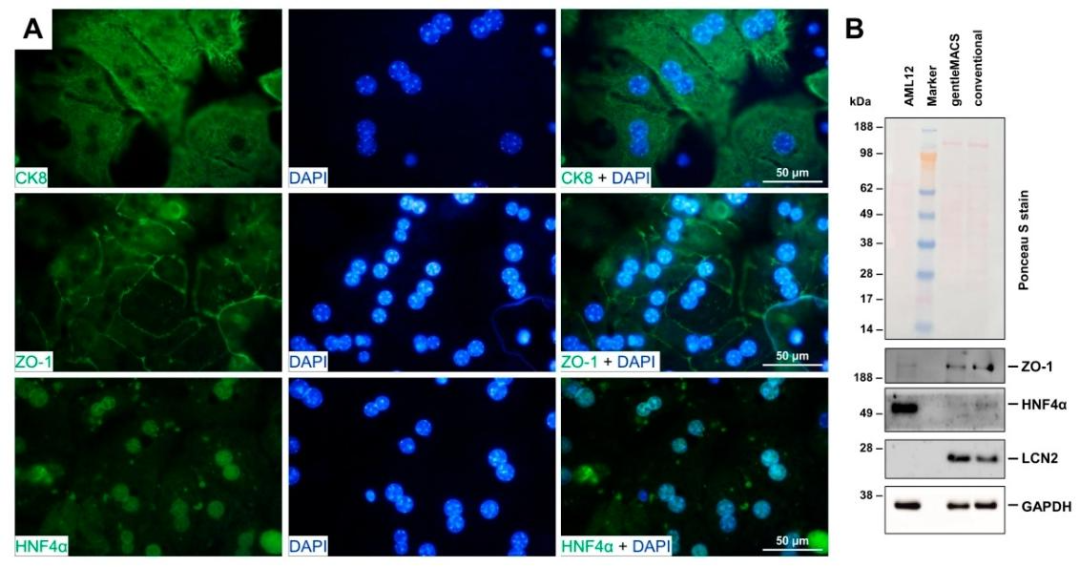
图5:肝细胞特异性标志物表达
该图验证表型纯度:(A)免疫荧光显示,肝细胞高表达 CK8(细胞骨架标志物)、ZO-1(紧密连接标志物)、HNF4α(肝细胞分化关键因子),DAPI 染色显示核形态正常;(B)Western blot 证实上述标志物在分离肝细胞中稳定表达,与阳性对照(AML12 肝细胞系)一致。结果确认,分离细胞为高纯度肝细胞。
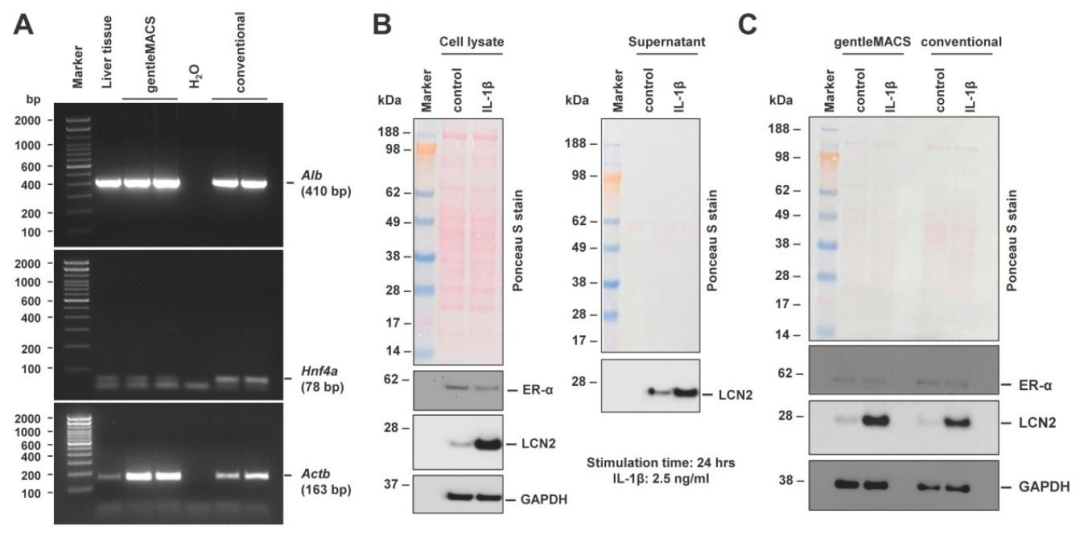
图6:肝细胞功能完整性验证
该图证明功能正常:(A)RT-PCR 显示,分离肝细胞与传统方法分离的肝细胞均高表达 Alb 和 HNF4α mRNA;(B)Western blot 显示,肝细胞可分泌 LCN2,且 IL-1β 刺激后分泌增加;(C)IL-1β 敏感性实验显示,分离肝细胞与传统方法分离的肝细胞对炎症刺激反应一致。结果证实,分离的肝细胞功能完整,可用于后续生理 / 病理研究。
本研究的核心创新是开发半自动灌注分离系统,解决传统方法的核心痛点:1)技术优势:无需门静脉插管,操作门槛低,标准化试剂和程序减少人为误差,一次性耗材降低污染风险;2)伦理与效率:使用切除的肝组织,无需在体灌注,符合 3R 原则,无需复杂伦理审批,支持 8 个样本并行,提升实验效率;3)性能优势:肝细胞产量、纯度、活力稳定,表型和功能与传统方法一致,适配不同品系 / 年龄小鼠,可扩展至人类肝组织和疾病模型(如脂肪肝);4)应用价值:适用于药物代谢、肝疾病机制、类器官构建等研究,为原代肝细胞分离提供标准化解决方案。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:肝癌小鼠中髓系来源抑制细胞(MDSC)对库普弗细胞表型与功能的调控