常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-14 17:00:00 细胞资源库平台 访问量:11
枯否细胞(KC)作为肝脏主要驻留巨噬细胞,在肝稳态维持及炎症反应中发挥核心作用,高纯度原代 KC 培养是其功能机制研究的关键。传统 KC 分离方法(如单一密度梯度离心或离心淘洗)存在明显缺陷:肝非实质细胞(KC、肝窦内皮细胞 SEC、星形细胞 SC)的密度与大小高度重叠,难以有效分离,导致 KC 纯度不足 80%。
希腊克里特大学医学院的团队在《Cell Biology International》发表联合优化方案:整合 “酶解灌注 + 密度梯度离心 + 离心淘洗 + 选择性贴壁” 四步技术,实现单只大鼠肝脏 KC 产量达 80-100×10⁶个,纯度 > 95%(ED-2 阳性)、活力 > 98%,且功能完整,为 KC 体外研究提供高效标准化技术支撑。
1. 肝窦细胞分离(酶解灌注 + 密度梯度离心)
原位 / 体外双阶段酶解:大鼠戊巴比妥(50mg/kg)腹腔麻醉,门静脉插管,先以无钙镁 HBSS(10ml/min,37℃)灌注 200ml 洗去血液;肝脏离体后,依次用 0.2% 链霉蛋白酶(60ml)、0.01% 胶原酶(225ml)体外灌注消化,随后组织剪碎,加入含 0.03% 链霉蛋白酶和 0.01% DNase 的 HBSS,37℃振荡孵育 30min,125μm 尼龙网过滤获得单细胞悬液。
Iodixanol 密度梯度离心:细胞悬液与 29.4% Iodixanol 混合制成 11.7% 梯度液,叠加于 17.6% Iodixanol 梯度层上,1400×g、4℃离心 17min(无刹车);收集梯度顶层(含非实质细胞)与界面层(含少量 KC 与肝细胞),HBSS 洗涤后重悬,经 20G 针头分散细胞团块。
2. KC 纯化(离心淘洗 + 选择性贴壁)
(1)离心淘洗
采用 J2-MC 离心机(JE-6B 转子),25℃、2500rpm 条件下,以 HBSS 为洗脱液,18.5ml/min 流速加载细胞悬液;逐步提升流速至 25、35、45、60、80、100ml/min,每流速收集 100ml 组分,其中 45-60ml/min 组分富含 KC(ED-2 阳性率 60%-95%)。
(2)选择性贴壁
收集 45-60ml/min 淘洗组分,400×g、4℃离心 7min,沉淀重悬于含 10% 胎牛血清的 DMEM 培养基,以 1-3×10⁶个 / 孔接种至 6 孔板,37℃、5% CO₂孵育 2h,洗涤去除未贴壁细胞,剩余贴壁细胞即为高纯度 KC。
3. KC 鉴定与功能验证
纯度与活力鉴定:ED-2 单克隆抗体免疫细胞化学染色(KC 特异性标志物)、非特异性酯酶组织化学染色;台盼蓝拒染法检测活力。
功能验证:KC 接种后培养 24h,加入不同浓度脂多糖(LPS,0.1-10μg/ml),分别培养 24h 和 48h,ELISA 检测上清 TNF-α 水平,Griess 法检测一氧化氮(NO)产量(NOₓ浓度)。
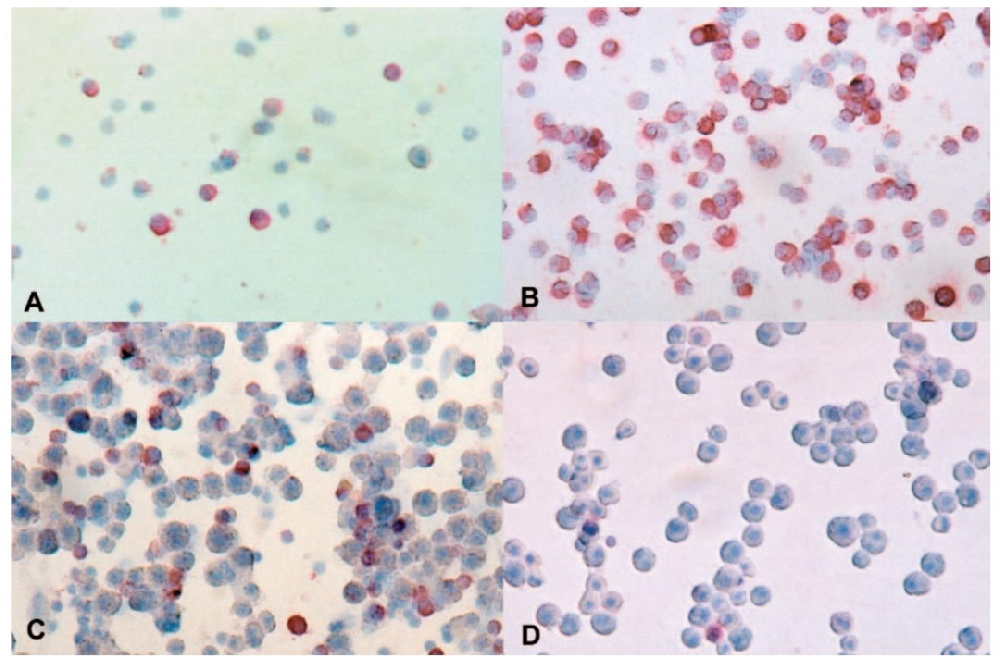
图1:ED-2 免疫细胞化学染色鉴定 KC 分布
A 图为密度梯度离心前细胞悬液(ED-2 阳性 KC 占 30-35%);B 图为 11.7% 梯度顶层细胞(ED-2 阳性率 40-60%);C 图为梯度界面层细胞(ED-2 阳性率仅 15-20%,以肝细胞为主);D 图为离心淘洗后丢弃的肝细胞(无 ED-2 阳性细胞)。
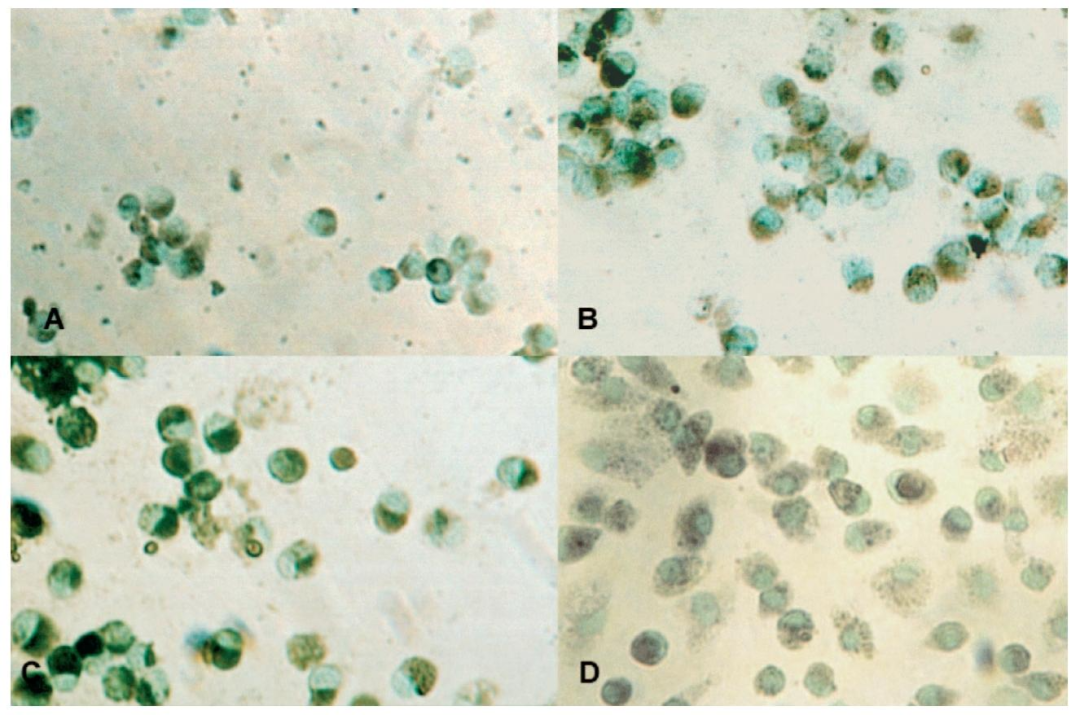
图2:非特异性酯酶组织化学染色
A-C 图为淘洗组分 II、III、IV 的细胞,>95% 细胞呈酯酶阳性;D 图为培养后 KC,>95% 保持酯酶阳性(400×),证实酯酶活性广泛存在于肝非实质细胞,无法单独作为 KC 特异性标志。
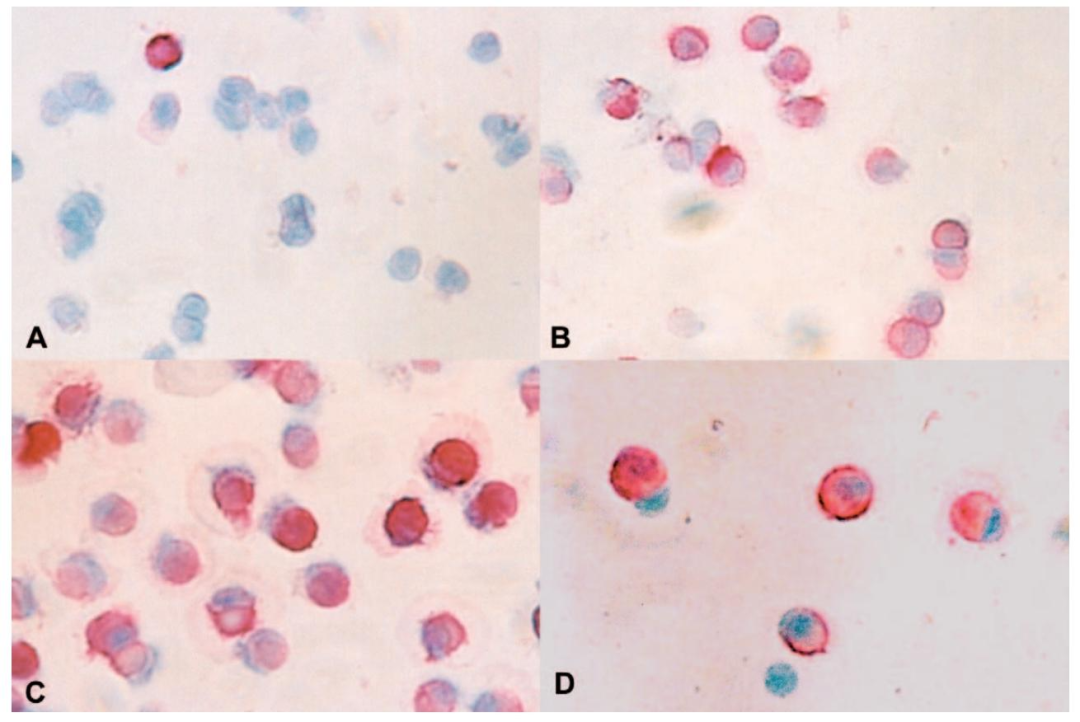
图3:不同淘洗组分的 ED-2 免疫染色
A 图为组分 II(35ml/min,ED-2 阳性率 < 10%);B-C 图为组分 III(45ml/min,阳性率 60-70%)、组分 IV(60ml/min,阳性率 90-95%);D 图为组分 V(80ml/min,含大量肝细胞,KC 占比下降)。
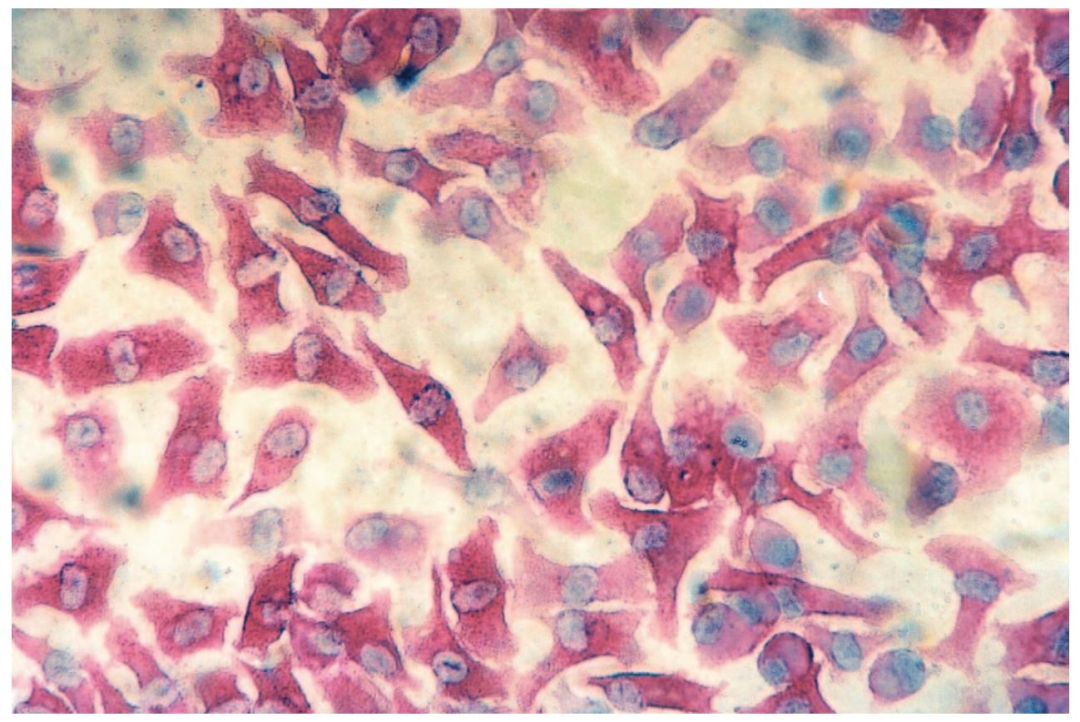
图4:培养后 KC 的 ED-2 免疫染色
400× 显微镜下,>95% 培养细胞呈 ED-2 阳性,细胞贴壁伸展,形态不规则,符合成熟 KC 的典型特征。
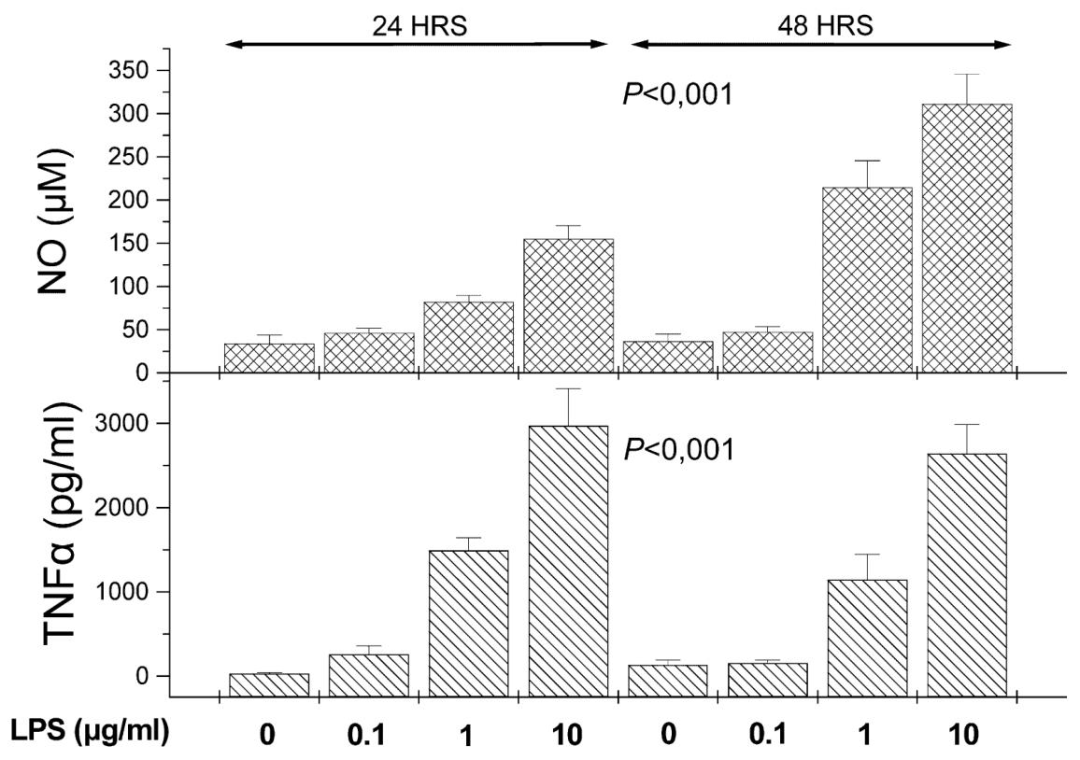
图5:LPS 诱导 KC 分泌 TNF-α 和 NO 的功能验证
柱状图显示,KC 分泌 TNF-α 和 NO 呈 LPS 浓度依赖性(P<0.01);NO 分泌随培养时间延长(24h→48h)显著增加,而 TNF-α 在 24h 达峰值后不再升高,提示存在反馈调控机制。
希腊克里特大学团队建立的四步联合方法,通过 “酶解灌注 - 密度梯度离心 - 离心淘洗 - 选择性贴壁” 协同优化,实现大鼠 KC 高效分离:单只肝脏产量达 80-100×10⁶个,纯度 > 95%(ED-2 阳性)、活力 > 98%,且功能完整(LPS 诱导下可分泌 TNF-α 和 NO)。该方案核心创新在于整合细胞密度、大小及贴壁特性多维度分离机制,解决传统单一方法杂细胞污染问题;局限性在于操作步骤繁琐、依赖离心淘洗专用设备,且大鼠年龄差异可能影响酶解效率。整体为 KC 相关肝炎症、免疫调控研究提供高可靠性细胞模型,具有重要方法论价值。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:头颈癌放疗新策略:稳健 VMAT 计划保障靶区覆盖并降低 NTCP