常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-13 09:00:00 细胞资源库平台 访问量:19
梅毒由梅毒螺旋体(Treponema pallidum subsp. pallidum)引起,是全球紧迫的公共卫生问题,每年新增 800 万例感染,先天性梅毒可导致 66.1 万不良出生结局。梅毒螺旋体具有强侵袭性,可通过血液扩散并穿透内皮屏障(如血脑屏障、胎盘屏障),但其与内皮细胞相互作用的分子机制尚未明确。血管内皮细胞是梅毒螺旋体附着、扩散及启动宿主免疫反应的关键靶点,此前研究仅聚焦单一通路,缺乏全局动态分子响应分析。
为此,加拿大维多利亚大学的团队在《Frontiers in Microbiology》上发表题为Time-course transcriptomics reveals the impact of Treponema pallidum on microvascular endothelial cell function and phenotype的研究,通过时间序列转录组学(0.75h、4h、12h、24h)分析梅毒螺旋体暴露的脑微血管内皮细胞(HBMECs),首次发现梅毒螺旋体可诱导内皮间质转化(EndMT)—— 一种与血管功能异常相关的细胞表型转化,同时揭示 ECM、TGFβ、Rho GTPase 等关键通路的动态调控,为梅毒发病机制及疫苗研发提供新依据。
梅毒螺旋体与细胞培养:新西兰白兔体内培养梅毒螺旋体 Nichols 株(验证运动性),体外用 Sf1Ep 细胞辅助培养;永生化脑微血管内皮细胞(hCMEC/d3,即 HBMECs)用 EndoGRO-MV 培养基培养至 90% 汇合,在微需氧环境(1.5% O₂、5% CO₂)中与活梅毒螺旋体(VTP 组)或去螺旋体的感染提取物(IEC 对照组)共培养,设置 0.75h、4h、12h、24h 四个时间点,每组 5 个生物学重复。
转录组与数据分析:用 Qiagen 试剂盒提取 HBMECs 总 RNA(RIN≥8),经 PolyA 富集后构建链特异性 cDNA 文库,Illumina HiSeqX 进行 150bp 双端测序;用 STAR 比对人类基因组(hg19),DESeq2 筛选差异基因(|FC|≥1.5、adj p≤0.05),通过 Reactome、MSigDB 数据库进行通路富集分析,Chea3 工具预测核心转录因子,maSigPro 分析基因表达时序变化。
分子与细胞验证:Western blot 检测 EndMT 关键转录因子 Snail 的蛋白表达(抗 Snail 抗体,GAPDH 内参);F-actin 荧光染色(Alexa Fluor 488 鬼笔环肽)结合高内涵成像,观察 HBMECs 形态变化(收缩、皮质肌动蛋白环形成);ELISA 检测细胞因子(如 IFN-γ)分泌,验证免疫通路调控。
ECM 与信号通路分析:通过 qPCR 验证 ECM 成分(胶原、纤连蛋白)、TGFβ 信号分子(SMAD3、SMAD7)及 Rho GTPase 家族成员(RHOB、RND1)的表达变化,结合通路网络分析(Jaccard 距离 < 0.85)揭示通路间关联。
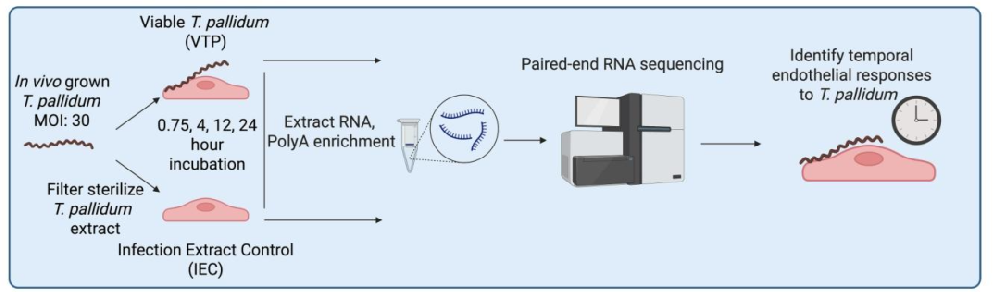
图1:RNA 测序实验流程
图示梅毒螺旋体与 HBMECs 共培养的样本制备流程:活梅毒螺旋体(VTP)或 IEC 处理 HBMECs 后,提取 RNA 进行双端测序,通过时序分析解析内皮细胞转录响应。该流程确保排除兔睾丸提取物背景干扰,聚焦梅毒螺旋体的特异性作用。
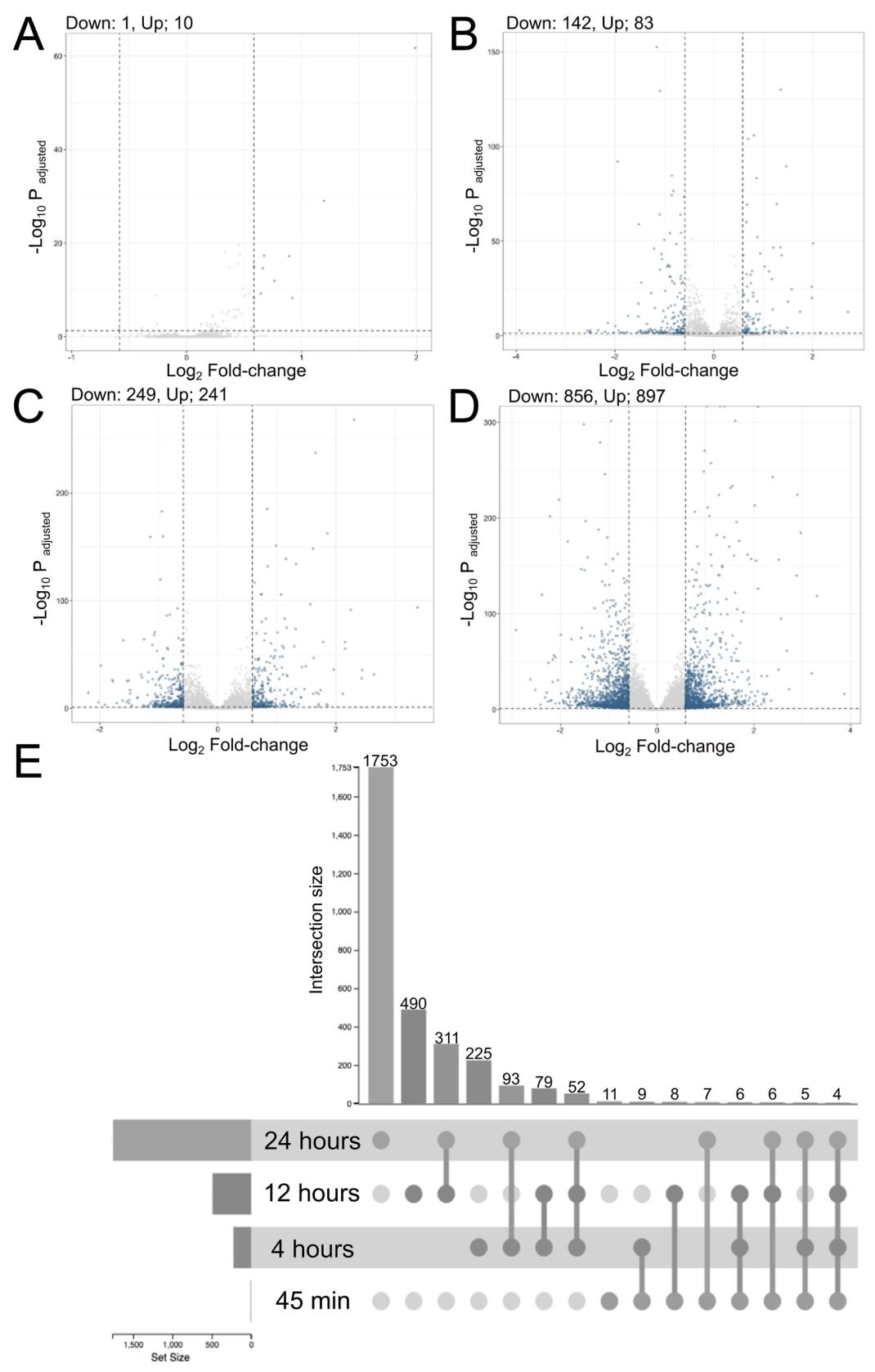
图2:差异基因(DEGs)随时间的动态变化
梅毒螺旋体暴露后,DEGs 数量随时间显著增加:0.75h 仅 11 个、4h 225 个、12h 490 个、24h 1753 个;311 个 DEGs 在 12h 和 24h 重叠,4 个 DEGs(如 SNAI1)在所有时间点均差异表达,提示内皮细胞响应呈 “渐进式激活”,晚期(24h)转录重编程最显著。
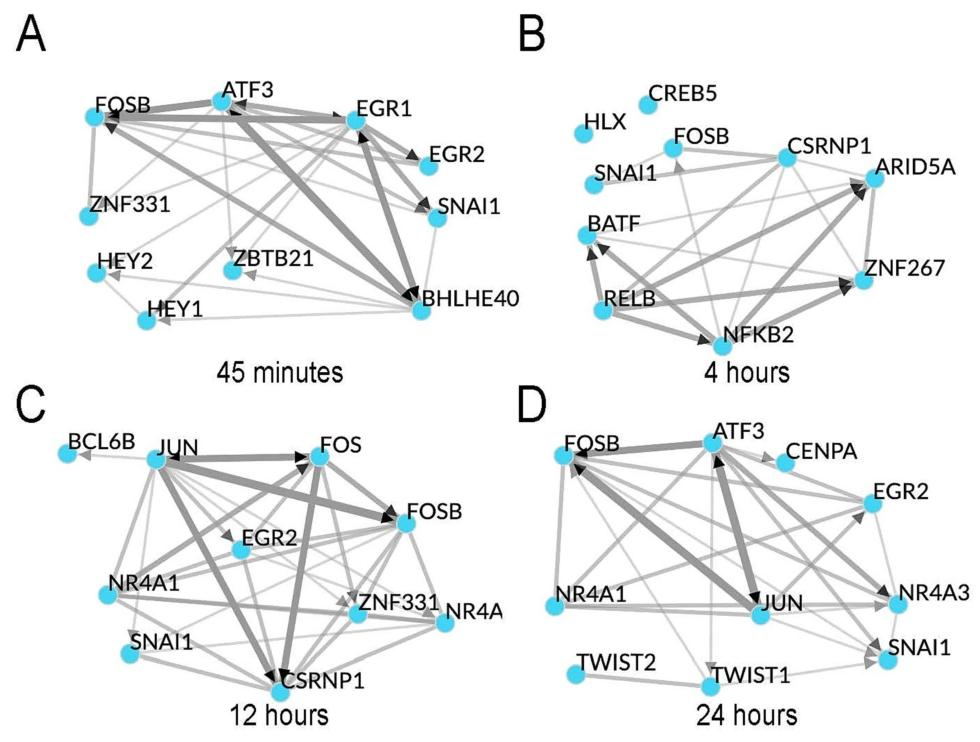
图3:核心转录因子(TF)网络
Chea3 分析显示,各时间点 Top10 TF 形成高度连接的共调控网络,均包含 AP-1 家族成员(Fos、Jun)及 EndMT 相关 TF:0.75h 已富集 HEY1(EndMT 调控因子),12-24h SNAI1(EndMT 核心 TF)、NR4A1(炎症调控)排名显著上升;SNAI1 转录本在 12h(FC=3.08)、24h(FC=3.11)显著上调,hIgG 对照组无变化,证实 EndMT 通路被特异性激活。
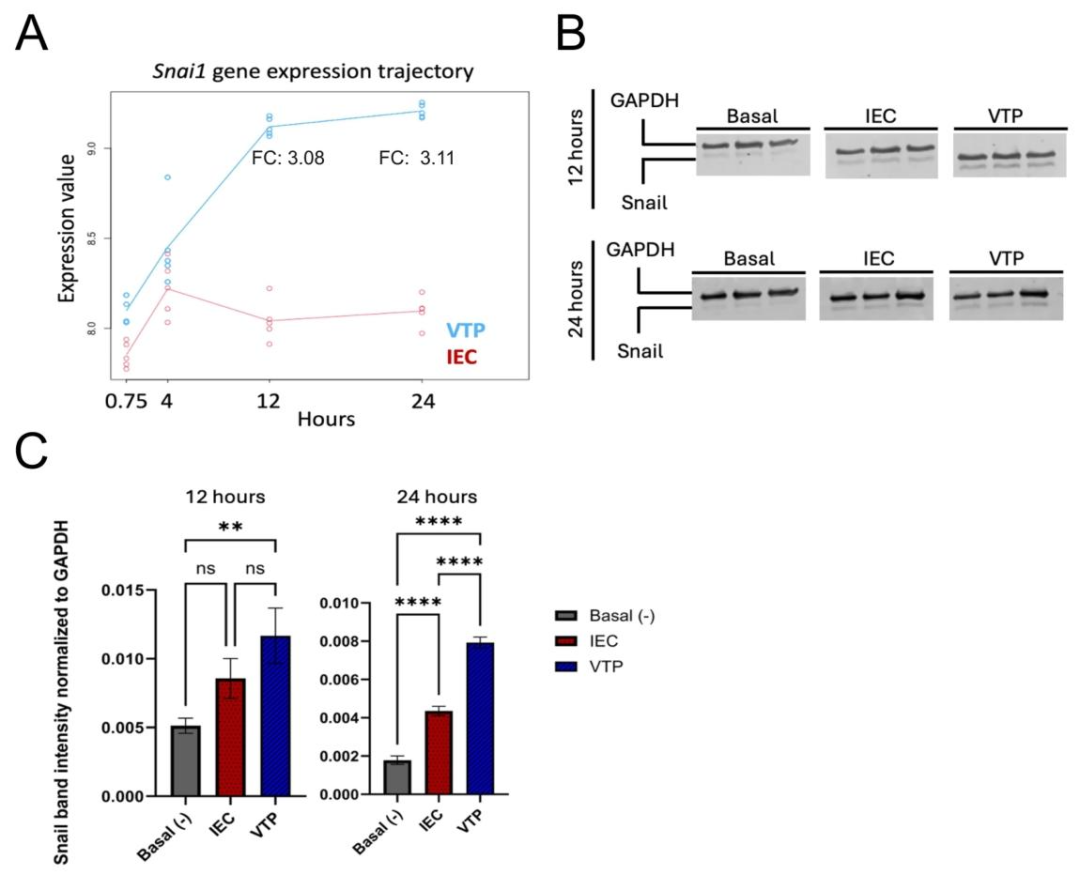
图4:Snail 蛋白表达验证
Western blot 显示,VTP 处理组 Snail 蛋白在 12h 开始升高,24h 显著高于 IEC 对照组(p<0.05);活细胞成像显示,Snail 上调伴随 caspase-3/7 激活(凋亡标志),24h 凋亡细胞比例达 35%(对照组仅 5%),提示 EndMT 与凋亡通路协同调控。
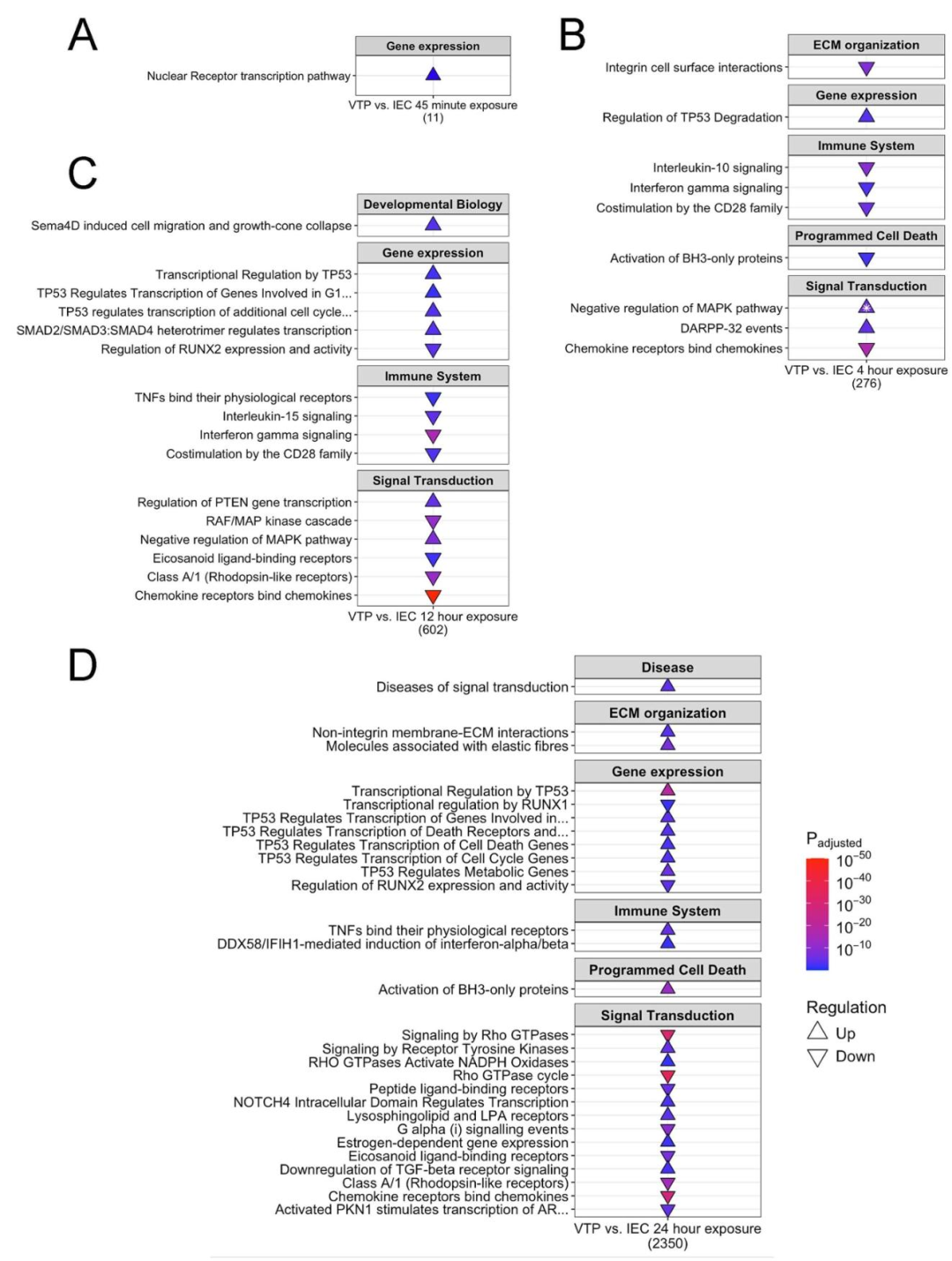 | 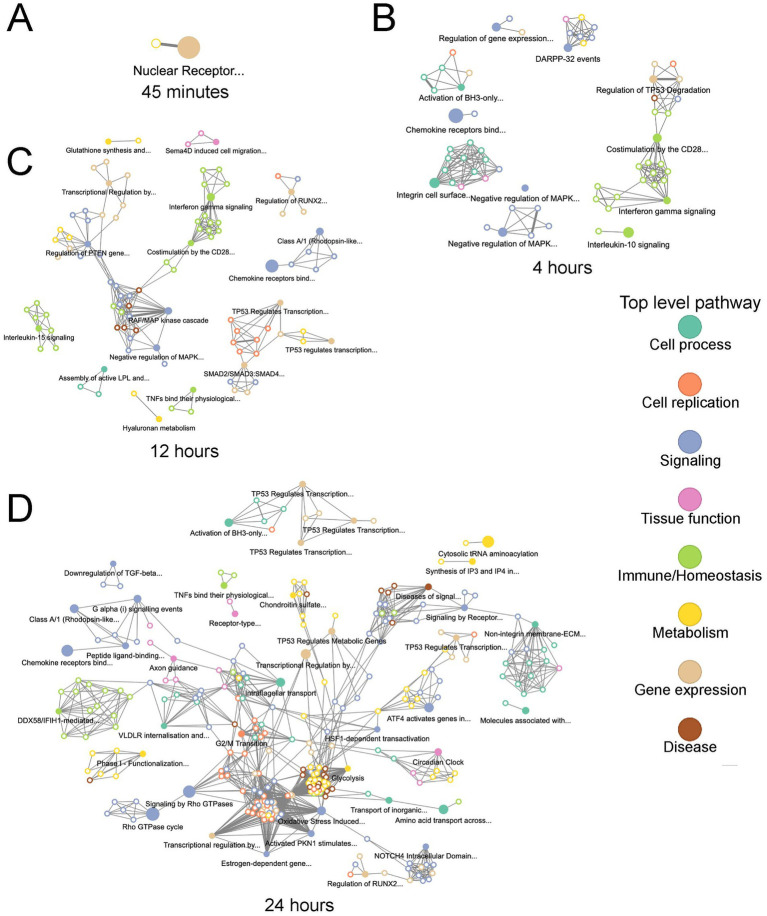 | 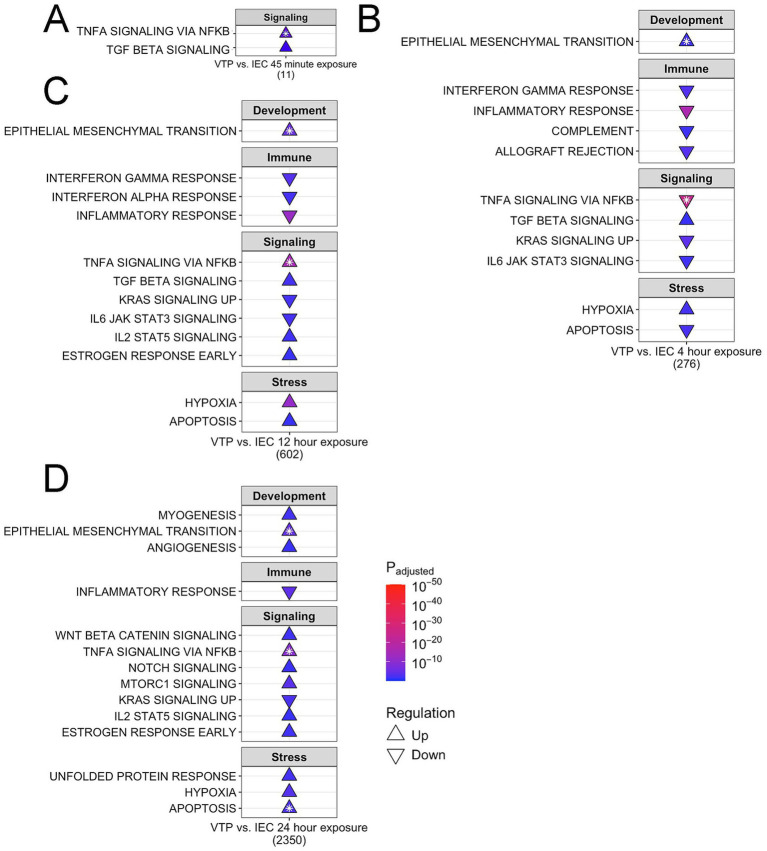 |
图5-7:通路富集与 hallmark 基因集分析
通路富集:0.75h 以 “核受体转录” 为主,4h 开始下调 “趋化因子受体结合”“IFN-γ 信号”(抑制免疫招募),12h 上调 “SMAD2/3-SMAD4 转录调控”(TGFβ 通路核心),24h 富集 “ECM 组织”“Rho GTPase 激活”“NOTCH 信号”,通路网络从早期分散聚类(免疫、信号)变为晚期高度互联,提示转录响应 “逐步收敛” 至 EndMT 相关通路。
hallmark 分析:“TGFβ 信号” 在 0.75-12h 持续上调,“上皮间质转化(EMT)” 基因集在 4-24h 双向调控(上调更显著),“TNF-α-NF-κB 信号” 同时存在上调和下调(反映通路复杂性),“KRAS 信号” 持续下调,“Wnt-β-catenin 信号” 在 24h 上调,均支持 EndMT 的动态激活。
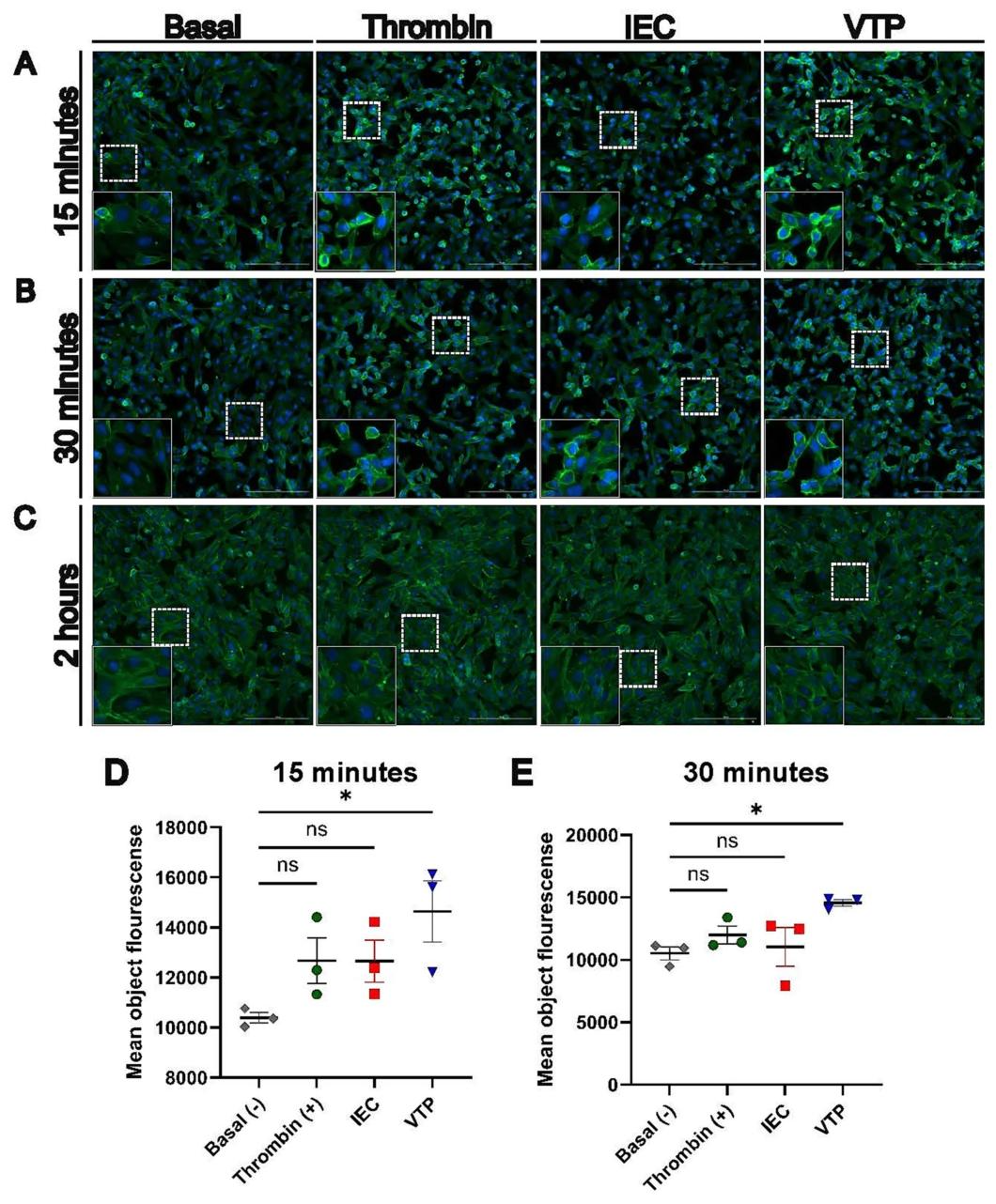
图8:HBMECs 形态与 F-actin 变化
VTP 处理 15-30min 后,HBMECs 出现显著收缩:皮质肌动蛋白环形成、细胞膜起泡,F-actin 荧光强度较对照组提升 2 倍;2h 后形态恢复,提示梅毒螺旋体诱导 “瞬时 cytoskeleton 重排”,与 Rho GTPase(RHOB、RND1)上调一致(RHOB 促进内皮通透性,RND1 破坏黏附连接);凝血酶阳性对照(10nM)呈现类似收缩形态,证实这种变化与血管功能异常相关。
本研究通过时间序列转录组首次证实:梅毒螺旋体通过诱导内皮间质转化(EndMT) 调控脑微血管内皮细胞功能,核心机制包括:1)EndMT 核心 TF Snail(转录 + 蛋白水平)上调,驱动内皮细胞向间质表型转化(下调内皮标志物 VCAM1、上调间质标志物 α-SMA);2)TGFβ-SMAD 通路双向调控(激活 SMAD2/3-SMAD4 复合物,同时诱导 SMAD7 负反馈),协同 Rho GTPase(RHOB、RND1)调控细胞形态与屏障功能;3)ECM 成分(胶原 4/5、纤连蛋白)与蛋白酶(MMP、ADAM)表达异常,可能促进梅毒螺旋体穿透内皮屏障;4)早期下调趋化因子(CCL2、CSF1)与 IFN 信号,帮助梅毒螺旋体逃避免疫清除。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:人源化抗 CD147 抗体 HuM6-1B9 激活 NK 细胞介导 ADCC,克服三阴性乳腺癌免疫耐药
下一篇:肝癌小鼠中髓系来源抑制细胞(MDSC)对库普弗细胞表型与功能的调控