常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-11 17:02:50 细胞资源库平台 访问量:15
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:Differential regulation of translation and endocytosis of alternatively spliced forms of the type II bone morphogenetic protein (BMP) receptor
中文标题:II 型骨形态发生蛋白(BMP)受体可变剪接体的翻译与内吞差异调控
发表期刊:《Molecular Biology of the Cell》
影响因子:2.7
作者单位:
1.Department of Neurobiology, George S. Wise Faculty of Life Sciences, Tel Aviv University, Tel Aviv 69978, Israel
2.Department of Cell Research and Immunology, George S. Wise Faculty of Life Sciences, Tel Aviv University, Tel Aviv 69978, Israel
3.Institute for Chemistry and Biochemistry, Freie Universität Berlin, 1495 Berlin, Germany
作者信息:
第一作者:Ayelet R. Amsalem
共同通讯作者:Yoav I. Henisa*、Marcelo Ehrlichb*
骨形态发生蛋白(BMPs)作为转化生长因子 -β(TGF-β)超家族最大亚群,在胚胎发育、器官形成及多种疾病发生发展中发挥关键调控作用,其信号传递依赖 I 型和 II 型跨膜丝氨酸 - 苏氨酸激酶受体的协同作用。II 型 BMP 受体(BMPRII)存在两种可变剪接体:长型(BMPRII-LF)和短型(BMPRII-SF),其中 BMPRII-LF 的胞质域含独特的约 500 个氨基酸 C 端延伸区,该区域与肺动脉高压(PAH)等疾病相关,被推测可调控受体信号输出,但对受体表达调控的作用尚未明确。BMPRII 的表达水平和细胞表面分布受多种分子机制调控,包括可变剪接、内吞转运、降解等,其中内吞作用对 BMP 信号通路的影响存在争议,且传统研究依赖非特异性内吞抑制剂,易干扰其他信号蛋白转运。本研究通过构建 BMPRII 剪接体及突变体,系统探究其合成、降解、分布及内吞转运的差异调控机制,明确 C 端延伸区的功能,为理解 BMPRII 表达调控与信号传导的关联提供实验依据。
本研究构建带 myc 标签的 BMPRII-SF、BMPRII-LF 及 LF 截短突变体(TC6、TC7、TC8)、丙氨酸替换突变体(BMPRII-LF-AA),以及融合 BMPRII-LF 3’端 99 个核苷酸的 BMPRII-SFM 和 GFP-C 突变体,转染 HEK293T 和 COS7 细胞后,通过免疫印迹检测受体稳态表达水平,qRT-PCR 验证 mRNA 表达差异。采用 [³⁵S](Met+Cys)脉冲标记结合免疫沉淀检测蛋白合成效率,脉冲追踪实验分析降解动力学;蔗糖垫离心法评估 mRNA 与核糖体的结合能力,探究翻译调控机制。通过蛋白酶 K 消化法检测细胞表面受体水平,EndoH 酶切实验验证受体糖基化成熟状态。利用免疫荧光标记结合共聚焦显微镜观察受体内吞过程,通过点扫描共聚焦技术定量内吞速率,采用高渗蔗糖、PitStop、制霉菌素等抑制剂鉴定内吞途径。CHX chase 实验结合溶酶体抑制剂(氯喹)和蛋白酶体抑制剂(MG132)分析受体降解途径。通过免疫印迹检测 Smad1/5/8 磷酸化水平,评估受体信号传导能力。所有实验数据采用 Student’s t 检验或方差分析,P<0.05 为差异具有统计学意义。
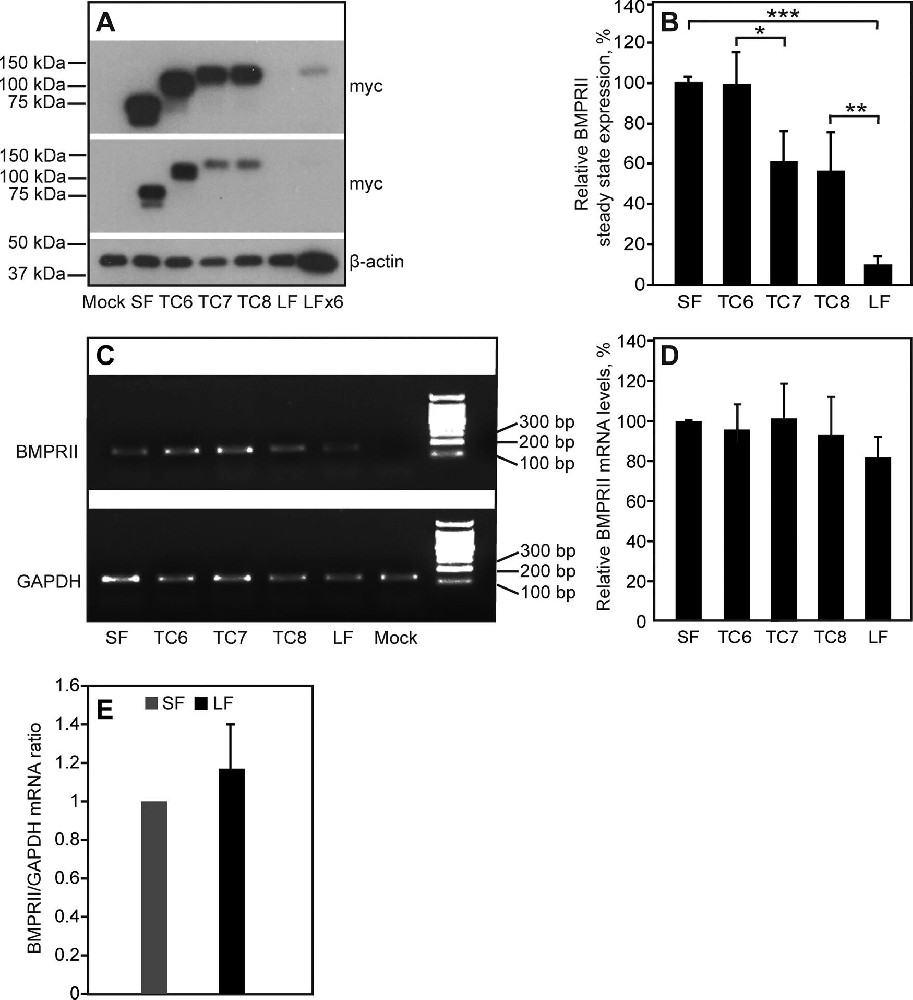
图1:BMPRII-LF 的 C 端延伸区调控受体稳态表达水平
HEK293T 细胞转染等摩尔量的 myc 标记 BMPRII 剪接体及截短突变体后,免疫印迹结果显示 BMPRII-SF 的稳态表达水平显著高于 BMPRII-LF(约 10 倍),COS7 细胞中也观察到类似趋势(7 倍差异);截短突变体分析表明,TC8 与 BMPRII-LF 之间 17 个氨基酸的编码序列是调控表达差异的主要区域,TC6 与 TC7 之间的区域也有部分贡献。qRT-PCR 和 PCR 检测证实,各剪接体及突变体的 mRNA 水平无显著差异,排除了转录水平调控的可能性,表明表达差异源于转录后机制。
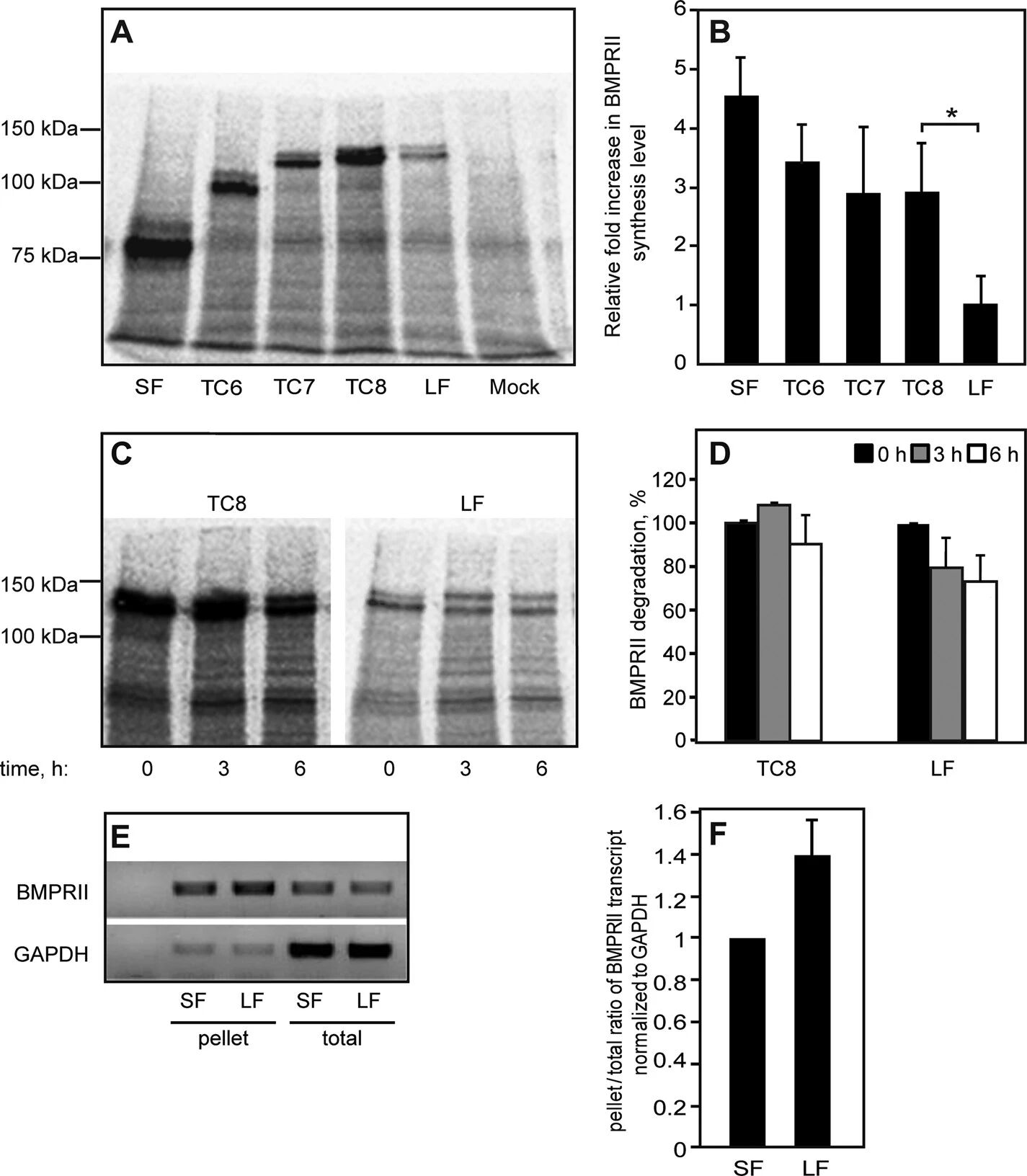
图2:BMPRII 剪接体的蛋白合成与降解差异分析
[³⁵S] 脉冲标记实验显示,BMPRII-SF、TC6、TC7、TC8 的蛋白合成效率无显著差异,而 BMPRII-LF 的合成效率显著低于 TC8;脉冲追踪实验表明,短期内(3-6 小时)BMPRII-LF 与 TC8 的降解速率无差异,说明合成效率差异是两者稳态水平不同的主要原因。蔗糖垫离心实验显示,BMPRII-LF 与 BMPRII-SF 的 mRNA 在核糖体 / 多聚核糖体富集组分中的比例无显著差异,表明 BMPRII-LF 合成效率降低并非由于 mRNA 与核糖体结合能力下降,可能源于翻译延伸阶段的调控。
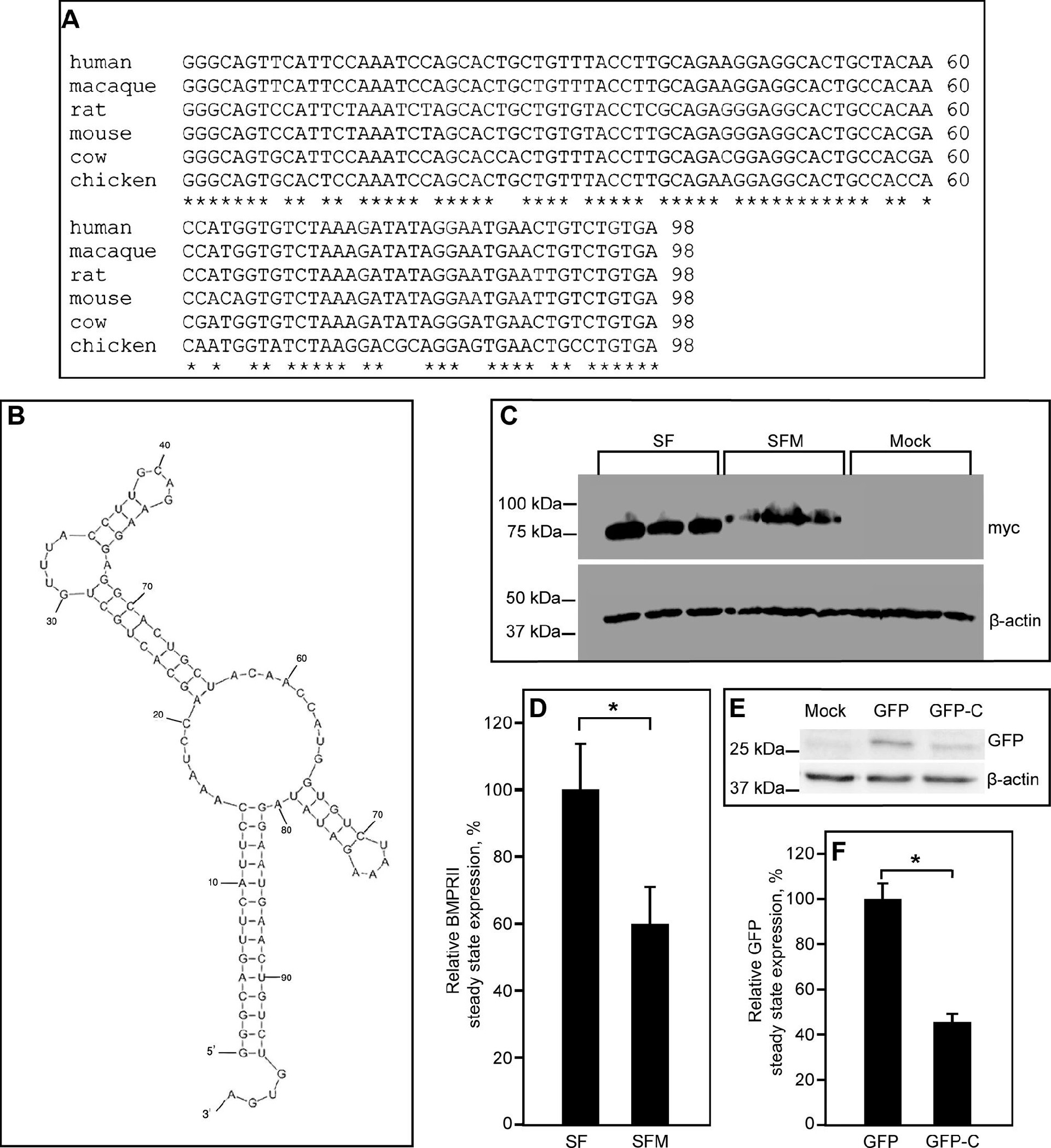
图3:BMPRII-LF 的 3’编码序列对表达的抑制作用
序列比对显示,BMPRII-LF 3’端 98 个核苷酸在不同物种间高度保守,Mfold 预测该区域可形成茎环二级结构(ΔG 为 - 28 至 - 35 kcal/mol)。将该区域(99 个核苷酸)融合到 BMPRII-SF 中构建 BMPRII-SFM,其表达水平显著低于 BMPRII-SF;将该序列融合到无关蛋白 GFP 中构建 GFP-C,同样导致 GFP 表达降低,证实该 3’端序列具有广泛的表达抑制作用,且其二级结构完整性对抑制功能至关重要,TC8 因缺失部分序列导致茎环结构破坏,表达水平显著高于 BMPRII-LF。
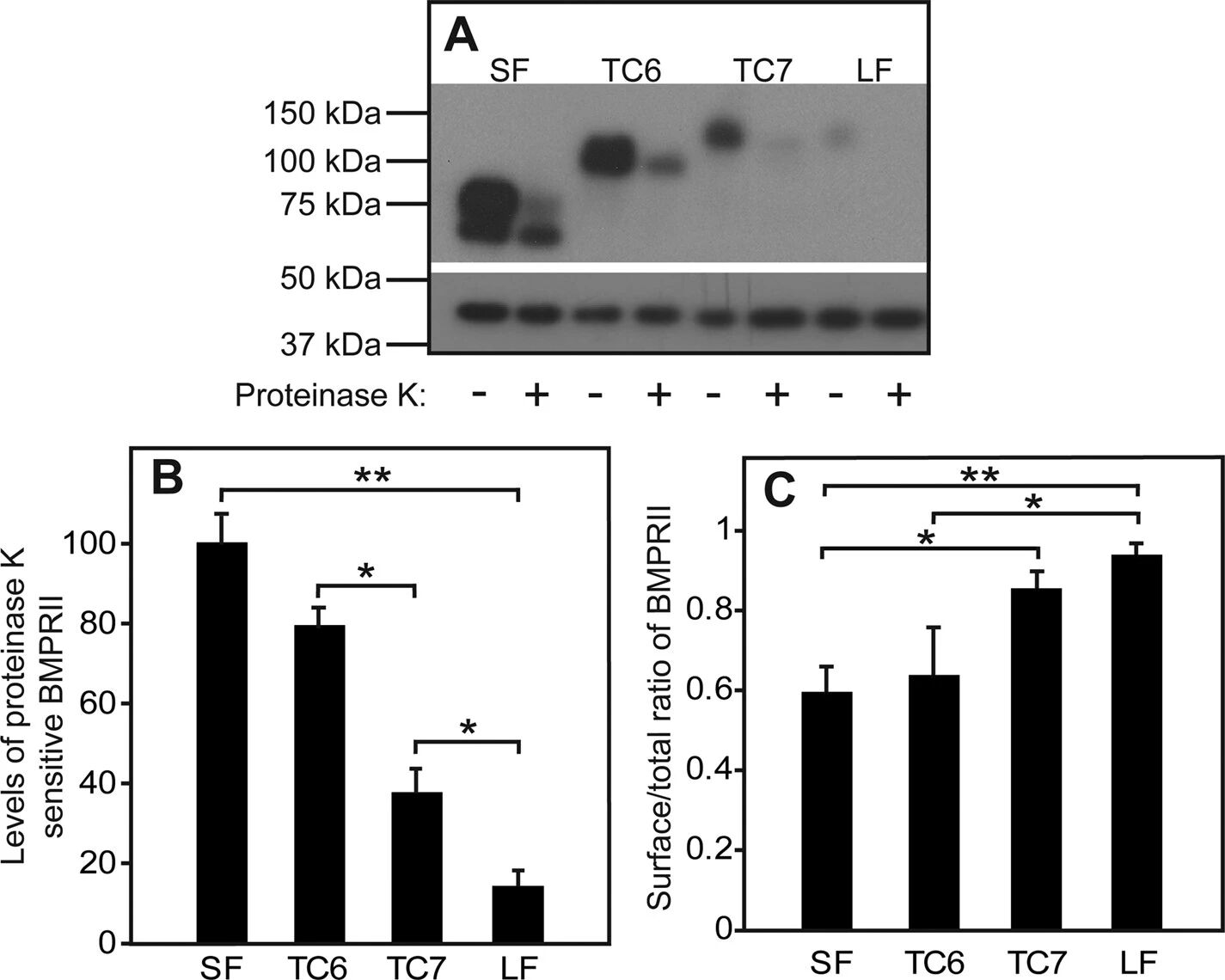
图4:C 端延伸区长度决定 BMPRII 的细胞表面稳态水平
蛋白酶 K 消化实验显示,BMPRII-LF 的细胞表面表达水平显著低于 BMPRII-SF,截短突变体中 TC6 的细胞表面水平高于 TC7,与稳态表达水平趋势一致;细胞表面 / 总受体比例分析表明,所有 BMPRII 构建体均主要定位于细胞膜,其中 BMPRII-LF 的膜定位比例最高(约 95% EndoH 抗性),BMPRII-SF 次之(约 78% EndoH 抗性)。结合前文结果,TC6 与 TC7 的合成效率无差异但细胞表面水平不同,提示除翻译调控外,还存在其他调控机制(如内吞转运)影响受体的细胞表面分布。
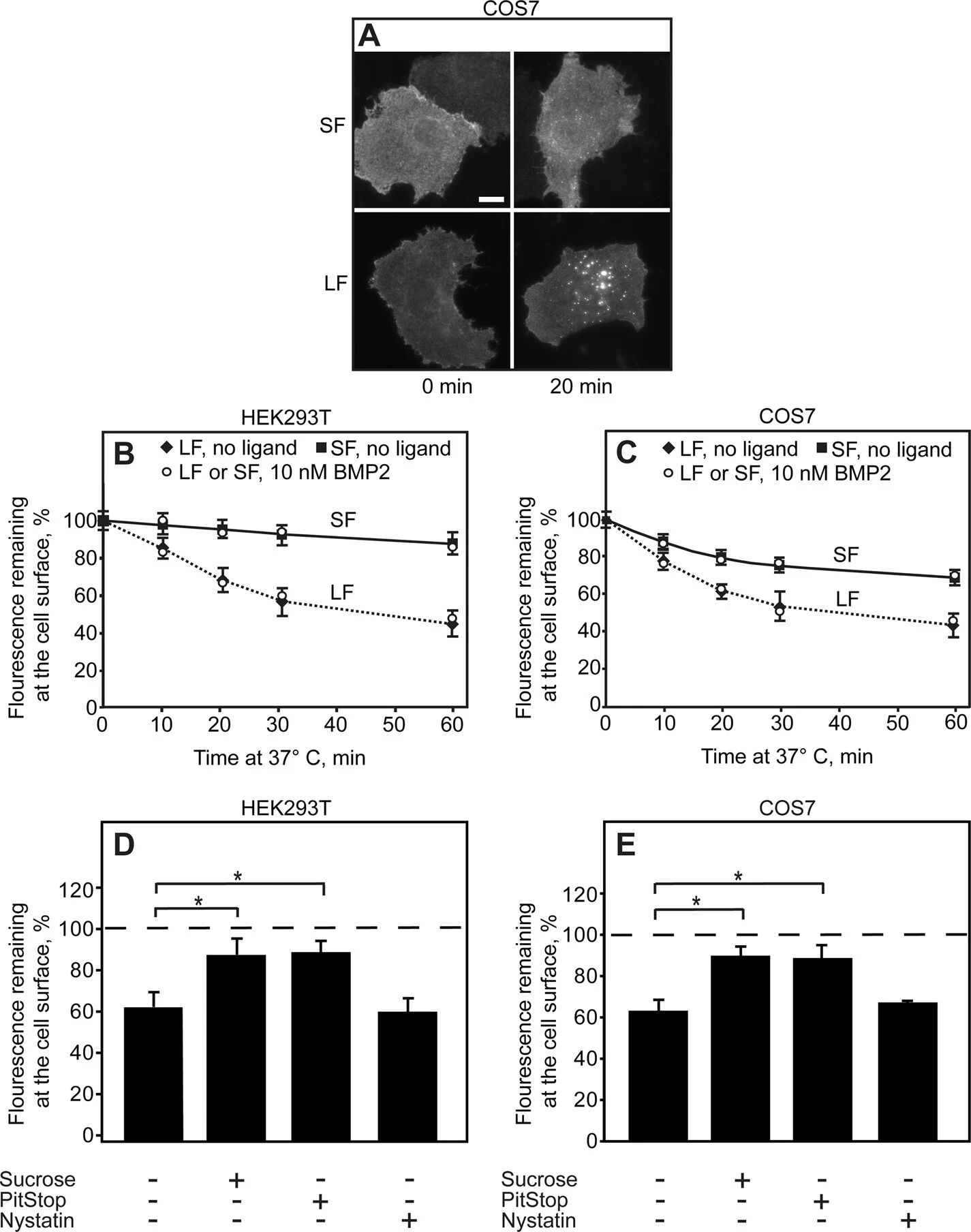
图5:BMPRII-LF 的 C 端延伸区介导网格蛋白依赖的内吞
共聚焦显微镜观察显示,BMPRII-LF 在 37℃孵育后呈现明显的囊泡样分布,而 BMPRII-SF 仍主要定位于细胞膜;定量分析表明,BMPRII-LF 的内吞速率显著快于 BMPRII-SF,HEK293T 和 COS7 细胞中均如此,且配体 BMP2 处理不影响内吞速率。内吞抑制剂实验显示,高渗蔗糖和 PitStop(网格蛋白介导内吞抑制剂)可显著抑制 BMPRII-LF 的内吞,而制霉菌素(小窝介导内吞抑制剂)仅轻微影响,证实 BMPRII-LF 主要通过网格蛋白介导的内吞(CME)进行内化,半衰期为 15-20 分钟。
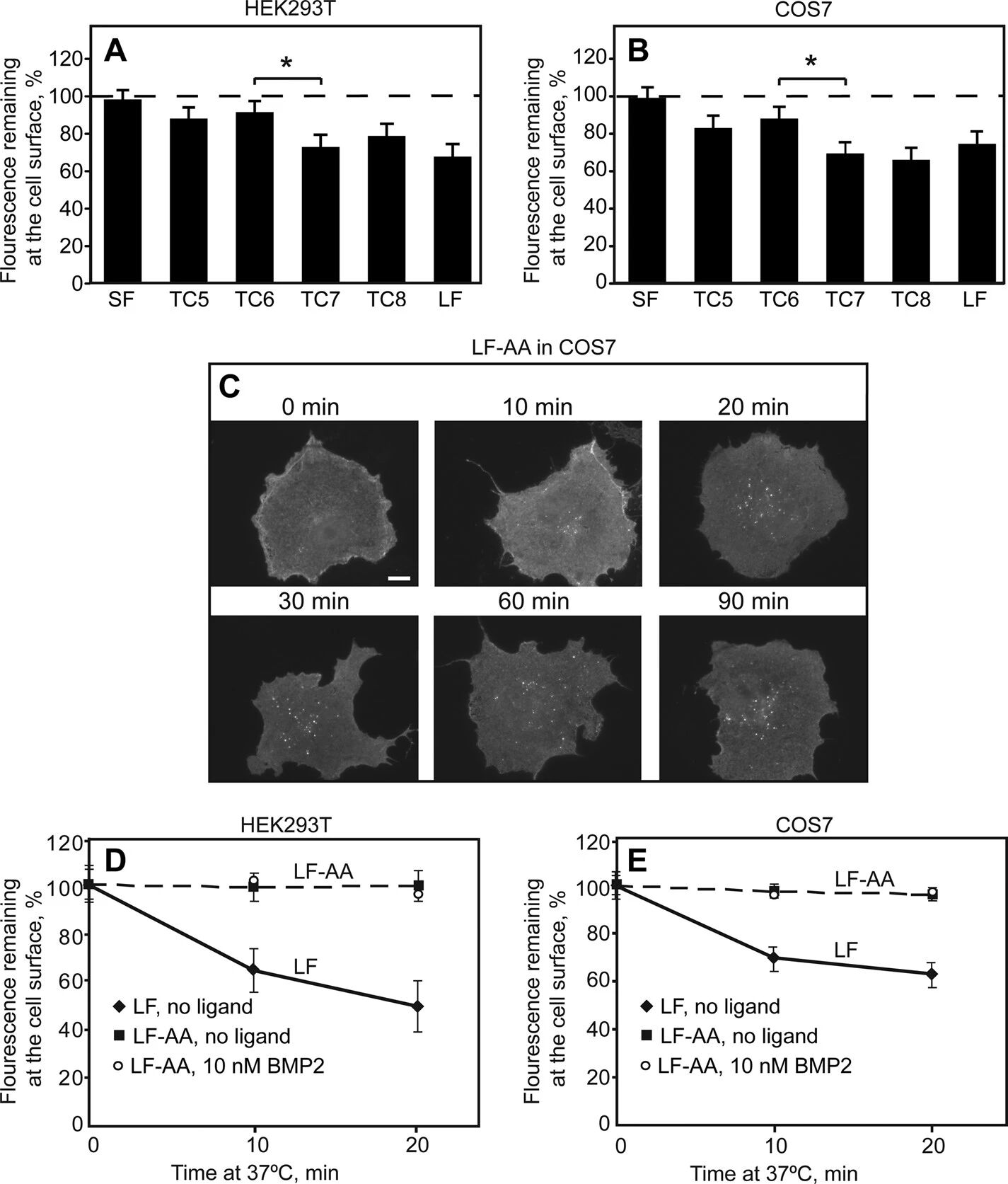
图6:BMPRII-LF 的内吞信号定位及突变体功能验证
截短突变体分析显示,BMPRII-SF、TC5、TC6 的内吞活性极低,而 BMPRII-LF、TC7、TC8 具有显著内吞活性,表明内吞信号位于 TC6 与 TC7 之间的序列中;序列分析发现该区域存在一个双亮氨酸基序(L870I871),将其突变为丙氨酸构建 BMPRII-LF-AA,其在 HEK293T 和 COS7 细胞中均丧失内吞活性,且配体 BMP2 处理无改善,证实 L870I871 是介导 BMPRII-LF 网格蛋白依赖内吞的关键信号。
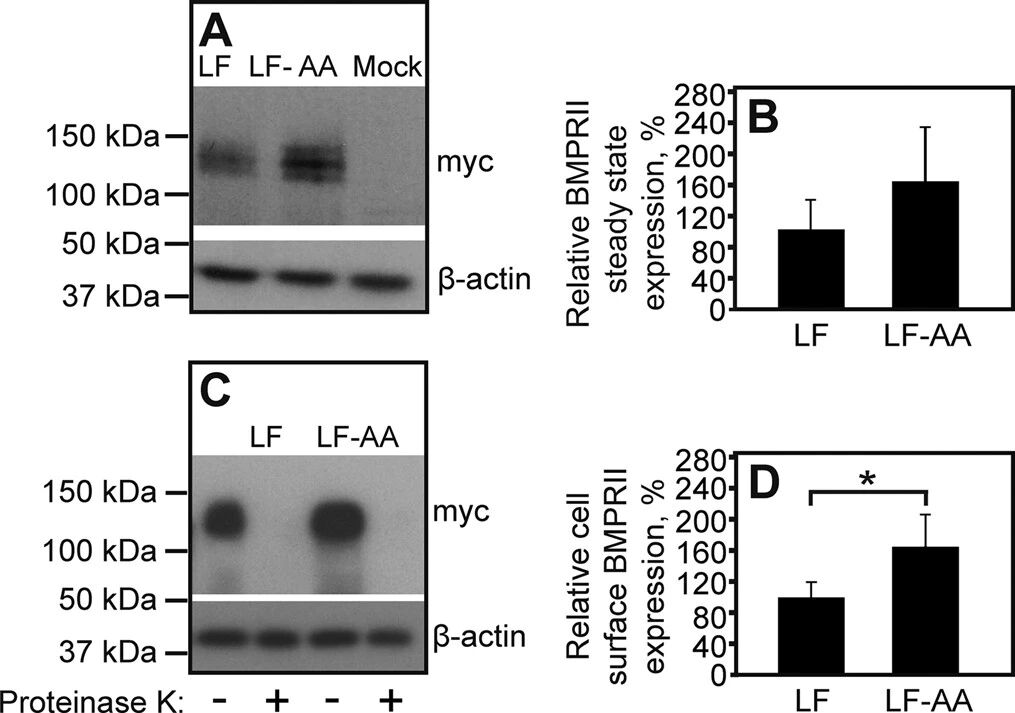
图7:网格蛋白介导的内吞降低 BMPRII-LF 的细胞表面表达
免疫印迹结果显示,BMPRII-LF-AA 的总稳态表达水平略高于 BMPRII-LF,而蛋白酶 K 消化实验表明其细胞表面水平显著高于 BMPRII-LF(近 2 倍);TC6(缺失内吞信号)与 TC7(保留内吞信号)的细胞表面水平也存在类似差异,证实内吞信号通过促进受体内化,降低其细胞表面稳态水平,对表达的调控起温和调节作用。
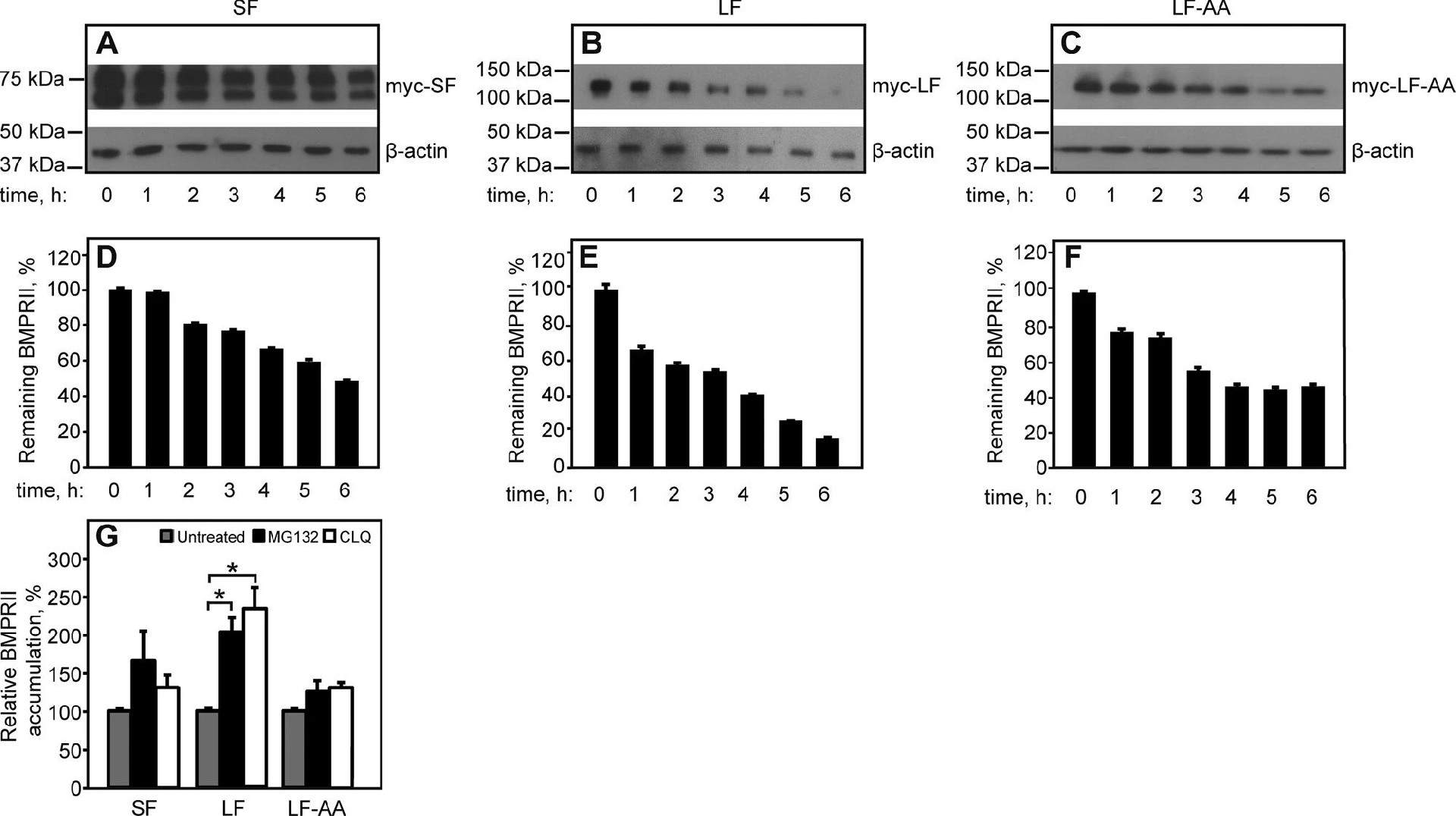
图8:BMPRII-LF 的降解依赖双亮氨酸内吞信号
CHX chase 实验显示,BMPRII-LF 的降解速率(约 20%/h)显著快于 BMPRII-SF(约 8%/h)和 BMPRII-LF-AA(约 11%/h);抑制剂实验表明,氯喹(溶酶体抑制剂)和 MG132(蛋白酶体抑制剂)均能显著增加 BMPRII-LF 的积累,而对 BMPRII-SF 仅 MG132 有轻微作用,说明 BMPRII-LF 的降解同时依赖溶酶体和蛋白酶体途径,且内吞信号通过促进受体内化加速其降解,而 BMPRII-SF 和 BMPRII-LF-AA 因内吞活性低,降解速率较慢。
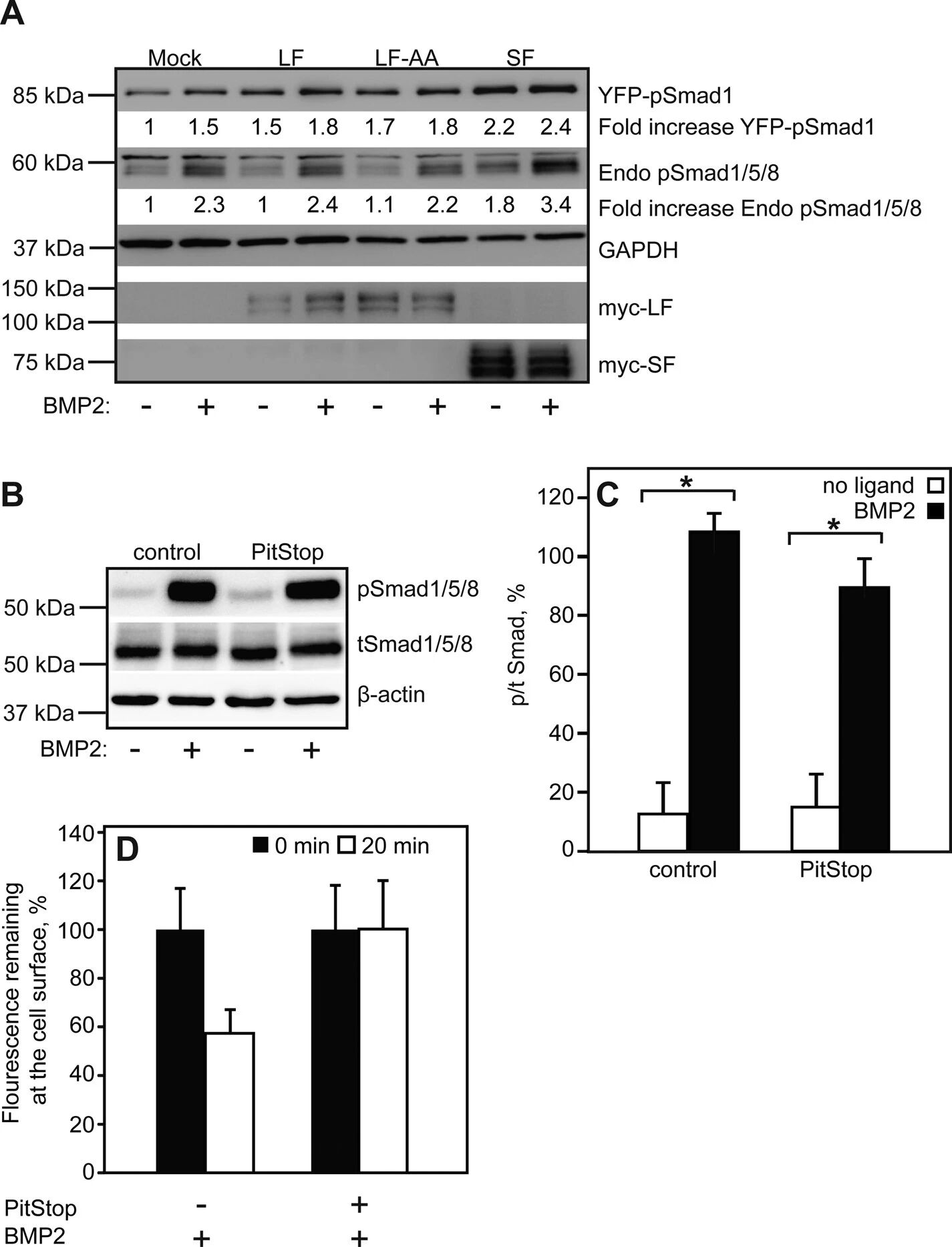
图9:BMPRII 的 Smad 信号激活与细胞表面表达相关,且不依赖内吞
COS7 细胞共转染 YFP-Smad1 与 BMPRII 剪接体或突变体,BMP2 刺激后,BMPRII-SF 因细胞表面水平高,其介导的内源性 Smad1/5/8 磷酸化水平显著高于 BMPRII-LF 和 BMPRII-LF-AA;未转染细胞经 PitStop 处理后,BMP2 诱导的 Smad1/5/8 磷酸化无显著抑制,且 PitStop 能有效阻断 BMPRII-LF 的内吞,证实 BMPRII 的内吞对 Smad1/5/8 信号激活并非必需,细胞表面受体水平是决定信号强度的关键因素。
本研究系统揭示了 II 型 BMP 受体可变剪接体(BMPRII-LF 和 BMPRII-SF)的多层级差异调控机制,明确 BMPRII-LF 的独特 C 端延伸区是核心调控元件。该区域通过两个关键机制调控受体表达:一是其 3’端 99 个核苷酸形成的保守茎环结构抑制翻译效率,导致 BMPRII-LF 的合成水平显著低于 BMPRII-SF;二是该区域含有的双亮氨酸基序(L870I871)介导网格蛋白依赖的内吞,加速受体内化与降解,进一步降低其细胞表面稳态水平。BMPRII-SF 因缺乏 C 端延伸区,翻译效率高且内吞活性极低,故细胞表面表达水平显著高于 BMPRII-LF,进而增强 Smad1/5/8 信号通路的激活。研究还证实,BMPRII 的内吞对 Smad 信号激活无必要,细胞表面受体丰度是决定信号强度的关键。这些发现阐明了 BMPRII 可变剪接通过调控翻译与内吞,实现对受体表达和信号传导的精细调控,为理解 PAH 等相关疾病的发病机制提供了新的分子视角,也为靶向 BMPRII 的治疗策略开发奠定了基础。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:CD40LG与ANXA5构象变化作为2,7-二溴咔唑诱导心肌毒性关键事件的体内与体外模型研究
下一篇:THP-1 单核细胞抑制 HSV-1 复制并调控病毒介导的趋化因子反应