常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-10 09:00:00 细胞资源库平台 访问量:17
荧光素酶报告基因系统是一种基于荧光素酶催化底物氧化反应产生生物发光的检测技术,广泛应用于细胞生物学研究。其中,萤火虫荧光素酶(firefly luciferase, Fluc)因其高灵敏度、宽线性检测范围(约7~8个数量级)以及较短的半衰期(在哺乳动物细胞中约为3小时,在植物细胞中约为3.5小时)而成为最常用的报告基因。其发光信号强度在酶浓度为10⁻¹⁶ mol/L至10⁻⁸ mol/L的范围内与酶活性呈线性关系,并且在理想条件下可检测到低至10⁻²⁰ mol/L的荧光素酶活性。此外,荧光素酶报告基因系统具有非放射性、检测快速、灵敏度高(比氯霉素乙酰转移酶CAT高100倍)等优点,特别适用于高通量筛选和活细胞检测。通过将荧光素酶报告基因载体转染至宿主细胞后,可利用荧光素酶检测系统灵敏且便捷地监测基因表达水平,已成为细胞生物学研究中的重要工具。
英文标题:Differential inclusion formation of an aggregation-prone protein reveals differences in the proteostasis capacity of neuronal cell lines
中文标题:易聚集蛋白的包涵体形成差异揭示神经元细胞系的蛋白质稳态能力不同
发表期刊:《BBA - Molecular Cell Research》
影响因子:4.6
作者单位:
1.Molecular Horizons and School of Science, University of Wollongong, Wollongong, Australia
2.Yusuf Hamied Department of Chemistry, University of Cambridge, Cambridge, UK
3.UK Dementia Research Institute, University of Cambridge, Cambridge, UK
4.Motor Neuron Disease Research Centre, Macquarie Medical School, Faculty of Medicine, Health and Human Sciences, Macquarie University, North Ryde, Australia
作者信息:
第一作者:Shannon McMahon
共同通讯作者:Justin.J. Yerbury*、Heath Ecroyd*
蛋白质稳态的维持对细胞功能和存活至关重要,其紊乱会导致蛋白质聚集形成包涵体,这是阿尔茨海默病、帕金森病、肌萎缩侧索硬化症等多种神经退行性疾病的核心病理特征。不同细胞类型对包涵体形成的易感性存在显著差异,神经元因无法通过细胞分裂稀释毒性蛋白聚集体、细胞寿命更长等特点成为易感群体,但该选择性易感性的分子机制尚未明确。细胞的蛋白质稳态能力是其抑制蛋白聚集形成包涵体的关键,依赖于蛋白质质量控制网络的调控,而目前缺乏定量评估细胞该能力的有效方法。萤火虫荧光素酶双突变体(FlucDM)是一种易聚集的报告蛋白,可作为蛋白质稳态传感器与细胞内稳态调控机制互作,且能在细胞和体内形成包涵体。本研究选取 Neuro-2a 小鼠神经母细胞瘤细胞、NSC-34 运动神经元样杂交细胞两种常用神经元细胞系,以 FlucDM 为探针探究其蛋白质稳态能力的差异,旨在建立定量评估细胞蛋白质稳态能力的平台,揭示细胞类型背景在蛋白质组维持中的作用,为理解蛋白质错误折叠疾病中神经元的选择性易感性提供实验依据。
本研究构建带 N 端 EGFP 标签的野生型萤火虫荧光素酶(FlucWT-EGFP)和双突变体(FlucDM-EGFP)质粒,瞬时转染 Neuro-2a 和 NSC-34 细胞后,通过共聚焦显微镜观察并盲法手动计数,检测细胞内包涵体的形成情况;利用流式细胞术的脉冲形状分析(PulSA)技术定量鉴定含包涵体的细胞比例,计算 PulSA 聚集指数以消除蛋白表达量差异的影响,同时将 EGFP 荧光强度分箱,分析蛋白表达水平与包涵体形成的关联性。采用 NP-40 裂解法提取细胞不溶性蛋白,经 SDS-PAGE 分离后切取含 FlucDM 包涵体的凝胶条带,通过凝胶内胰蛋白酶消化、反相 C18 液相色谱 - 质谱联用(RP-LC-MS/MS)进行蛋白质组学分析,结合 Venn 图、KEGG 通路富集、PANTHER 蛋白分类、STRING 蛋白互作网络分析,鉴定两细胞系中与 FlucDM 包涵体结合的蛋白特征及细胞类型特异性。通过免疫印迹实验验证 FlucDM 包涵体中关键稳态相关蛋白(Hsp90、Hsp105、DnaJB6)的表达与分布;利用定制 Python 脚本对两细胞系已发表的全蛋白质组数据进行基因本体(GO)映射,分析伴侣蛋白、泛素 - 蛋白酶体系统、自噬、未折叠蛋白反应等蛋白质稳态网络核心通路的蛋白表达差异,采用 Wilcoxon 秩和检验、线性回归等进行统计分析,P<0.05 为差异具有统计学意义。
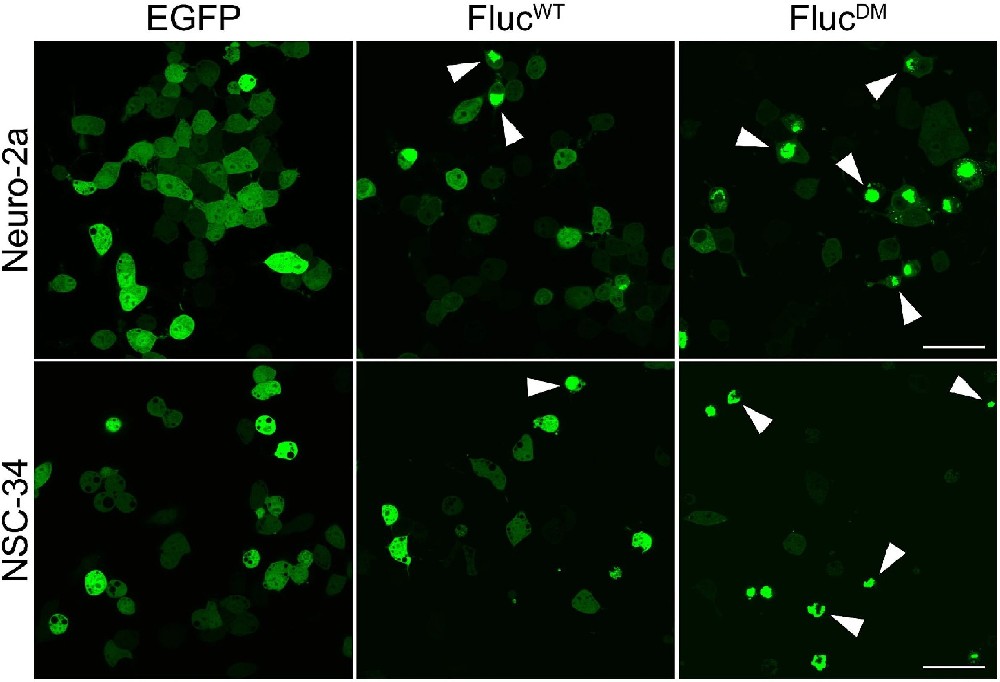
图1:共聚焦显微镜评估 Fluc 在 Neuro-2a 和 NSC-34 细胞中的包涵体形成
将 EGFP、FlucWT-EGFP、FlucDM-EGFP 分别转染 Neuro-2a 和 NSC-34 细胞,48 小时后共聚焦显微镜观察发现,仅表达 EGFP 的细胞在细胞质和细胞核中呈现弥散的绿色荧光,无包涵体形成;表达 FlucWT-EGFP 的细胞仅有少量点状包涵体,Neuro-2a 和 NSC-34 细胞中含包涵体的细胞比例分别为 3.5±0.6%、5.3±1.2%;表达 FlucDM-EGFP 的两细胞系含包涵体的细胞比例显著升高,分别为 11.4±2.1%、15.2±2.7%,证实 FlucDM 在两种神经元细胞系中均易形成包涵体,且 NSC-34 细胞的形成趋势更高。
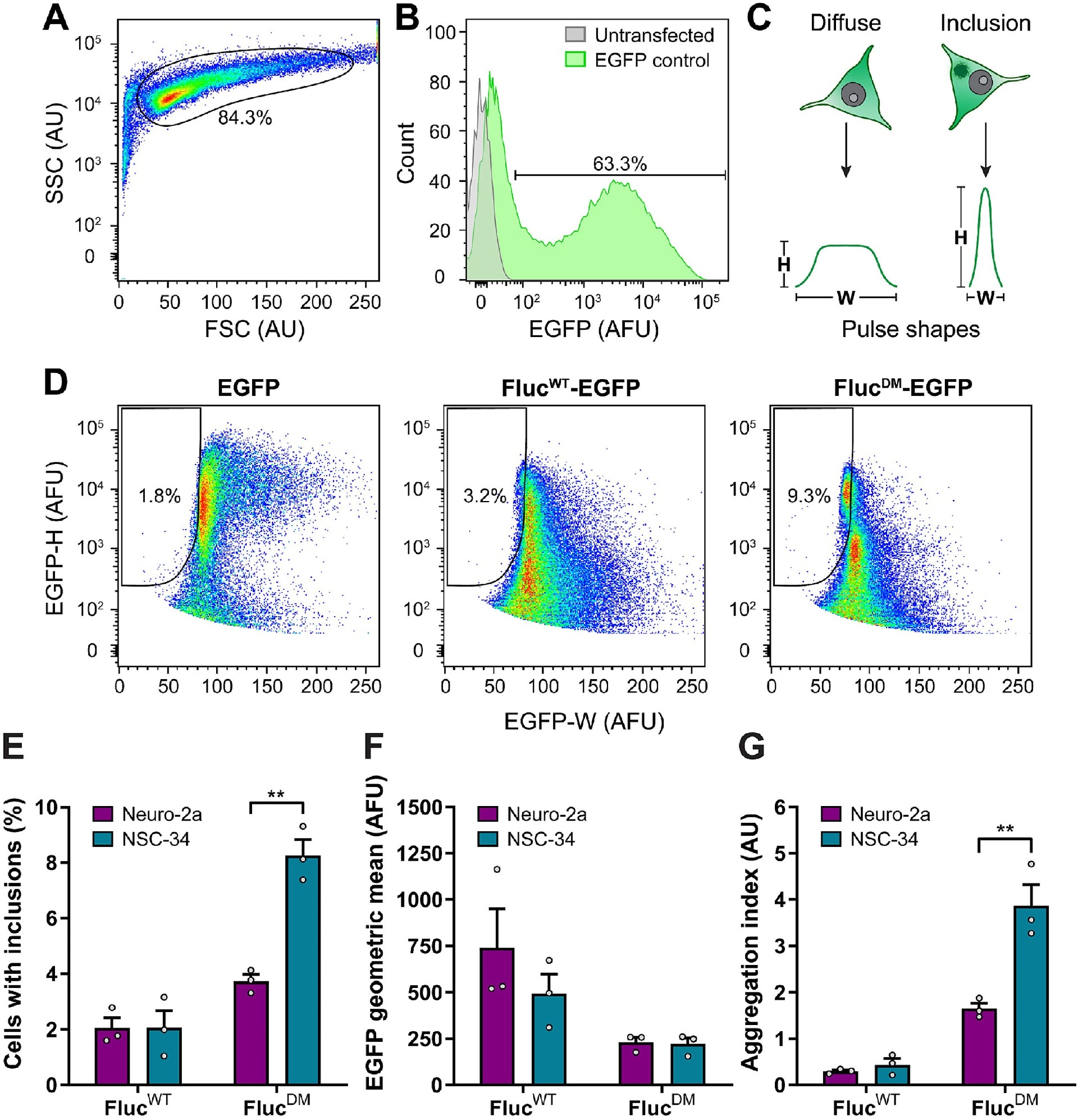
图2:脉冲形状分析(PulSA)评估 Fluc 在 Neuro-2a 和 NSC-34 细胞中介导的包涵体形成
通过流式 PulSA 技术对转染后的细胞进行分析,先通过前向 / 侧向散射筛选活细胞,再基于 EGFP 荧光筛选转染细胞,最后根据 EGFP 荧光脉冲宽度和高度的变化鉴定含包涵体的细胞,结果显示 Neuro-2a 细胞中 FlucWT-EGFP、FlucDM-EGFP 阳性细胞的包涵体形成比例为 2.0±0.4%、3.7±0.2%,NSC-34 细胞中则为 2.1±0.6%、8.3±0.8%;两细胞系的 FlucWT 和 FlucDM 表达量(EGFP 几何均值)无显著差异,基于此计算的 PulSA 聚集指数显示,NSC-34 细胞表达 FlucDM 后的聚集指数显著高于 Neuro-2a 细胞,明确 NSC-34 细胞抑制 FlucDM 聚集形成包涵体的蛋白质稳态能力更弱。
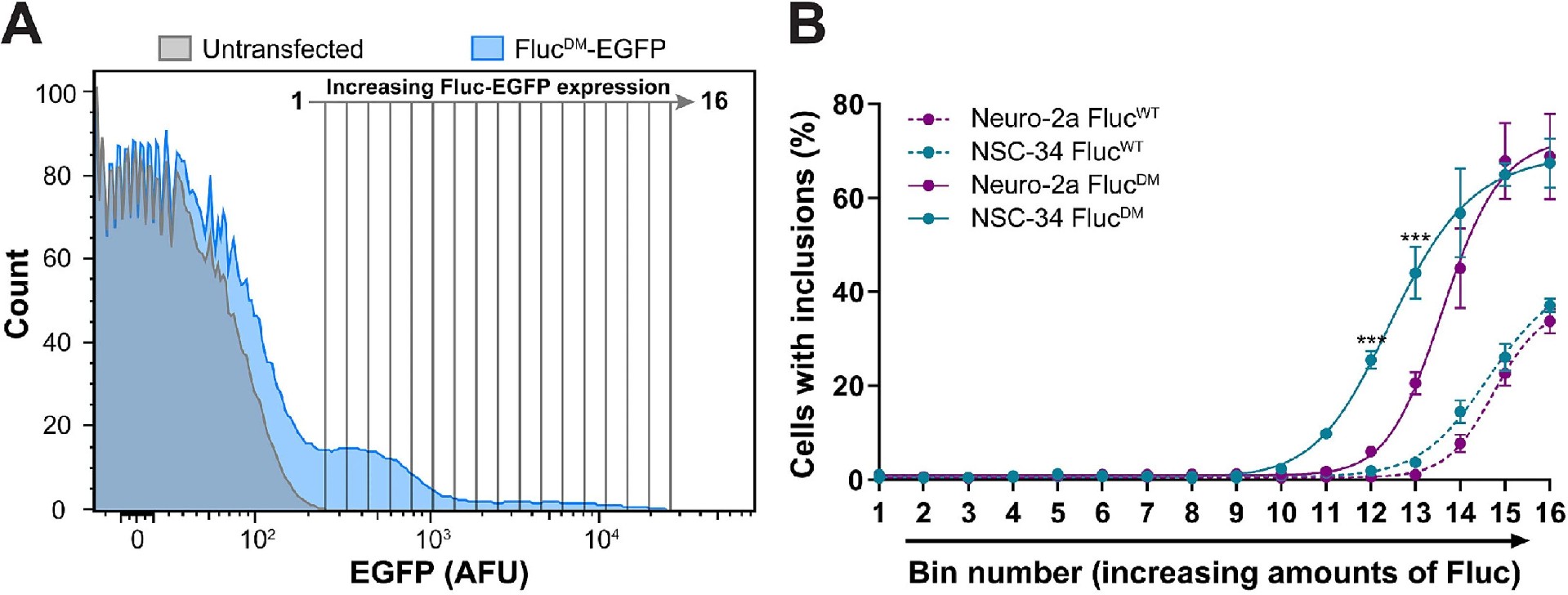
图3:Neuro-2a 和 NSC-34 细胞对 Fluc 基包涵体形成的相对易感性
将转染细胞的 EGFP 荧光强度按对数尺度分为 16 个等距分箱,对每个分箱进行 PulSA 分析发现,1-10 箱的细胞均无包涵体形成,从 11 箱开始,随 Fluc 表达量增加,含包涵体的细胞比例呈上升趋势;表达 FlucDM-EGFP 的 NSC-34 细胞在各分箱中形成包涵体的比例均显著高于 Neuro-2a 细胞,而两细胞系表达 FlucWT-EGFP 后,即使在最高表达量的分箱中,包涵体形成比例也均低于 40% 且无显著细胞间差异,进一步证实 NSC-34 细胞对易聚集蛋白 FlucDM 形成包涵体的易感性更高,蛋白质稳态调控能力更差。
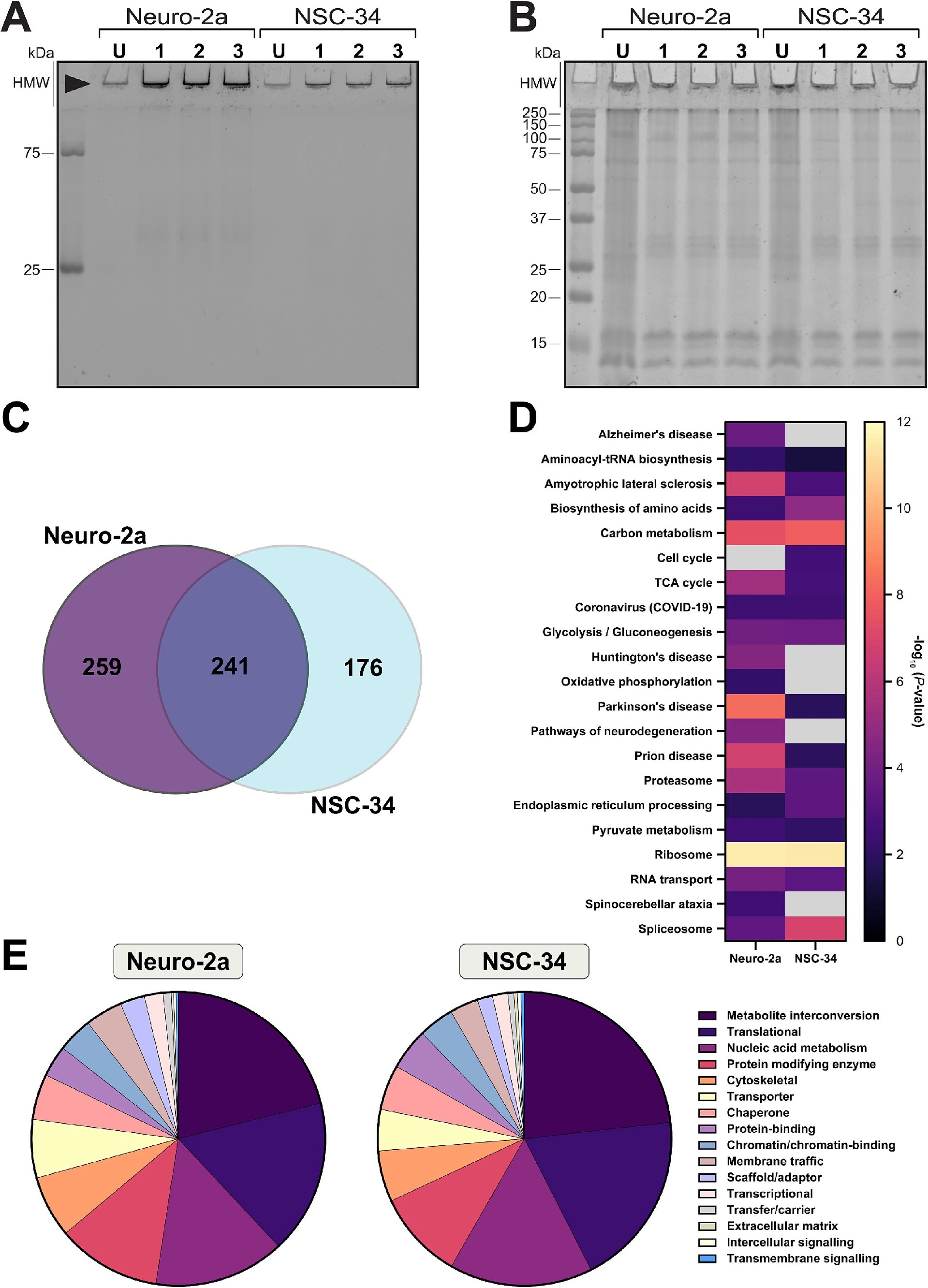
图4:蛋白质组学分析 FlucDM 包涵体中 KEGG 通路和蛋白类别的分布与富集
通过 SDS-PAGE 分离两细胞系的 FlucDM 包涵体蛋白,发现其因分子量较大被滞留在浓缩胶中,对该区域蛋白进行质谱分析共鉴定出 676 种蛋白,其中 241 种为两细胞系共有,259 种仅存在于 Neuro-2a 细胞,176 种仅存在于 NSC-34 细胞;KEGG 通路富集分析显示,两细胞系 FlucDM 包涵体中的蛋白均显著富集于阿尔茨海默病、帕金森病、肌萎缩侧索硬化症等神经退行性疾病相关通路,同时也富集了蛋白酶体降解、内质网蛋白加工等蛋白质稳态网络核心通路及转录、翻译、能量代谢相关通路;PANTHER 蛋白分类分析表明,两细胞系中与 FlucDM 包涵体结合的蛋白类别分布近乎一致,代谢酶、RNA 结合蛋白、细胞骨架蛋白、转运蛋白、伴侣蛋白为主要类别。
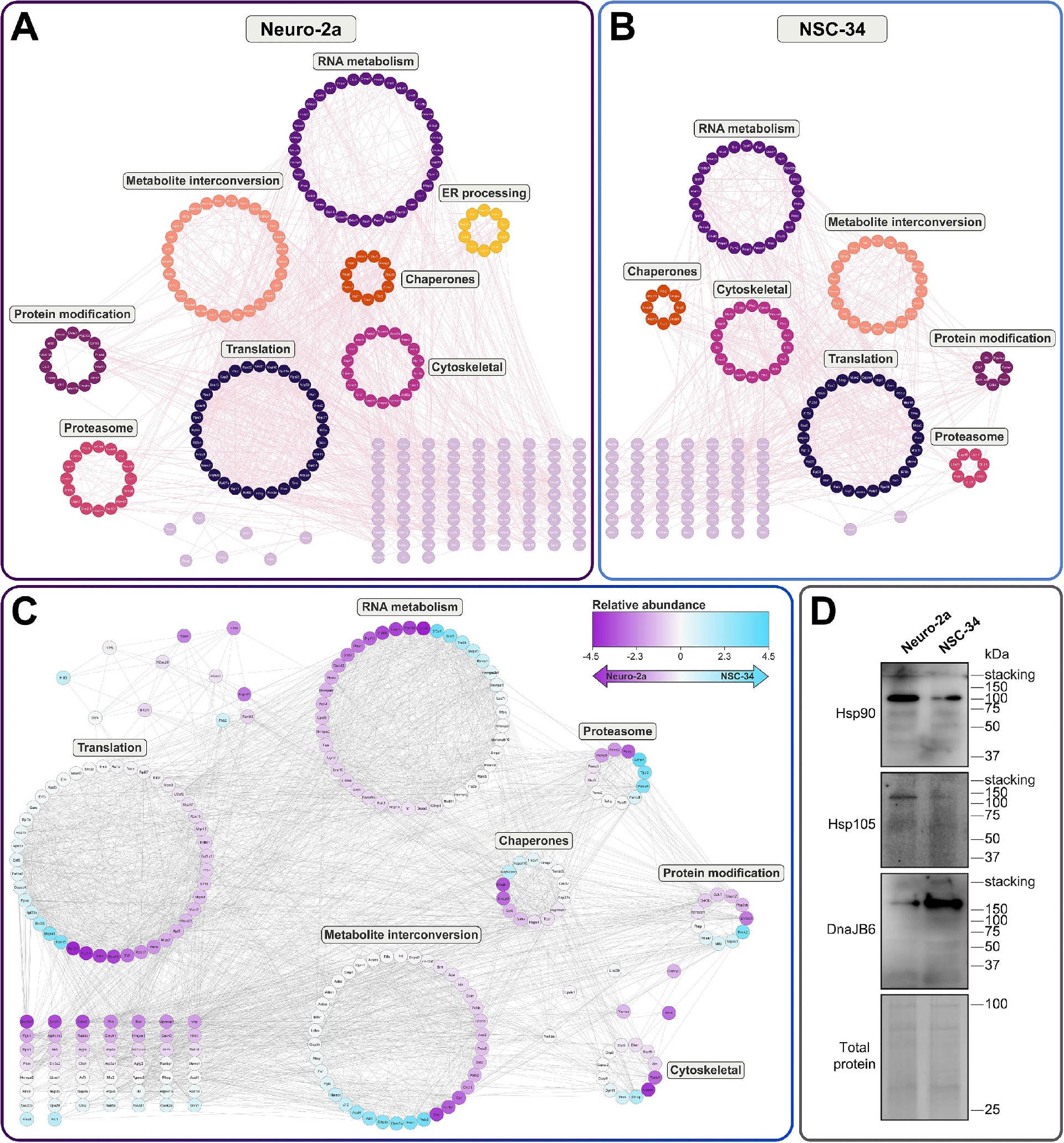
图5:FlucDM 包涵体中蛋白的 STRING 互作分析和关键分子的免疫印迹验证
对 FlucDM 包涵体中的蛋白进行 STRING 互作网络分析并按蛋白类别手动聚类,发现两细胞系的蛋白互作核心均为 RNA 代谢、翻译、蛋白修饰、伴侣蛋白、蛋白酶体降解等相关分子,且蛋白间的相互作用富集具有统计学意义,但存在细胞类型特异性,内质网加工相关蛋白仅在 Neuro-2a 细胞的 FlucDM 包涵体中被鉴定到;选取 Hsp90(两细胞系共有)、Hsp105(仅 Neuro-2a)、DnaJB6(仅 NSC-34)进行免疫印迹验证,结果与蛋白质组学数据一致,Hsp90 在两细胞系的不溶性蛋白组分中均有表达,Hsp105 仅在 Neuro-2a 细胞中检测到,DnaJB6 在 NSC-34 细胞的不溶性组分中高表达,且形成约 250kDa 的复合物。
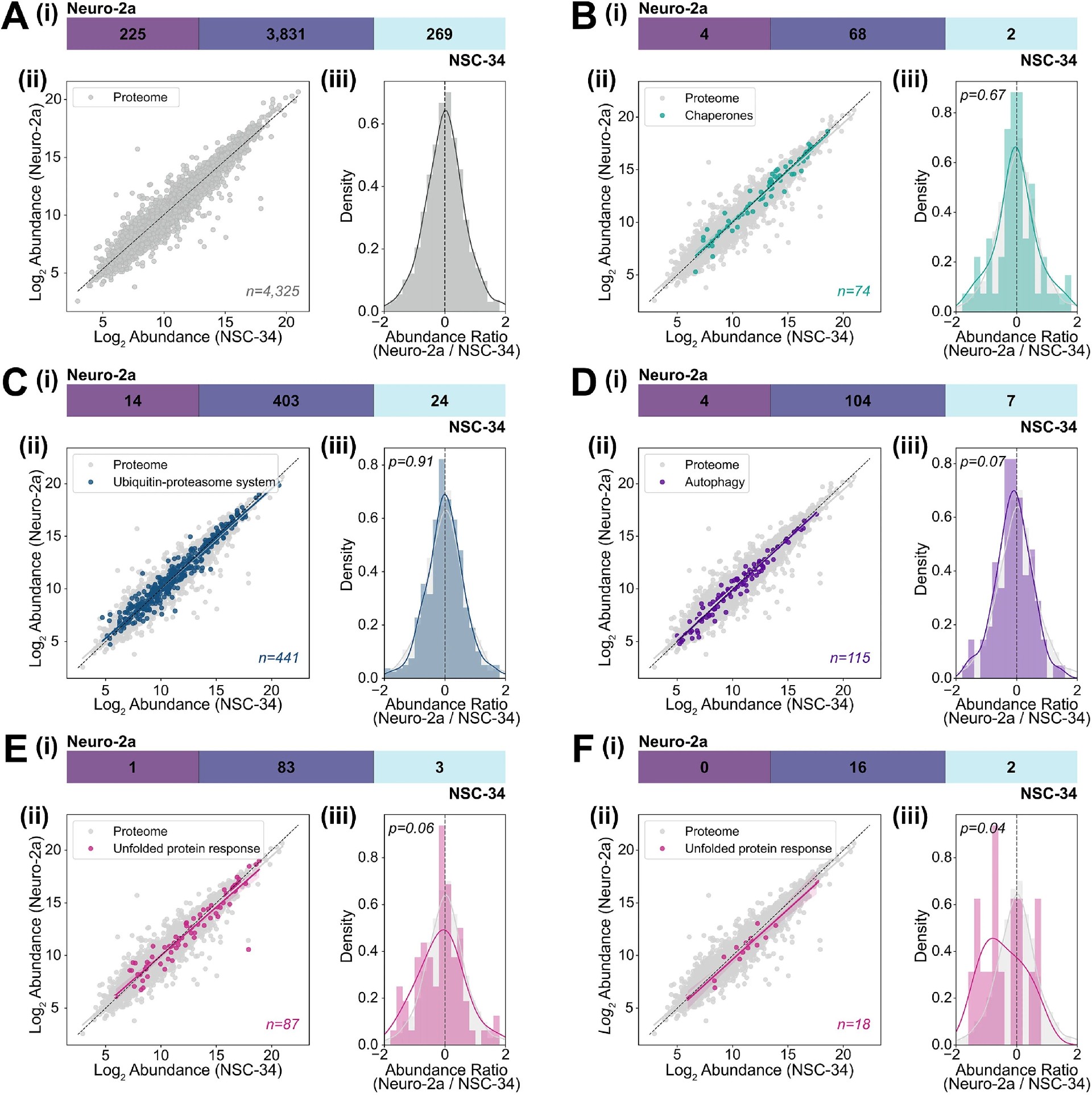
图6:Neuro-2a 和 NSC-34 细胞蛋白质稳态通路的基因本体(GO)映射分析
对两细胞系的全蛋白质组数据进行 GO 映射分析,发现 4325 个鉴定蛋白的表达量在两细胞系中呈强正相关,无整体差异;对蛋白质稳态网络各核心通路的分析显示,伴侣蛋白、泛素 - 蛋白酶体系统、自噬相关蛋白的表达在两细胞系中无显著差异;未折叠蛋白反应相关蛋白的表达虽呈高度相关,但表达比例分布与全蛋白质组相比存在偏移趋势;进一步分析内质网未折叠蛋白反应(ER UPR)的 18 种相关蛋白,发现其表达量在两细胞系中虽相关,但表达比例分布呈显著左偏,与全蛋白质组相比差异具有统计学意义(P=0.04),证实两细胞系的蛋白质稳态能力差异主要源于内质网未折叠蛋白反应的表达特异性。
本研究以易聚集的 FlucDM 为蛋白质稳态报告蛋白,结合共聚焦显微镜和流式细胞术 PulSA 技术,首次定量证实 NSC-34 运动神经元样杂交细胞相比 Neuro-2a 小鼠神经母细胞瘤细胞,对蛋白聚集形成包涵体的易感性更高,其抑制易聚集蛋白聚集、维持蛋白质稳态的能力更弱。通过蛋白质组学分析发现,两种神经元细胞系的 FlucDM 包涵体中结合的蛋白类别整体高度相似,均富集了翻译机制、伴侣蛋白、蛋白酶体组分等蛋白质稳态网络核心分子,同时也包含神经退行性疾病相关蛋白,但存在明显的细胞类型特异性,如内质网加工相关蛋白仅在 Neuro-2a 细胞的包涵体中被鉴定到,免疫印迹实验进一步验证了包涵体中 Hsp90、Hsp105、DnaJB6 等关键稳态蛋白的特异性分布。通过 GO 映射分析对两细胞系的蛋白质稳态网络进行系统解析,发现伴侣蛋白、泛素 - 蛋白酶体系统、自噬等通路的蛋白表达无显著差异,而内质网未折叠蛋白反应相关蛋白的表达存在显著的细胞类型特异性,这是导致两细胞系蛋白质稳态能力差异的核心原因。本研究成功建立了定量评估细胞蛋白质稳态能力的实验平台,阐明了细胞类型背景在蛋白质组维持中的重要性,为理解蛋白质错误折叠疾病中神经元的选择性易感性提供了新的分子见解,也为神经退行性疾病的靶向治疗研究奠定了重要的实验基础。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:酒精相关性肝炎诊断新突破!胆汁酸谱成精准区分关键标志物!
下一篇:正汉坦病毒检测新突破!NanoLuc-LIPS 检测法灵敏度超 97%!