常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-04 17:01:57 细胞资源库平台 访问量:85
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:The lysine methyltransferase SMYD2 methylates the kinase domain of type II receptor BMPR2 and stimulates bone morphogenetic protein signaling
中文标题:赖氨酸甲基转移酶 SMYD2 甲基化 II 型受体 BMPR2 的激酶结构域并刺激骨形态发生蛋白信号传导
发表期刊:《The Journal of Biological Chemistry》(JBC)
影响因子:3.9
作者单位:
1.Shanghai Key Laboratory of Regulatory Biology, the Institute of Biomedical Sciences and School of Life Sciences, East China Normal University, Shanghai 200241, China; the Joint Research Center for Translational Medicine, East China Normal University and Shanghai Fengxian District Central Hospital, Shanghai 201499, China
2.Life Sciences Institute and Innovation Center for Cell Signaling Network, Zhejiang University, Hangzhou, Zhejiang 310058, China
3.Michael E. DeBakey Department of Surgery and Department of Molecular and Cellular Biology, Baylor College of Medicine, Houston, Texas 77030, USA
作者信息:
共同第一作者:Shuman Gao、Zhiqiang Wang
通讯作者:Jiemin Wong(E-mail:jmweng@bio.ecnu.edu.cn)、James X. Du(E-mail:jxdu@bio.ecnu.edu.cn)
赖氨酸甲基化作为表观遗传调控机制在组蛋白中研究已较为深入,但该蛋白修饰在信号转导中的作用尚知之甚少;哺乳动物基因组中存在大量赖氨酸甲基转移酶(KMT),非组蛋白的赖氨酸甲基化现象逐渐被发现,且该修饰可被去甲基化酶动态调控,是潜在的信号转导调控方式,但目前仅少数研究证实其对信号蛋白的调控作用。TGF-β/BMP 超家族细胞因子参与胚胎发育、分化等多种生理过程,其通过结合 I/II 型丝氨酸 / 苏氨酸激酶受体激活下游 SMAD 蛋白,进而调控靶基因表达,TGF-β 主要激活 SMAD2/3,BMP 则激活 SMAD1/5/8,该通路的调控机制尚未完全阐明,仅发现甲基转移酶 SET 可通过甲基化 SMAD7 增强 TGF-β 信号。SMYD 家族 KMT 具有独特的结构特征,且主要定位于细胞质,可能参与信号转导的早期调控,本研究通过 RNAi 筛选 SMYD 家族成员,探究其对 TGF-β/BMP 信号通路的调控作用及分子机制。
本研究以 HaCaT 人角质形成细胞为模型,采用 RNAi 技术敲低 SMYD 家族 5 个成员,通过 qRT-PCR 检测 TGF-β 和 BMP2 靶基因的表达,筛选出调控 BMP 信号的关键成员 SMYD2;构建靶向 SMYD2 的 shRNA 慢病毒载体,建立稳定敲低细胞系,同时利用 CRISPR/Cas9 技术构建 SMYD2 敲除细胞系,通过 qRT-PCR 验证其对 BMP 和 TGF-β 靶基因表达的特异性调控;采用 Western blot 检测 SMYD2 敲低 / 敲除后 BMP2 诱导的 SMAD1/5 磷酸化水平,通过免疫荧光染色观察 SMAD1 的核定位,利用免疫共沉淀检测 SMAD1 与 SMAD4 的相互作用,通过 CCK8 实验检测细胞增殖情况;通过核质分离和免疫荧光确定 SMYD2 的亚细胞定位,使用 SMYD2 特异性抑制剂 AZ505 处理细胞,同时过表达酶活失活型 SMYD2 Y240A 突变体,验证其 KMT 活性对 BMP 信号的必要性;在 293T 细胞中通过免疫共沉淀检测 SMYD2 与 TGF-β/BMP 通路多个组分的相互作用,以及 BMP2 对相互作用的调控;利用泛单 / 双甲基化赖氨酸抗体,结合免疫共沉淀和体外甲基化实验,鉴定 SMYD2 的特异性底物;构建 BMPR2 不同结构域的截短体,通过甲基化检测确定 SMYD2 的甲基化位点。
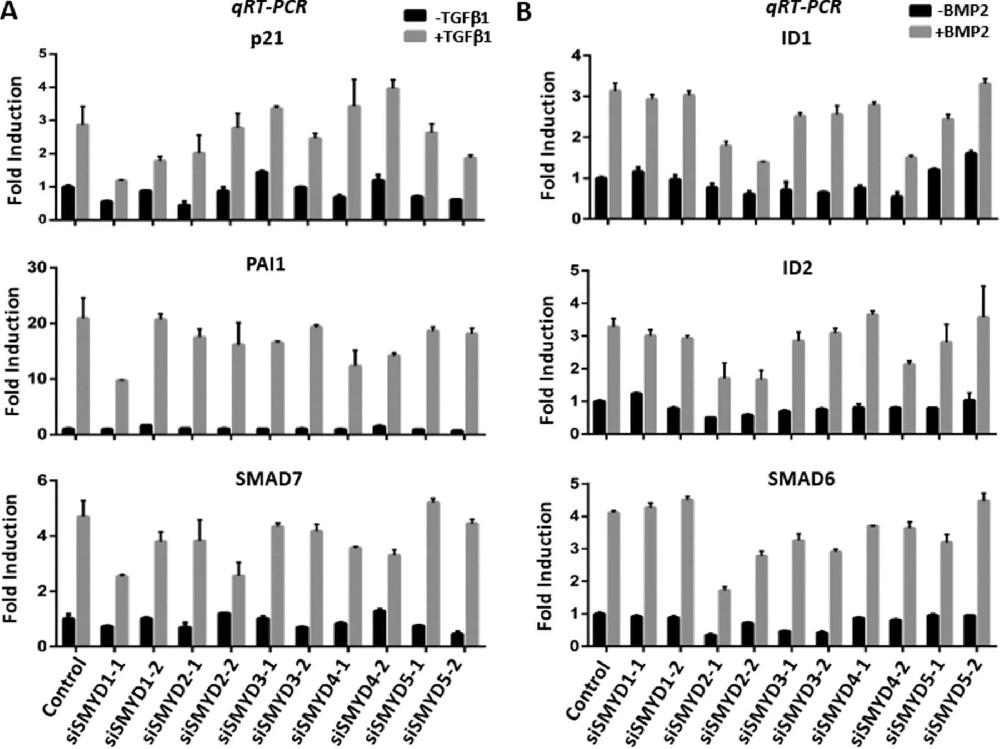
图1:基于 siRNA 的筛选揭示 SMYD2 在 BMP2 诱导的靶基因表达中的特异性作用
该图为 qRT-PCR 检测 SMYD 家族成员敲低后 TGF-β 和 BMP2 靶基因的表达情况;敲低 SMYD1-5 各成员后,TGF-β 诱导的 p21、PAI1、SMAD7 等靶基因表达均无显著变化;而仅 SMYD2 的两个特异性 siRNA 敲低后,BMP2 诱导的 ID1、ID2、SMAD6 等靶基因的基础表达和诱导表达均显著降低,其他 SMYD 家族成员敲低无明显影响,表明 SMYD2 特异性调控 BMP2 信号通路,而非 TGF-β 信号通路。
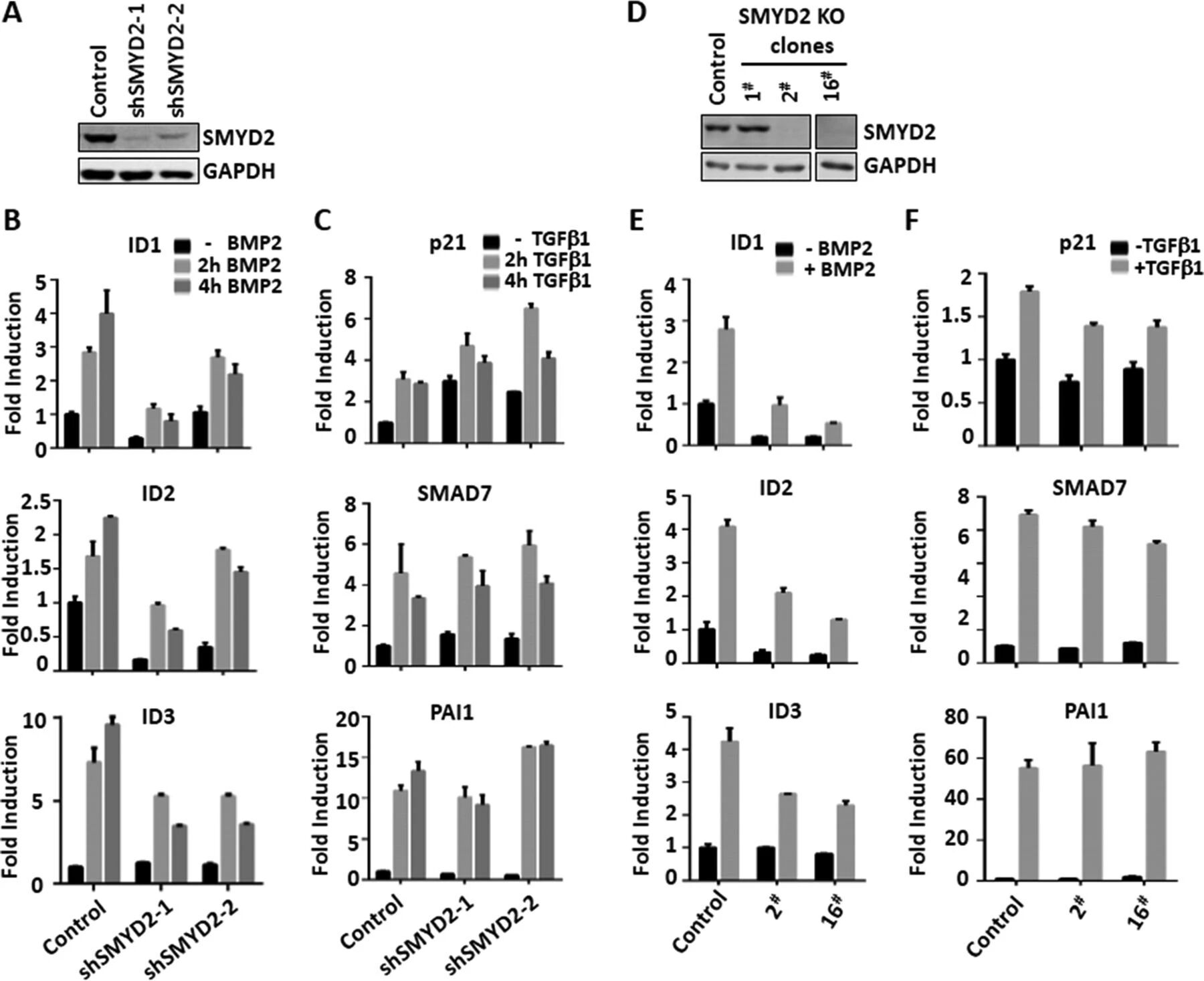
图2:验证 SMYD2 在调控 BMP 而非 TGF-β 信号通路中的作用
该图包含 Western blot 验证 SMYD2 稳定敲低 / 敲除效率,以及 qRT-PCR 检测靶基因表达结果;慢病毒介导的 shRNA 敲低可显著降低 HaCaT 细胞中 SMYD2 的蛋白水平,且敲低后 BMP2 诱导的 ID1、ID2、ID3 表达显著减弱,而 TGF-β 靶基因 p21、SMAD7、PAI1 表达无明显变化;CRISPR/Cas9 构建的 SMYD2 敲除细胞系中检测不到 SMYD2 蛋白,敲除后同样特异性抑制 BMP2 靶基因的激活,对 TGF-β 靶基因无影响,进一步证实 SMYD2 是 BMP 信号通路的特异性正调控因子。
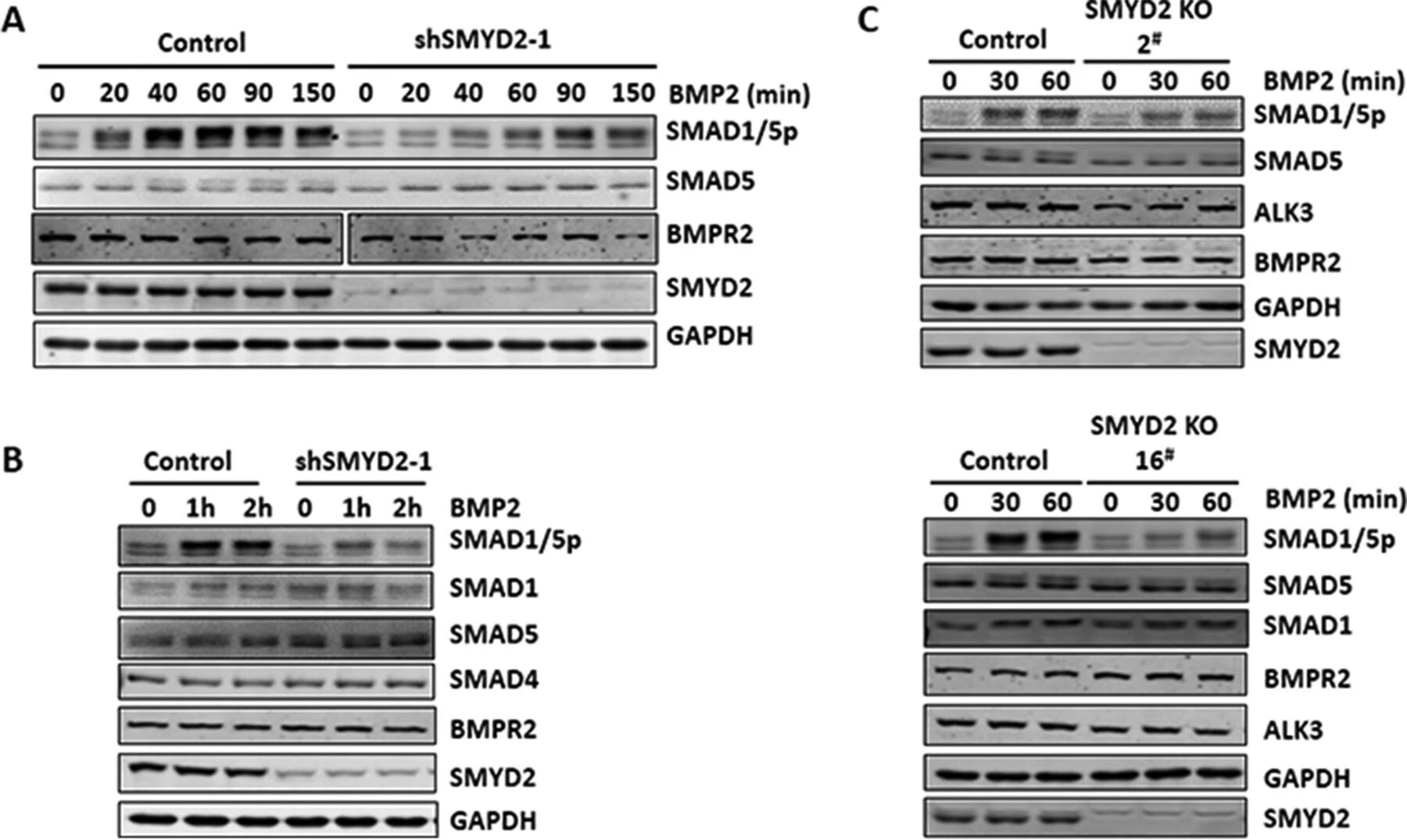
图3:SMYD2 敲低或敲除抑制 BMP2 诱导的 SMAD1/5 磷酸化
该图为 Western blot 检测 SMYD2 敲低 / 敲除后 BMP2 处理不同时间的 SMAD1/5 磷酸化水平;SMYD2 siRNA 和 shRNA 敲低均显著降低 BMP2 诱导的 SMAD1/5 磷酸化,且不影响 SMAD1、SMAD5、SMAD4、BMPR2 等蛋白的基础表达水平;SMYD2 敲除细胞系中,ALK3、BMPR2 等受体蛋白表达正常,但 BMP2 诱导的 SMAD1/5 磷酸化被显著抑制,表明 SMYD2 通过促进 SMAD1/5 的磷酸化调控 BMP 信号通路。
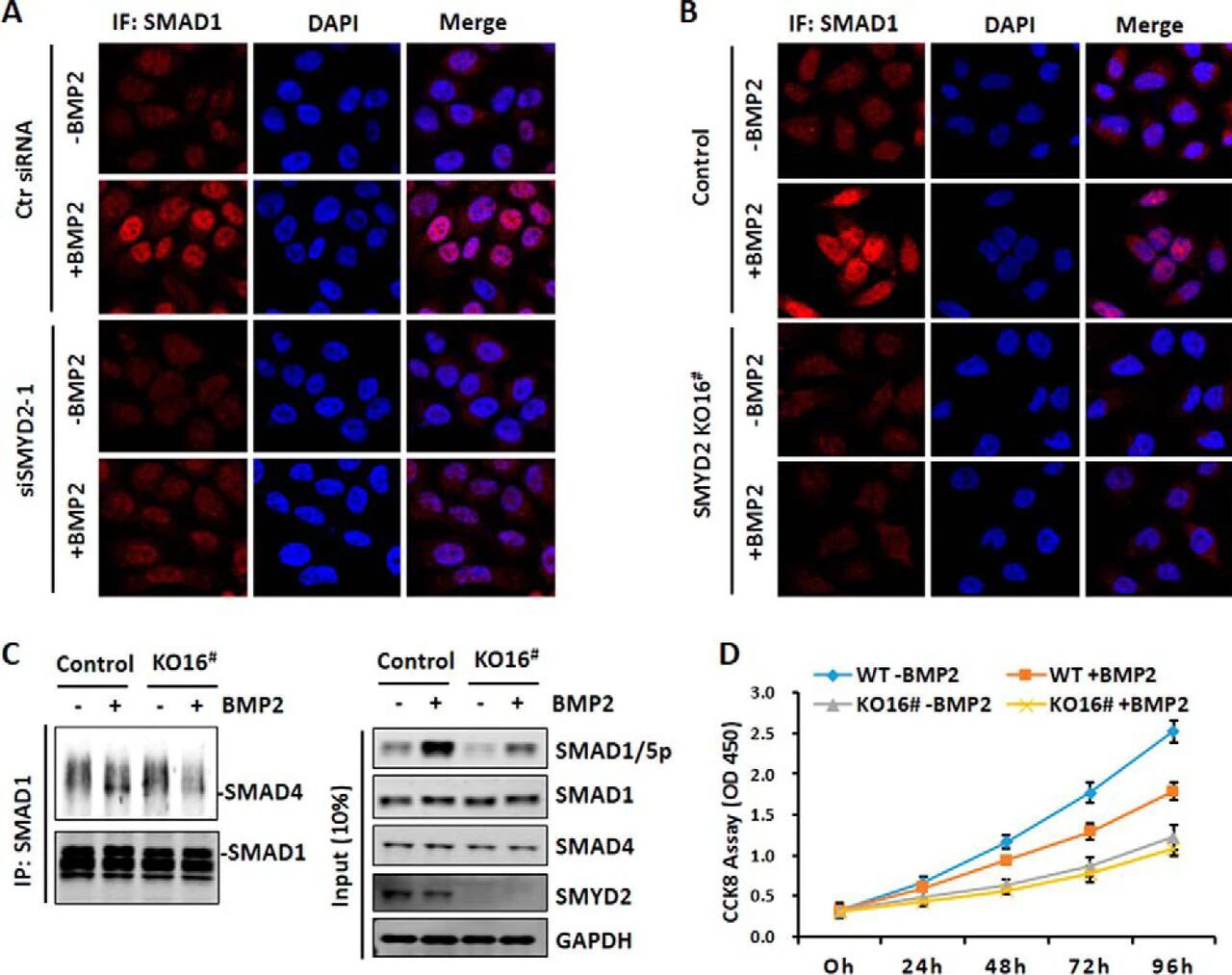
图4:SMYD2 敲低或敲除抑制 BMP2 诱导的 SMAD1/5 核转位、与 SMAD4 的结合及细胞增殖抑制
该图包含免疫荧光、免疫共沉淀和细胞增殖实验结果;免疫荧光显示,SMYD2 敲低和敲除均显著减少 BMP2 诱导的 SMAD1 核内积累;免疫共沉淀实验表明,BMP2 可促进野生型细胞中 SMAD1 与 SMAD4 的结合,而 SMYD2 敲除细胞中该相互作用显著减弱;CCK8 实验显示,SMYD2 敲除本身会轻微降低细胞增殖,且 BMP2 对野生型细胞的增殖抑制作用在敲除细胞中完全消失,表明 SMYD2 介导 BMP2 的生物学功能。
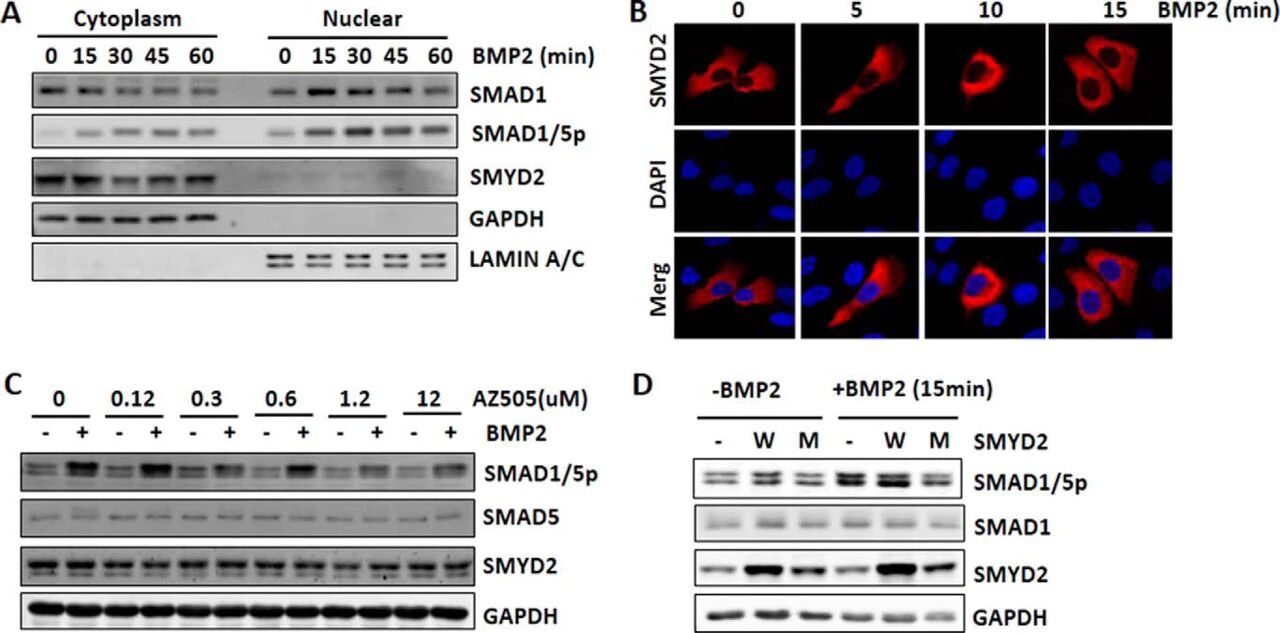
图5:SMYD2 在细胞质中以 KMT 活性依赖的方式调控 BMP 信号转导
该图包含核质分离、免疫荧光、抑制剂处理和突变体过表达实验结果;核质分离和免疫荧光均证实,SMYD2 始终定位于细胞质,不受 BMP2 处理的影响,表明其在细胞质中调控 BMP 信号;SMYD2 特异性抑制剂 AZ505 以剂量依赖的方式抑制 BMP2 诱导的 SMAD1/5 磷酸化,且不影响相关蛋白表达;过表达野生型 SMYD2 可增强 BMP2 诱导的 SMAD1/5 磷酸化,而过表达酶活失活的 Y240A 突变体则显著抑制该磷酸化,证实 SMYD2 的甲基转移酶活性是其调控 BMP 信号的必要条件。
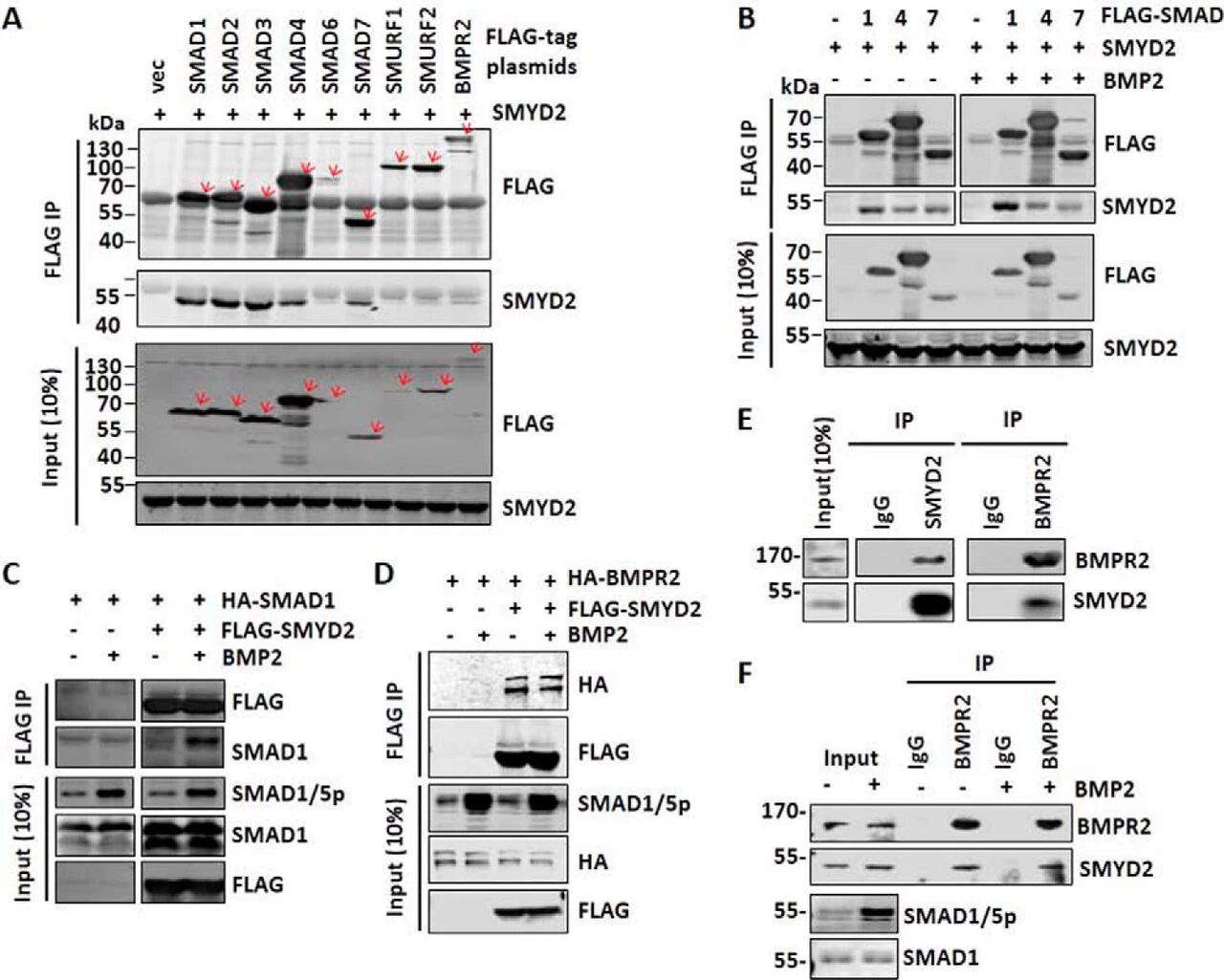
图6:SMYD2 与 TGF-β/BMP 信号通路的多个组分相互作用
该图为一系列免疫共沉淀实验结果;SMYD2 可与 SMAD1-4、SMAD7、SMURF2、BMPR2 等多个通路组分相互作用,且单独表达时不被 FLAG 抗体沉淀,证实相互作用的特异性;BMP2 处理可显著增强 SMYD2 与 SMAD1 的相互作用,对 SMYD2 与 SMAD4、SMAD7 的相互作用无影响,该结果经反向免疫共沉淀验证;SMYD2 与 BMPR2 的相互作用经反向免疫共沉淀证实,且该相互作用为组成型,不受 BMP2 处理调控;内源性蛋白水平也证实 SMYD2 与 BMPR2 存在相互作用,且不依赖 BMP2 刺激。
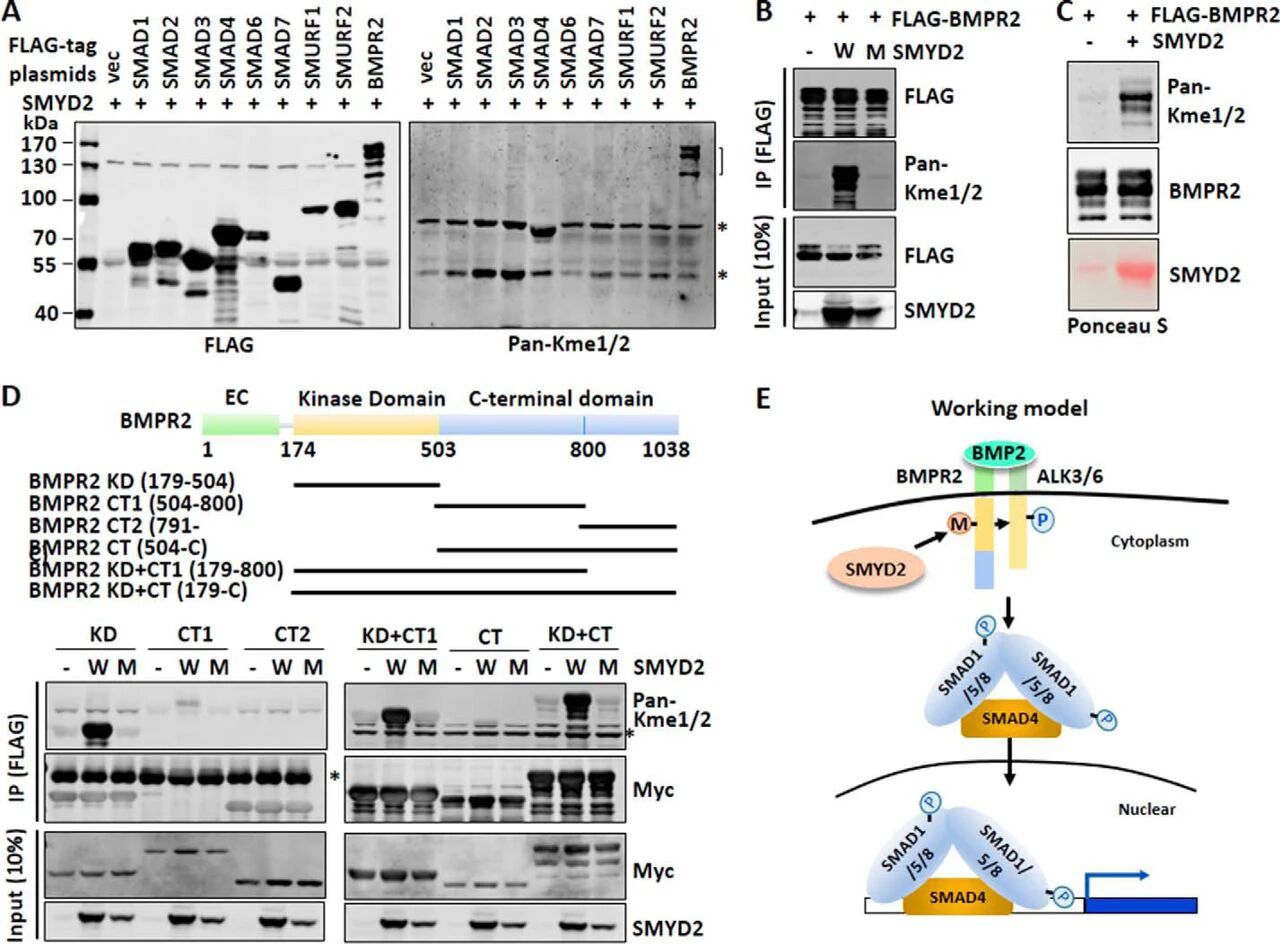
图7:SMYD2 特异性甲基化 BMPR2 的激酶结构域
该图包含甲基化检测、体外甲基化实验、截短体验证及工作模型;利用泛单 / 双甲基化赖氨酸抗体检测发现,SMYD2 可特异性甲基化 BMPR2,对其他相互作用的通路组分无甲基化作用;该甲基化依赖 SMYD2 的酶活,Y240A 突变体无法介导 BMPR2 的甲基化;体外甲基化实验证实,重组 SMYD2 可直接甲基化纯化的 BMPR2;BMPR2 截短体验证显示,SMYD2 优先甲基化 BMPR2 的激酶结构域,C 端结构域仅有微弱的甲基化信号;最后提出工作模型:SMYD2 在细胞质中与 BMPR2 结合并甲基化其激酶结构域,增强 BMPR2 的激酶活性,进而促进 I 型受体的磷酸化,激活下游 SMAD1/5 的磷酸化、核转位及与 SMAD4 的结合,最终调控 BMP 靶基因表达。
本研究通过 RNAi 全家族筛选发现,赖氨酸甲基转移酶 SMYD2 是 BMP 信号通路的特异性正调控因子,对 TGF-β 信号通路无明显调控作用,该结果经 shRNA 稳定敲低和 CRISPR/Cas9 敲除实验验证;SMYD2 通过促进 BMP2 诱导的 SMAD1/5 磷酸化,调控其核转位及与 SMAD4 的相互作用,进而介导 BMP2 的靶基因激活和细胞增殖抑制等生物学功能;SMYD2 定位于细胞质,其甲基转移酶活性是调控 BMP 信号的必要条件,抑制剂 AZ505 和酶活失活突变体均可抑制 BMP 信号;SMYD2 可与 TGF-β/BMP 通路多个组分相互作用,但仅特异性甲基化 II 型受体 BMPR2,且优先甲基化其激酶结构域,体外实验证实 SMYD2 可直接甲基化 BMPR2;本研究提出 SMYD2 调控 BMP 信号的工作模型,即 SMYD2 通过甲基化 BMPR2 的激酶结构域增强其激酶活性,进而激活下游 SMAD 通路,该发现揭示了赖氨酸甲基化在 BMP 信号转导中的新机制,拓展了非组蛋白甲基化在膜受体信号调控中的研究,同时为 SMYD 家族蛋白的功能研究提供了新方向。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:酒制诱导黄精多糖结构修饰并通过菌群介导的丁酸代谢增强Tc1细胞免疫调节活性
下一篇:iPSC 衍生肝类器官:预测 AAV 基因治疗转导效率与安全性的新型体外平台