常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-04 00:00:00 细胞资源库平台 访问量:165
英文标题:Wine processing induced structural modification of Polygonati Rhizoma polysaccharide and their enhancement of Tc1 cell immunomodulatory activity via microbiota-mediated butyrate metabolism
中文标题:酒制诱导黄精多糖结构修饰并通过菌群介导的丁酸代谢增强Tc1细胞免疫调节活性
发表期刊:《Carbohydrate Polymers》
影响因子:12.5
作者单位:
中国中医科学院中医基础理论研究所
香港浸会大学中医药学院
作者信息:
Fenghe Yang, Chun Wang, Zhiqian Song, Shitao Peng, Ziqi Tian, Wenjie Lu, Tao Lin, Qiao He, Aiping Lyu, Zhangchi Ning
黄精(Polygonati Rhizoma)作为一种药食同源的中药,其多糖成分具有显著的免疫调节活性。在中国传统医学中,黄精经酒制后被认为能增强其补益功效,尤其是免疫增强作用。
尽管酒制增效的临床经验丰富,但酒制如何改变黄精多糖(PRP)的精细化学结构,以及结构变化如何影响其免疫调节活性,其潜在机制尚不明确。
研究创新点:
本研究首次系统地揭示了酒制对黄精多糖的“结构重塑”作用,并从“多糖-肠道菌群-代谢物-免疫轴”的角度,阐明了酒制黄精多糖(WPRP)通过选择性富集产丁酸菌、促进丁酸生成,进而特异性激活CD8+ T细胞亚群(Tc1)并增强肠道屏障功能的免疫增强新机制。这一发现为传统中药炮制理论的现代化解读提供了科学依据。
研究方法
1.多糖提取与纯化:
原料:生黄精(PR)和酒制黄精(WPR)。
提取:水提醇沉法获得粗多糖。
纯化:通过DEAE-52离子交换层析和BRT-75凝胶过滤层析,从<50 kDa的组分中分别纯化得到PRP和WPRP。
2.多糖结构表征:
分子量测定:采用高效凝胶渗透色谱法(HPGPC)。
单糖组成分析:采用高效离子色谱法(HPIC)。
糖苷键连接分析:采用甲基化结合气相色谱-质谱联用(GC-MS)分析。
核磁共振分析:采用1D/2D NMR(1H, 13C, DEPT, COSY, HSQC, HMBC, NOESY)解析多糖的精细结构。
3.动物实验:
模型:使用环磷酰胺(CTX)诱导的免疫抑制BALB/c小鼠模型。
分组:正常组、模型组、阳性药(盐酸左旋咪唑)组、PRP低/高剂量组、WPRP低/高剂量组。
指标:体重、脏器指数、HE染色(肠组织)、ELISA(血清免疫球蛋白IgA, IgG, IgM)、粪便白蛋白(肠通透性)。
4.肠道菌群分析:
16S rRNA测序:分析菌群组成和丰度变化。
宏基因组测序:深入分析菌群物种和功能基因(KEGG通路)。
短链脂肪酸(SCFAs)检测:
方法:采用超高效液相色谱-三重四极杆质谱联用(UHPLC-TQ-MS)检测粪便中丁酸等SCFAs含量。
5.流式细胞术:
样本:小鼠结肠组织。
标志物:分析淋巴细胞、T细胞、B细胞及T细胞亚群(Th1, Th2, Th17, Treg, Tc1, Tc2, Tc17等)的比例。
6.体外共培养体系:
细胞:NCM460人正常结肠上皮细胞与Tc1细胞。
干预:使用含药血清(PRP/WPRP)及丁酸钠(模拟丁酸)。
检测:流式细胞术检测IL-1β,免疫荧光检测紧密连接蛋白(ZO-1和Occludin)的表达。
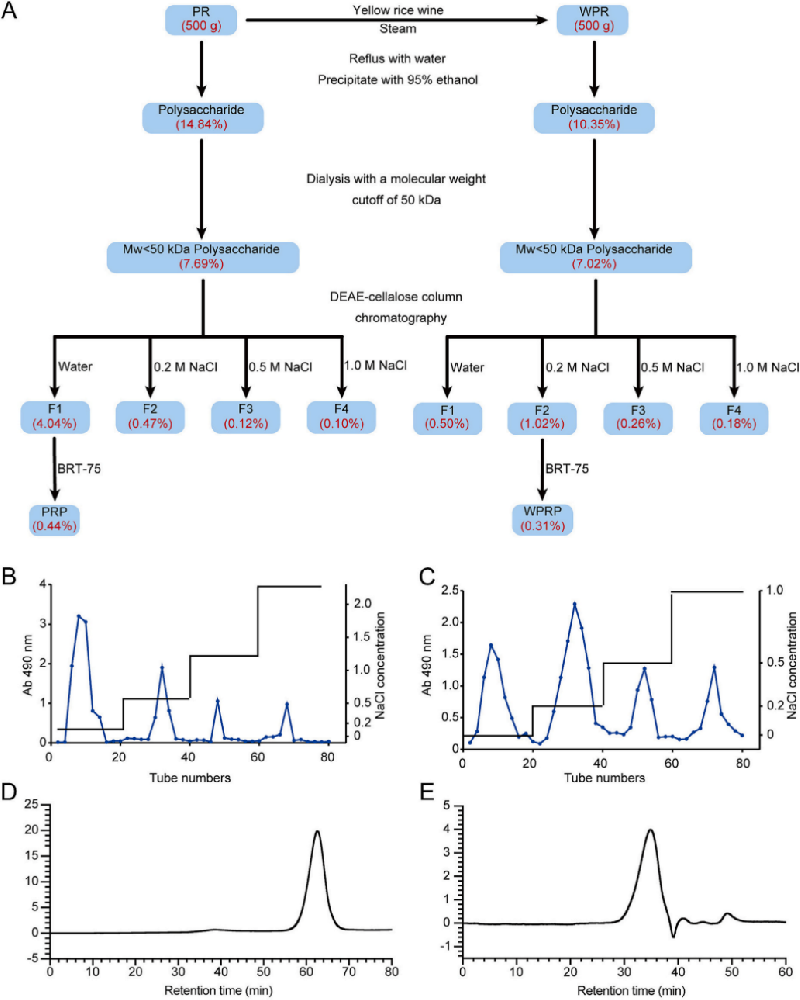
图1 | 研究概览与多糖纯化流程
(A)PRP和WPRP的提取、分离、纯化流程图。(B)黄精生品和酒制品的外观。
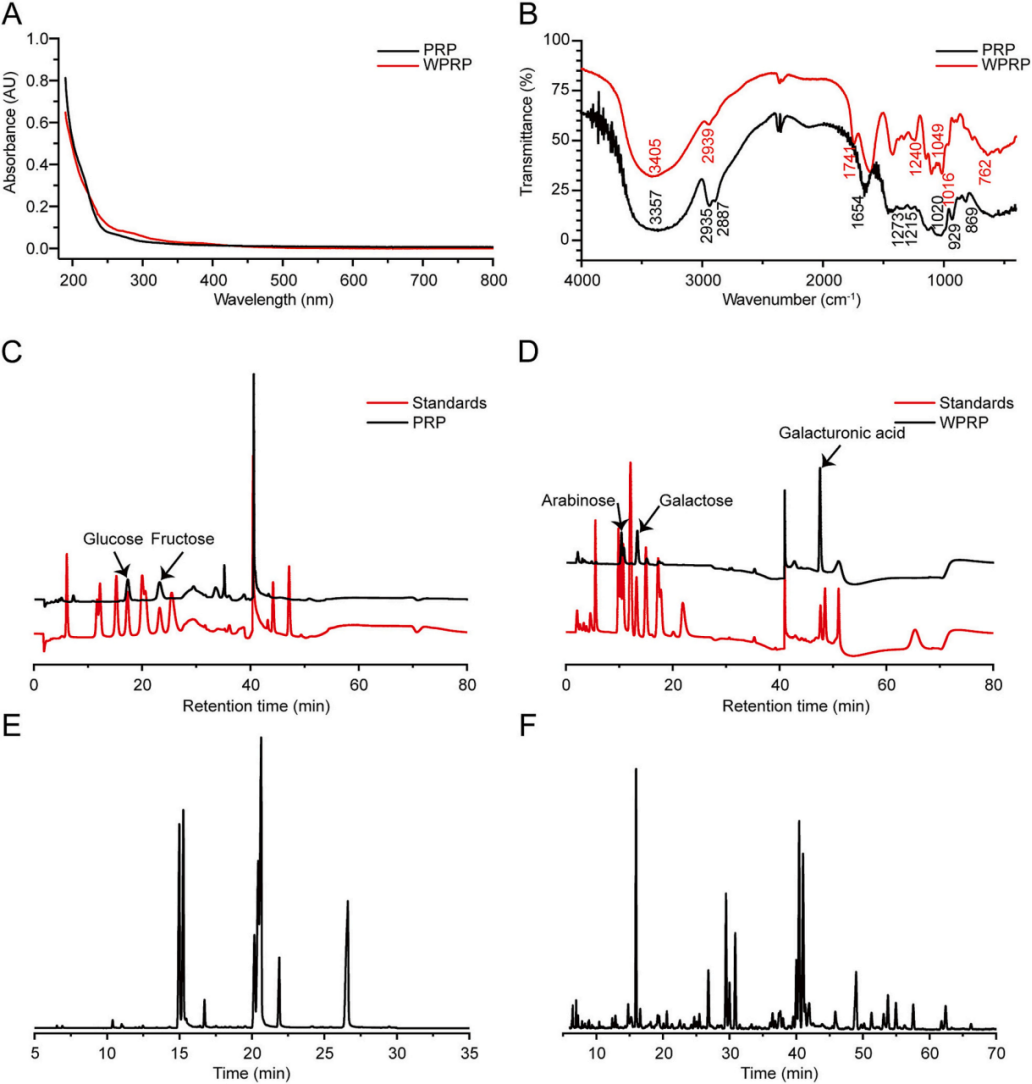
图2 | PRP和WPRP的UV-vis、FT-IR、单糖组成及甲基化分析
(A)UV-vis光谱。(B)FT-IR光谱。(C和D)PRP和WPRP的单糖组成。(E和F)PRP和WPRP的甲基化分析。
揭示了酒制导致多糖的单糖组成发生根本性变化,PRP以果糖和葡萄糖为主,而WPRP则富含半乳糖醛酸、半乳糖和阿拉伯糖。
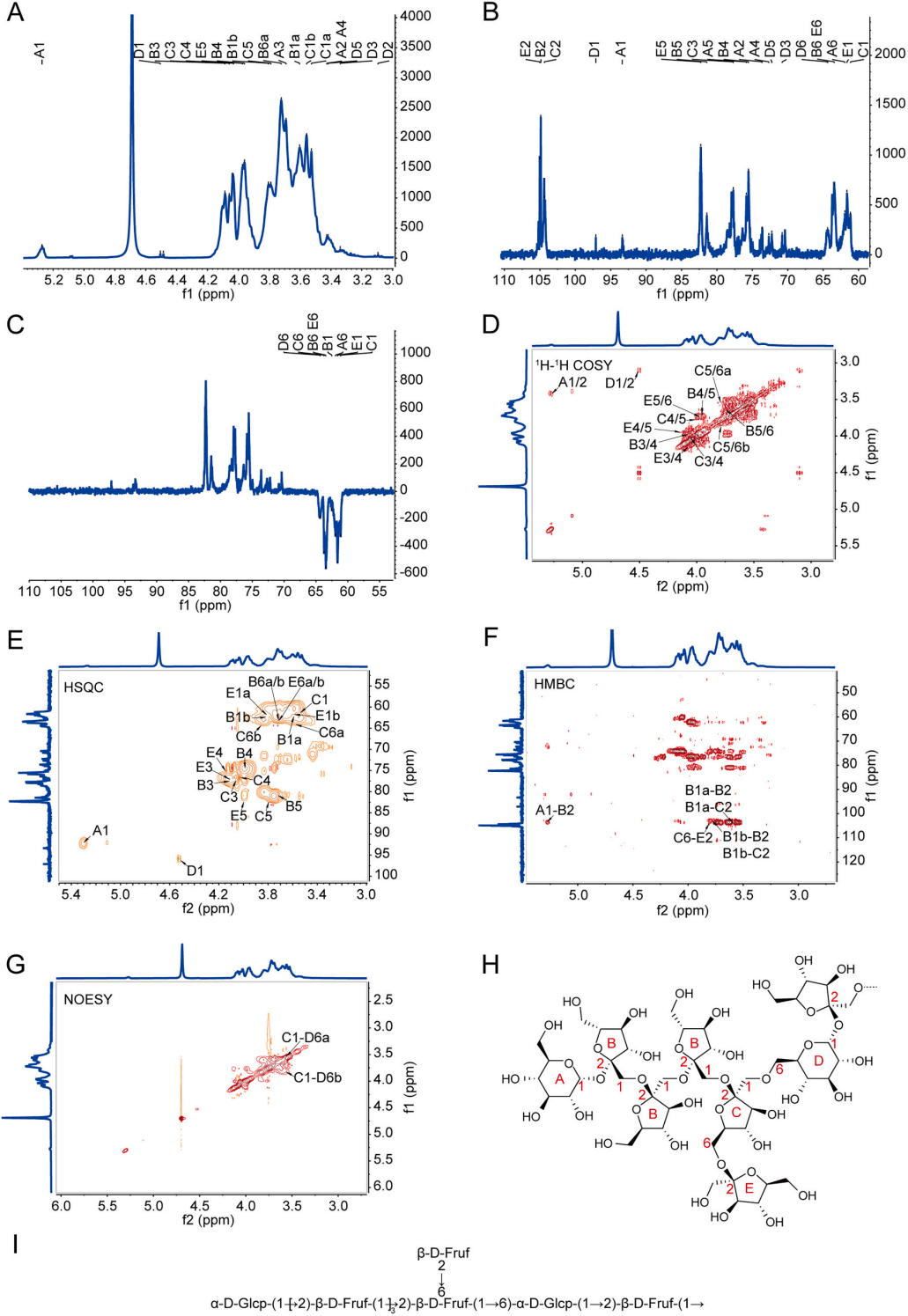
图3 | PRP的核磁共振分析
(A)1H NMR。(B)13C NMR。(C)DEPT 135。(D)1H-1H COSY。(E)HSQC。(F)HMBC。(G)NOESY。(H和I)PRP的结构示意图。
图3通过多维核磁共振技术解析了PRP的精细结构,其主链为α-D- Glcp → [2)-β-D-Fruf-(1) → 2)-β-D-Fruf-(1 → 6)-α-D-Glcp-(1 → 2)-β-D-Fruf →,是一种低分子量(1.85 kDa)的果聚糖。
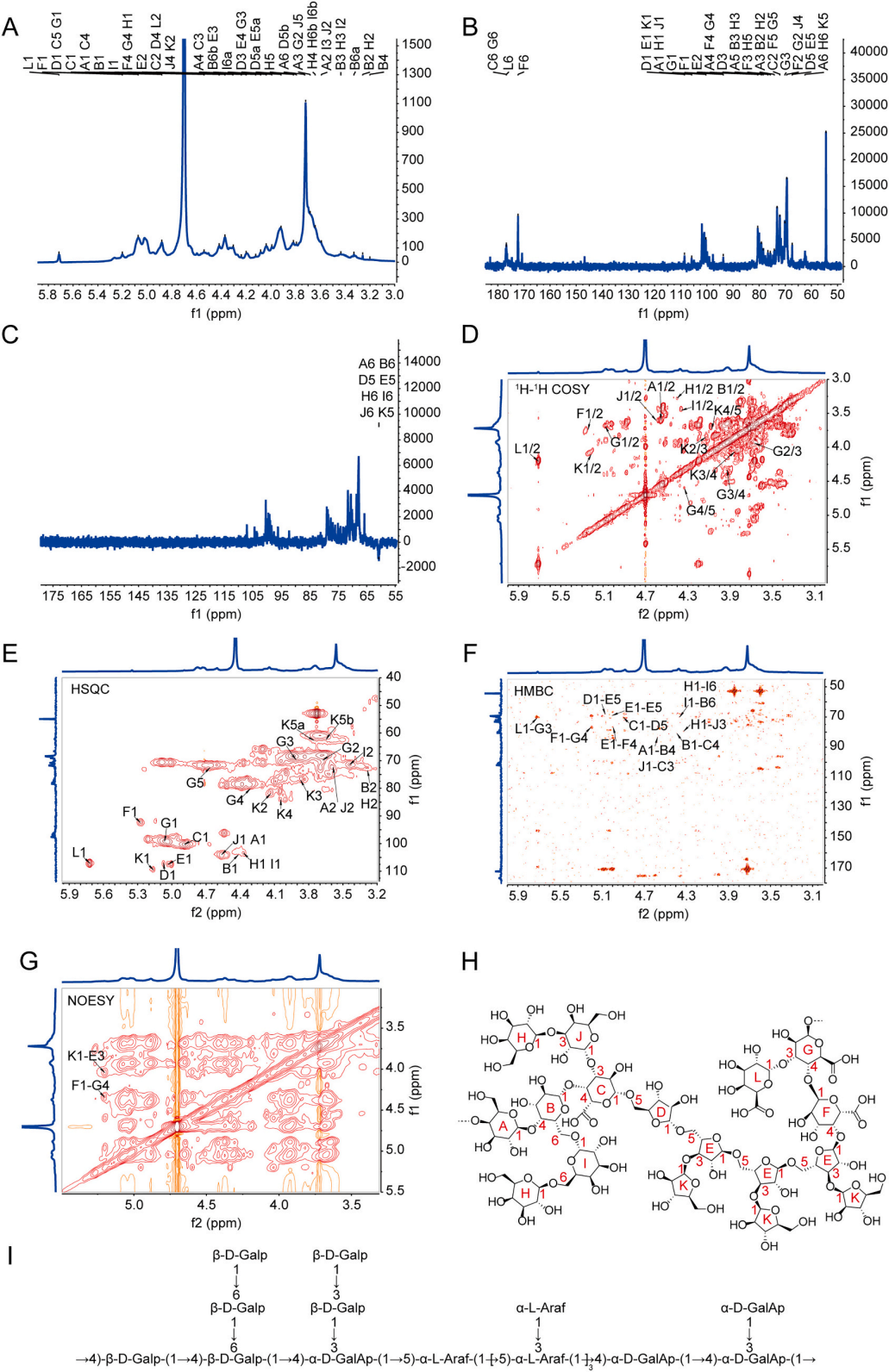
图4 | WPRP的核磁共振分析
(A)1H NMR。(B)13C NMR。(C)DEPT 135。(D)1H-1H COSY。(E)HSQC。(F)HMBC。(G)NOESY。(H和I)WPRP的结构示意图。
图4解析了WPRP的精细结构,其主链为→4)-β-D-Galp-(1 → 4)-β-D-Galp-(1 → 4)-α-D-GalAp-(1 → 5)-α-L-Araf-(1 → 4)-α-D-GalAp-(1 → 4)-α-D-GalAp-(1 →,是一种高分子量(7.31 kDa)、富含半乳糖醛酸的果胶类多糖。
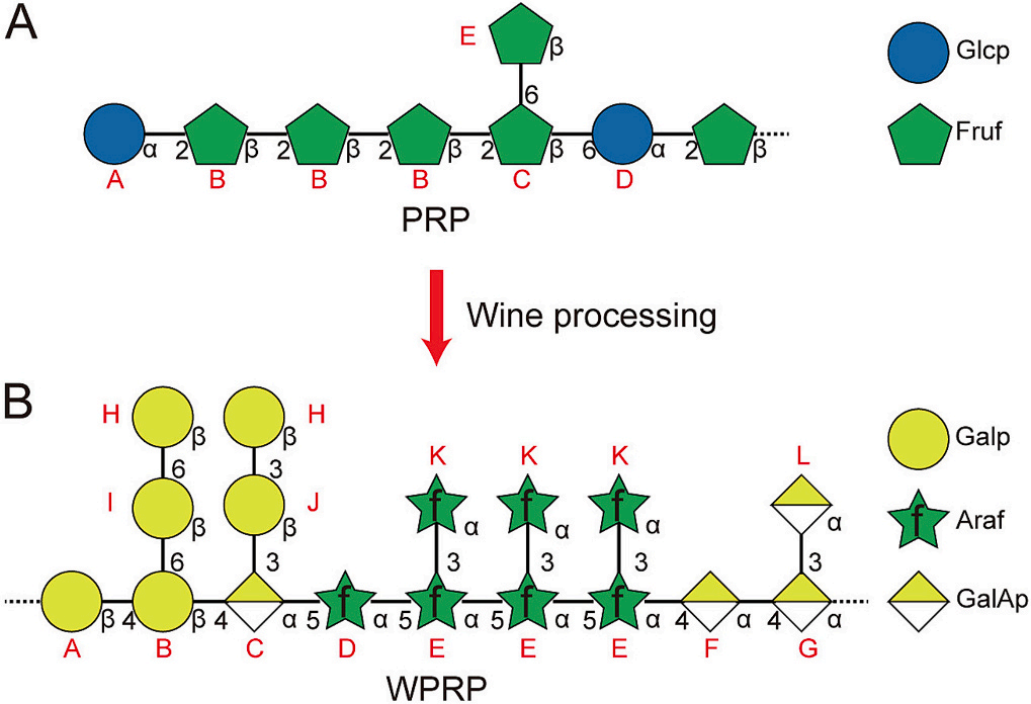
图5 | PRP与WPRP的糖结构符号表示(SNFG)对比
(A)PRP的SNFG表示。(B)WPRP的SNFG表示。
图5直观地对比了PRP(A)和WPRP(B)的结构差异,清晰地展示了酒制从果聚糖到果胶多糖的结构转变。
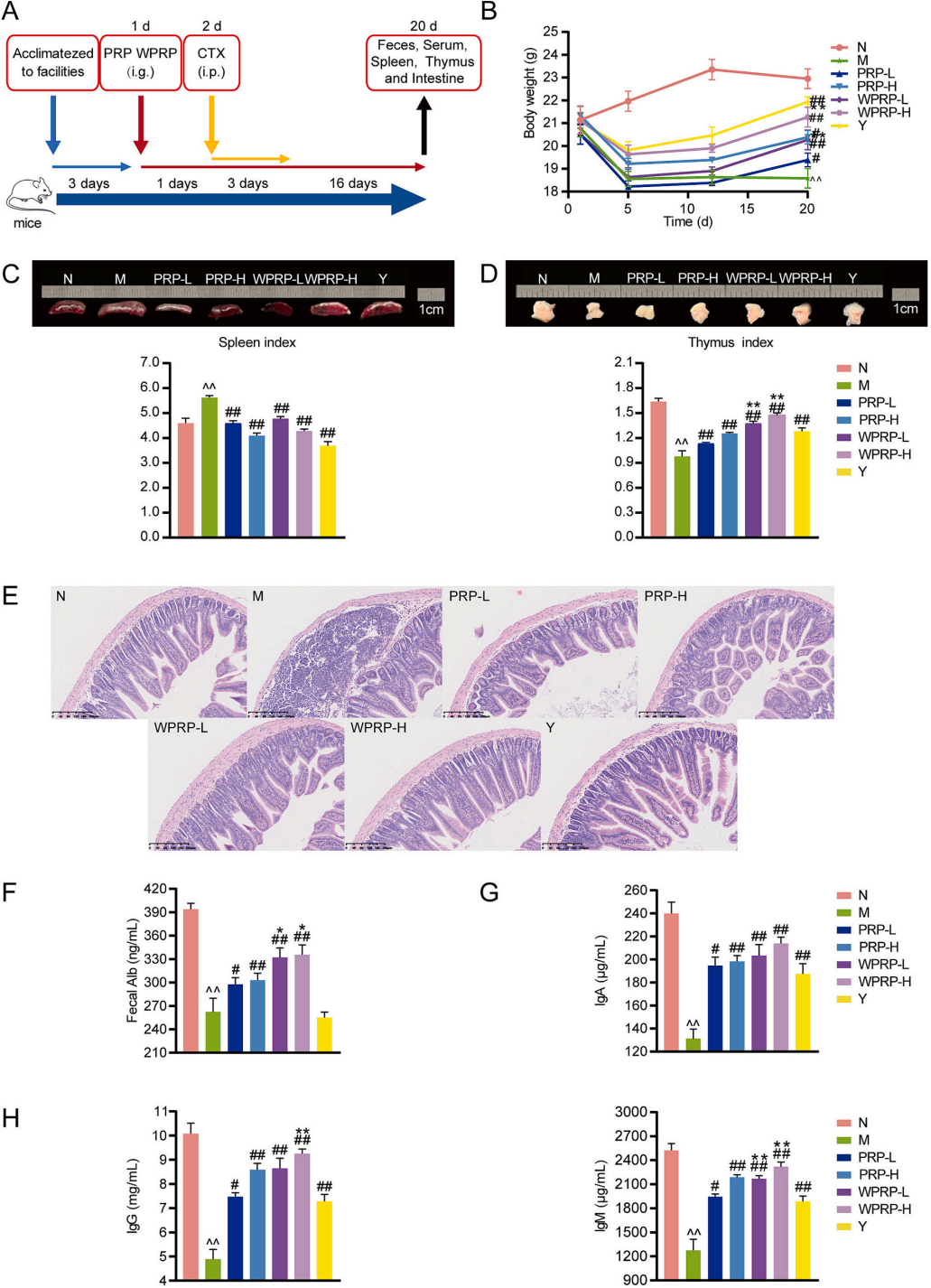
图6 | PRP和WPRP改善CTX诱导的免疫抑制小鼠症状
(A)实验流程图。(B)体重。(C)脾脏指数。(D)胸腺指数。(E)HE染色(10×),比例尺=40 μm。(F)粪便白蛋白。(G和H)IgA、IgG和IgM。与N组相比,^P< 0.01;与M组相比,#P< 0.05,##P< 0.01;与PRP组相比,*P< 0.05,**P< 0.01。
图6显示WPRP比PRP更能有效地恢复免疫抑制小鼠的体重、脏器指数、肠道屏障功能和血清免疫球蛋白水平,改善肠道病理损伤。
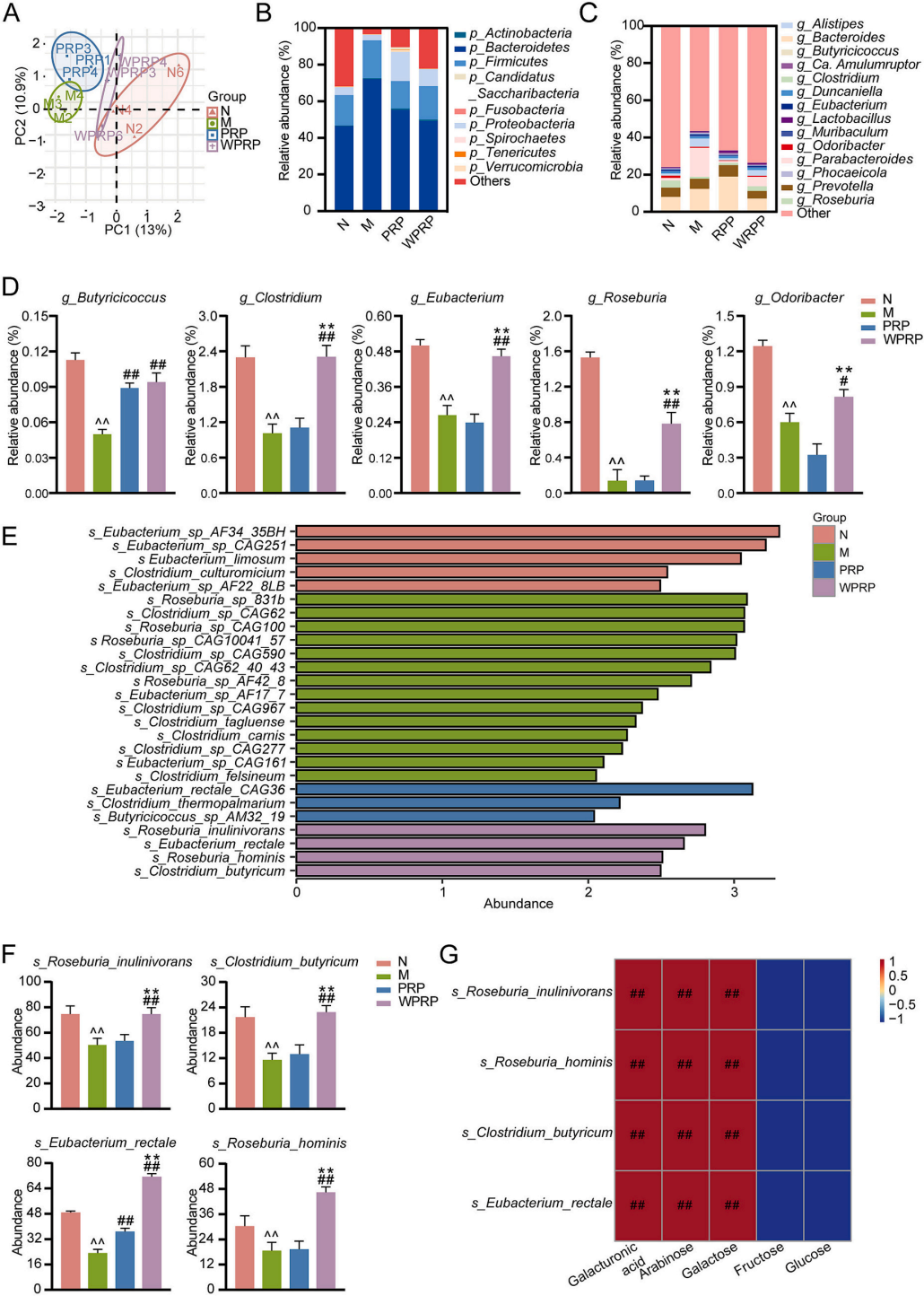
图7 | PRP和WPRP增加免疫抑制小鼠中产丁酸菌的丰度
(A)主成分分析(PCA)。(B)门水平菌群组成。(C)属水平菌群组成。(D)属水平产丁酸菌丰度。(E)线性判别分析(LDA)。(F)种水平产丁酸菌丰度。(G)产丁酸菌与单糖的相关性分析。与N组相比,^P< 0.05,^^P< 0.01;与M组相比,#P< 0.05,##P< 0.01;与PRP组相比,*P< 0.05,**P< 0.01。
图7表明WPRP能特异性富集Clostridium butyricum、Roseburia hominis等产丁酸菌,并且这些菌的丰度与WPRP中的阿拉伯糖、半乳糖和半乳糖醛酸结构呈正相关。
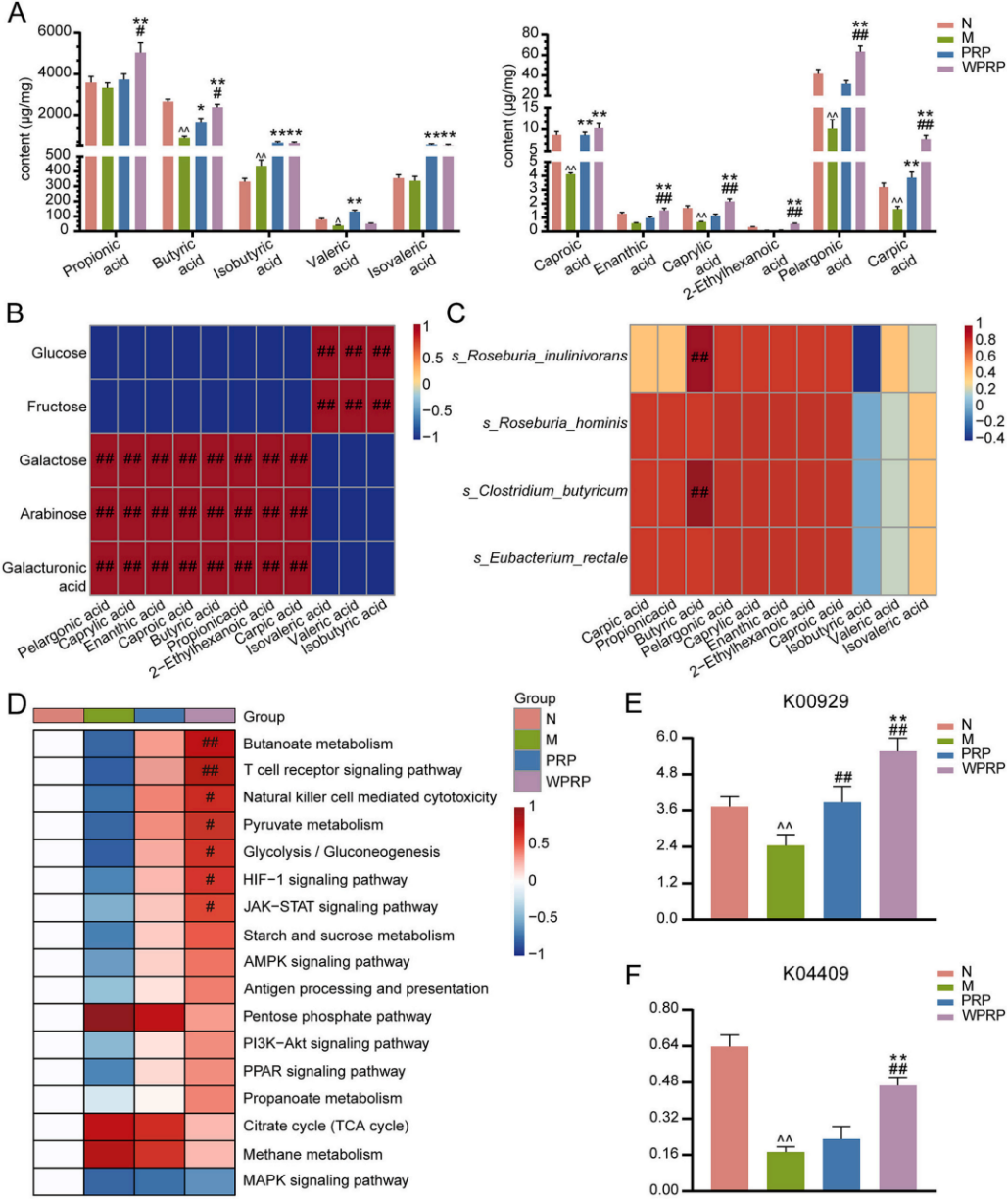
图8 | PRP和WPRP影响免疫抑制小鼠肠道丁酸水平和丁酸代谢
(A)短链脂肪酸(SCFAs)含量。(B)SCFAs与单糖的相关性。(C)SCFAs与产丁酸菌的相关性。(D)KEGG通路富集分析。(E)K00929(丁酸代谢相关蛋白)表达。(F)K04409(T细胞信号通路相关蛋白)表达。与N组相比,^P< 0.05,^^P< 0.01;与M组相比,#P< 0.05,##P< 0.01;与PRP组相比,*P< 0.05,**P< 0.01。
图8显示WPRP处理能显著提高粪便丁酸水平,激活丁酸代谢通路,并且这种变化与T细胞受体信号通路的激活同步。
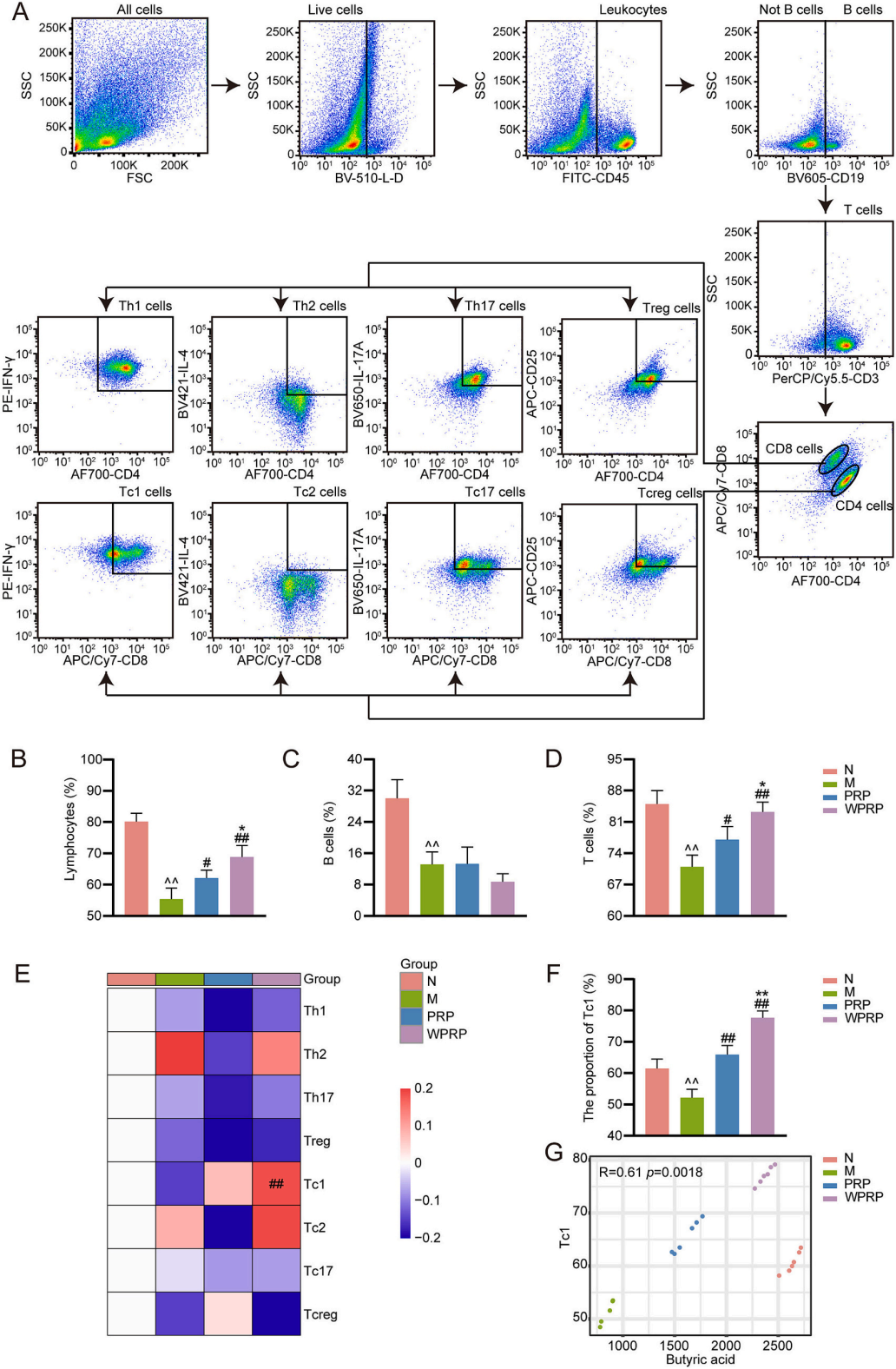
图9 | PRP和WPRP通过调节Tc1细胞亚群改善免疫抑制
(A)流式细胞术设门策略。(B)淋巴细胞。(C)B细胞。(D)T细胞。(E)T细胞亚群的Heatmap分析。(F)Tc1细胞。(G)丁酸与Tc1细胞的相关性分析。与N组相比,^P< 0.01;与M组相比,#P< 0.05,##P< 0.01;与PRP组相比,*P< 0.05,**P< 0.01。
图9揭示了PRP和WPRP主要影响T细胞,尤其是Tc1细胞。WPRP能更有效地恢复Tc1细胞比例,并且Tc1细胞比例与肠道丁酸水平呈正相关。
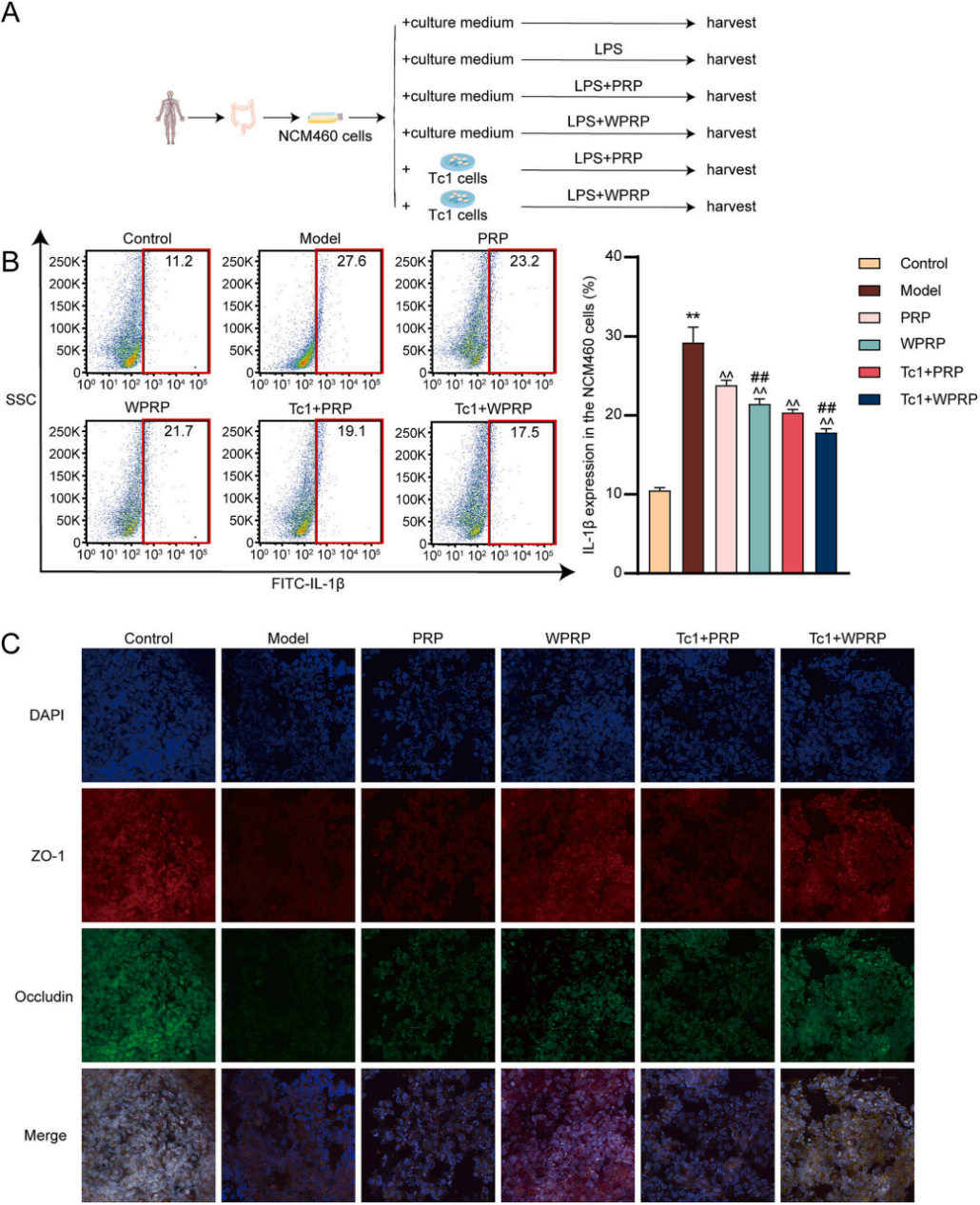
图10 | PRP和WPRP通过调节Tc1细胞增强抗炎作用和肠道屏障修复
(A)实验流程图。(B)IL-1β。(C)ZO-1和Occludin。与对照组相比,**P< 0.01;与模型组相比,##P< 0.01;与PRP组相比,&&P< 0.01。
图10在体外NCM460/Tc1共培养模型中证实,WPRP能更显著地降低促炎因子IL-1β的表达,并恢复紧密连接蛋白ZO-1和Occludin的水平,这些作用依赖于Tc1细胞。
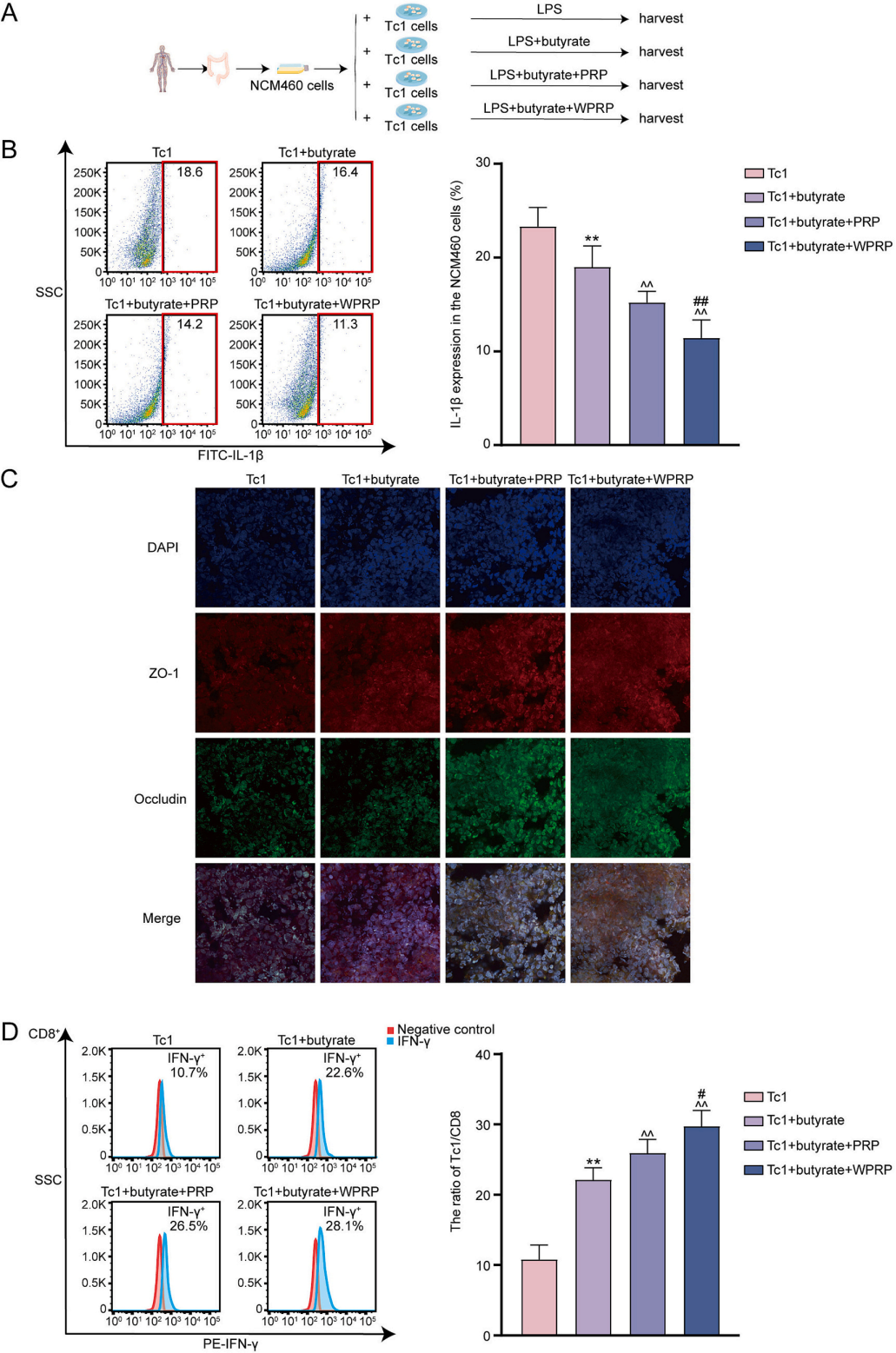
图11 | PRP和WPRP与丁酸协同,通过调节Tc1细胞增强肠道上皮保护作用
(A)实验流程图。(B)IL-1β。(C)ZO-1和Occludin。(D)Tc1细胞比例。与Tc1组相比,**P< 0.01;与Tc1 + 丁酸组相比,^^P< 0.01;与Tc1 + 丁酸 + PRP组相比,#P< 0.05,##P< 0.01。
图11进一步证明,WPRP与丁酸在增强肠道上皮保护和促进Tc1细胞分化方面具有协同作用,且效果优于PRP。
1.结构重塑:酒制显著改变了黄精多糖的结构。PRP是一种低分子量(1.85 kDa)的菊粉型果聚糖,而WPRP则转变为高分子量(7.31 kDa)、富含半乳糖醛酸、半乳糖和阿拉伯糖的果胶类多糖。
2.菌群调节:WPRP的结构变化使其成为产丁酸菌(如Clostridium butyricum, Roseburia spp.)的优选发酵底物,从而在免疫抑制小鼠中特异性富集这些有益菌。
3.代谢激活:WPRP通过重塑菌群,显著提高了肠道中丁酸的产量,并激活了宿主的丁酸代谢通路。
4.免疫增强:丁酸水平的升高与Tc1细胞(一种CD8+ T细胞亚群)的比例呈正相关。WPRP通过“多糖-菌群-丁酸”轴,促进了Tc1细胞的活化和分化,从而增强了肠道免疫屏障功能,改善了全身免疫抑制状态。
科学意义:本研究首次揭示了酒制通过“结构重塑”增强黄精多糖免疫调节活性的科学内涵,为传统中药炮制理论提供了现代科学解释,并为开发基于菌群调节的新型免疫增强剂提供了新思路。
文献意义:
本研究不仅在化学层面清晰地描绘了酒制对黄精多糖结构的“精准重塑”过程,更重要的是在生物学层面打通了“结构-功能”的桥梁。它创新性地提出了“炮制诱导的结构变化决定了多糖在肠道中的菌群偏好性”这一概念,并成功验证了WPRP通过富集产丁酸菌、促进丁酸生成,进而特异性激活Tc1细胞的“菌群-代谢-免疫”级联反应。这一发现颠覆了传统上认为多糖免疫调节主要依赖“非特异性”激活的观点,为基于“药食同源”物质和肠道菌群互作的新型精准免疫疗法提供了理论依据和候选药物。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:蛋白酶检测新突破:基于 BRET 的融合底物实现灵敏定量检测!
下一篇:赖氨酸甲基化再添新功能:SMYD2 特异性调控 BMP 信号通路