常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-03 17:03:33 细胞资源库平台 访问量:124
在生物医学研究和药物开发领域,生物发光成像技术因其高信噪比而被广泛应用于细胞测定和动物成像研究。然而,传统的荧光素酶种类有限,限制了同时成像多个分子和细胞事件的能力。为了突破这一限制,科学家们开发了一种新型的ATP非依赖性荧光素酶——NanoLuc(NL),它源自深海虾Oplophorus gracilirostris,并经过工程改造以增强蛋白质稳定性。NanoLuc作为一种小型(19 kDa)、高亮度的荧光素酶,其亮度是传统萤火虫或海肾荧光素酶的100倍,并且使用furimazine作为底物产生明亮的辉光型发光。NanoLuc的意义在于其为双报告基因生物发光分子成像提供了新的可能。它不仅可以在活体小鼠的表层和深层组织中成像,而且其生物发光随时间的变化可以用来定量肿瘤生长,甚至在少量血清中也能检测到分泌的NL。此外,NanoLuc与萤火虫荧光素酶的结合使用,为在完整细胞和活体小鼠中定量TGF-β信号传导的两个关键步骤提供了一种新型双荧光素酶成像策略,从而在正常生理、疾病和药物开发中扩展了信号转导的成像能力。NanoLuc的作用不仅体现在其高灵敏度和高稳定性上,它还具有更小的尺寸,这使得在标记细胞和蛋白质时对样本的侵入性更小,有助于保持细胞或组织的天然状态。NanoLuc的快速反应、低背景发光和多样灵活等特点,使其在生物学和医学研究中具有广泛的应用前景。因此,NanoLuc作为一种新的报告基因,不仅增强了我们对生物过程的理解和疾病机理的研究,而且在开发潜在治疗方法和疗法方面发挥了重要作用。
英文标题:Engineering GFP–NanoLuc fusion substrates for sensitive, quantitative detection of protease activity via BRET
中文标题:工程化 GFP-NanoLuc 融合底物,通过生物发光共振能量转移实现蛋白酶活性的灵敏、定量检测
发表期刊:《Analytical Biochemistry》
影响因子:2.5
作者单位:
Department of Applied Chemistry, Faculty of Engineering, University of Toyama, 3190 Gofuku, Toyama, Toyama, 930-855, Japan
作者信息:
第一作者:Mitsuki Nakamura
通讯作者:Masafumi Sakono(E-mail:msakono@eng.u-toyama.ac.jp)
蛋白酶在多种生物过程中发挥关键作用,其活性失调与癌症、神经退行性疾病等多种疾病相关,是诊断和药物研发的重要靶点,因此亟需可靠灵敏的蛋白酶活性检测方法;传统检测方法多依赖生色或荧光底物,需有机合成导致成本高、可及性低,而荧光共振能量转移(FRET)检测法虽应用广泛,但需外部激发光,易引发细胞自发荧光和光漂白,同样存在合成成本问题;生物发光共振能量转移(BRET)无需外部光照,能减少背景信号和光毒性,且其底物可由基因编码蛋白构建,能通过大肠杆菌表达,是解决上述问题的理想策略,目前 BRET 检测法的性能受融合结构影响较大,因此本研究旨在构建基于 NanoLuc(NLuc)/GFP 对的可工程化、通用型 BRET 底物框架。
本研究采用三步 In-Fusion 克隆策略构建含 TEV 蛋白酶切割位点(TEVcs)的 GFP-NLuc 融合蛋白,以 pH6HTN His₆-HaloTag T7 为载体,插入 NLuc、GFP 基因及不同切割位点序列(含无接头、单 G3S 接头、双 G3S 接头的 TEVcs,以及对照随机序列,后通过重叠延伸 PCR 将 TEVcs 替换为 caspase-3 特异性序列 Casp3cs),在大肠杆菌中表达并经钴亲和层析、柱缓冲液置换纯化,通过 SDS-PAGE 检测蛋白纯度、紫外吸光度法测定浓度;制备 TEV 蛋白酶(市售)和 caspase-3(大肠杆菌 Rosetta 2 表达、Ni-NTA 琼脂糖纯化),采用分光荧光计测定融合蛋白在 BisZ 作用下的发射光谱,利用多功能酶标仪在 96 孔板中检测 460nm(NLuc)和 538nm(GFP)处的发光强度;将融合底物与蛋白酶在适宜缓冲液中 37℃孵育,通过时间进程实验、终点滴定和校准实验检测蛋白水解切割效果,以 NLuc/GFP 发光比为信号指标,采用 4 参数逻辑模型拟合数据,基于空白组 3σ 准则计算检测限(LOD)。
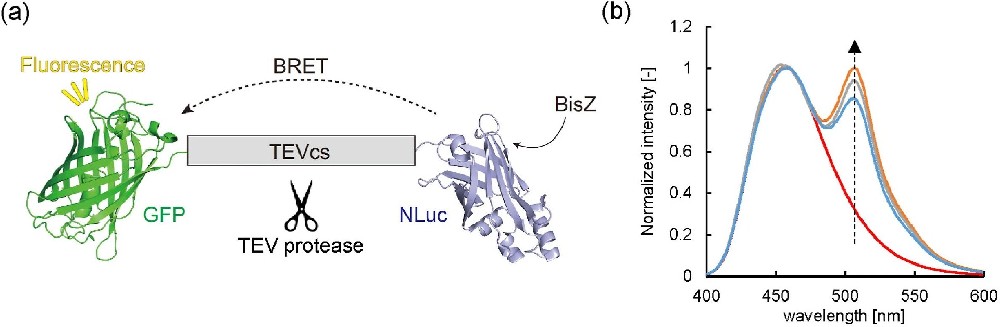
图1:蛋白酶敏感型 BRET 底物的设计与光谱表征
该图包含底物设计示意图和纯化融合蛋白的发射光谱图,设计上构建了无接头、单 G3S 接头、双 G3S 接头的 GFP-TEVcs-NLuc 三种融合底物,完整底物中 BisZ 诱导 NLuc 发光并通过 BRET 激发 GFP 产生绿色荧光;光谱结果显示,三种融合蛋白均在 460nm(NLuc 特征峰)和 508nm(BRET 介导的 GFP 发射峰)出现特征峰,证实均能实现 BRET,且 GFP 发射峰强度随接头长度增加而降低,说明接头延长会增大 NLuc 与 GFP 的空间距离,降低 BRET 效率。
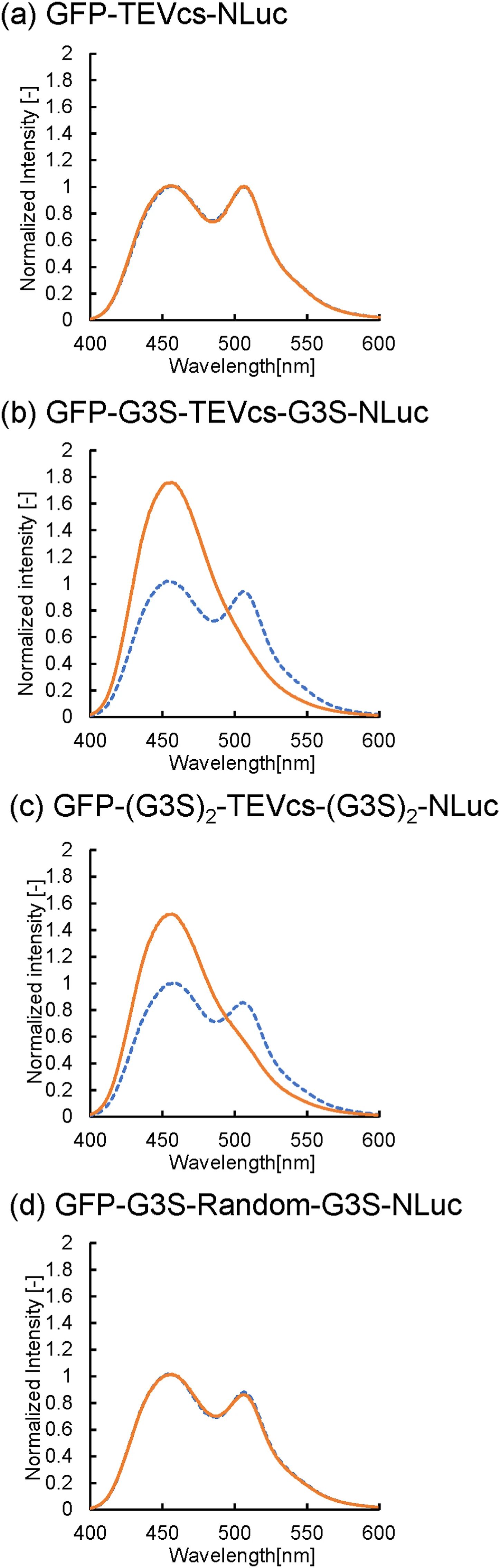
图2:TEV 蛋白酶切割下的 BRET 信号变化
该图展示了四种融合底物经 TEV 蛋白酶处理前后的发射光谱,无接头的 GFP-TEVcs-NLuc 处理后光谱无明显变化,说明蛋白酶切割效率极低;含单 G3S、双 G3S 接头的 TEVcs 底物处理后,508nm GFP 峰显著降低、460nm NLuc 峰升高,表明蛋白酶切割使两结构域分离,BRET 被破坏;含随机序列的对照底物处理后光谱无变化,证实 TEV 蛋白酶的切割具有序列特异性,且切割位点两侧的柔性接头能缓解空间位阻,提高蛋白酶的可及性。
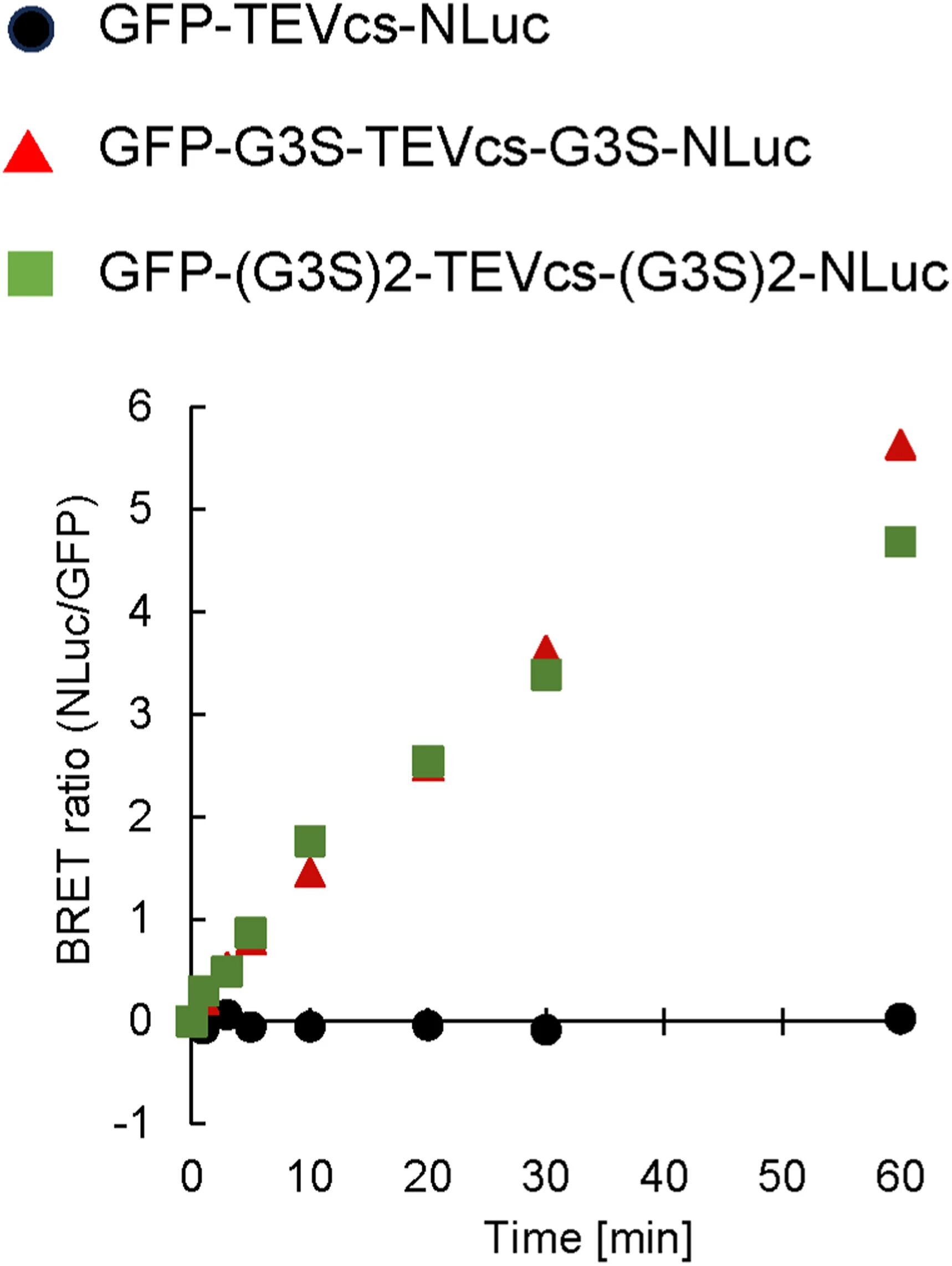
图3:TEV 蛋白酶处理后 BRET 信号的时间依赖性变化
该图监测了三种 TEVcs 融合底物的 NLuc/GFP 发光比随孵育时间的变化,无接头底物在 60min 内发光比无明显变化,进一步证明其无法被有效切割;单 G3S 和双 G3S 接头底物的发光比均随时间逐渐升高,且前期变化趋势基本一致,60min 时双 G3S 接头底物发光比略低,原因是其本身 BRET 效率更低,切割后 GFP 强度变化幅度更小,说明单 G3S 接头的 GFP-G3S-TEVcs-G3S-NLuc 是信号响应更优的底物。
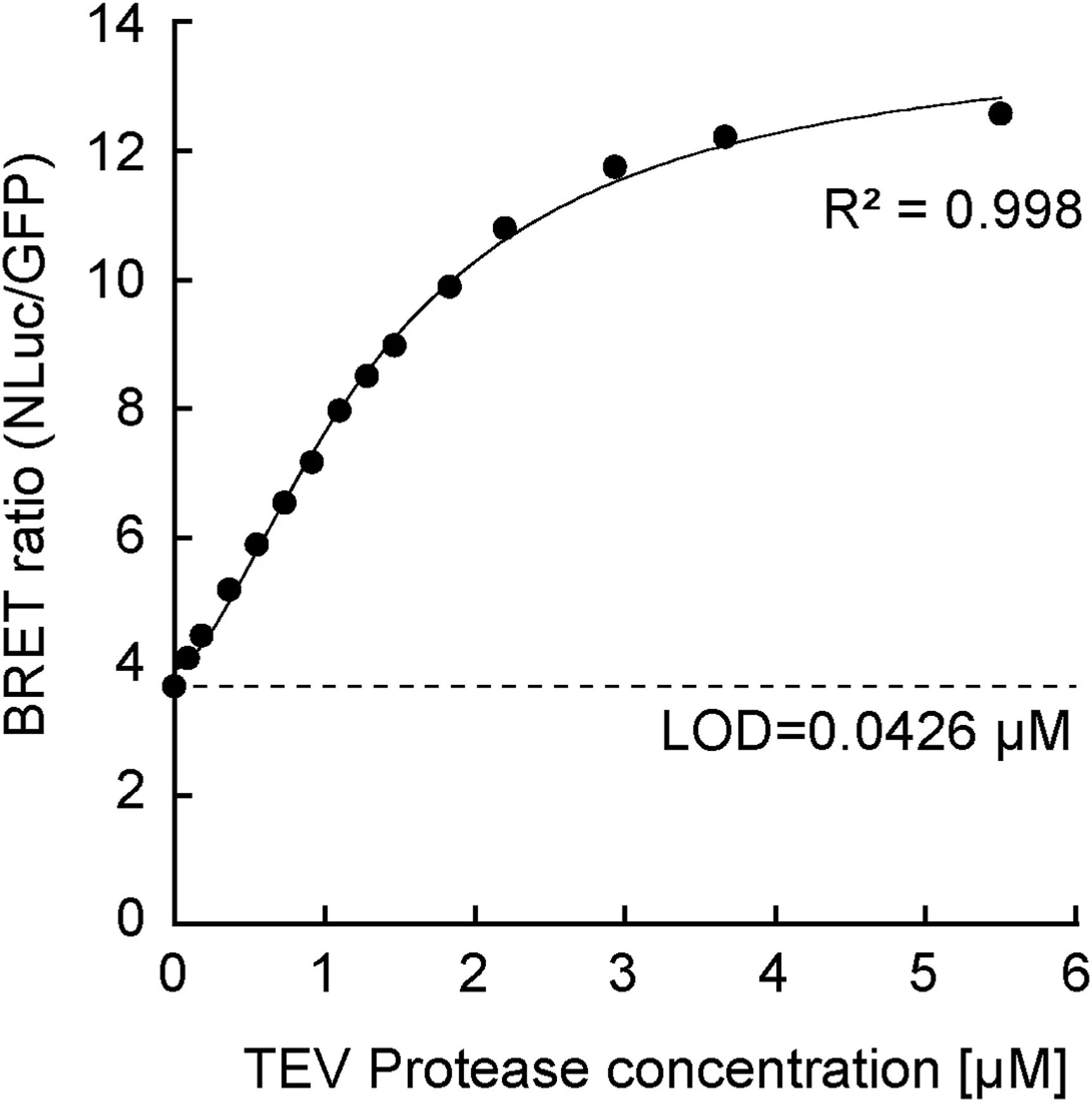
图4:基于 BRET 底物的 TEV 蛋白酶定量检测
该图为 GFP-G3S-TEVcs-G3S-NLuc 底物检测 TEV 蛋白酶的校准曲线,NLuc/GFP 发光比随 TEV 蛋白酶浓度增加呈浓度依赖性升高,数据与 4 参数逻辑模型拟合度极高(R²=0.998),基于 3σ 准则计算得检测限为 0.0426μM,证实该系统能以摩尔单位在宽动态范围内灵敏、定量检测 TEV 蛋白酶活性。
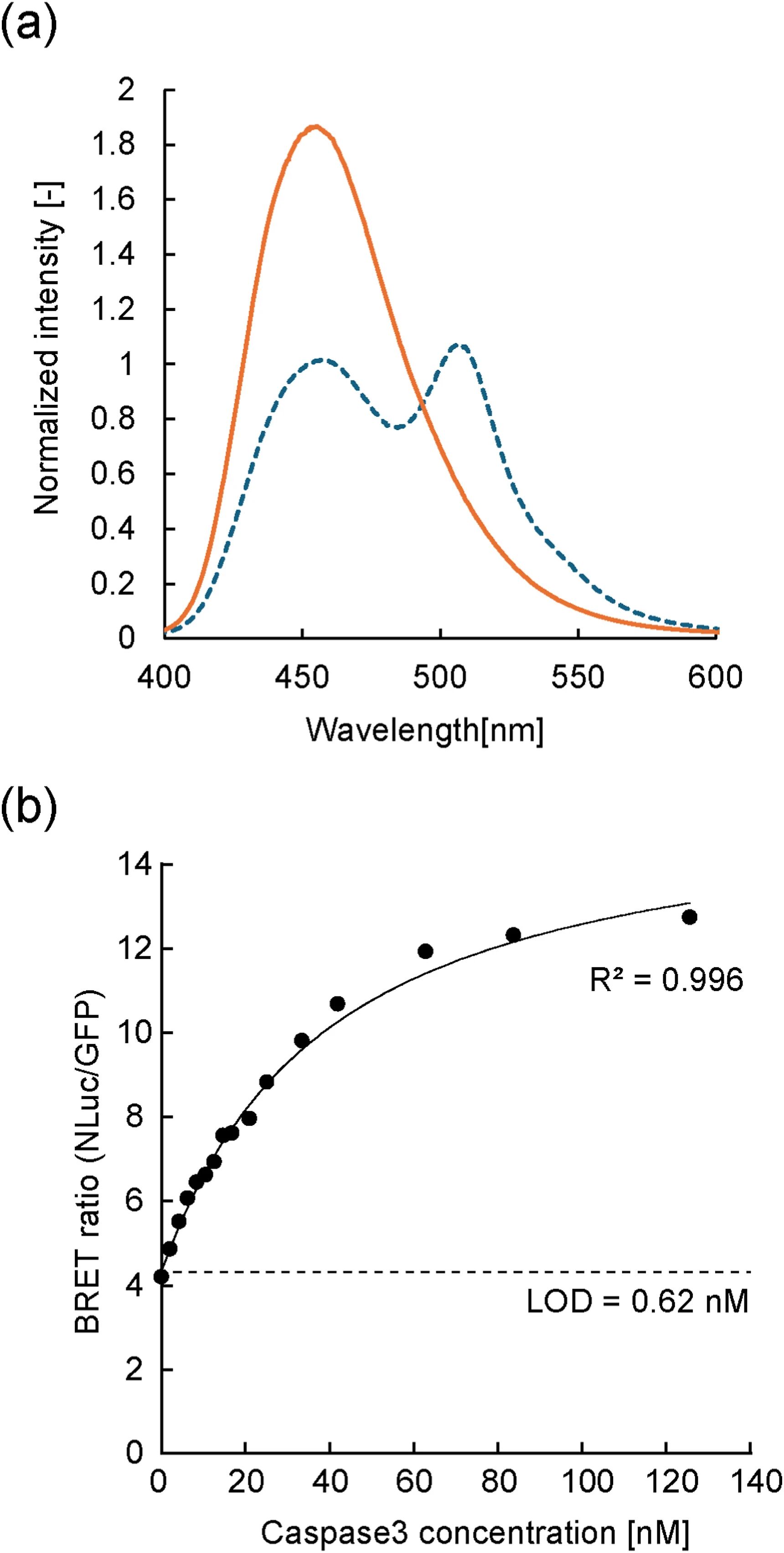
图5:BRET 系统在 caspase-3 检测中的应用
该图包含 caspase-3 特异性底物的发射光谱和定量检测校准曲线,光谱结果显示,底物经 caspase-3 处理后 508nm GFP 峰降低、460nm NLuc 峰升高,证实 caspase-3 切割能破坏 BRET;校准曲线显示 NLuc/GFP 发光比与 caspase-3 浓度呈良好的剂量依赖性,4 参数逻辑模型拟合度高(R²=0.996),检测限低至 0.62nM,证明该融合蛋白底物设计具有模块化特性,可拓展至其他蛋白酶的灵敏定量检测。
本研究开发了基于 GFP 与 NLuc 之间 BRET 的通用型蛋白酶检测系统,将蛋白酶特异性切割序列插入两个报告结构域之间构建融合蛋白底物,以 TEV 蛋白酶为模型证实切割位点两侧引入甘氨酸 - 丝氨酸(G3S)柔性接头是实现高效蛋白水解和 BRET 信号破坏的关键,优化后的 GFP-G3S-TEVcs-G3S-NLuc 底物对 TEV 蛋白酶的检测限达 0.0426μM;通过将切割位点替换为 caspase-3 特异性序列,成功将该平台拓展至 caspase-3 检测,检测限低至 0.62nM,且该底物可通过标准大肠杆菌表达系统制备,无需化学合成,兼具成本效益;该 BRET 底物设计具有模块化、灵敏性和广泛适用性,可实现多种蛋白酶活性的定量检测,且 caspase-3 响应性底物为后续通过细胞内表达融合构建体、比率型 BRET 读数实现活细胞凋亡监测奠定了基础,在生化检测和活细胞研究领域具有良好的应用前景。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:点亮胰腺神经内分泌肿瘤(PNETs):利用新型双标记细胞系构建小鼠模型
下一篇:酒制诱导黄精多糖结构修饰并通过菌群介导的丁酸代谢增强Tc1细胞免疫调节活性