常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-02 17:00:02 细胞资源库平台 访问量:132
传统 CRISPR-Cas9 基因编辑依赖 DNA 双链断裂(DSB),易引发染色体异常、细胞毒性等安全风险,且 CRISPRi/a 需持续表达 Cas 蛋白导致免疫排斥,限制其在 T 细胞疗法中的应用。为此,加州大学旧金山分校团队在《Nature Biotechnology》上发表题为Integrated epigenetic and genetic programming of primary human T cells的文章,开发全 RNA 表观遗传编辑平台:通过瞬时递送 CRISPRoff(dCas9 融合 DNMT3A/3L/KRAB)和 CRISPRon(dCas9 融合 TET1)mRNA,实现原代人 T 细胞基因的持久沉默或激活 ——CRISPRoff 介导的基因沉默可维持 28 天(约 30-80 次细胞分裂),无 CGI 基因也可稳定沉默,且多靶点编辑无 Cas9 介导的毒性;CRISPRon 可靶向 FOXP3 增强子(TSDR)诱导其稳定表达;进一步通过正交 Cas 系统(Cas12a 介导 CAR-KI + dCas9 介导表观沉默),构建 RASA2 沉默的 TRAC-CAR-T 细胞,显著提升体外杀伤持久性及体内肿瘤控制效果。该平台无需 DSB,安全性高、可多靶点调控,为 T 细胞疗法优化提供新工具。
1. 关键材料
编辑工具:CRISPRoff mRNA(7 种设计,优化后选 CRISPRoff7:Cap1 修饰、1-Me ps-UTP 碱基修饰、密码子优化);CRISPRon mRNA(TET1-dCas9 融合,3 种变体,优化 linker 长度);sgRNA(化学修饰,靶向基因 TSS 或增强子)。
细胞与模型:原代人 T 细胞(健康供体 PBMC 分离,EasySep 试剂盒);CD19⁺ A375 黑色素瘤细胞、Nalm6 白血病细胞(体内移植模型);NSG 小鼠(免疫缺陷,用于体内实验)。
辅助试剂:AsCas12a RNP(用于 TRAC 位点 CAR-KI);AAV6 载体(携带 CD19-28z CAR 的 HDR 模板);WGBS/RNA-seq 试剂盒;FOXP3 抗体、RASA2 抗体。
2. 核心流程
2.1 CRISPRoff/CRISPRon 的优化与验证
CRISPRoff 优化:电转 7 种 CRISPRoff mRNA 至 T 细胞,靶向 CD151(含 CGI),流式检测沉默效率,筛选出 CRISPRoff7(低剂量即可高效沉默);对比 CRISPRi(瞬时沉默)、Cas9(DSB 介导 KO),通过 RNA-seq(28 天)验证特异性,WGBS 检测靶位点甲基化。
CRISPRon 激活:CD4⁺CD25ᵢₒᵥ Tconv 细胞电转 CRISPRon mRNA,sgRNA 靶向 FOXP3 的 TSDR 增强子(而非 TSS),流式检测 FOXP3⁺细胞比例,靶向 bisulfite 测序验证 TSDR 去甲基化。
2.2 多靶点沉默与 CAR-T 整合编辑
多靶点沉默:电转 CRISPRoff mRNA 同时靶向 3-5 个基因(CD151、CD81 等),对比 Cas9 多靶点编辑的细胞毒性(活细胞计数),流式检测沉默效率(30 天)。
遗传 + 表观结合编辑:AsCas12a RNP(TRAC crRNA)+ CRISPRoff mRNA(RASA2 sgRNA)共电转 T 细胞,AAV6 递送 CD19-CAR HDR 模板;体外重复刺激实验(5 轮 CD19⁺肿瘤细胞共培养)验证杀伤效率,体内 NSG 小鼠 Nalm6 移植模型评估肿瘤控制与存活。
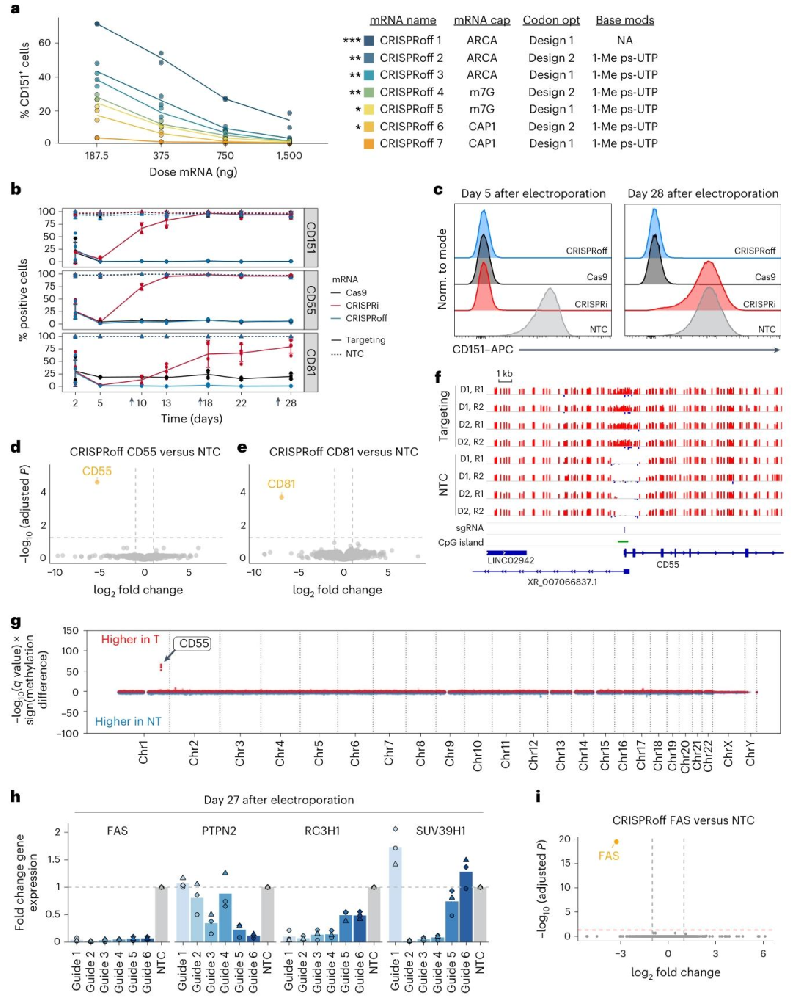
图1:CRISPRoff 在原代 T 细胞中的持久沉默与特异性
该图验证 CRISPRoff 的功能优势:A 为 7 种 CRISPRoff mRNA 的 CD151 沉默效率,CRISPRoff7 最 potent(低剂量即可显著沉默);B-C 为时间曲线与流式图,CRISPRoff 沉默 CD151/CD55/CD81 达 28 天(>93% 细胞阴性),CRISPRi 效果随时间衰减,Cas9 虽持久但有 DSB 风险;D-E 为 RNA-seq,仅靶基因(CD55/CD81)下调,无其他差异基因;F-G 为 WGBS,靶位点(CD55 TSS)甲基化显著升高,全基因组仅靶区域为差异甲基化区(DMR)。结果证实 CRISPRoff 的持久特异性,无脱靶效应。
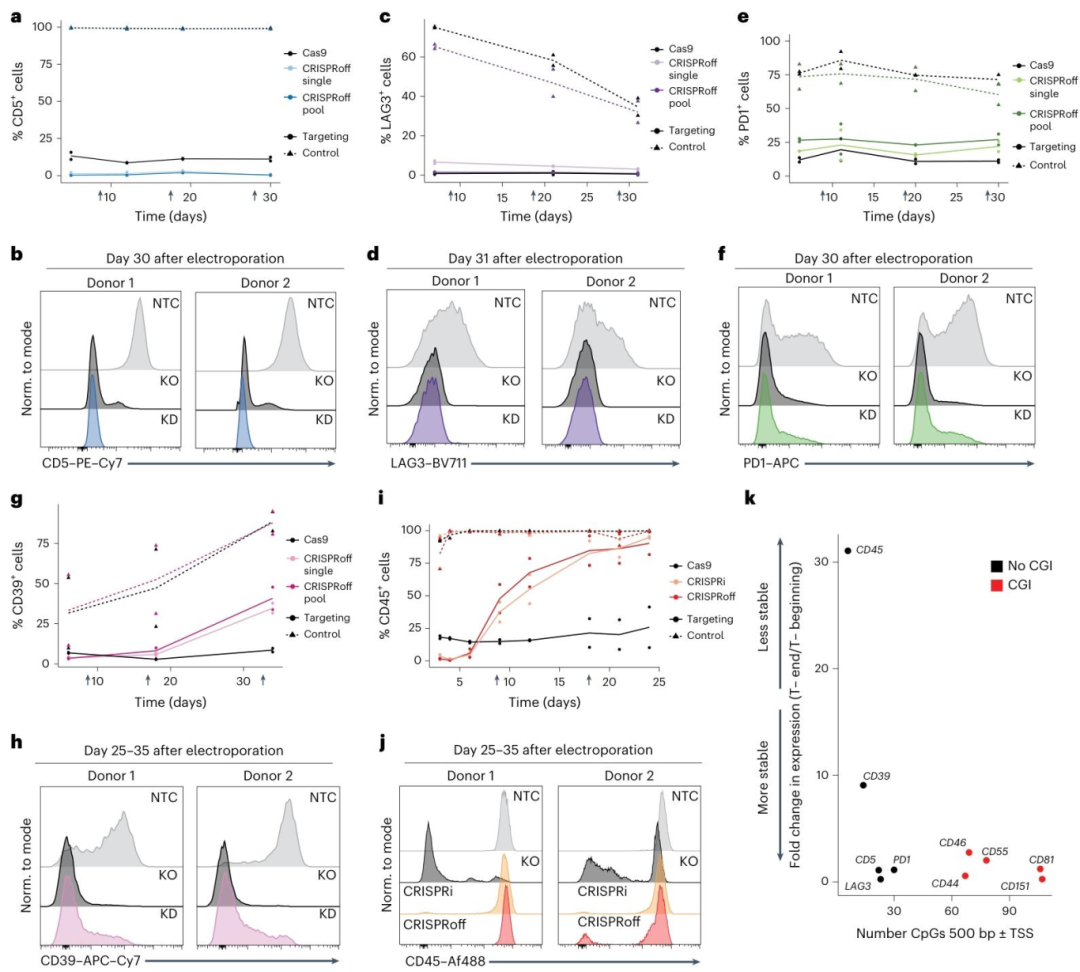
图2:CRISPRoff 沉默无 CGI 注释的基因
该图探索非 CGI 基因的沉默效果:A-D 为 CD5、LAG3 的沉默,CRISPRoff(单 sgRNA 或 sgRNA 池)效率接近或优于 Cas9,30 天仍稳定(CD5 沉默 99.5%、LAG3 沉默 99.1%);E-H 为 PD1、CD39,PD1 沉默 78.15%(接近 Cas9 的 90%),CD39 部分稳定(35 天 53% 细胞阴性);I-J 为 CD45,CRISPRoff 与 CRISPRi 均随时间失效;K 为相关性分析,TSS 附近 CpG 数量越少,沉默越不稳定。结果表明 CRISPRoff 可沉默部分非 CGI 基因,稳定性与 CpG 密度相关。
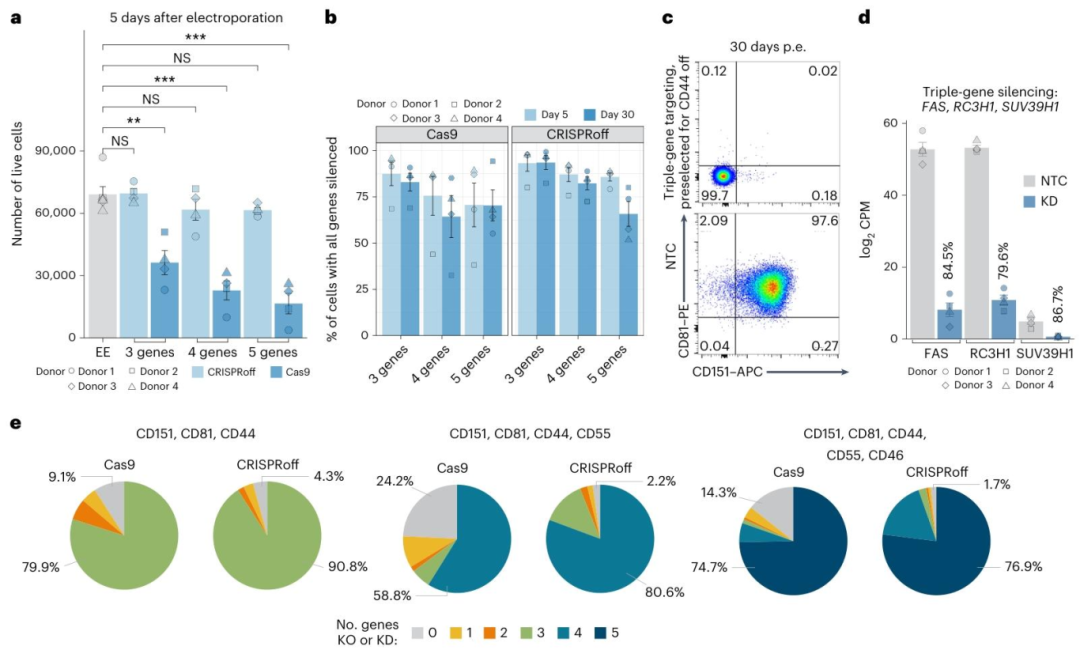
图3:CRISPRoff 的多靶点沉默安全性
该图对比 CRISPRoff 与 Cas9 的多靶点编辑:A 为细胞毒性,Cas9 靶向 3-5 个基因时活细胞数显著减少(DSB 导致毒性),CRISPRoff 无明显毒性;B-E 为沉默效率,CRISPRoff 靶向 3/4/5 个基因时,30 天沉默率分别达 93.5%/82.4%/65.8%,且 FAS/RC3H1/SUV39H1 的转录本下调~80%;流式图显示多靶点沉默细胞比例高,Cas9 多靶点易出现染色体异常。结果证实 CRISPRoff 的多靶点安全性与效率,避免 DSB 相关毒性。
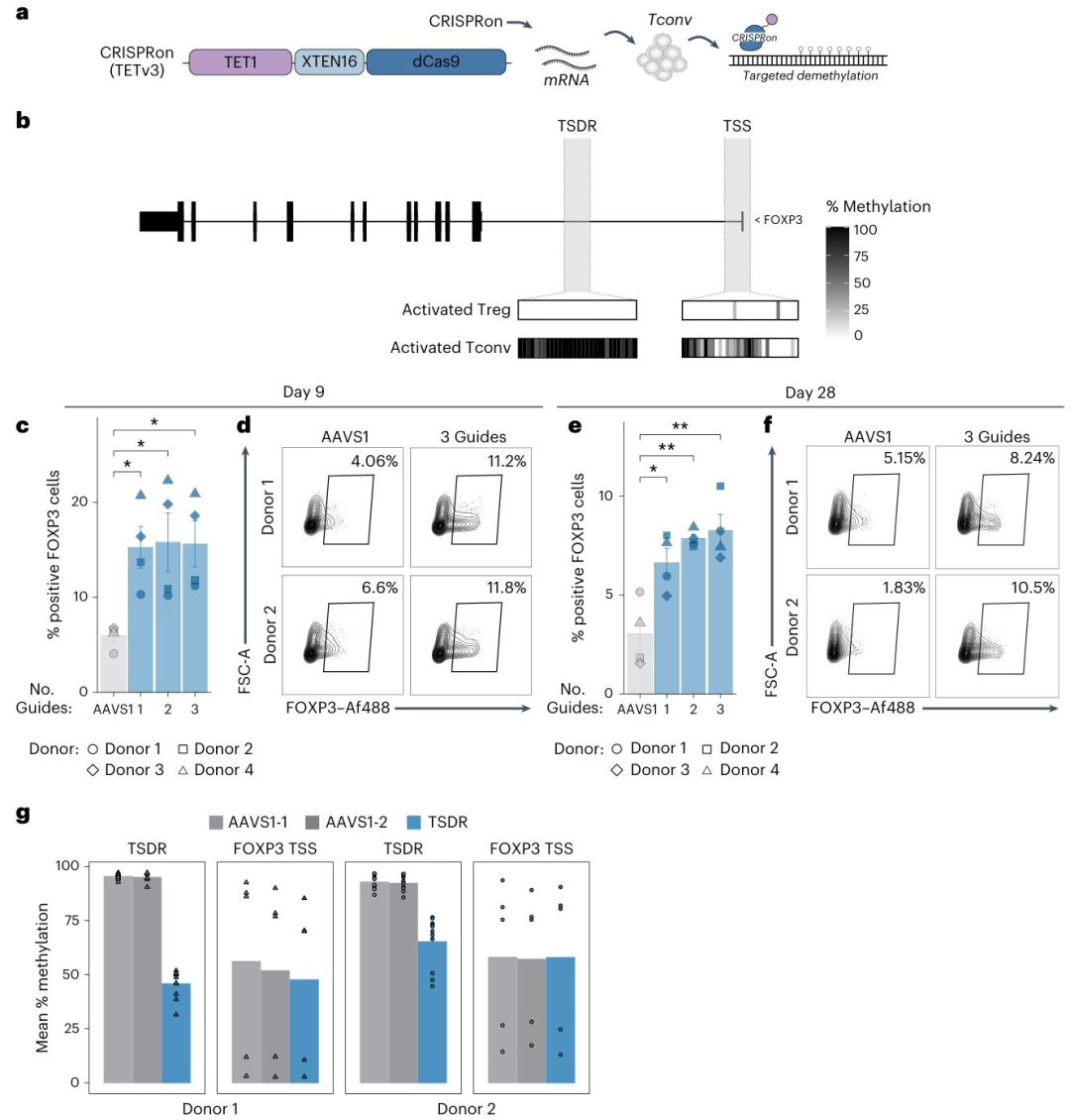
图4:CRISPRon 靶向增强子激活 FOXP3
该图验证 CRISPRon 的激活功能:A 为 CRISPRon-TETv3 结构(TET1-dCas9)与实验流程;B 为 FOXP3 locus,TSDR 增强子在 Treg 中去甲基化、Tconv 中高甲基化;C-D 为 9 天流式,CRISPRon 靶向 TSDR(1-3 个 sgRNA)显著提升 FOXP3⁺细胞比例(vs AAVS1 对照);E-F 为 28 天结果,FOXP3⁺细胞仍稳定存在,荧光强度高;G 为靶向 bisulfite 测序,TSDR 甲基化显著降低,TSS 无变化。结果表明 CRISPRon 可通过靶向增强子去甲基化,在 Tconv 中稳定激活 FOXP3。
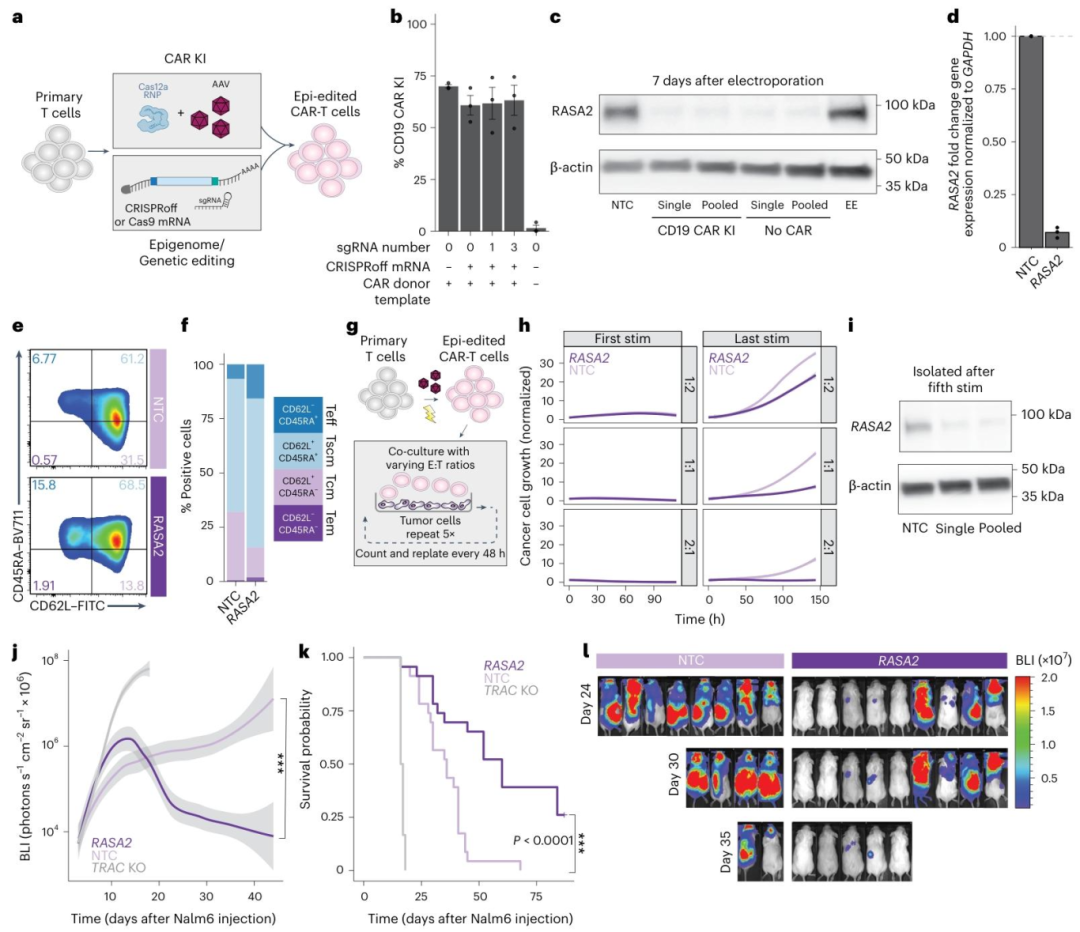
图5:遗传 + 表观整合编辑优化 CAR-T 功能
该图展示 CAR-T 的联合编辑效果:A 为实验设计,AsCas12a 介导 TRAC-CAR KI + CRISPRoff 沉默 RASA2;B 为 CAR KI 效率,CRISPRoff 不影响 KI yield;C-D 为 RASA2 沉默,蛋白与转录本均显著下调(无论是否 CAR-KI);E-F 为 T 细胞表型,RASA2 沉默细胞略向效应型偏移;G-H 为体外重复刺激,RASA2 沉默 CAR-T 经 5 轮杀伤仍高效,对照则杀伤能力下降;I 为 Western blot,5 轮刺激后 RASA2 仍沉默;J-L 为体内实验,RASA2 沉默 CAR-T 显著降低 Nalm6 肿瘤负荷,延长小鼠存活(P<0.0001)。结果证实联合编辑可提升 CAR-T 的持久杀伤与体内疗效。
本研究开发了基于全 RNA 的 CRISPRoff/CRISPRon 表观遗传编辑平台,解决了传统 CRISPR-Cas9 基因编辑的 DSB 毒性、染色体异常及 CRISPRi/a 需持续表达的问题 —— 通过瞬时递送 mRNA,实现原代人 T 细胞基因的持久沉默(达 28 天,覆盖 30-80 次细胞分裂)与特异性激活,且支持多靶点调控(3-5 个基因无毒性);CRISPRoff 可沉默含 CGI 与部分非 CGI 基因,CRISPRon 通过靶向 FOXP3 的 TSDR 增强子诱导其稳定表达;进一步结合 AsCas12a 的正交遗传编辑(TRAC-CAR KI)与 CRISPRoff 介导的 RASA2 沉默,显著提升 CAR-T 的体外持久杀伤与体内肿瘤控制效果。该平台具有临床转化潜力,可优化 CAR-T 等细胞疗法;局限性包括部分非 CGI 基因沉默不稳定、CRISPRon 仅验证 FOXP3 一个增强子,未来需进一步解析非 CGI 基因沉默规则、拓展增强子靶向范围,以实现更精准的 T 细胞功能编程。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:人源化抗 CD147 抗体 HuM6-1B9 通过 ADCC 克服 TNBC NK 细胞抗性
下一篇:点亮胰腺神经内分泌肿瘤(PNETs):利用新型双标记细胞系构建小鼠模型