常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-01 17:12:59 细胞资源库平台 访问量:165
骨细胞是骨组织中占比 95% 的终末分化细胞,嵌于骨基质的陷窝 - 小管网络中,是关键的力敏感细胞 —— 通过感知间隙液流将机械信号转化为生化信号,调控成骨细胞与破骨细胞活性,维持骨重塑平衡。然而体外研究面临两大难题:常用骨细胞系(如 MLO-Y4)缺乏体内关键标志物(如硬化蛋白),OCY454 细胞系虽表达硬化蛋白,但钙响应不稳定且需特殊温度培养;原代骨细胞因深埋骨基质、终末分化特性难以分离,现有方案仅局限于胶原酶分离,流程不完善。
加拿大多伦多大学 Kimberly Seaman、李丹团队在《Current Protocols》上发表题为Integration of Primary Murine Osteocytes for In Vitro Mechanobiology Studies的研究,提出四套优化方案:用 Liberase TM 分离原代小鼠骨细胞、传代与特异性染色、实时钙成像检测力响应、微流控平台整合用于骨转移研究。方案解决原代细胞分离效率低、功能验证难的问题,为骨力生物学和骨转移研究提供更具生理相关性的模型。
1.原代小鼠骨细胞分离(基础方案 1)
样本处理:取 2-24 月龄 C57BL/6 小鼠股骨和胫骨,10 分钟内浸入预冷 DPBS/BSA 液,24 小时内运至实验室,去除肌肉、肌腱和骨骺,冲洗骨髓至液体澄清。
消化流程:用 Liberase TM(高纯度胶原酶混合物)与 EDTA 交替消化 9 轮 —— 前 2 轮 Liberase TM(37℃、200 RPM、20 分钟 / 轮),第 3 轮 EDTA(30 分钟),后续重复 Liberase TM 与 EDTA 消化,收集 7-9 轮上清,离心(200×g、10 分钟)后用骨细胞培养基重悬,接种于胶原包被培养皿,37℃、5% CO₂培养,4 天后部分换液去除消化残留。
2.原代骨细胞传代与特异性染色(基础方案 2)
传代:培养 1 周后,用 4ml 胰酶 - EDTA 消化 5 分钟,显微镜下确认细胞脱落,加 4ml 培养基中和,制成单细胞悬液,台盼蓝计数(典型产量 1-2×10⁶细胞 / 100mm 皿),离心(250×g、7 分钟)后按 7500 细胞 /cm² 接种于胶原包被板。
E11/podoplanin 染色:细胞培养过夜后,4% 多聚甲醛固定 15 分钟,0.1% Triton X-100 透化 10 分钟,封闭液孵育 1 小时,一抗(1:100)4℃孵育过夜,二抗(Alexa Fluor 488,1:100)室温孵育 2 小时,DAPI 染核 10 分钟,荧光显微镜成像,确认骨细胞特异性(阳性率 95-97%)。
3.原代骨细胞实时钙成像(基础方案 3)
样本制备:ibidi μ-Slide VI 0.4 通道用 0.15mg/ml 胶原包被 1 小时,接种 2.5×10⁵细胞 /ml 的原代骨细胞悬液,37℃孵育 1 小时后加培养基培养过夜。
染色与成像:避光环境下,FURA-2 AM 染料(用 DMSO 溶解)与成像培养基混合,细胞染色 35 分钟,DPBS 和成像培养基冲洗去除残留染料;连接含 α-MEM 的注射器与线性致动器,施加 2 Pa、1 Hz 振荡流,33℃加热台平衡 20 分钟后,用 EasyRatioPro 软件记录 5 分钟(1 分钟基线、3 分钟流刺激、1 分钟恢复),以 340/380nm 荧光比判断钙响应(响应幅度≥基线 2 倍为显著)。
4.原代骨细胞的微流控平台整合(基础方案 4)
微流控器件制备:PDMS 按 10:1 混合固化,与载玻片等离子键合,70% 乙醇灭菌,胶原(0.15mg/ml)包被骨细胞通道 1 小时,纤连蛋白(100μg/ml)包被管腔通道 40 分钟。
水凝胶管腔构建:混合胶原 I(5.5mg/ml)与 Matrigel(2.5mg/ml),注入管腔通道 30 秒后移除,37℃聚合 45 分钟,分别向管腔通道加 HUVEC 培养基、骨细胞通道加骨细胞培养基。
细胞接种:HUVEC(2×10⁶细胞 /ml)倾斜接种(左、右、倒置)形成内皮管腔,培养 6 小时;原代骨细胞(1.25×10⁶细胞 /ml)接种于骨细胞通道,孵育 5 小时;PC-3 癌细胞(4×10⁶细胞 /ml,CellTracker Green 染色)接种于管腔,37℃孵育 20 分钟,后续每天换液 2 次(管腔用 1:1 癌细胞 - 内皮培养基,骨细胞用专用培养基),培养 5 天观察癌细胞外渗。
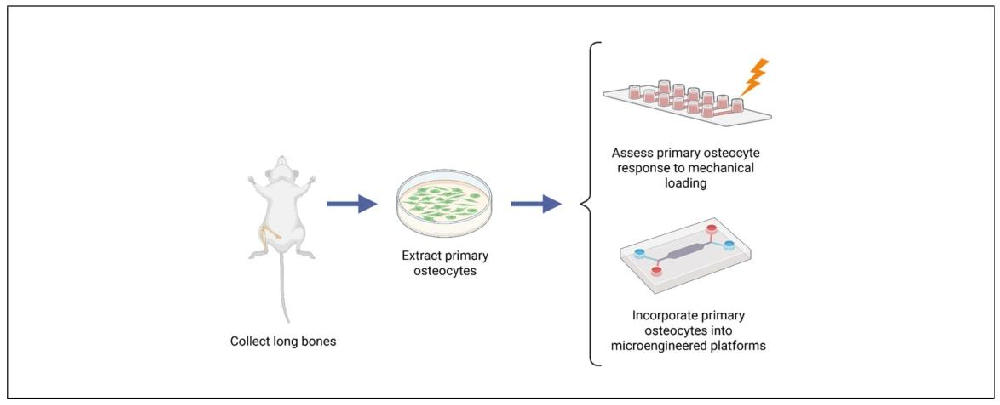
图1:原代骨细胞体外研究的实验 workflow
该图呈现四套基础方案的整体实验流程:从原代小鼠骨细胞的分离(基础方案 1)开始,依次进行细胞传代与 E11/podoplanin 特异性染色(基础方案 2)以验证细胞纯度,再通过实时钙成像检测细胞对机械载荷的响应(基础方案 3),最后将功能合格的原代骨细胞整合到微流控平台,用于骨转移相关研究(如观察癌细胞外渗,基础方案 4)。图中清晰标注各步骤的衔接关系,为实验操作提供标准化流程指引,确保各环节可重复。
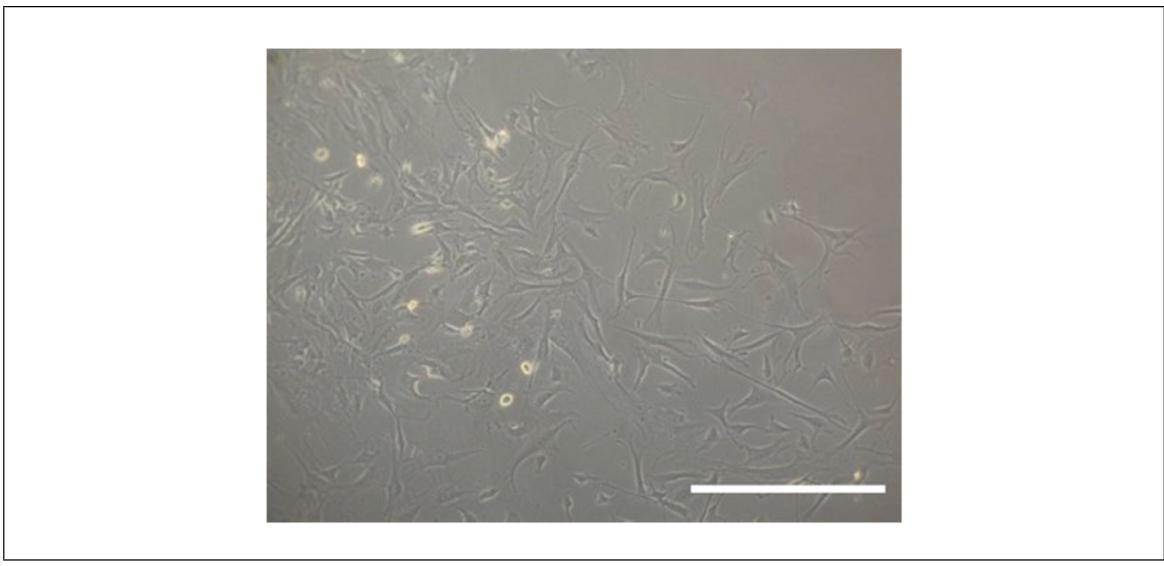
图2:原代骨细胞分离后的形态特征
该图展示分离后原代骨细胞的典型形态:分离培养 1 周后,细胞呈三维树突状结构,无实体聚集,符合体内骨细胞嵌于陷窝 - 小管网络的形态特征,标尺为 100μm。通过明场显微镜观察,可见细胞铺展均匀,树突相互连接,与传统胶原酶分离的细胞相比,Liberase TM 消化的细胞树突更完整、活性更高,证实该分离方案能更好保留骨细胞的生理形态,为后续功能实验奠定基础。
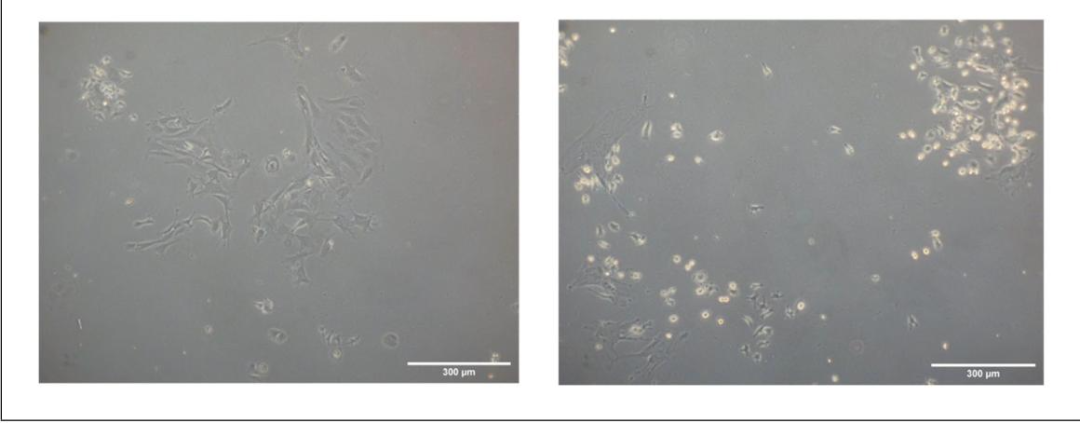
图3:Liberase TM 与胶原酶分离原代骨细胞的形态对比
该图对比两种酶分离后的细胞差异:左侧为 Liberase TM 分离的原代骨细胞(4 天后),右侧为胶原酶分离的细胞。Liberase TM 组细胞树突更长、铺展更均匀,细胞间连接更紧密,保持典型骨细胞形态;胶原酶组细胞部分呈圆形,树突短且数量少,细胞活性较低。图中还标注细胞铺展面积量化结果,Liberase TM 组显著高于胶原酶组,证实 Liberase TM(高纯度胶原酶混合物)能减少对细胞的损伤,提升分离后细胞的存活质量与形态完整性。
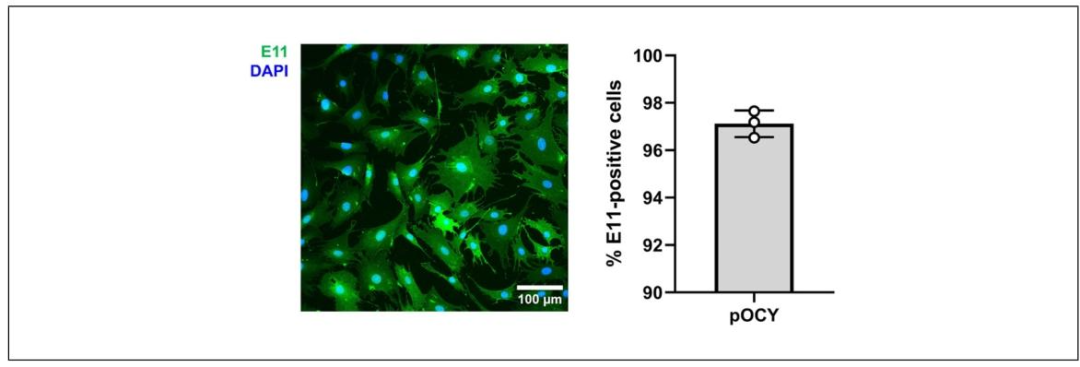
图4:原代骨细胞的 E11/podoplanin 特异性染色结果
该图通过免疫荧光染色验证细胞纯度:样本为 2 月龄雄性小鼠分离的原代骨细胞,E11/podoplanin(骨细胞特异性标志物)一抗结合 Alexa Fluor 488 荧光二抗,呈绿色信号,DAPI 染核呈蓝色。图像显示 95%-97% 的细胞为 E11 阳性,且阳性信号主要分布于细胞膜,符合骨细胞标志物表达特征;右侧量化图表标注 3 个样本的阳性率(分别为 96.2%、95.8%、97.1%),进一步证实该分离方案能获得高纯度原代骨细胞,排除其他骨组织细胞(如成骨细胞、破骨细胞)污染。
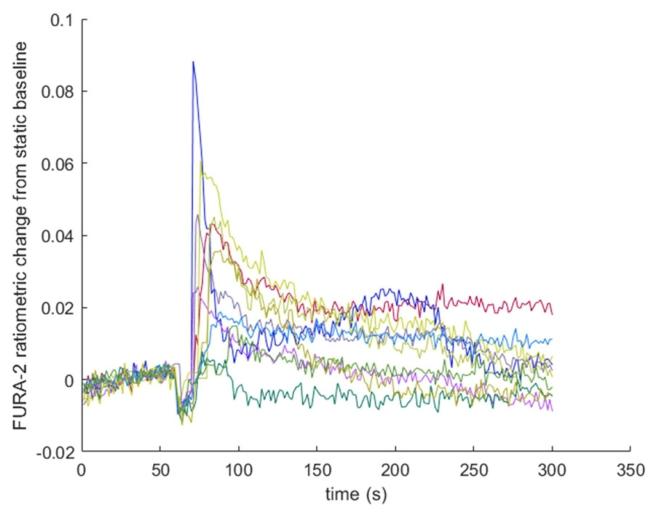
图5:原代骨细胞实时钙成像的原始响应数据
该图记录 10 个原代骨细胞在 5 分钟内的钙响应变化:横坐标为时间(0-350 秒),纵坐标为 340/380nm 荧光比值(反映胞内钙浓度)。前 60 秒为静态基线(无流体刺激),荧光比稳定在 0.02-0.04;60-240 秒施加 2 Pa、1 Hz 振荡流刺激,荧光比快速升高至 0.08-0.1,且维持稳定;240 秒后停止刺激,1 分钟内荧光比恢复至基线水平。每个细胞的响应曲线均显示 “升高 - 稳定 - 恢复” 的典型趋势,且响应幅度均≥基线 2 倍,证实原代骨细胞保留对机械信号的感知与钙信号转导功能。
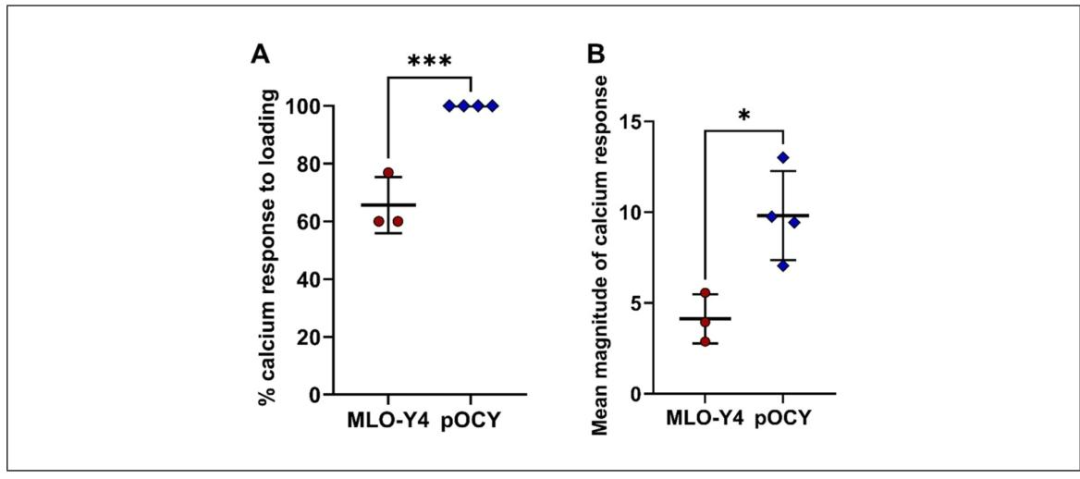
图6:原代骨细胞与 MLO-Y4 细胞的钙响应对比
该图对比两种细胞的机械响应差异,分为 A、B 两个子图:
子图 A(响应细胞百分比):原代骨细胞(pOCY)中对振荡流产生显著响应的细胞比例约为 80%,而 MLO-Y4 细胞(骨细胞系对照)仅为 40%,差异具有统计学意义(***p<0.001,双尾 t 检验);
子图 B(钙响应幅度):原代骨细胞的平均荧光比变化为 0.08±0.02,MLO-Y4 细胞为 0.04±0.01,原代细胞响应幅度显著更高(*p<0.05,双尾 t 检验)。
结果证实原代骨细胞对机械载荷的响应更灵敏,比细胞系更贴近体内骨细胞的力感知特性。

图7:微流控平台中原代骨细胞的培养时序与癌细胞外渗观察
该图展示原代骨细胞在微流控平台的培养过程及时序形态:
左上为接种 30 分钟后:原代骨细胞开始贴壁,呈散在圆形;
右上为接种 4.5 小时后:细胞伸展形成短树突,开始适应微流控环境;
左下为实验第 1 天:细胞树突完整,与通道壁结合紧密,无脱落;
右下为实验第 5 天:细胞保持树突状形态,同时可见 PC-3 癌细胞(绿色荧光标记)向骨细胞方向迁移,部分已发生外渗。
所有图像均在低光环境下明场拍摄,标尺统一,证实原代骨细胞可在微流控平台稳定培养 5 天,且能与癌细胞共培养,为研究骨微环境与癌细胞相互作用提供可行模型。
本研究针对原代小鼠骨细胞体外研究的痛点,优化并标准化四套核心方案:Liberase TM 分离能保留细胞形态与活性,E11 染色确保 95% 以上纯度,钙成像验证力响应功能,微流控整合实现骨转移研究应用。通过依次验证各环节(图1-7),证实该体系比传统细胞系更具生理相关性,解决原代骨细胞分离难、功能验证缺的问题。局限性在于仅用小鼠样本,未拓展至人类原代骨细胞,且微流控平台未纳入血管内皮以外的其他微环境成分。未来可结合患者来源细胞,进一步提升模型的临床转化价值,为骨力生物学机制研究与骨转移药物筛选提供可靠工具。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:乙肝治疗新靶点:MOGAT2 抑制剂有望成为抗 HBV 新武器
下一篇:人源化抗 CD147 抗体 HuM6-1B9 通过 ADCC 克服 TNBC NK 细胞抗性