常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-01 09:01:08 细胞资源库平台 访问量:110
乙肝病毒(HBV)感染是全球主要公共卫生问题之一,有超过2.5亿人慢性感染HBV。而其中有超三分之一的人口集中在我国,人数接近1亿人。NTCP工具细胞,特别是外源表达NTCP的肝癌细胞系如HepG2-NTCP和Huh7-NTCP,因其易操作、短周期、重现性佳的特点,在乙肝病毒(HBV)研究中扮演着至关重要的角色。这些细胞模型能够有效模拟HBV的感染过程,为研究HBV的生命周期、宿主限制因子、病毒复制以及药物筛选提供了一个强大而便捷的体外平台。它们不仅有助于揭示HBV感染的分子机制,如DDX3作为宿主限制因子阻碍cccDNA转录,GPC5作为附着因子在感染入胞过程中的作用,还能通过直接与NTCP相互作用或下调NTCP表达来筛选和验证抗病毒药物的活性,例如环孢菌素A及其衍生物、雷帕霉素及其衍生物等。此外,这些工具细胞还促进了对HBV宿主特异性分子的发现,为发展支持HBV感染的小动物模型提供了可能,这对于乙肝相关研究和药物开发具有重大意义。
英文标题:A CRISPR-based genome-wide loss-of-function screen defines a role of host metabolism in regulating hepatitis B virus infection
中文标题:基于 CRISPR 的全基因组功能缺失筛选揭示宿主代谢在调控乙型肝炎病毒感染中的作用
发表期刊:《Molecular Therapy》
影响因子:12
作者单位:
1.Liver Diseases Branch, National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK), National Institutes of Health, Bethesda, MD 20814, USA
2.Department of Gastroenterology and Hepatology, Kyoto University, Graduate School of Medicine, Kyoto, Japan
3.Department of Gastroenterology and Hepatology, Oita University, Graduate School of Medicine, Oita, Japan
4.Division of Travel Medicine and Health, Research Center for GLOBAL and LOCAL Infectious Diseases, Oita University, Oita, Japan
作者信息:
共同第一作者:Tadashi Inuzuka、Karim Mouzannar
通讯作者:T. Jake Liang(E-mail:jakel@bdg10.niddk.nih.gov)
乙肝病毒(HBV)全球感染人数众多,是慢性肝病、肝硬化和肝癌的主要诱因,现有干扰素和核苷(酸)类似物疗法仅能抑制病毒复制,无法彻底清除共价闭合环状 DNA(cccDNA),实现 HBV 治愈仍是临床难题;靶向宿主因子的药物成为 HBV 治疗新方向,NTCP 作为 HBV 功能受体已得到验证,而全基因组筛选是发现病毒宿主依赖因子的重要手段,但此前针对 HBV 的筛选多使用整合 HBV 的细胞系,无法模拟真实感染过程,且高效的 HBV 报告病毒因病毒基因组紧凑、复制机制复杂难以构建;因此,本研究构建可表达红色荧光蛋白的 HBV 报告病毒(HBV-RFP),并通过 CRISPR 全基因组功能缺失筛选,挖掘 HBV 感染的新型宿主依赖因子,为 HBV 治疗提供新靶点。
本研究基于 D 型 HBV 构建表达 TurboRFP 的报告病毒 HBV-RFP,通过共转染互补质粒优化病毒制备,经密度梯度离心鉴定其感染性;构建组成型表达 NTCP、诱导型表达 Cas9 的 HepG2^NTCP/Cas9 细胞系,验证 Cas9 编辑功能和细胞 HBV 易感性后,用靶向 19114 个人类基因的 Brunello 慢病毒 sgRNA 文库以低感染复数转染该细胞,经嘌呤霉素筛选、多西环素和 Shield1 诱导 Cas9 表达实现基因编辑,再用 HBV-RFP 感染细胞,通过流式细胞术分选 RFP 低表达细胞,经三轮感染 - 分选富集目标细胞后,提取 DNA 进行二代测序和生物信息学分析;利用 MAGeCK 软件筛选候选宿主因子,结合人肝组织 RNA 测序数据筛选出 63 个候选基因,构建对应 sgRNA 慢病毒并在 HepG2^NTCP/Cas9 细胞中敲除,通过检测 HBV RNA、HBeAg 和 HBsAg 验证其对 HBV 复制的影响;在原代人肝细胞(PHH)中通过 siRNA 敲低验证候选基因,聚焦 MOGAT2 后,利用 siRNA 敲低和 MGAT2 抑制剂(JTP-103237、Cpd24d)处理,检测 HBV 标志物变化并计算 IC50 和 CC50;通过丁型肝炎病毒(HDV)感染实验、cccDNA 定量、HBV 启动子报告基因实验探究 MOGAT2 在 HBV 生命周期中的作用阶段;对 MGAT2 抑制的 PHH 进行转录组测序,结合 IPA 通路分析、RT-qPCR 验证,探究 MOGAT2 调控 HBV 感染的分子机制。
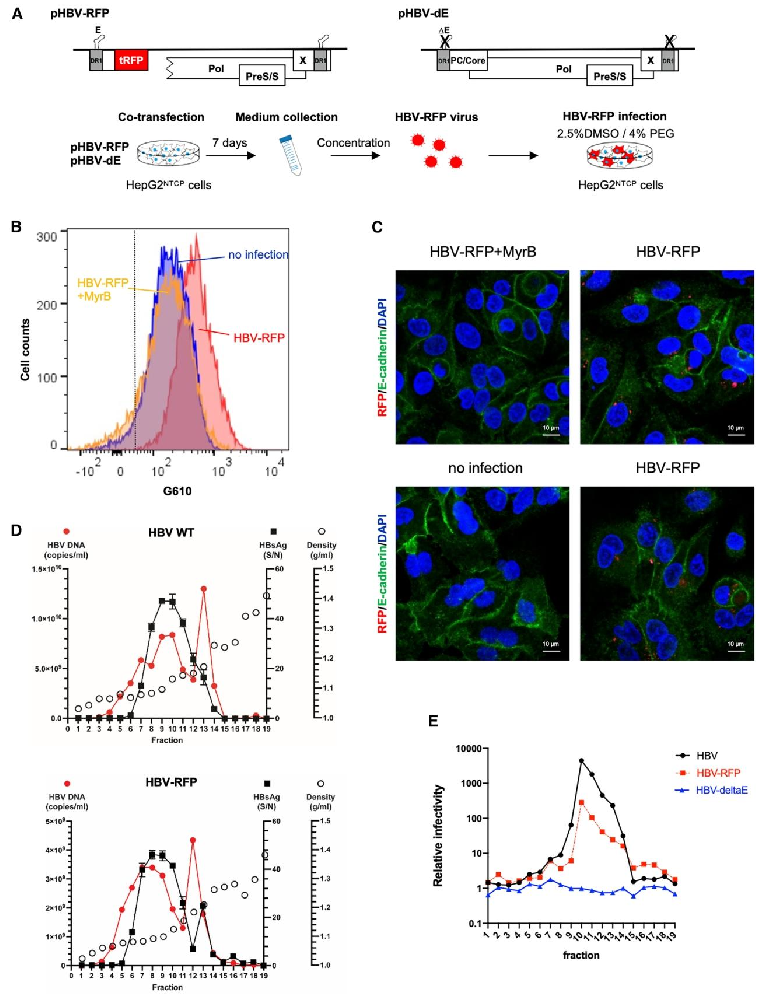
图1:表达红色荧光蛋白的 HBV-RFP 病毒的构建与鉴定
该图包含 HBV-RFP 构建流程、感染后流式检测、免疫荧光、密度梯度离心分析及各组分感染性检测结果;构建上通过共转染 pHBV-RFP 和 pHBV-dE 质粒获得 HBV-RFP,流式和免疫荧光显示 HepG2^NTCP 细胞感染后可检测到 RFP 信号,且 HBV 进入抑制剂 MyrB 能显著抑制该信号;密度梯度离心显示 HBV-RFP 与野生型 HBV 的 HBsAg 峰均在 7-10 组分,HBV DNA 在 7-10 和 12-13 组分出现两个峰;感染性实验证实 10 组分的 HBV-RFP 和野生型 HBV 均具有最高感染性,且 HBV-RFP 感染性约为野生型的 1/10,证实 HBV-RFP 可产生具有感染性的病毒颗粒,适用于后续筛选实验。
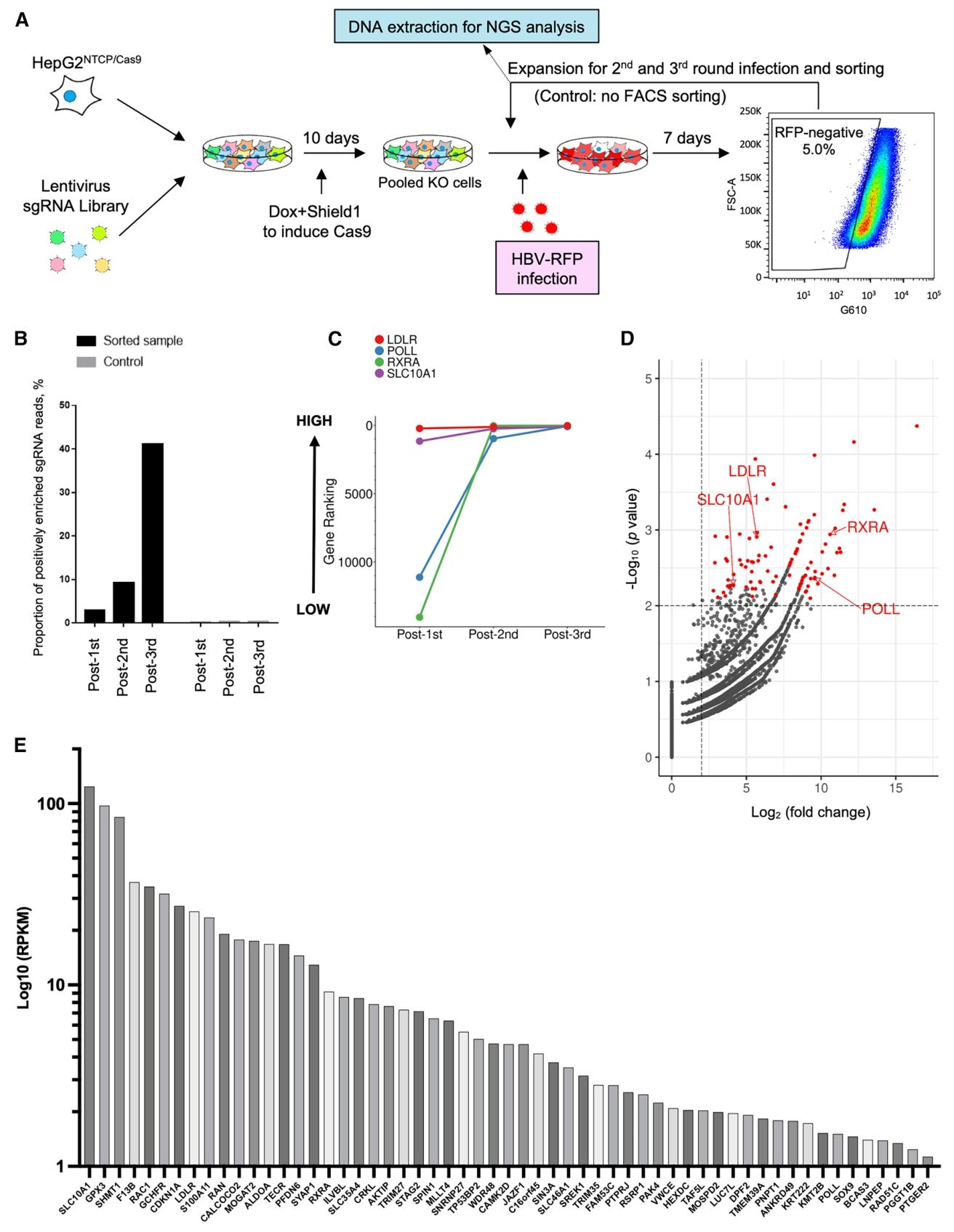
图2:全基因组 CRISPR 筛选鉴定 HBV 感染的宿主依赖基因
该图展示了 CRISPR 筛选流程、各轮筛选中阳性富集 sgRNA 的读数占比、已知 HBV 促病毒因子的富集排名、火山图及候选基因在人肝组织的表达情况;筛选流程经三轮感染 - 分选 - 富集实现目标基因筛选,阳性富集 sgRNA 的读数占比随筛选轮次逐步升高;已知促病毒因子 RXRA、POLL、LDLR、NTCP 的 RRA 评分随筛选轮次逐渐降低,富集程度不断提高;火山图筛选出 log2 倍变化 > 2 且 - log10p>2 的候选基因,其中包含上述已知因子;人肝组织表达分析显示,筛选出的前 100 个基因中 57 个 RPKM>1,最终选定 63 个基因进行后续验证,证实筛选方法的可靠性。
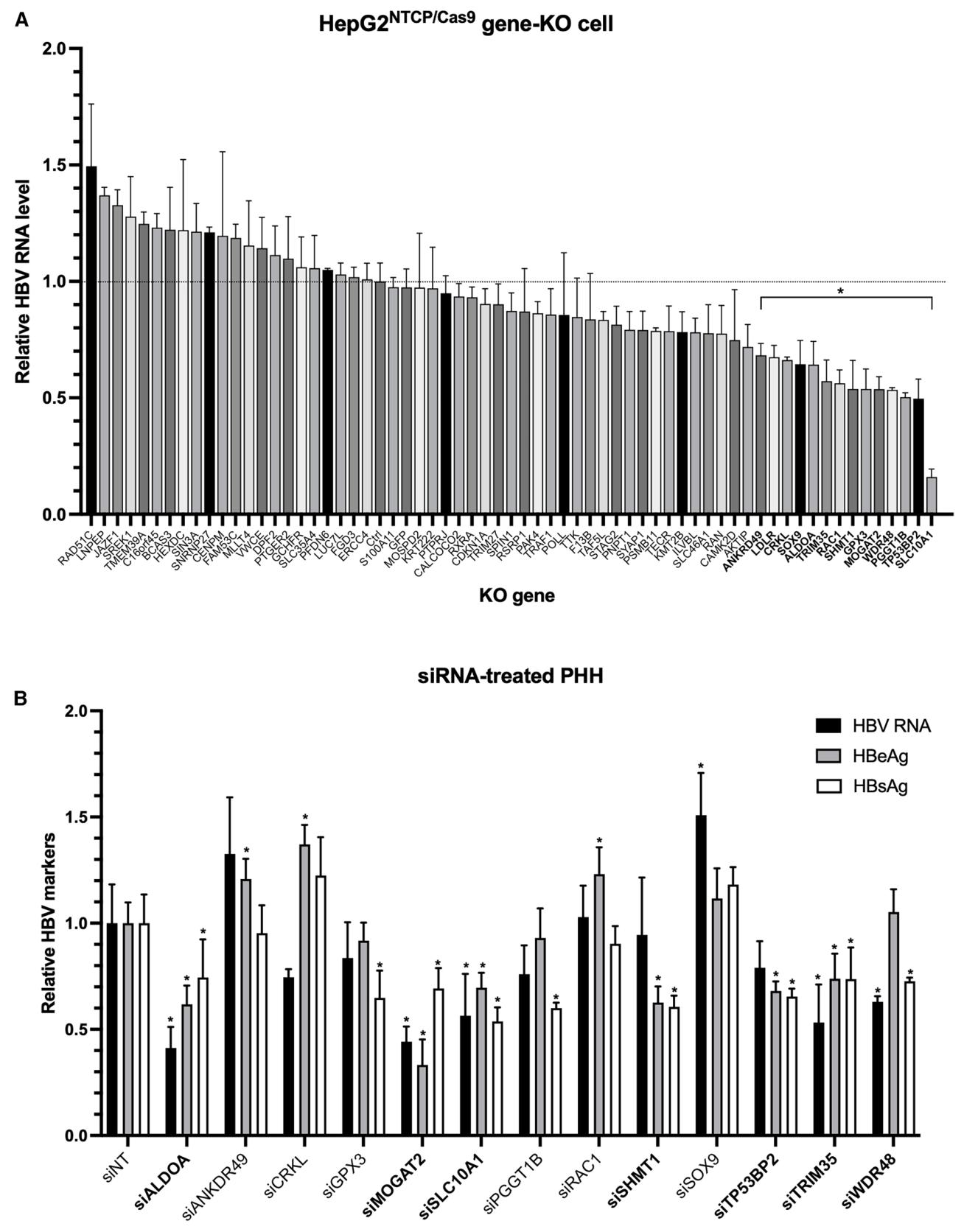
图3:HBV 感染候选宿主依赖基因的验证
该图包含 HepG2^NTCP/Cas9 基因敲除细胞的 HBV RNA 检测结果,以及 PHH 中 siRNA 敲低候选基因后的 HBV 标志物检测结果;在 63 个基因敲除细胞中,14 个基因敲除后 HBV RNA 水平显著降低,其中 NTCP 敲除的抑制效果最显著;在 PHH 中对这 14 个基因进行 siRNA 敲低验证,结果显示 ALDOA、MOGAT2、TRIM35 敲低后,HBV RNA、HBeAg、HBsAg 均显著降低,SHMT1、TP53BP2、WDR48 敲低后两个及以上 HBV 标志物显著降低,证实这些基因为 HBV 感染的潜在宿主依赖因子,最终选定 MOGAT2 进行深入研究。
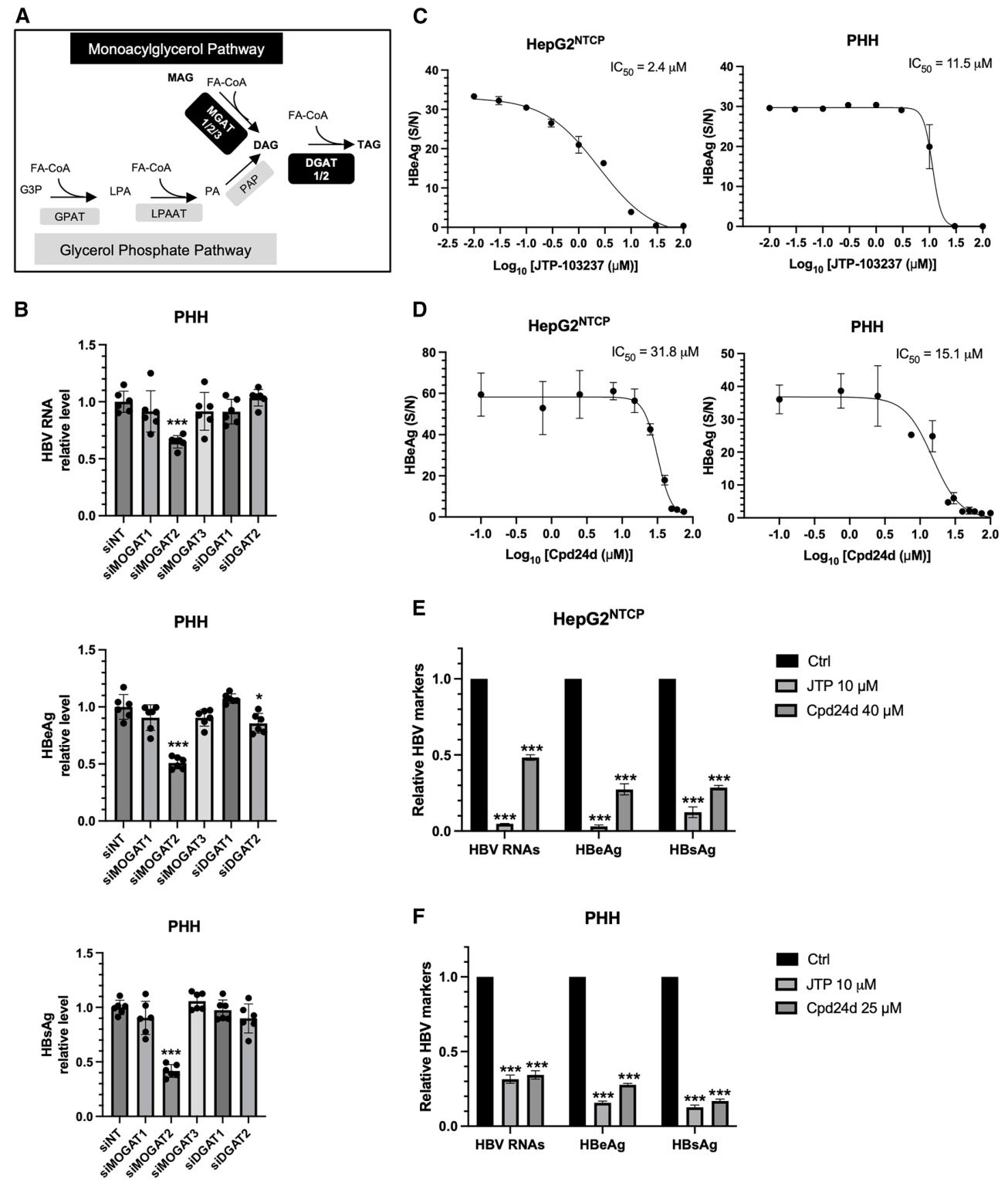
图4:MOGAT2 表达下调及抑制剂处理降低 HBV 感染相关标志物
该图包含甘油三酯合成通路示意图、PHH 中脂代谢相关基因敲低后的 HBV 标志物检测、MGAT2 抑制剂的剂量效应及抑制剂处理对 HepG2^NTCP 细胞和 PHH 中 HBV 标志物的影响;脂代谢通路显示 MOGAT2 催化单酰甘油生成二酰甘油(DAG),是单酰甘油通路的关键酶;PHH 中仅 MOGAT2 敲低能显著降低所有 HBV 标志物,其他 MOGAT 家族和 DGAT 家族基因敲低无显著效果;MGAT2 抑制剂 JTP 和 Cpd24d 对 HepG2^NTCP 细胞和 PHH 的 HBeAg 均呈剂量依赖性抑制,且具有不同的 IC50;在适宜浓度下,两种抑制剂处理均能显著降低 HepG2^NTCP 细胞和 PHH 中的 HBV RNA、HBeAg、HBsAg 水平,证实 MOGAT2 的特异性调控作用及抑制剂的抗 HBV 效果。
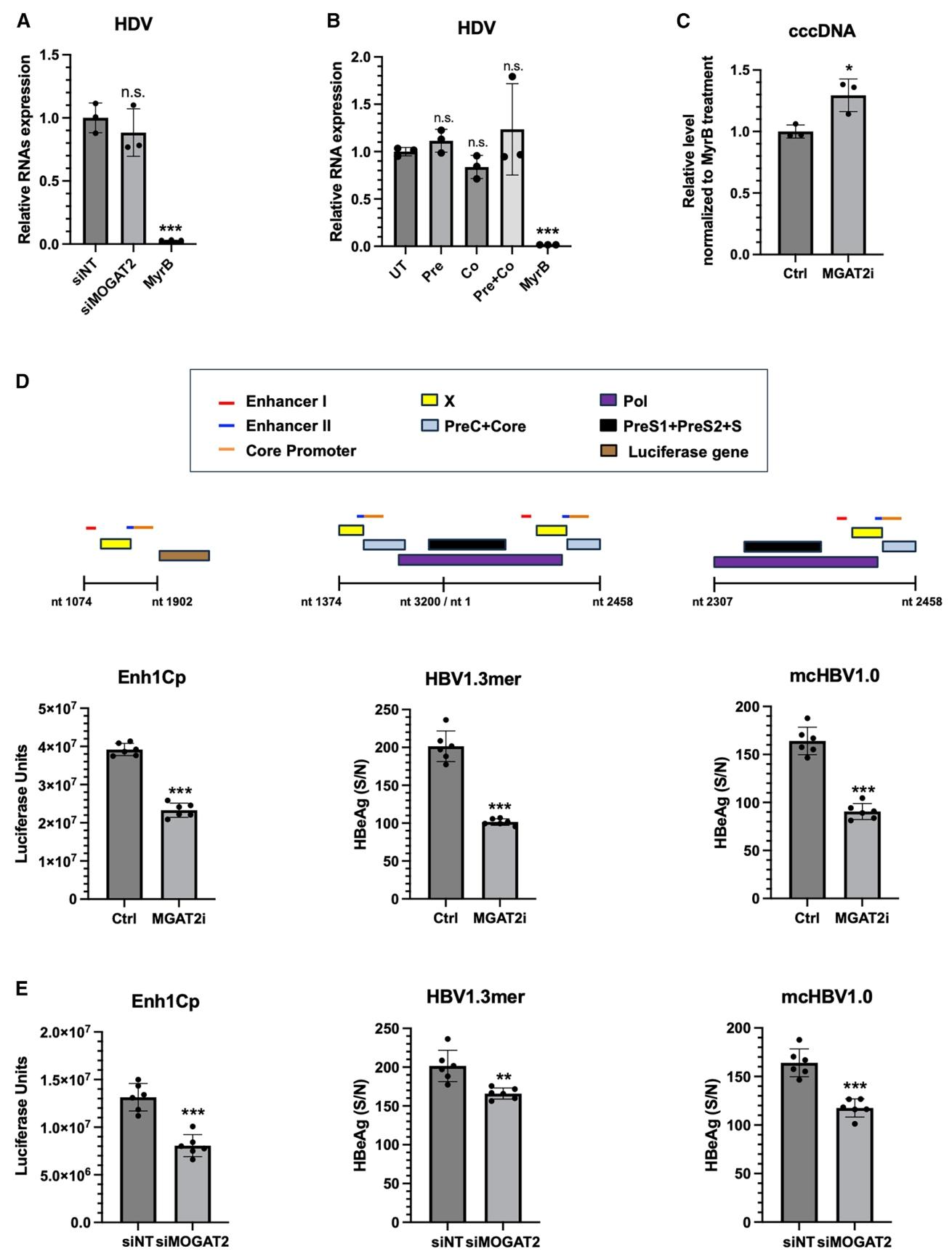
图5:MOGAT2 在 HBV 生命周期中的作用阶段鉴定
该图包含 siRNA 敲低和 MGAT2 抑制剂处理对 HDV 感染的影响、MGAT2 抑制剂对 cccDNA 水平的影响、抑制剂和 siRNA 敲低对 HBV 启动子报告基因及复制子的调控作用;HDV 感染实验显示,MOGAT2 敲低或抑制剂处理均未影响细胞内 HDV RNA 水平,说明 MOGAT2 不参与 HBV 的进入过程;cccDNA 定量显示,MGAT2 抑制剂处理对 HBV cccDNA 水平无显著负面影响;报告基因实验显示,MGAT2 抑制剂处理能显著抑制 HBV Enh1-Core 启动子驱动的荧光素酶表达,以及 HBV1.3mer 和 mcHBV1.0 复制子的 HBeAg 表达,MOGAT2 siRNA 敲低也呈现类似抑制效果,证实 MOGAT2 主要调控 HBV 的转录过程。
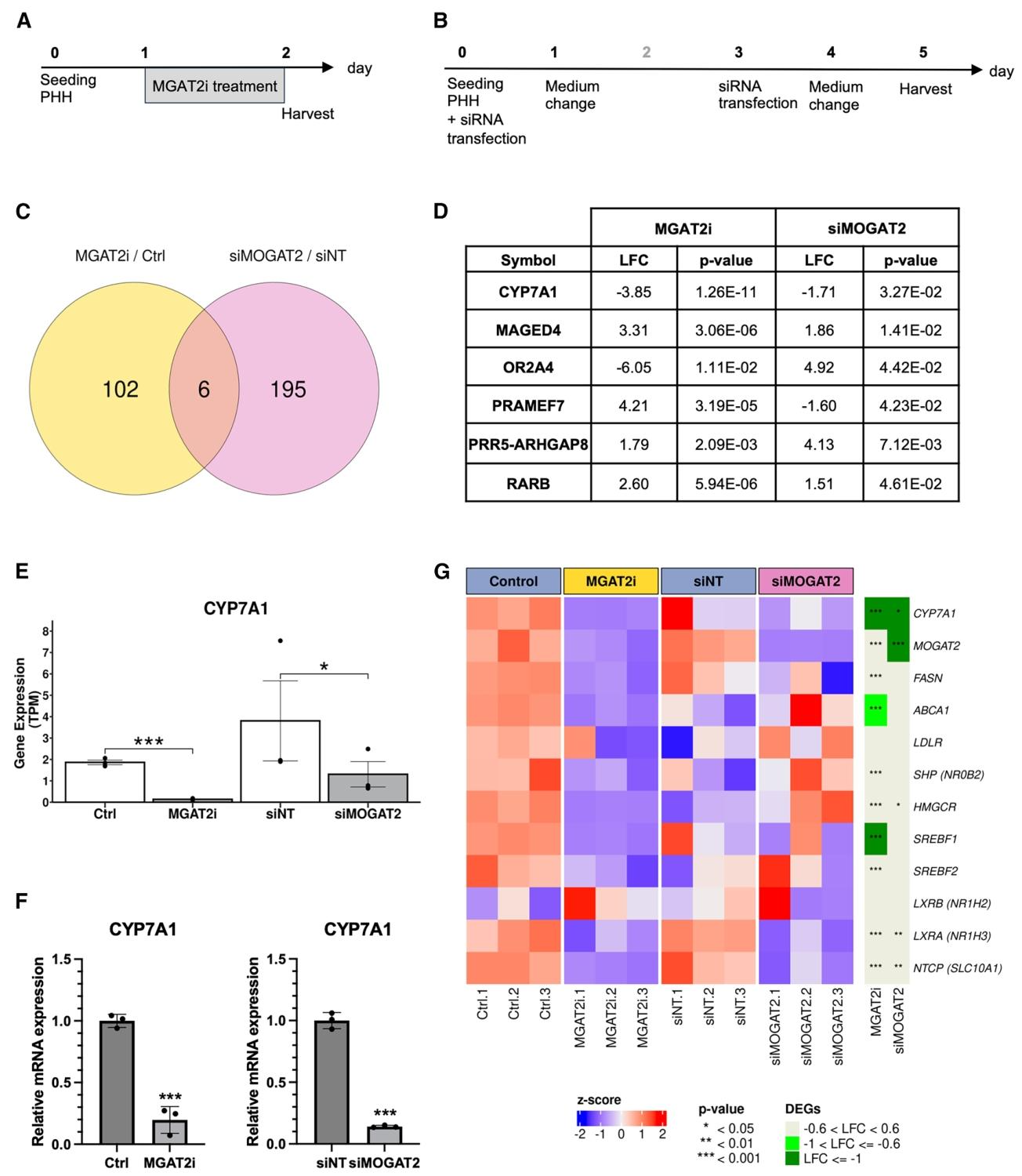
图6:MGAT2 抑制的原代人肝细胞转录组分析
该图包含 MGAT2 抑制剂处理和 siRNA 敲低的 RNA-seq 实验设计、差异表达基因韦恩图、重叠差异基因表达情况、CYP7A1 表达验证及 LXR 信号通路相关基因热图;RNA-seq 鉴定出抑制剂处理和 siRNA 敲低的重叠差异表达基因共 6 个,其中 CYP7A1 在两种处理中均显著下调;RT-qPCR 验证证实 MGAT2 抑制剂处理和 siRNA 敲低均能显著降低 CYP7A1 的表达;IPA 通路分析显示 LXR 通路富集,热图显示 LXR 信号通路相关基因(包括 LXRA、SREBF1/2、FASN 等)在 MGAT2 抑制后均显著下调,证实 MOGAT2 通过调控 LXR/CYP7A1 信号通路参与 HBV 转录的调控。
本研究成功构建了具有感染性的 D 型 HBV-RFP 报告病毒,利用该病毒结合 CRISPR 全基因组功能缺失筛选,在 HepG2^NTCP/Cas9 细胞中鉴定出 63 个 HBV 感染候选宿主促病毒因子,其中包含 RXRA、LDLR、NTCP 等已知因子,证实了筛选体系的可靠性;通过在细胞系和原代人肝细胞中的层层验证,发现并鉴定 MOGAT2 为新型 HBV 宿主促病毒因子,其敲低或特异性抑制剂处理能显著降低 HBV RNA 和抗原水平;机制研究表明 MOGAT2 不参与 HBV 的进入和 cccDNA 形成,而是通过调控 HBV 的转录过程影响病毒复制,且 MGAT2 抑制会下调 LXR/CYP7A1 信号通路相关基因的表达,该通路是其调控 HBV 转录的关键分子机制;此外,MGAT2 抑制剂已被开发用于代谢综合征的治疗,本研究为其拓展应用于 HBV 治疗提供了实验依据,也为 HBV 治愈提供了新的宿主靶向靶点,提示 MGAT2 抑制剂或可与核苷(酸)类似物联合用于慢性 HBV 感染的治疗。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:天然抗炎好物!槲皮素通过双重通路抑制胃上皮细胞炎症!
下一篇:原代小鼠骨细胞的体外力生物学研究:分离、培养与微流控整合方案优化