常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-31 09:00:00 细胞资源库平台 访问量:107
CDKL5 缺乏症(CDD)是一种罕见的发育性癫痫性脑病,由 X 染色体上 CDKL5 基因变异导致激酶功能异常引起,以婴儿期耐药性癫痫、神经发育迟滞为核心特征。现有研究多依赖小鼠模型或 NGN2 诱导神经元(iNs),但存在局限:小鼠模型难以复现人类皮质病理,iNs 虽能快速获得均一神经元,却缺乏皮质特异性,无法捕捉 CDD 关键的皮质神经元兴奋性异常。此外,CDD 患者神经元表型(如 neurite 长度、突触功能)存在研究争议,需更贴近人类皮质的模型验证。本研究通过对比 iNs 与引导皮质类器官分化的神经元(ACTX),明确皮质特异性对 CDD 病理建模的重要性,为 CDD 治疗靶点筛选提供可靠体外模型。
来自美国波士顿儿童医院、意大利 Telethon 遗传学与医学研究所的团队在《Neurobiology of Disease》发表题为Excitatory cortical neurons from CDKL5 deficiency disorder patient-derived organoids show early hyperexcitability not identified in neurogenin2 induced neurons的研究。
iPSC 来源与培养
样本:6 例 CDD 患者 iPSC(含截短突变 / 剪接突变)及同源对照(男性通过无变异克隆筛选,女性通过 X 染色体失活筛选),培养于 Stemflex/mTeSR Plus 培养基,验证核型正常且无支原体污染。
两种神经元模型构建
NGN2 诱导神经元(iNs):iPSC 经 Accutase 解离后,用含 DOX、BDNF、NT3、层粘连蛋白的 N2 培养基诱导 NGN2 过表达,2 天后换 B27 培养基并加 Ara-C 抑制胶质细胞,6 天后与健康星形胶质细胞共培养或用星形胶质细胞条件培养基。
皮质类器官来源神经元(ACTX):iPSC 先经双 Smad 抑制剂(SB431542、LND193189)诱导神经干细胞,再悬浮培养为 3D 类球体,21 天后用 CHIR99021(Wnt 激动剂)+PD0325901(MEK 抑制剂)分化,28 天后加 DAPT(Notch 抑制剂)等加速成熟,解离后接种为 2D 培养,验证皮质标志物(TBR1、FOXG1)。
分子与功能检测
Western blot:检测 CDKL5 靶蛋白 p-EB2(Ser222)及微管 / 信号通路蛋白(p-AKT、p-GSK 等);
转录组分析:iNs 用 Ampliseq,ACTX 用 bulk RNA-seq,筛选差异基因(DEG),与原代胎儿皮质 / 背根神经节数据做 Spearman 相关;
形态分析:免疫荧光(MAP2、TBR1)结合高内涵成像,Incucyte 活细胞成像量化 24 小时内 neurite 长度;
功能检测:多电极阵列(MEA)记录神经元同步指数、加权平均放电率,评估网络兴奋性(iNs 从第 8 天、ACTX 从解离后开始记录)。
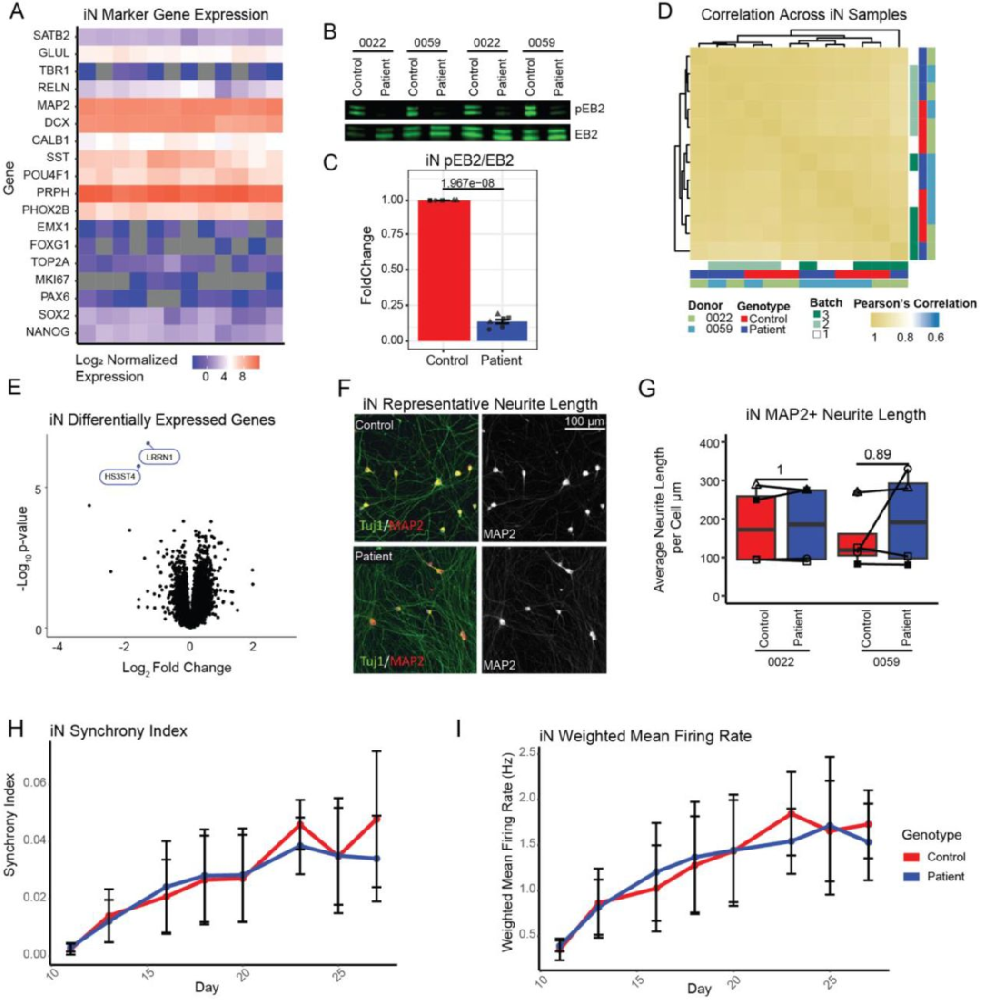
图 1:NGN2 诱导神经元(iNs)的分子特征与功能缺失
该图验证 iNs 的 CDKL5 分子缺陷但无病理表型:(A-B)Western blot 显示 CDD 患者 iNs 的 p-EB2/EB2 比值显著降低(p=1.97e-8),确认 CDKL5 功能异常;(C-D)基因表达分析:5000 个最可变基因的 Pearson 相关系数达 0.92-0.99,仅 HS3ST4、LRRN1 两个基因差异表达;(E-H)形态学:iNs 的 MAP2+ neurite 长度在患者与对照间无显著差异;(I-J)MEA 结果:同步指数、加权平均放电率无组间差异。图示 iNs 虽能复现 CDKL5 分子缺陷,但因缺乏皮质身份,无法模拟 CDD 的神经元功能异常。
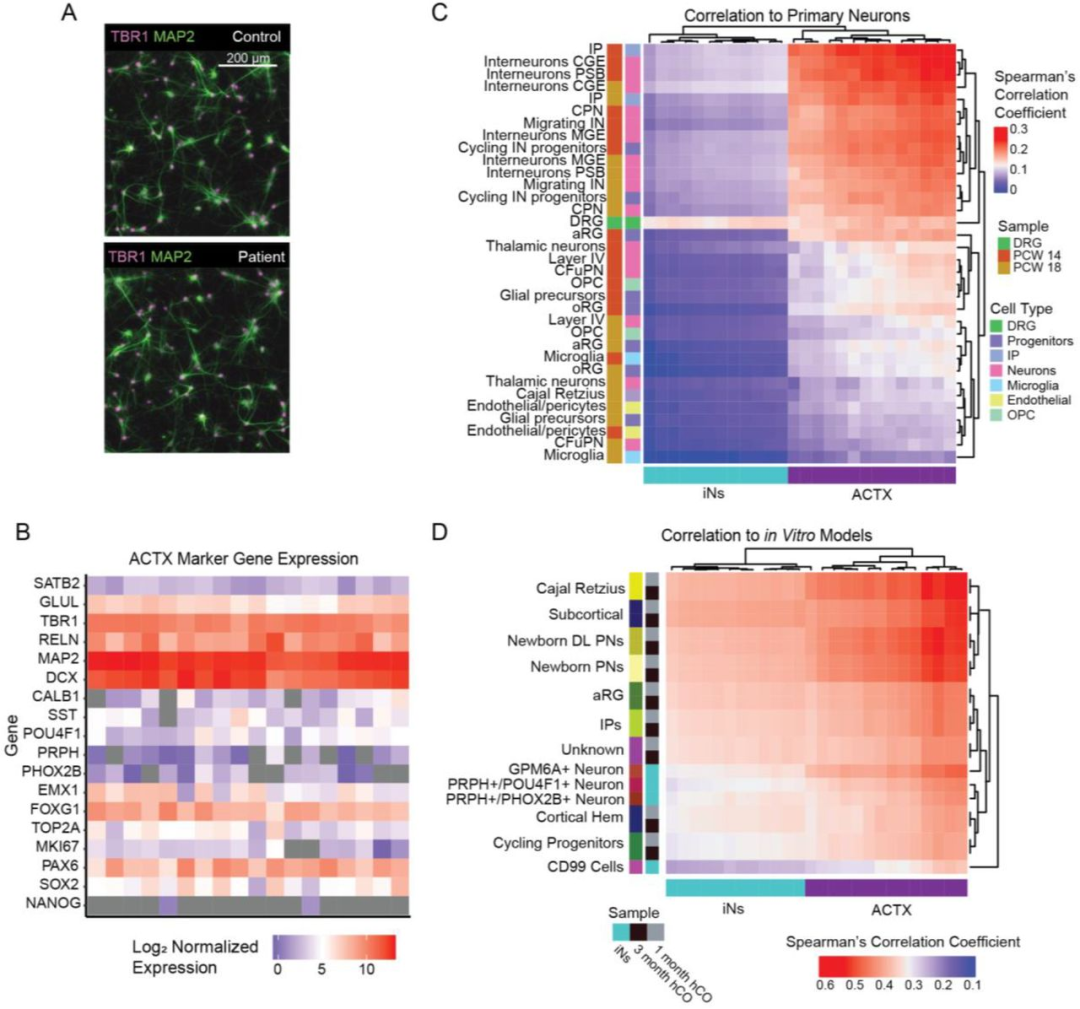
图 2:ACTX 神经元的皮质身份验证
该图对比 iNs 与 ACTX 的细胞类型特异性:(A)免疫荧光显示 ACTX 神经元共表达皮质标志物 TBR1 与神经元标志物 MAP2;(B)基因表达:ACTX 高表达皮质标志物 FOXG1、EMX1,低表达祖细胞基因(TOP2A、PAX6);(C-D)相关性分析:ACTX 与原代胎儿皮质中间祖细胞 / Spearman 相关系数达 0.29-0.32,与已发表皮质类器官相关系数 0.6,而 iNs 更贴近背根神经节(相关系数 0.2)。图示 ACTX 具备明确的皮质神经元身份,优于 iNs 的外周神经元特征。
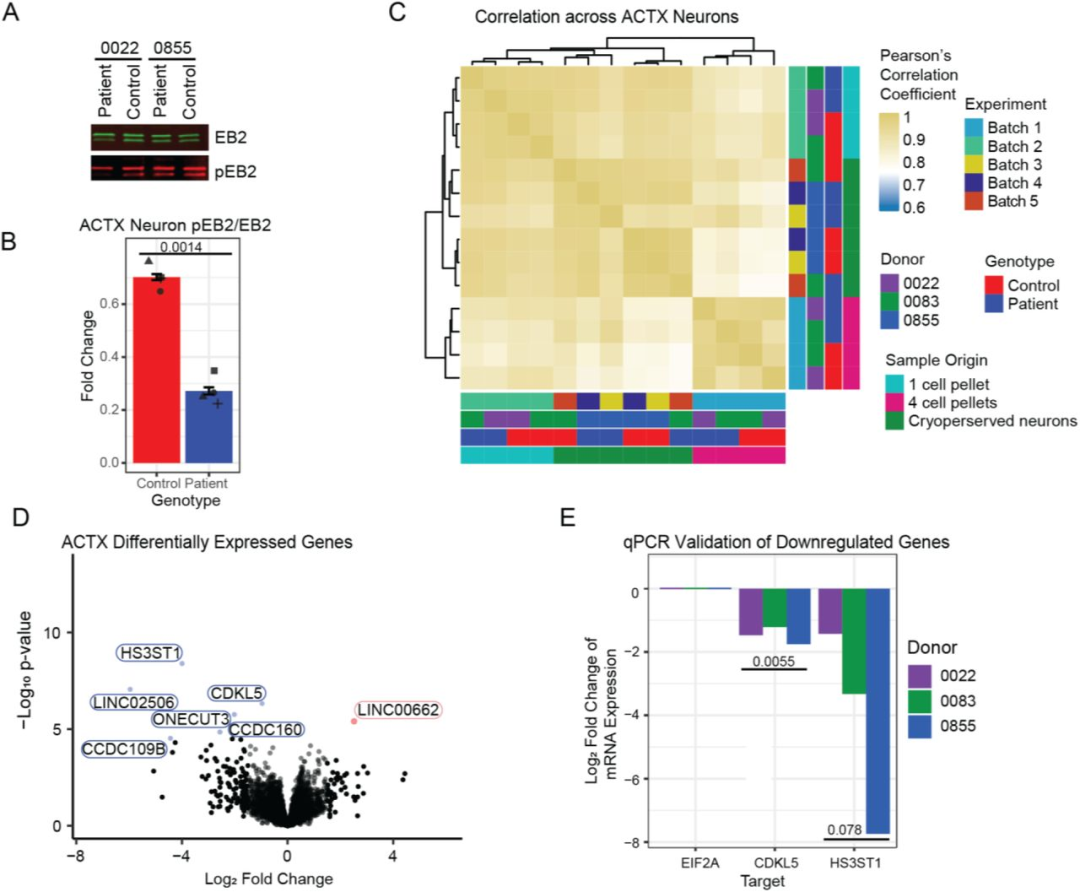
图 3:ACTX 神经元的 CDKL5 缺陷与基因表达变化
该图展示 ACTX 的分子病理特征:(A-B)Western blot 确认 CDD 患者 ACTX 的 p-EB2/EB2 比值降低(p=0.0014);(C)基因表达相关性:患者与对照 ACTX 的 Pearson 相关系数达 0.9-0.99,样本重复性好;(D-E)差异基因:共筛选 7 个 DEG,CDKL5(p=0.0055)、HS3ST1(p=0.078)显著下调,qPCR 验证 CDKL5 表达降低,HS3ST1 趋势一致。图示 ACTX 不仅复现 CDKL5 分子缺陷,还存在突触相关基因表达变化,提示 extracellular matrix 可能参与病理。
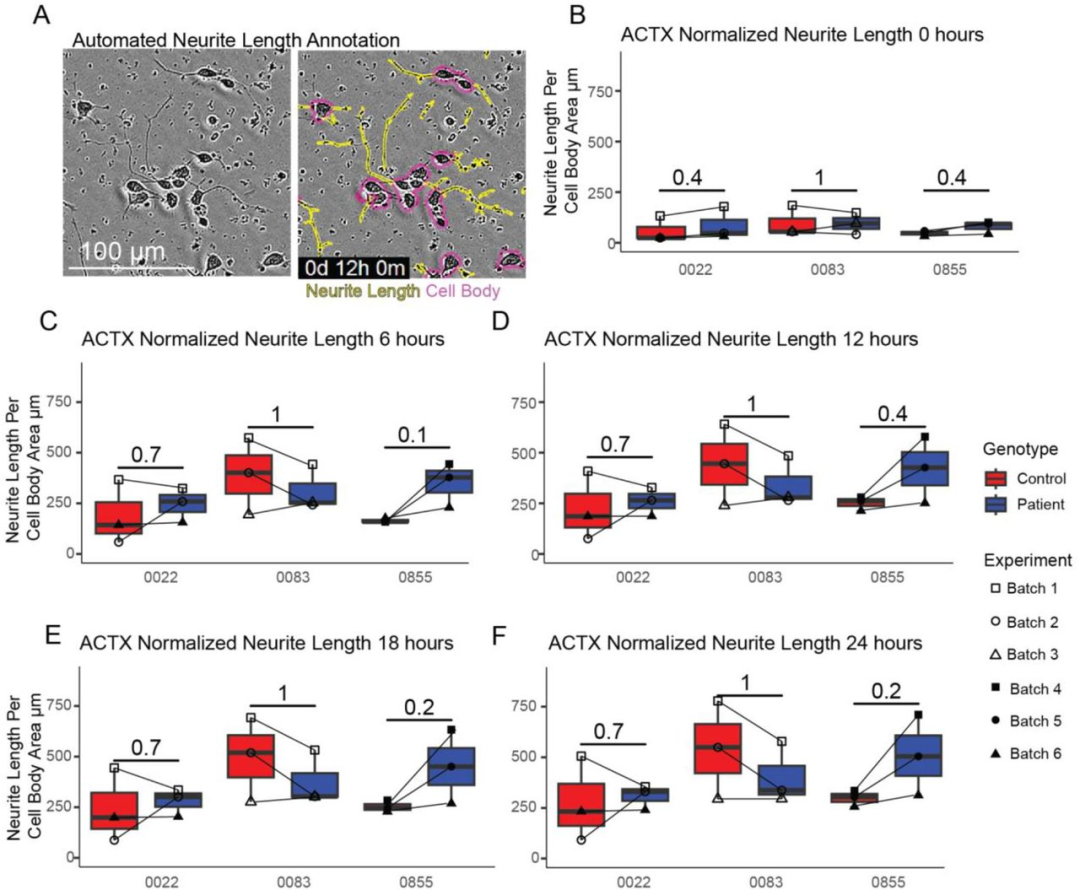
图 4:ACTX 神经元的 neurite 长度无差异
该图量化 ACTX 的形态表型:(A)Incucyte 活细胞成像的 neurite 分割示例;(B-F)24 小时内(0、6、12、18、24 小时),3 例 CDD 患者与同源对照的 normalized neurite 长度无显著差异(所有时间点 p>0.05)。图示 CDKL5 截短突变不影响皮质神经元的短期 neurite 生长,与部分既往研究的 neurite 异常结论差异可能源于神经元亚型或培养时长。
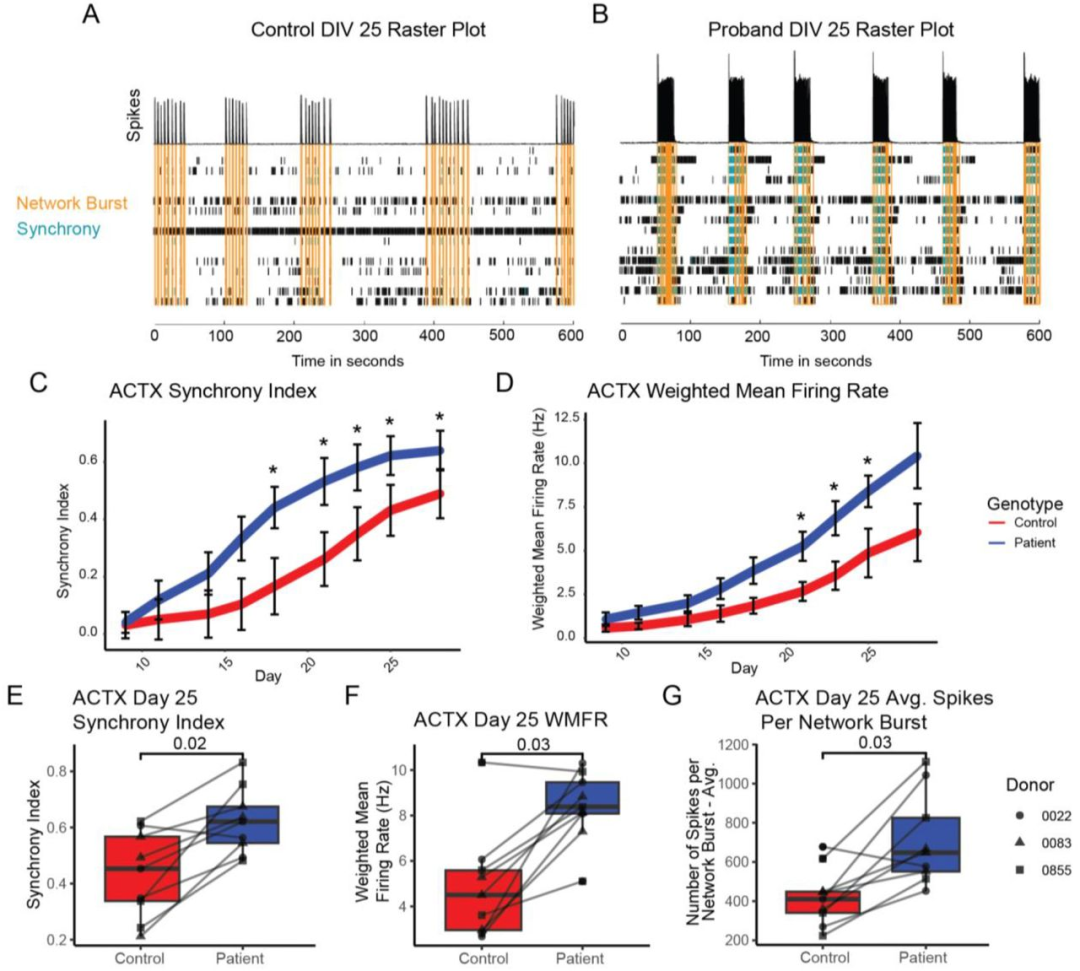
图 5:ACTX 神经元的早期网络高兴奋性
该图验证 ACTX 的功能病理:(A-B) raster 图显示第 25 天对照(A)与 CDD 患者(B)ACTX 的网络爆发差异,患者神经元同步性更高;(C-D)MEA 量化:第 20-28 天,患者 ACTX 的同步指数(p<0.05)、加权平均放电率(p<0.05)显著高于对照;(E-G)第 25 天单独分析:患者的同步指数、加权平均放电率、每爆发尖峰数均显著升高。图示 CDD 患者皮质神经元在网络成熟早期即出现高兴奋性,且此表型仅在 ACTX 中存在。
本研究对比两种 CDD 体外模型,发现 NGN2 诱导神经元(iNs)虽能复现 CDKL5 靶蛋白 p-EB2 降低的分子缺陷,但因缺乏皮质身份,无 neurite 形态异常及网络功能异常;而引导皮质类器官分化的 ACTX 神经元,不仅具备明确的皮质标志物(TBR1、FOXG1),还能模拟 CDD 核心病理 —— 早期网络高兴奋性,同时发现 CDKL5、HS3ST1 下调可能参与突触微环境异常。研究明确 “皮质特异性” 是 CDD 病理建模的关键,ACTX 模型为 CDD 的兴奋性机制研究及治疗药物筛选提供可靠工具。局限性包括:iNs 样本量较小(2 例患者)、ACTX 长期培养(>30 天)后高兴奋性表型因细胞死亡 / 聚集消失,未来需优化培养条件并扩大样本验证基因型 - 表型关联。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:漂浮子宫内膜类器官模型:体外复现上皮 - 基质细胞互作,助力生殖医学研究
下一篇:天然抗炎好物!槲皮素通过双重通路抑制胃上皮细胞炎症!