常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-28 09:00:00 细胞资源库平台 访问量:108
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:BMPR2 Preserves Mitochondrial Function and DNA Integrity During Reoxygenation to Promote Endothelial Survival and Reverse Pulmonary Hypertension
中文标题:在复氧过程中维持线粒体功能和 DNA 完整性以促进内皮细胞存活并逆转肺动脉高压
发表期刊:《Cell Metab》
影响因子:30.9
作者单位:
1.Department of Pediatrics, Cardiovascular Institute, Stanford University School of Medicine, Stanford, CA 94305, USA
2.The Vera Moulton Wall Center for Pulmonary Vascular Disease, Stanford University School of Medicine, Stanford, CA 94305, USA
3.Department of Medicine, Weill Cornell Medical College, New York, NY 10065, USA
作者信息:
Isabel Diebold、Jan K. Hennigs、Kazuya Miyagawa、Caiyun G. Li、Nils P. Nickel、Mark Kaschwich、Aiqin Cao、Lingli Wang、Sushma Reddy、Pin-I Chen、Miguel A. Alejandre Alcazar、Rachel K. Hopper、Lijuan Ji、Brian J. Feldman(共一作),通讯作者:Marlene Rabinovitch
肺动脉高压(PAH)是一种无法治愈的疾病,其特征为肺动脉内皮细胞(PAEC)凋亡、微血管减少和闭塞性血管重塑,线粒体功能障碍、炎症反应及骨形态发生蛋白受体 2(BMPR2)突变均与该病相关。约 70% 的家族性 PAH 患者和 20% 的散发性特发性 PAH 患者存在 BMPR2 基因突变,且无论是否存在突变,PAH 患者均存在 BMPR2 表达降低的情况。BMPR2 信号受损与 PAEC 凋亡倾向增强、促炎状态放大相关,而 PAEC 功能障碍是导致肺血管阻力增加的核心病理变化。线粒体作为内皮细胞耐受损伤刺激的能量核心,其在缺氧 - 复氧过程中的适应能力异常可能参与 PAH 相关的 EC 功能障碍,但 BMPR2 与线粒体功能之间的直接关联尚未明确。已知 BMPR2 可调节过氧化物酶体增殖物激活受体 γ(PPARγ)介导的基因转录,而 PPARγ 共激活因子 1α(PGC1α)在 mitochondrial 生物发生中起关键作用,且受肿瘤抑制因子 p53 调控,PGC1α 还可激活转录因子 NRF1/2,进而调控线粒体转录因子 A(TFAM)等线粒体 DNA 复制相关基因的表达,基于此,本研究推测 BMPR2 可能通过调控 p53-PGC1α-NRF2-TFAM 通路影响线粒体功能,进而参与 PAH 的发病机制。
本研究采用内皮细胞特异性 Bmpr2 敲除(EC-Bmpr2⁻/⁻)小鼠、BMPR2 siRNA 转染的正常人 PAEC 及携带 BMPR2 突变的 PAH 患者来源 PAEC 三种模型;小鼠经他莫昔芬诱导激活 CRE 重组酶实现 EC 特异性 Bmpr2 敲除,随后暴露于 3 周缺氧(10% O₂)+4 周复氧环境或持续常氧环境,检测右心室收缩压(RVSP)、右心室肥厚(RVH)、肺小动脉肌化程度及微血管数量等指标;通过免疫印迹检测 p53、PGC1α、NRF2、TFAM 等蛋白表达,利用 JC-1、TMRE 荧光探针检测线粒体膜电位(Δψₘ),借助 MitoSOX Red 和二氢乙锭(DHE)染色检测活性氧(ROS)水平;采用 SeaHorse 细胞外通量分析仪测定线粒体耗氧率(OCR)和糖酵解相关指标(胞外酸化率);通过 PCR 和 qPCR 检测线粒体 DNA(mtDNA)4977bp 缺失(ΔmtDNA⁴⁹⁷⁷),利用 caspase 3/7 活性测定、Sub G1 流式分析评估细胞凋亡;通过 Transwell 迁移实验、Matrigel 管形成实验检测 EC 功能;在 PAH 患者来源 PAEC 中验证上述关键指标,并通过 TLR9 抑制剂处理探究炎症因子 IL8 的调控机制;所有实验数据采用双因素方差分析结合 Bonferroni、Newman Keul´s 或 Fisher LSD 多重比较检验,p<0.05 为差异显著。
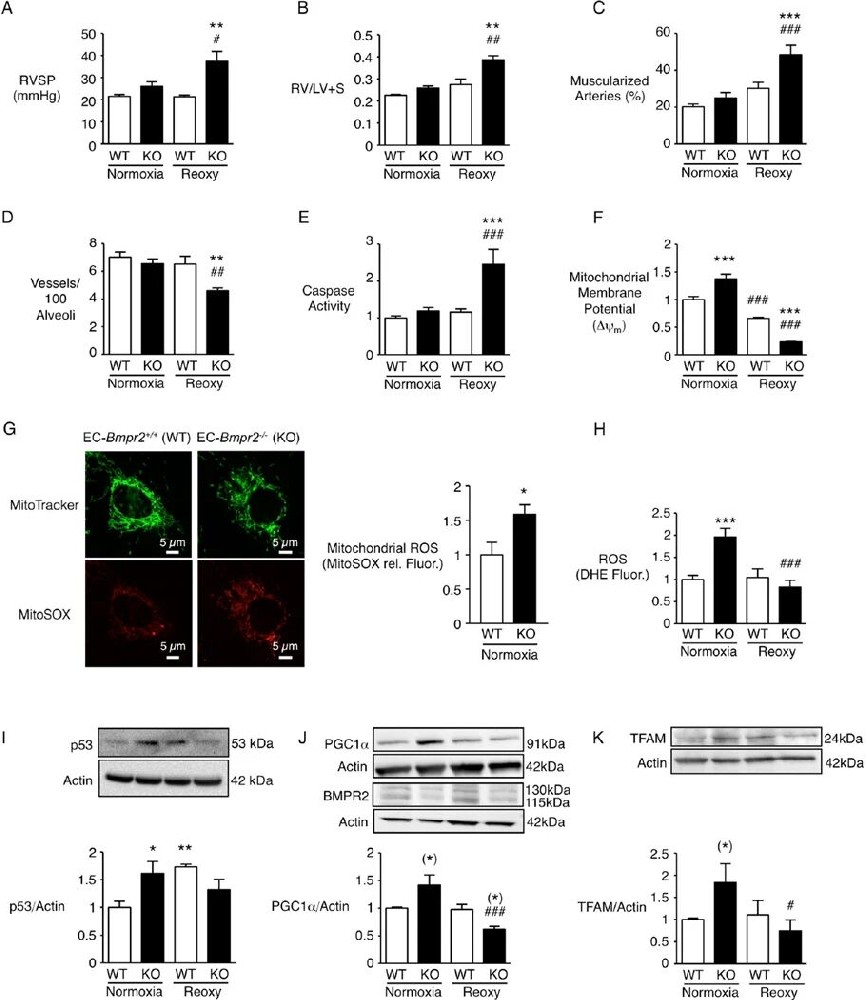
图1:EC-Bmpr2⁻/⁻小鼠在缺氧 - 复氧后表现为持续性肺动脉高压及线粒体功能异常
该图对比了 EC-Bmpr2⁻/⁻(KO)小鼠与野生型(WT)小鼠在常氧和缺氧 - 复氧(Reoxy)条件下的核心指标:复氧后 WT 小鼠 RVSP 恢复至缺氧前水平,而 KO 小鼠 RVSP 显著升高,且存在明显 RVH(RV/LV+S 比值升高)、远端肺动脉肌化程度增加及每 100 个肺泡对应的微血管数量减少;KO 小鼠肺 EC 的 caspase 3/7 活性升高,凋亡增强,常氧下线粒体膜电位和 ROS 水平升高,复氧后则显著降低;免疫印迹结果显示,KO 小鼠肺 EC 在常氧下 p53、PGC1α、TFAM 蛋白表达升高,复氧后均低于 WT 小鼠水平,证实 Bmpr2 缺失导致小鼠缺氧 - 复氧后肺动脉高压无法逆转,且与线粒体功能异常及 p53-PGC1α-TFAM 通路调控异常相关。
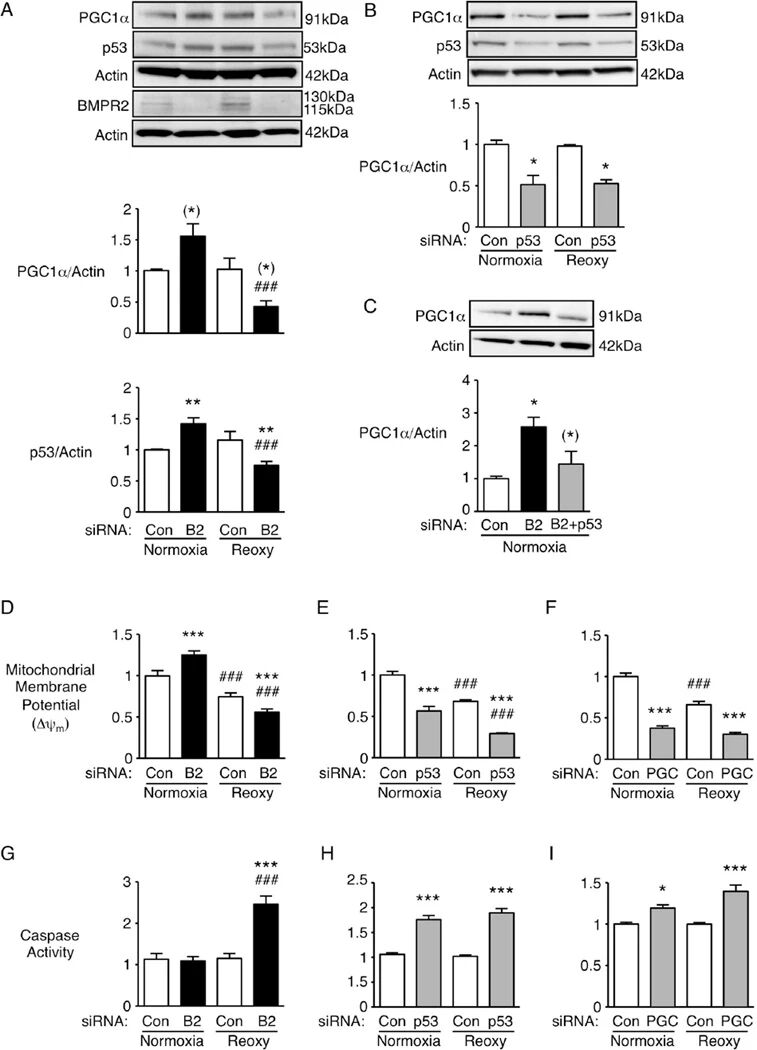
图2:BMPR2 通过调控 p53 和 PGC1α 影响 PAEC 的线粒体膜电位和凋亡
该图通过 BMPR2、p53、PGC1α siRNA 转染的人 PAEC 实验明确三者调控关系:BMPR2 siRNA 转染后,PAEC 在常氧下 p53、PGC1α 表达升高,复氧后则降低,且 p53 位于 BMPR2 下游并调控 PGC1α 表达;BMPR2 缺失在常氧下升高线粒体膜电位,复氧后进一步降低,而 p53 或 PGC1α 敲低均会降低两种条件下的线粒体膜电位;BMPR2 缺失显著增加复氧条件下 PAEC 的 caspase 3/7 活性,p53 或 PGC1α 敲低也会升高两种条件下的细胞凋亡,提示 p53 和 PGC1α 在 PAEC 中具有促存活作用,BMPR2 通过调控二者表达影响线粒体功能和细胞凋亡。
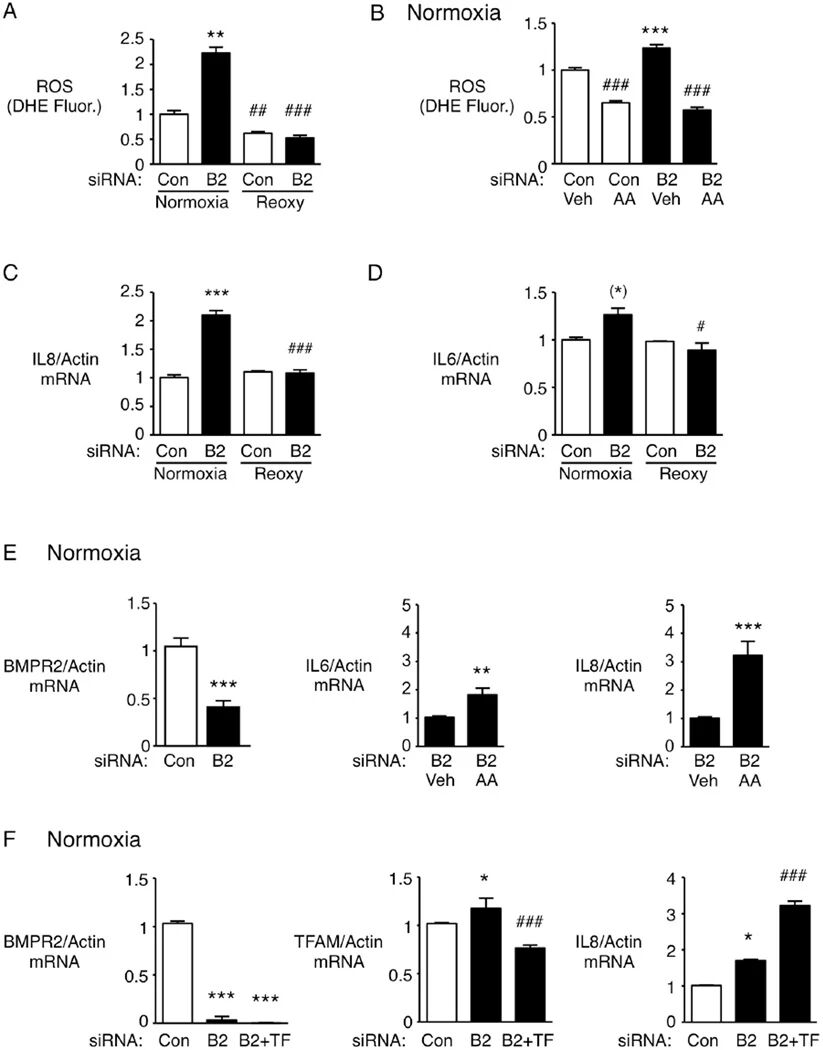
图3:BMPR2 降低在常氧下诱导 PAEC 的促炎反应
该图聚焦 BMPR2 缺失对 PAEC 炎症反应的影响:BMPR2 siRNA 转染的 PAEC 在常氧下 ROS 水平升高,复氧后 ROS 水平降低,线粒体复合体 III 抑制剂抗霉素 A(AA)可阻断 BMPR2 缺失诱导的 ROS 升高;BMPR2 缺失在常氧下显著上调 IL8 和 IL6 mRNA 表达,复氧后表达降低,且 AA 处理可进一步升高 IL8 和 IL6 mRNA 水平;TFAM siRNA 转染会加剧 BMPR2 缺失诱导的 IL8 mRNA 升高,证实 BMPR2 缺失在常氧下通过线粒体 ROS 和 TFAM 调控促炎因子表达,引发促炎状态。
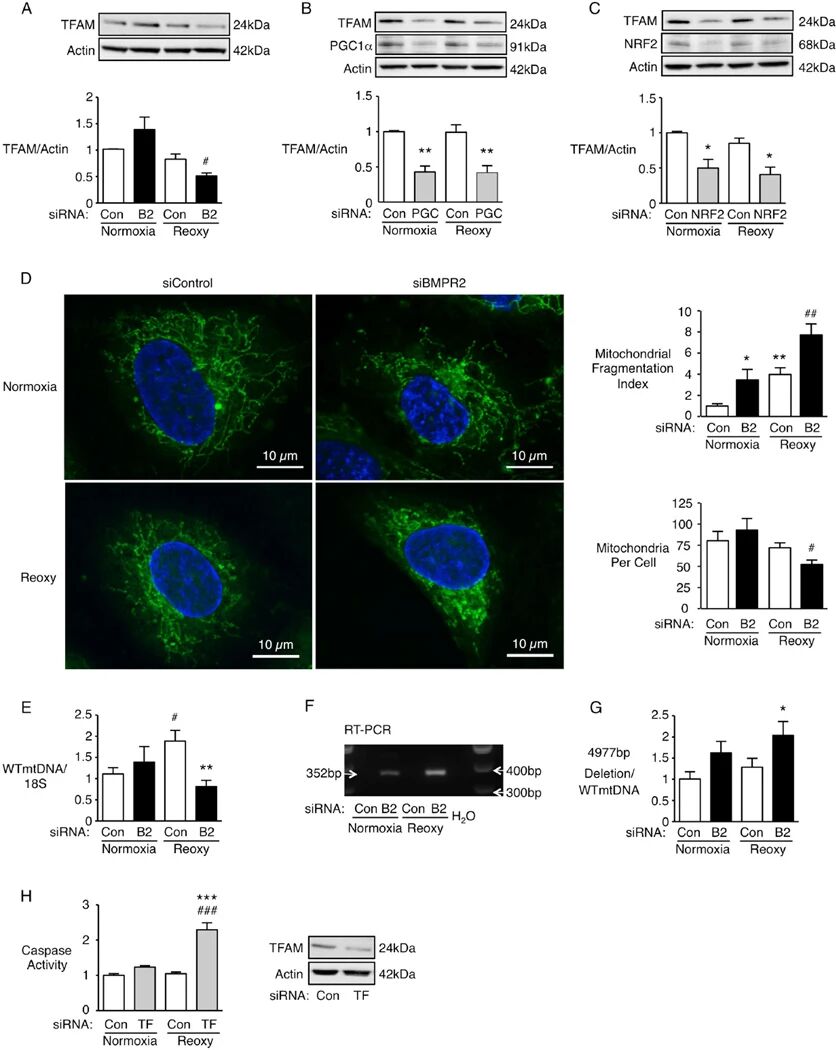
图4:BMPR2 降低导致缺氧 - 复氧条件下 TFAM 减少、mtDNA 缺失及细胞凋亡增加
该图揭示 BMPR2 对 mtDNA 完整性的调控作用:BMPR2、PGC1α 或 NRF2 siRNA 转染均会降低 PAEC 在常氧和复氧下的 TFAM 蛋白表达;BMPR2 缺失在常氧下诱导线粒体分裂增加,复氧后分裂进一步加剧,且复氧下 mtDNA 总量减少;PCR 和 qPCR 证实,BMPR2 缺失显著增加复氧条件下 ΔmtDNA⁴⁹⁷⁷的丰度;TFAM siRNA 转染可模拟 BMPR2 缺失的效应,在复氧下显著升高 PAEC 的 caspase 活性,表明 TFAM 减少是 BMPR2 缺失诱导 mtDNA 损伤和细胞凋亡的关键中介。
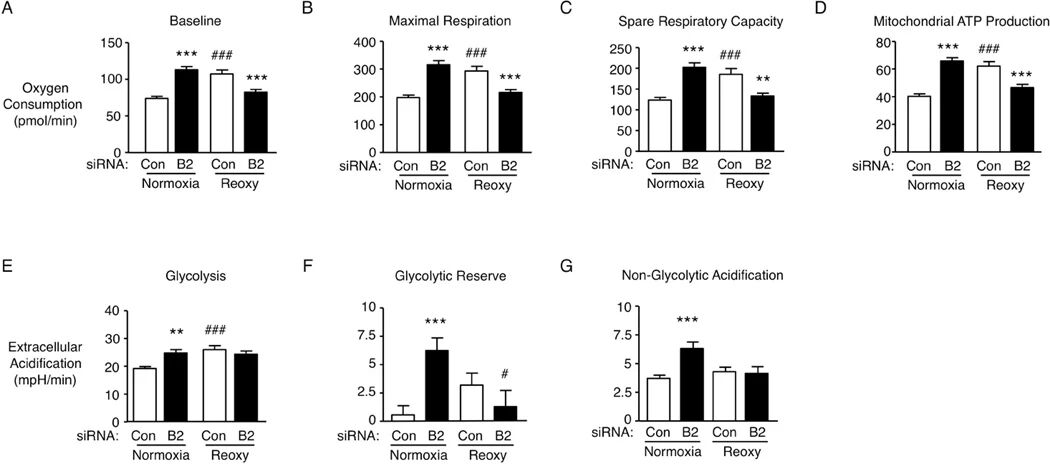
图5:BMPR2 缺失改变 PAEC 的线粒体代谢和葡萄糖利用
该图通过 SeaHorse 分析检测线粒体功能和糖酵解指标:BMPR2 siRNA 转染的 PAEC 在常氧下基础耗氧率、最大耗氧率、备用呼吸容量及线粒体 ATP 生成均升高,而复氧后这些指标均显著低于对照组;BMPR2 缺失在常氧下升高糖酵解水平和糖酵解储备,复氧后糖酵解储备显著降低,非糖酵解性酸化无明显差异,证实 BMPR2 缺失对 PAEC 代谢的调控具有氧环境依赖性,复氧后线粒体能量代谢和糖酵解储备均受损。
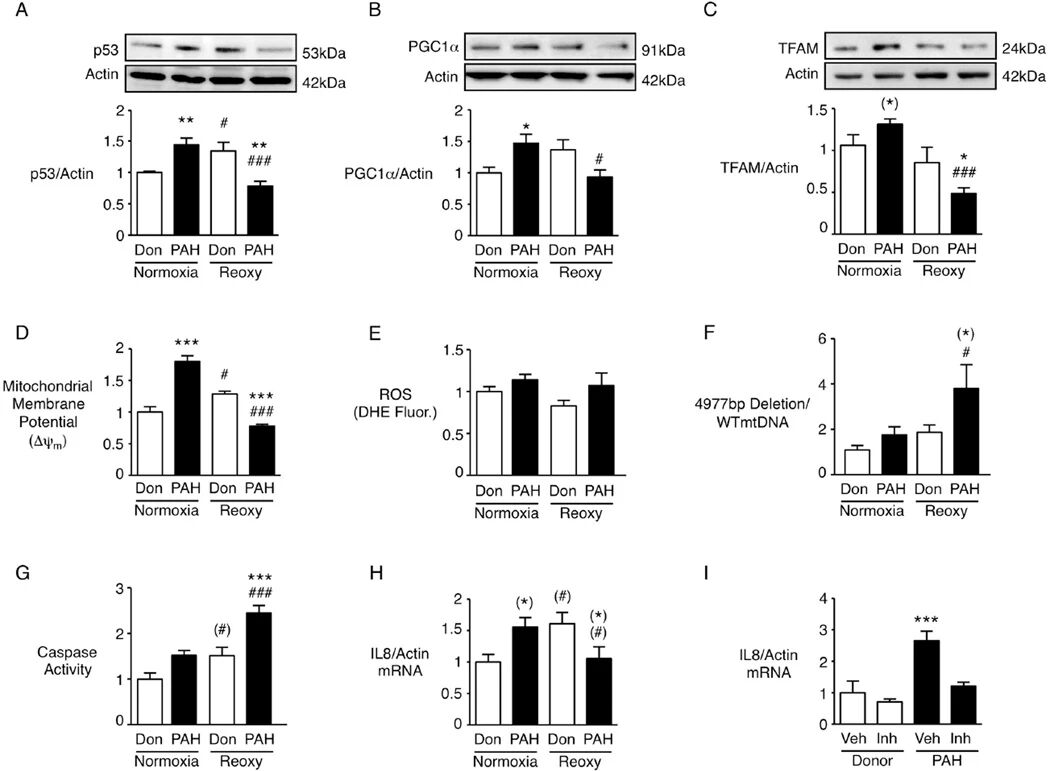
图6:PAH 患者来源 PAEC 重现常氧下促炎状态和缺氧 - 复氧下促凋亡状态
该图验证了 PAH 患者 PAEC 的核心表型:患者 PAEC 在常氧下 p53、PGC1α、TFAM 蛋白表达升高,复氧后均降低;常氧下线粒体膜电位升高,复氧后降低;复氧后 ΔmtDNA⁴⁹⁷⁷丰度显著升高,caspase 活性显著增强;常氧下 IL8 mRNA 表达升高,复氧后降低;TLR9 抑制剂可显著降低患者 PAEC 的 IL8 mRNA 水平,证实 TLR9 介导了 PAH 患者 PAEC 的 IL8 表达调控,且患者 PAEC 重现了 BMPR2 缺失相关的核心表型。
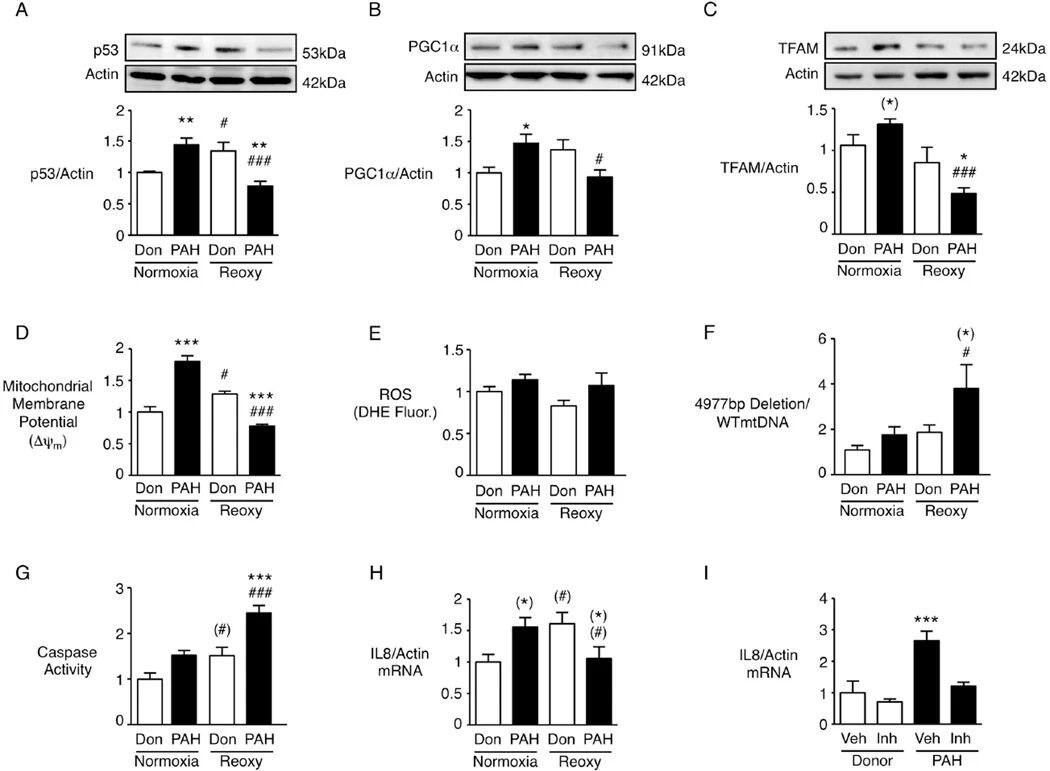
图7:BMPR2 信号与线粒体功能关联的工作模型图
该图总结了 BMPR2 调控 PAEC 功能的核心机制:常氧条件下,BMPR2 缺失通过增强 p53-PGC1α-NRF2-TFAM 通路活性,升高线粒体膜电位、ATP 生成和糖酵解水平,诱导线粒体分裂,引发 IL8、IL6 等促炎因子表达(TFAM 可部分缓解 IL8 升高);缺氧 - 复氧条件下,BMPR2 缺失抑制 p53-PGC1α-NRF2-TFAM 通路,导致线粒体膜电位和 ATP 生成降低,线粒体分裂加剧及 mtDNA⁴⁹⁷⁷缺失,最终诱导 PAEC 凋亡;上述两种状态分别通过炎症反应和 EC 凋亡导致肺微血管减少、血管重塑,最终引发肺动脉高压。
本研究通过三种实验模型证实,BMPR2 在维持肺动脉内皮细胞(PAEC)功能和线粒体稳态中发挥关键作用,其表达异常参与肺动脉高压(PAH)的发病机制。BMPR2 缺失在常氧下会激活 p53-PGC1α-NRF2-TFAM 通路,升高线粒体膜电位、活性氧(ROS)生成和糖酵解水平,诱导线粒体分裂,引发 IL8、IL6 等促炎因子表达,形成促炎状态;而在缺氧 - 复氧条件下,BMPR2 缺失会抑制该通路,导致线粒体膜电位和 ATP 生成降低,线粒体分裂加剧及 mtDNA⁴⁹⁷⁷缺失,最终诱导 PAEC 凋亡。携带 BMPR2 突变的 PAH 患者来源 PAEC 重现了上述核心表型,且 TLR9 抑制剂可缓解其 IL8 介导的炎症反应。该研究揭示了 BMPR2 通过调控 p53-PGC1α-NRF2-TFAM 通路维持线粒体功能和 DNA 完整性的分子机制,为 PAH 的治疗提供了新的靶点,同时提示缺氧 - 复氧环境可能加剧 BMPR2 功能异常相关的 PAEC 损伤,为临床干预提供了理论依据。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:PD-1仿生纳米囊泡介导线动力-化学-免疫三模态治疗乳腺癌并抑制肺转移
下一篇:脱细胞羊膜 + 胶原 VI 增强 iPSC 胰岛类器官存活与功能,移植快速逆转糖尿病