常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-27 17:14:42 细胞资源库平台 访问量:110
英文标题:Biomimetic PD-1-nanovesicles inducing trimodal sonodynamic-chemo-immunotherapy for breast cancer therapy and lung metastasis inhibition
中文标题:PD-1仿生纳米囊泡介导线动力-化学-免疫三模态治疗乳腺癌并抑制肺转移
发表期刊:《Journal of Nanobiotechnology》
影响因子:12.6
作者单位:
1. 福建医科大学附属协和医院超声科
2. 福建医科大学附属协和医院心内科
3. 福建中医药大学第二附属医院超声科
4. 闽江学院福州海洋药物发现产业技术创新中心
作者信息:
Wenjin Lin, Zhenhu Lin, Fen Fu, Zhiyong Li, Haidong Dong, Leilei Liu*, Xiaodong Xie*, Xiujuan Zhang*
1. 临床问题:乳腺癌是全球高发恶性肿瘤,现有手术、放疗、化疗、免疫治疗等标准治疗方案疗效有限,且难以有效抑制肿瘤转移,同时化疗耐药、免疫治疗相关毒性等问题进一步导致治疗失败,亟需开发新型高效的治疗策略。
2. 各治疗方式的局限性与优势:声动力治疗(SDT)具有组织穿透性强、无创、对恶性组织选择性杀伤等优势,金纳米颗粒(AuNPs)可在超声激活下产生活性氧(ROS),但传统声动力纳米药物存在ROS生成机制单一、难以突破肿瘤内屏障的问题;免疫检查点抑制剂(如抗PD-1/PD-L1抗体)为晚期癌症治疗带来新希望,但存在肿瘤相关抗原释放不足、肿瘤微环(TME)高度免疫抑制导致的疗效偏低问题;化疗药物阿霉素(DOX)是乳腺癌治疗常用药物,但全身给药易产生脱靶毒性,且单一化疗难以激活抗肿瘤免疫。
3. 仿生纳米递送系统的潜力:细胞膜包被的纳米颗粒可结合纳米载体的载药能力与细胞膜的生物功能,实现长循环、归巢靶向和免疫逃逸,工程化细胞膜还可表达特异性靶向蛋白,提升肿瘤靶向性;超声触发的控释系统可实现药物在肿瘤部位的时空精准释放,减少非肿瘤组织的药物暴露。
研究切入点与创新点:将PD-1工程化巨噬细胞膜、超声响应AuNPs与化疗药物DOX整合,构建PD-1-Au@DOX仿生纳米平台,实现肿瘤靶向PD-L1阻断、化疗、声动力治疗三模态协同治疗。该平台利用PD-1/PD-L1相互作用实现肿瘤靶向递送,同时在肿瘤微环境中局部阻断PD-1/PD-L1通路,避免全身免疫激活带来的毒性;超声激活下AuNPs产生活性氧,同时促进DOX释放,二者协同诱导铁死亡(免疫原性细胞死亡),激活抗肿瘤免疫,最终实现原发肿瘤抑制和肺转移阻断,为转移性乳腺癌提供了精准、协同的新型治疗方案。
1. 细胞培养
培养小鼠乳腺癌细胞系4T1、人乳腺癌细胞系MCF-7,以及慢病毒转染构建的PD-1⁺永生化小鼠骨髓来源巨噬细胞(iBMDMs),分别采用含10%胎牛血清(FBS)的RPMI 1640和DMEM培养基,在37℃、5% CO₂恒温培养箱中培养。
2. 金纳米颗粒(AuNPs)的合成与过氧化物酶样活性检测
采用CTAB辅助法分步合成球形AuNPs;通过TMB氧化法检测AuNPs的过氧化物酶样活性,设置超声处理组(1.0 MHz,0.5 W/cm²,20%占空比,5 min)和无超声组,通过微板阅读器定量吸光度值,评估ROS生成能力。
3. PD-1-Au@DOX的制备与表征
细胞膜提取:裂解PD-1⁺巨噬细胞,经差速离心获得细胞膜组分,超声匀浆后制备细胞膜悬液。
纳米平台制备:将AuNPs、DOX与细胞膜悬液共孵育,涡旋结合冰浴超声促进膜包被,差速离心收集纳米颗粒,经400 nm、200 nm、100 nm聚碳酸酯膜依次挤出,获得粒径均一的PD-1-Au@DOX。
表征检测:采用动态光散射(DLS)测定AuNPs和PD-1-Au@DOX的水合粒径;透射电镜(TEM)观察形貌;ELISA试剂盒检测表面PD-1表达;分光光度法测定AuNPs(530 nm)和DOX(485 nm)的包封效率(EE)。
4. 体外药物释放实验
分别在pH 7.4(生理环境)和pH 5.5(肿瘤酸性微环境)的PBS中孵育PD-1-Au@DOX,检测不同时间点DOX的累积释放量;设置超声处理组,评估超声对DOX和AuNPs释放的触发作用,通过标准曲线计算释放效率。
5. 体外细胞实验
细胞摄取实验:将4T1、MCF-7细胞与Au@DOX、PD-1-Au@DOX共孵育,部分细胞预先用抗PD-L1抗体封闭表面PD-L1,通过流式细胞术和激光共聚焦显微镜定量和定性分析细胞摄取效率。
细胞毒性实验:采用MTT法检测游离DOX、Au@DOX、PD-1-Au@DOX在有无超声处理下对4T1、MCF-7细胞的毒性,设置空白对照组。
细胞内GSH和ROS检测:采用GSH ELISA试剂盒检测不同处理后细胞内谷胱甘肽(GSH)的时间依赖性变化;利用DCFH-DA探针标记ROS,通过激光共聚焦显微镜和流式细胞术定量检测细胞内ROS水平。
PD-L1阻断能力检测:将肿瘤细胞与Au@DOX、PD-1-Au@DOX或抗PD-L1抗体共孵育,PE标记的抗PD-L1抗体染色后,通过流式细胞术和共聚焦显微镜检测肿瘤细胞表面PD-L1表达水平。
细胞凋亡与免疫杀伤实验:将不同处理的肿瘤细胞与CD8⁺T细胞共培养,通过细胞内裂解型caspase-3染色,流式细胞术定量肿瘤细胞凋亡水平,评估T细胞介导的细胞毒性。
6. 体内动物实验
所有动物实验均经福建医科大学实验动物伦理委员会批准,采用BALB/c雌性小鼠构建乳腺癌模型:
原位肿瘤模型:皮下接种4T1细胞,肿瘤体积达100 mm³时,将小鼠随机分为7组,尾静脉注射不同试剂(PBS、Au@DOX、PD-1-Au@DOX、游离DOX等),每4天给药1次,共5次,部分组在给药6 h后进行超声照射,记录小鼠体重、肿瘤体积,绘制生存曲线,实验终点取肿瘤和主要脏器(心、肝、脾、肺、肾)进行后续检测。
肺转移模型:将4T1细胞接种于小鼠乳腺脂肪垫,1周后随机分组,给予不同处理,21天后处死小鼠,收集肺组织,定量肺转移结节数,组织学验证转移情况。
7. 组织学与分子生物学检测
肿瘤组织行H&E染色观察细胞坏死,TUNEL免疫荧光检测细胞凋亡,Ki67、GPX4免疫组化检测肿瘤增殖和铁死亡水平;
主要脏器H&E染色评估系统毒性;
ELISA试剂盒检测肿瘤组织中促炎细胞因子(TNF-α、IFN-γ、IL-6、IL-12)水平;
激光共聚焦显微镜检测肿瘤组织中CD8⁺T细胞浸润情况。
8. 统计学分析
采用GraphPad Prism 8.0.2软件进行统计分析,两组间比较采用双侧Student’s t检验,多组间比较采用单因素或双因素方差分析(ANOVA),生存曲线采用log-rank(Mantel–Cox)检验,*P*<0.05为差异具有统计学意义。
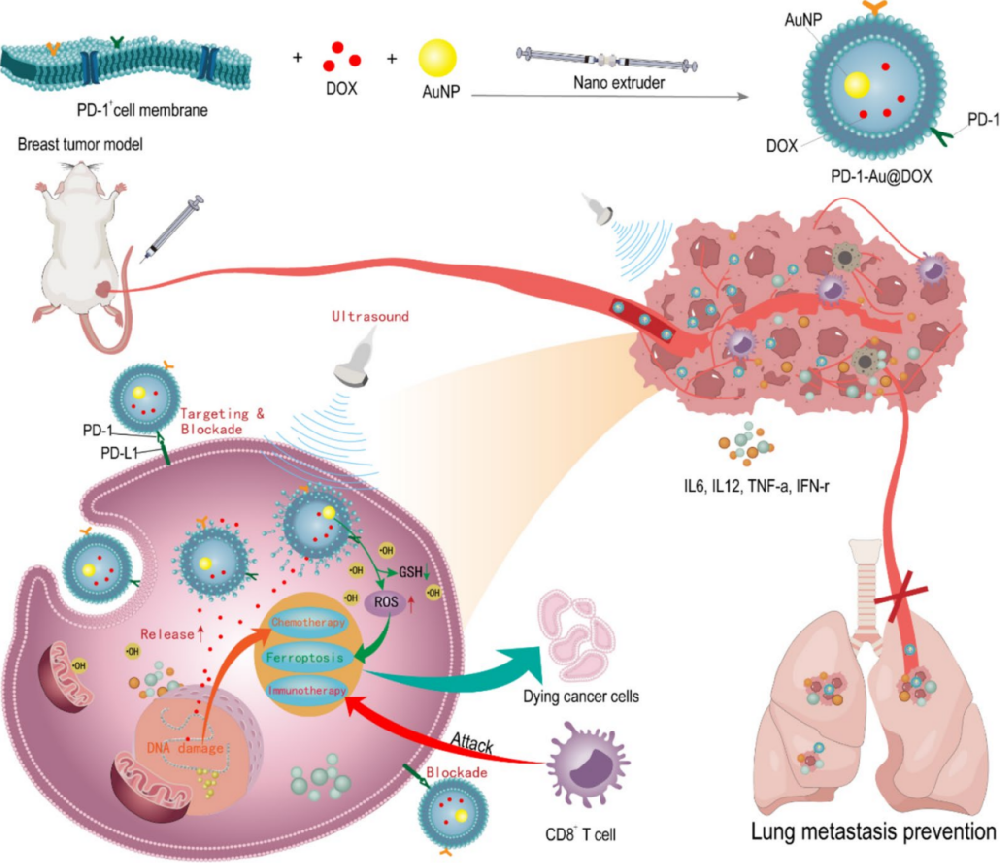
图 1 | 示意图展示了在超声辅助下,PD-1-Au@DOX 在乳腺癌治疗中的协同机制
AuNP 诱导肿瘤细胞发生铁死亡,而 DOX 提供化疗。PD-1-Au@DOX 上的 PD-1 成分通过阻断 PD-1/PD-L1 通路进一步增强细胞毒性,从而通过多模式治疗方法放大 T 细胞介导的免疫反应并减少肺转移。
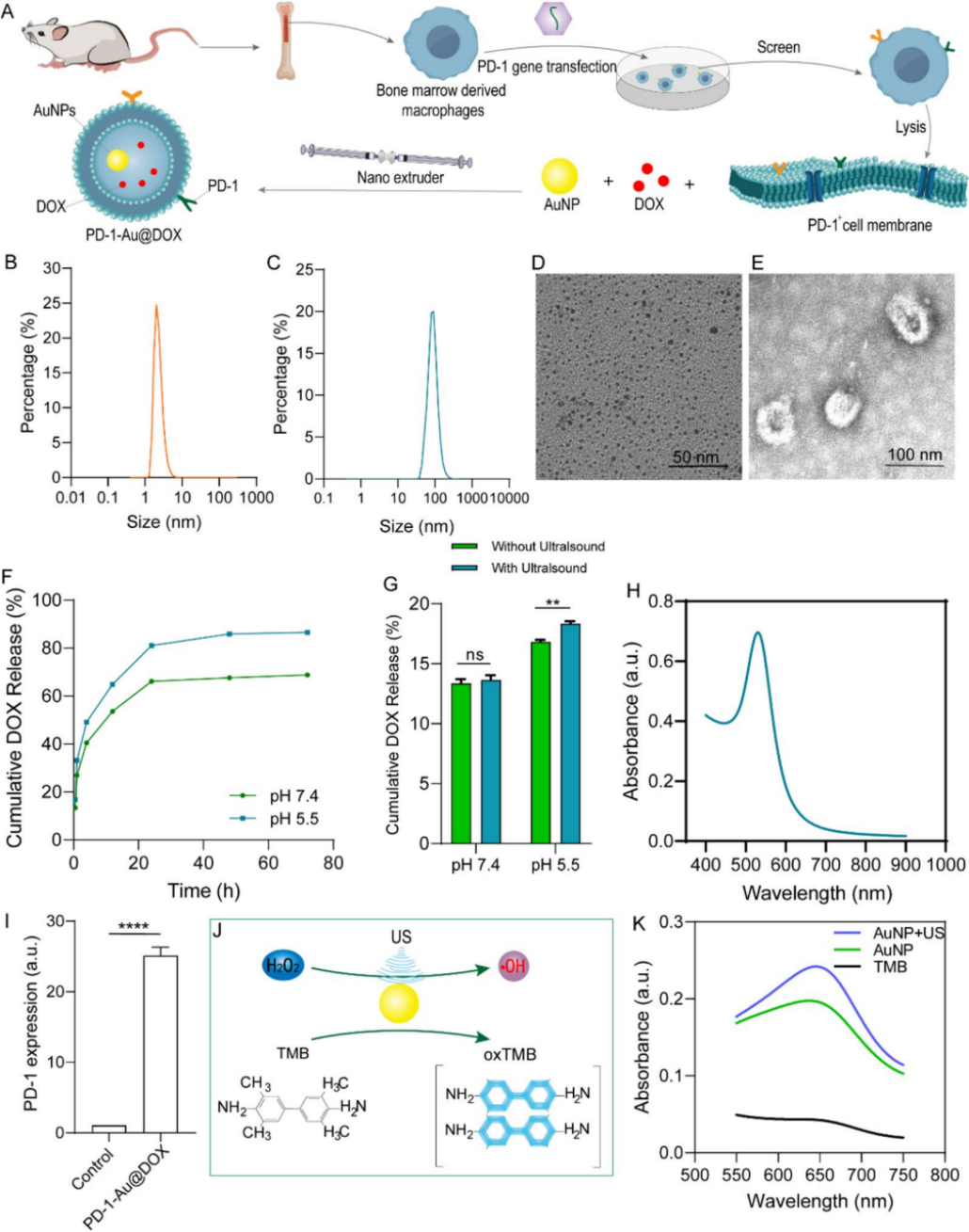
图 2 | PD-1-Au@DOX 的合成与表征
(A) PD-1-Au@DOX 合成示意图。
(B-C) 通过 DLS 测量 AuNPs (B) 和 PD-1-Au@DOX (C) 的尺寸分布。
(D-E) AuNP (D) 和 PD-1-Au@DOX (E) 的 TEM 图像。
(F) 在不同时间点测量 PD-1-Au@DOX 在 pH 5.5 和 pH 7.4 下的 DOX 累积释放量。
(G) 在 pH 5.5 和 pH 7.4 条件下,超声和非超声处理 20 分钟时,PD-1-Au@DOX 中 DOX 的累积释放量。
(H) AuNP 的紫外-可见吸收光谱。
(I) PD-1-Au@DOX 和对照组 (Au@DOX) 上 PD-1 的表达。
(J) 说明超声作用下 ROS 生成的示意图。
(K) AuNP 在有/无超声条件下对 H₂O₂ 的催化分解。
数据显示为平均值 ± SD,通过双尾学生 t 检验计算 (G, I)。显著性差异表示为 *P < 0.05, **P < 0.01, ***P < 0.001, 和 ****P < 0.0001。ns,不显著。
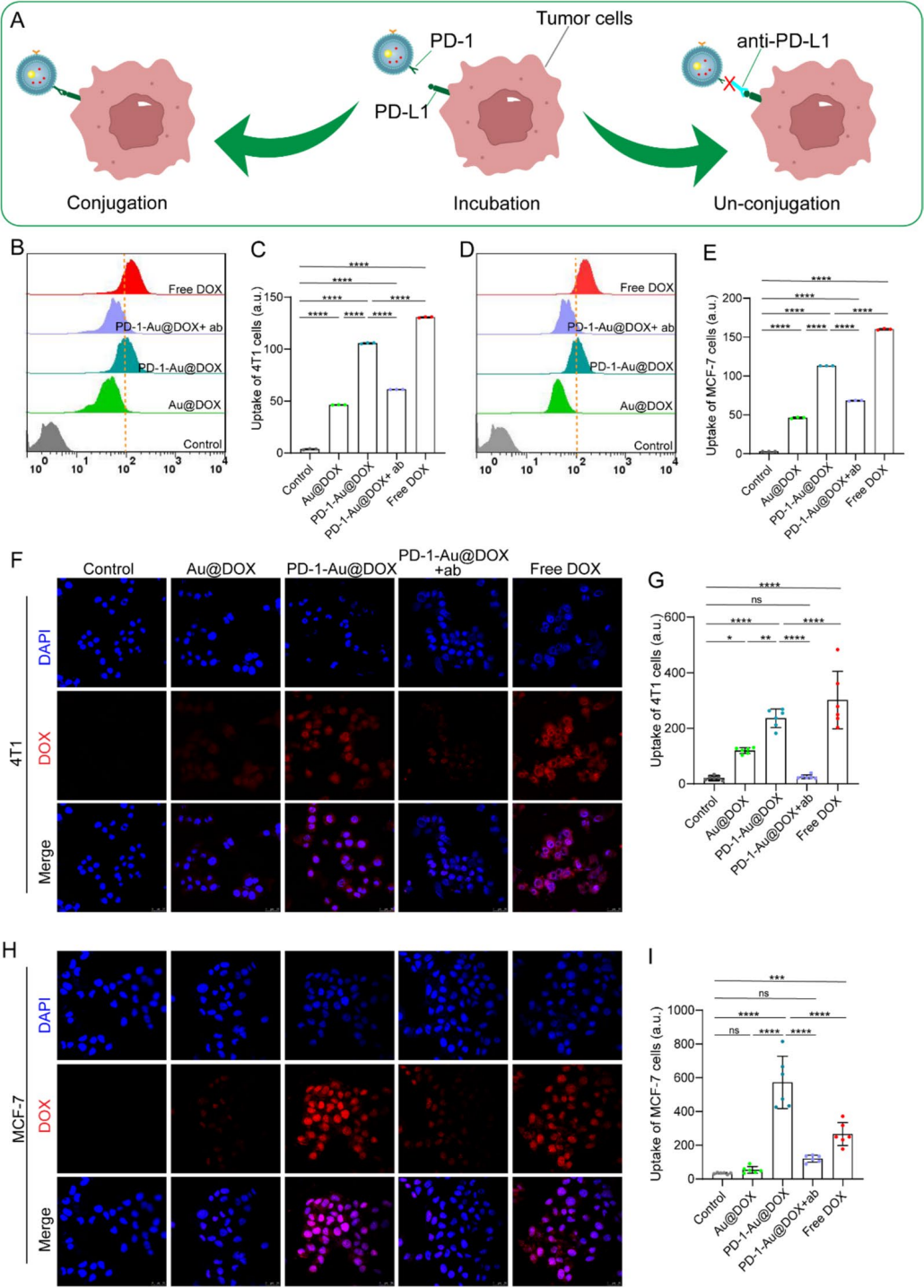
图 3 | PD-1-Au@DOX 特异性靶向肿瘤细胞
(A) PD-1-Au@DOX 通过 PD-1 靶向 PD-L1 实现肿瘤细胞特异性递送的示意图。
(B-E) 流式细胞术分析及定量显示,4T1 (B-C) 和 MCF-7 (D-E) 细胞与 Au@DOX、PD-1-Au@DOX、PD-1-Au@DOX(肿瘤细胞预先用 PD-L1 抗体封闭)和游离 DOX 共孵育 4 小时后的摄取情况。
(F-I) 共聚焦显微镜显示 4T1 (F-G) 和 MCF-7 (H-I) 细胞与 Au@DOX、PD-1-Au@DOX、PD-1-Au@DOX(肿瘤细胞预先用 PD-L1 抗体封闭)和游离 DOX 共孵育 4 小时后的细胞内摄取情况。
数据显示为平均值 ± SD,通过单因素方差分析计算 (C, E, G, I)。显著性差异表示为 *P < 0.05, **P < 0.01, ***P < 0.001, 和 ****P < 0.0001。ns,不显著。
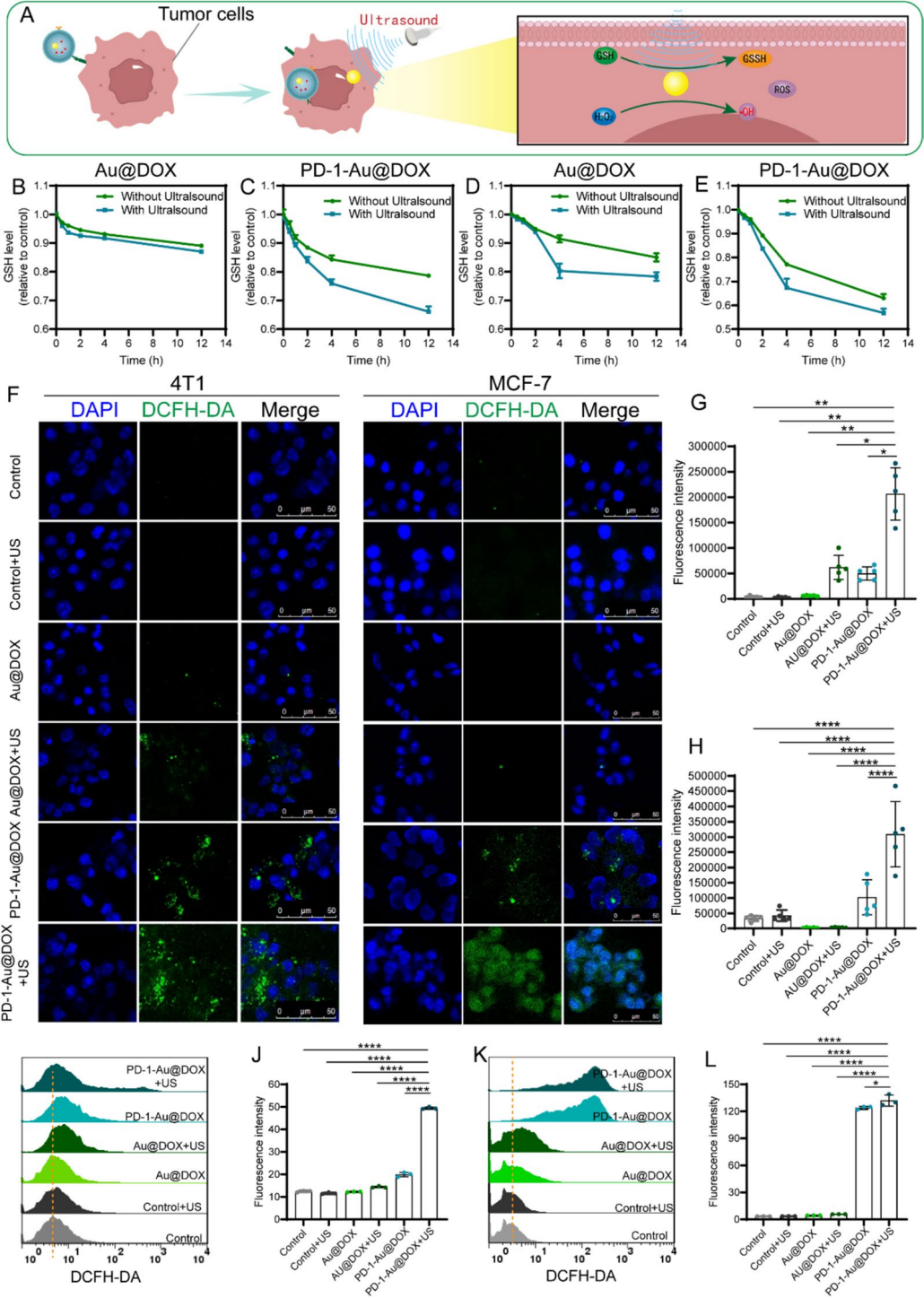
图 4 | 体外 ROS 生成
(A) 超声辐照下 PD-1-Au@DOX 诱导细胞内 ROS 生成和 GSH 耗竭的示意图。
(B-D) 4T1 (B-C) 和 MCF-7 (D-E) 细胞经 Au@DOX 或 PD-1-Au@DOX(有/无超声)处理后,在不同时间点的细胞内 GSH 水平。
(F-H) 共聚焦显微镜显示 4T1 细胞内的 ROS 水平 (F) 及其定量 (G),以及 MCF-7 细胞内的 ROS 水平 (F) 及其定量 (H)(比例尺 = 50 μm)。
(I-L) 流式细胞术显示 4T1 细胞内的 ROS 水平 (I) 及其定量 (J),以及 MCF-7 细胞内的 ROS 水平 (K) 及其定量 (L)。
数据显示为平均值 ± SD,通过单因素方差分析计算 (G, H, J, L)。显著性差异表示为 *P < 0.05, **P < 0.01, ***P < 0.001, 和 ****P < 0.0001。ns,不显著。
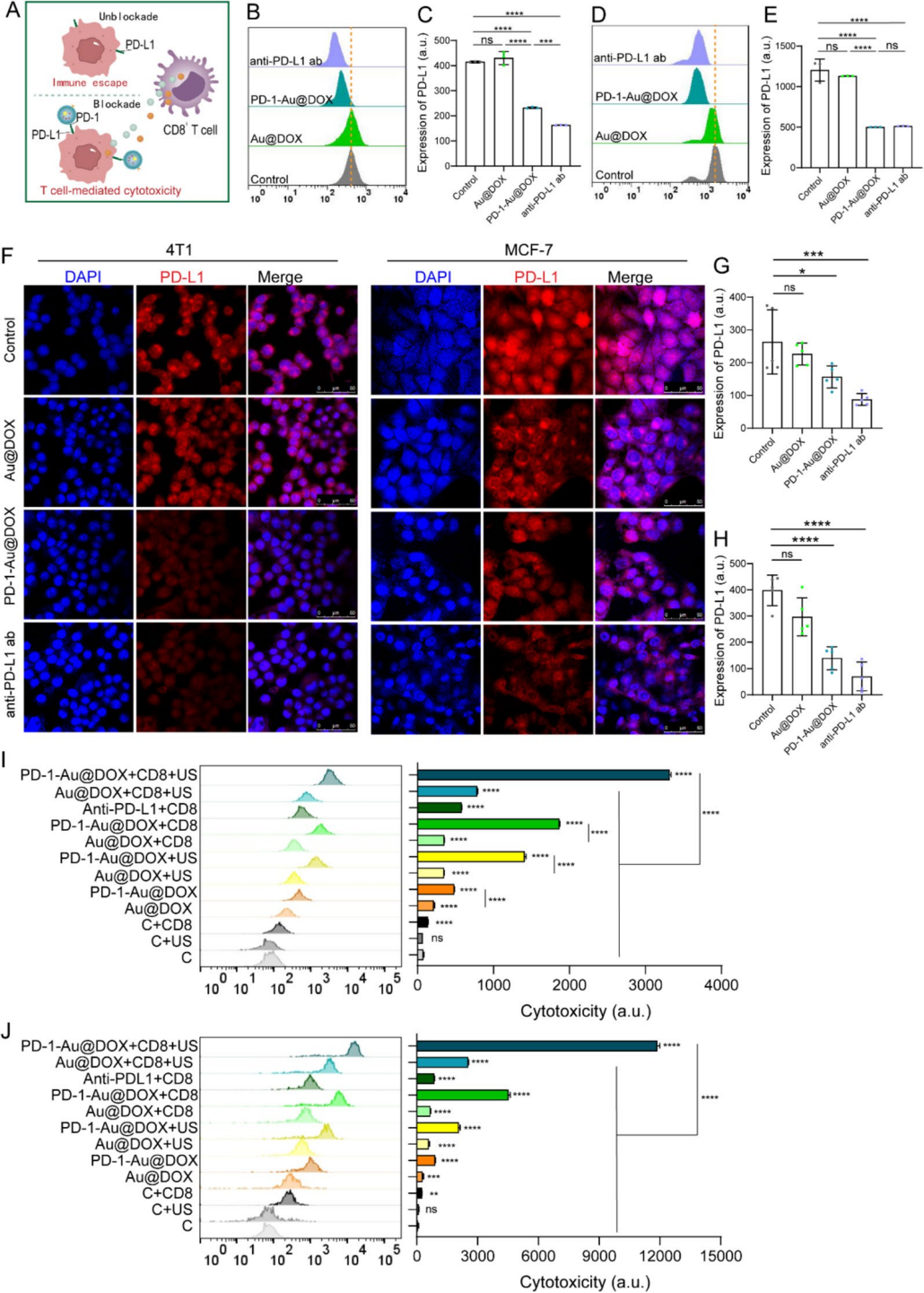
图 5 | PD-1-Au@DOX 的体外免疫检查点抑制
(A) PD-1-Au@DOX 诱导 T 细胞介导免疫疗法的示意图。
(B-E) 流式细胞术显示 4T1 细胞中的 PD-L1 表达 (B) 及其定量 (C),以及 MCF-7 细胞中的 PD-L1 表达 (D) 及其定量 (E)。
(F-H) 共聚焦显微镜显示 4T1 细胞中的 PD-L1 表达 (F) 及其定量 (G),以及 MCF-7 细胞中的 PD-L1 表达 (F) 及其定量 (H)(比例尺 = 50 μm)。
(I-J) 将 4T1 (I)、MCF-7 (J) 细胞与 Au@DOX 或 PD-1-Au@DOX(有/无超声)共培养 24 小时,然后与 CD8+ T 细胞共培养 48 小时。抗 PD-L1 抗体作为阳性对照。通过细胞内 cleaved caspase-3 的流式细胞术评估肿瘤细胞凋亡(左图),并定量(右图)。
数据显示为平均值 ± SD,通过单因素方差分析计算 (C, E, G, H, I, J)。显著性差异表示为 *P < 0.05, **P < 0.01, ***P < 0.001, 和 ****P < 0.0001。ns,不显著。
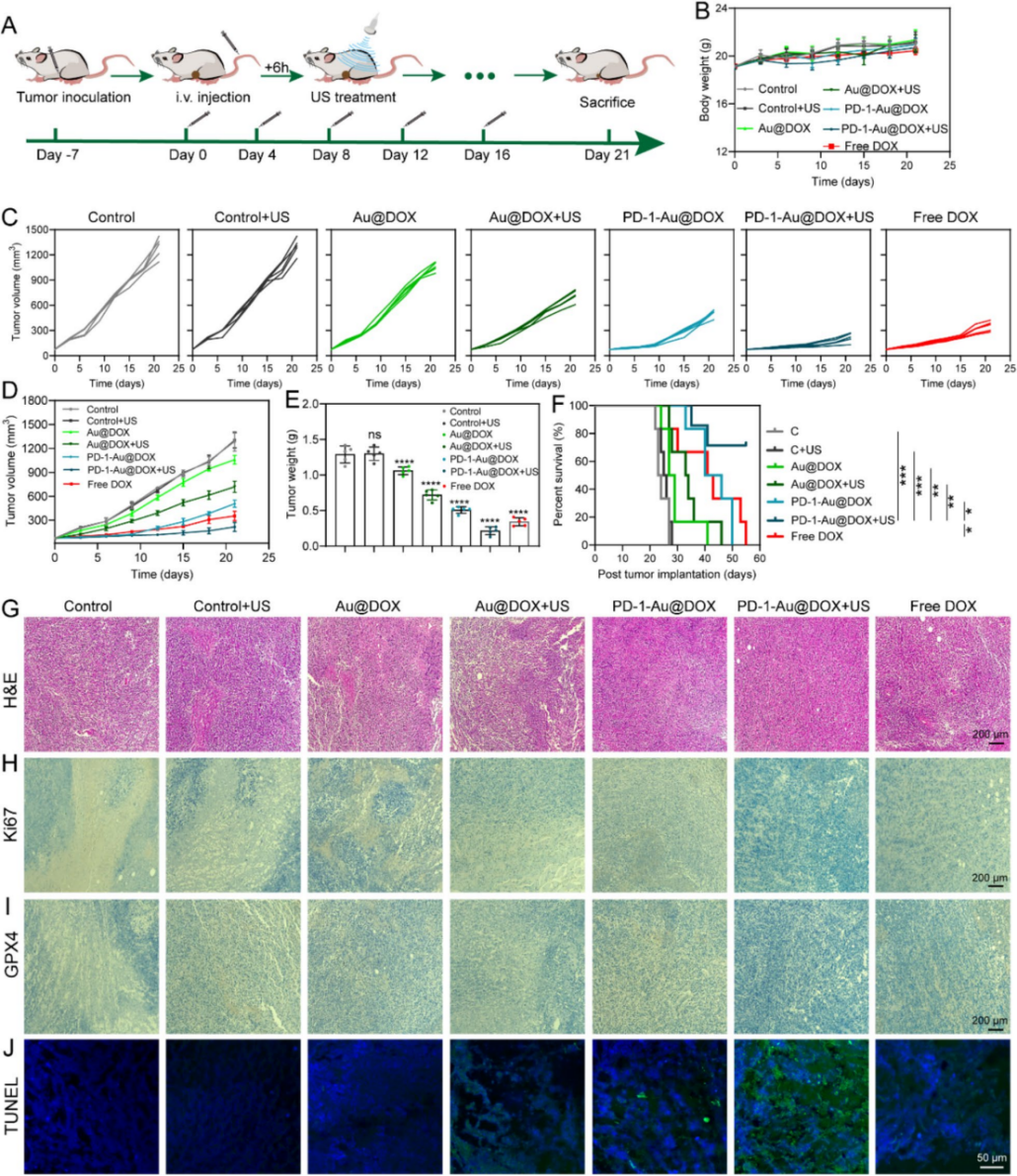
图 6 | 体内肿瘤抑制
(A) 动物实验治疗程序的时间表。
(B) 治疗期间的小鼠体重。
(C) 通过动态记录治疗过程中的肿瘤体积绘制的肿瘤生长曲线。
(D) 不同组别的肿瘤体积变化。
(E) 第 21 天不同组别的肿瘤重量。
(F) 不同治疗组的存活率。
(G-J) 治疗结束后切除肿瘤的 H&E (G)、Ki67 (H)、GPX4 (I) 免疫组织化学染色和 TUNEL (J) 免疫荧光。
数据以平均值 ± s.d. 表示,并使用单因素方差分析 (E) 或对数秩(Mantel-Cox)检验 (F) 进行分析。*, P < 0.05; **, P < 0.01; ***, P < 0.001, 和 ****, P < 0.0001。ns,不显著。
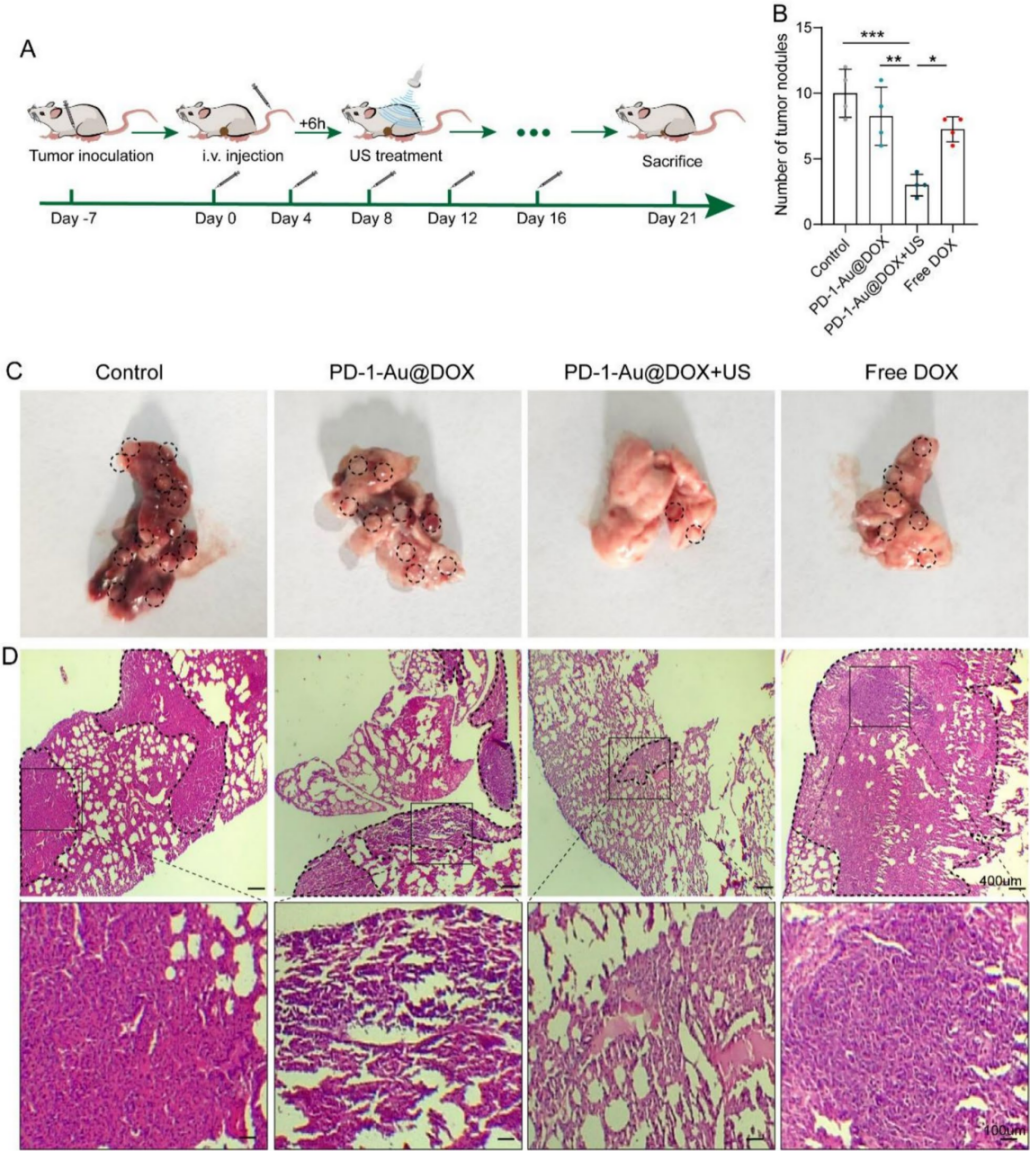
图 7 | 体内肺转移抑制效果评估。
(A) 实验方案示意图。
(B) 不同治疗组小鼠肺部代表性照片(白色箭头指示转移结节)。
(C) 各组肺部转移结节数量的定量统计。
(D) 各组肺组织的 H&E 染色图像,用于组织学评估转移灶(比例尺 = xxx μm)。
(注:图C中数据比较了Control、PD-1-Au@DOX、Free DOX与PD-1-Au@DOX+US组,结果显示联合治疗组转移抑制率最高,达70.0%)
1. 纳米平台的理化特性:成功构建的PD-1-Au@DOX仿生纳米平台粒径均一(约100 nm),表面高表达PD-1,具有pH响应性和超声触发的药物控释特性,可在肿瘤酸性微环境和超声照射下实现DOX和AuNPs的精准释放,减少全身毒性。
2. 体外作用机制验证:PD-1-Au@DOX通过PD-1/PD-L1特异性结合实现乳腺癌细胞(4T1、MCF-7)的靶向递送,超声激活下AuNPs产生活性氧并耗竭细胞内GSH,与DOX协同诱导肿瘤细胞铁死亡;同时,膜表面PD-1有效阻断肿瘤细胞PD-L1,激活CD8⁺T细胞介导的免疫杀伤,化疗、声动力治疗、免疫治疗三模态协同显著诱导肿瘤细胞凋亡。
3. 体内抗肿瘤与抗转移效果:在小鼠乳腺癌模型中,PD-1-Au@DOX联合超声可显著抑制原发肿瘤生长,肿瘤生长抑制率达83.14%,并显著延长小鼠生存期;同时可有效阻断乳腺癌肺转移,转移抑制率达70.0%,远优于游离DOX等对照组。
4. 作用核心:三模态治疗的协同作用是其高效抗肿瘤的关键——铁死亡诱导的免疫原性细胞死亡与PD-1/PD-L1通路阻断协同重塑肿瘤微环境,促进CD8⁺T细胞浸润和促炎细胞因子释放,实现局部肿瘤杀伤和全身抗肿瘤免疫激活,从而同时抑制原发肿瘤和远处转移。
5. 研究局限性与展望:本研究虽证实了PD-1-Au@DOX的抗转移效果,但未完全阐明其抑制肿瘤转移的分子和细胞机制;同时缺乏物理混合制剂等对照,未能进一步验证纳米平台结构整合的必要性。后续研究将深入探究抗转移的分子通路,并设置更多对照组,为该平台的临床转化提供更充分的依据。
本研究首次将PD-1工程化巨噬细胞膜、超声响应AuNPs与化疗药物DOX整合,构建了兼具靶向递送、控释给药、三模态协同的仿生纳米治疗平台,突破了单一治疗方式的局限性,实现了乳腺癌的高效治疗和肺转移的有效阻断。该研究的创新点在于将细胞膜从被动的“隐身涂层”改造为主动的“免疫调节界面”,PD-1同时发挥靶向配体和免疫检查点抑制剂的双重作用,既提升了肿瘤靶向性,又实现了肿瘤微环境的局部免疫激活,避免了全身免疫治疗的毒性;同时,超声触发的声动力治疗与化疗协同诱导铁死亡,进一步增强免疫原性细胞死亡,实现“化疗-声动力-免疫”的级联放大效应。
该研究为仿生纳米药物的设计提供了新范式,也为转移性乳腺癌的治疗提供了全新的候选方案,有望推动纳米生物技术与肿瘤多模态治疗的临床转化,同时为其他恶性肿瘤的治疗提供借鉴。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:NanoLuc-GFP 双报告系统解锁基因表达定量新方式
下一篇:突破 PAH 治疗困境:BMPR2 调控通路为肺血管保护提供新靶点