常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-22 17:06:10 细胞资源库平台 访问量:94
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:MicroRNA-885-3p inhibits the growth of HT-29 colon cancer cell xenografts by disrupting angiogenesis via targeting BMPR1A and blocking BMP/Smad/Id1 signaling
中文标题:微小 RNA-885-3p 通过靶向骨形态发生蛋白受体 1A 并阻断 BMP/Smad/Id1 信号通路破坏血管生成,抑制 HT-29 结肠癌细胞异种移植物生长
发表期刊:《Oncogene》
影响因子:7.3
作者单位:
Glycochemistry and Glycobiology Laboratory, Shanghai Institute of Materia Medica, Chinese Academy of Sciences, Shanghai, China
作者信息:
F Xiao, H Qiu, H Cui, X Ni, J Li, W Liao, L Lu and K Ding
微小 RNA(miRNAs)可在转录后水平沉默基因表达,参与肿瘤进展包括血管生成过程,血管生成是肿瘤发生发展的关键环节,DNA 结合蛋白抑制剂 Id1 作为促血管生成因子是公认的抗血管生成靶点;骨形态发生蛋白(BMPs)通过 BMPR1A 等受体激活 BMP/Smad 信号通路调控 Id1 表达,阻断该通路或为抑制 Id1 的理想策略,但 miRNAs 是否通过调控 BMPs 或其受体影响肿瘤生长和血管生成仍不明确。miRNAs 在结肠癌等肿瘤发展中发挥关键作用,然而 miR-885-3p 在结肠癌中的作用及作用机制尚未阐明,此前研究发现 miR-885-3p 受结合 BMPR1A 的硫酸化多糖调控并抑制血管生成,本研究旨在探究 miR-885-3p 在结肠癌血管生成中的具体作用及通过调控 BMPR1A 和 BMP/Smad/Id1 信号通路发挥作用的分子机制。
本研究首先在人微血管内皮细胞 HMEC-1 和人脐静脉内皮细胞 HUVEC 中过表达或沉默 miR-885-3p,通过管形成、划痕愈合和 Transwell 实验检测其对体外血管生成的影响;利用慢病毒感染系统在 HMEC-1 中过表达 miR-885-3p,结合基质胶栓实验通过 CD31 免疫染色检测其体内血管生成作用。借助 miRNA 靶标预测软件筛选靶点,构建 BMPR1A 3'UTR 野生型和突变型荧光素酶报告载体,通过双荧光素酶报告实验验证 miR-885-3p 与 BMPR1A 的直接靶向关系;采用 RT-PCR、Western blot 检测 miR-885-3p 对 BMPR1A 及 BMP/Smad/Id1 信号通路相关分子(Smad1/5/8、Id1)表达和磷酸化的影响。通过 shRNA 敲低、过表达质粒转染 BMPR1A,结合血管生成相关功能实验验证其作用,并开展回补实验明确 miR-885-3p 通过靶向 BMPR1A 发挥作用。检测多种肿瘤细胞系中 miR-885-3p 和 BMPR1A 的表达相关性,重点在 HT-29 结肠癌细胞中验证 miR-885-3p 对 BMP/Smad/Id1 信号通路的调控。构建稳定过表达 miR-885-3p 的 HT-29 细胞系,建立裸鼠异种移植瘤模型,检测肿瘤生长情况;收集结肠癌临床配对标本,检测 miR-885-3p 和 BMPR1A 的表达水平。通过免疫组化检测移植瘤组织中 CD31、BMPR1A 表达,结合 RT-PCR、Western blot 验证移植瘤中 miR-885-3p 对 BMP/Smad/Id1 信号通路和血管生成的调控;同时检测 miR-885-3p 对 VEGFA、TGFβ1 等其他促血管生成因子的影响,通过中和抗体、外源性蛋白回补实验比较其与 BMPR1A 介导的抗血管生成作用强度。实验采用 MTT 法检测细胞活力,利用 Image Pro Plus 进行免疫组化图像定量分析,统计学分析采用 Student’s t 检验和单因素方差分析,p<0.05 为差异有统计学意义。
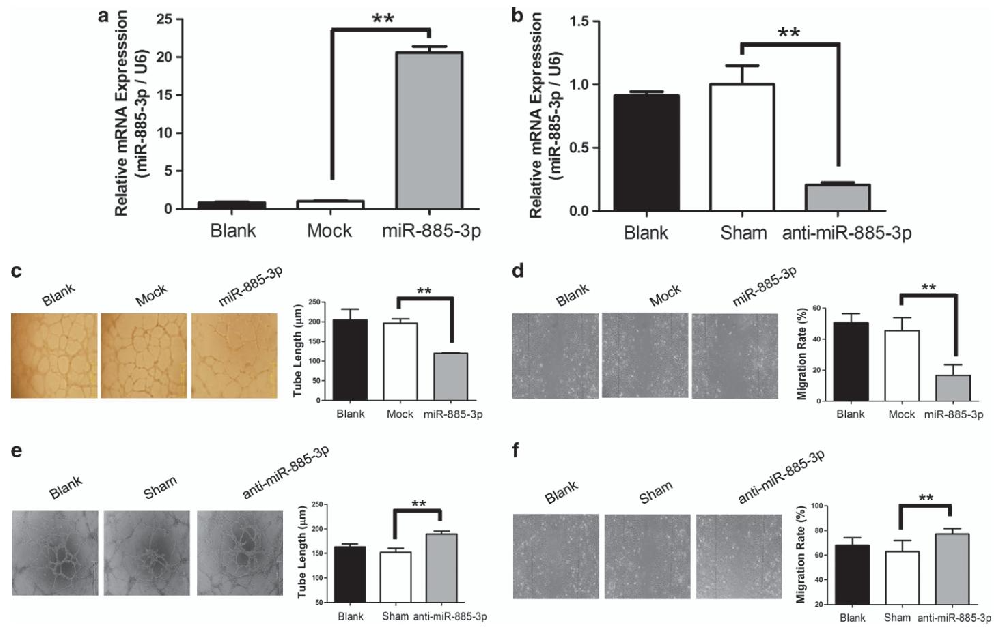
图1:miR-885-3p 在体外抑制血管生成
该图通过 qPCR 验证 HMEC-1 细胞中转染 miR-885-3p 模拟物可显著过表达 miR-885-3p,转染抑制剂则显著沉默其表达;管形成实验显示 miR-885-3p 过表达可显著减少 HMEC-1 细胞的管结构长度,而沉默 miR-885-3p 则促进管形成;划痕愈合实验表明 miR-885-3p 过表达显著抑制 HMEC-1 细胞的迁移能力,沉默后则促进细胞迁移,在 HUVEC 细胞中也得到一致的体外血管生成抑制结果,证实 miR-885-3p 可在体外直接抑制内皮细胞的血管生成相关功能。
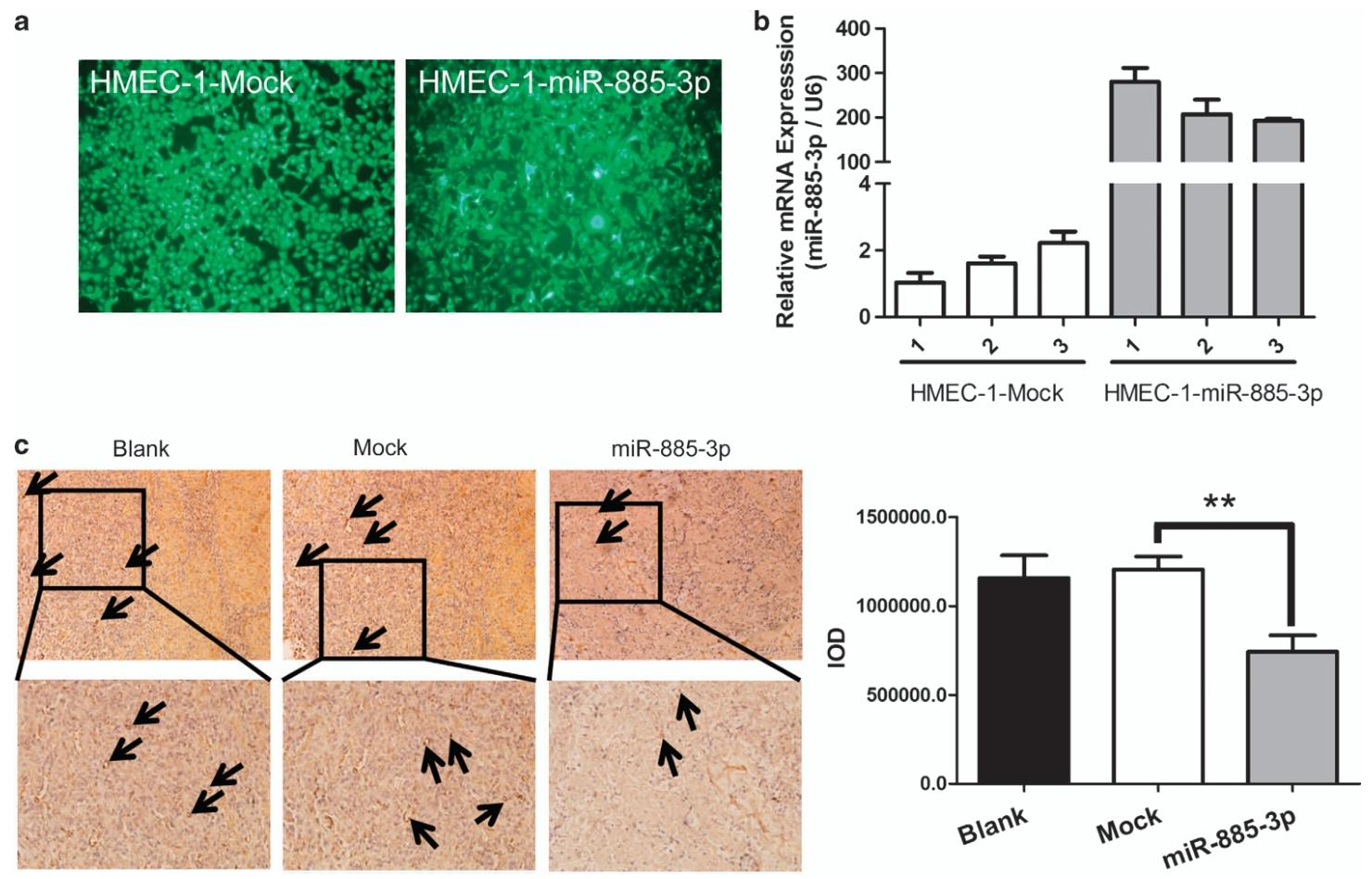
图2:miR-885-3p 在体内抑制血管生成
该图先验证慢病毒感染可有效在 HMEC-1 细胞中过表达 miR-885-3p;基质胶栓实验结合 CD31 免疫染色显示,含 miR-885-3p 过表达 HMEC-1 细胞的基质胶栓中 CD31 阳性血管数量显著少于对照组,光学密度定量分析也证实 CD31 表达水平显著降低,结合体外实验结果,明确 miR-885-3p 在体内外均具有抑制血管生成的作用。
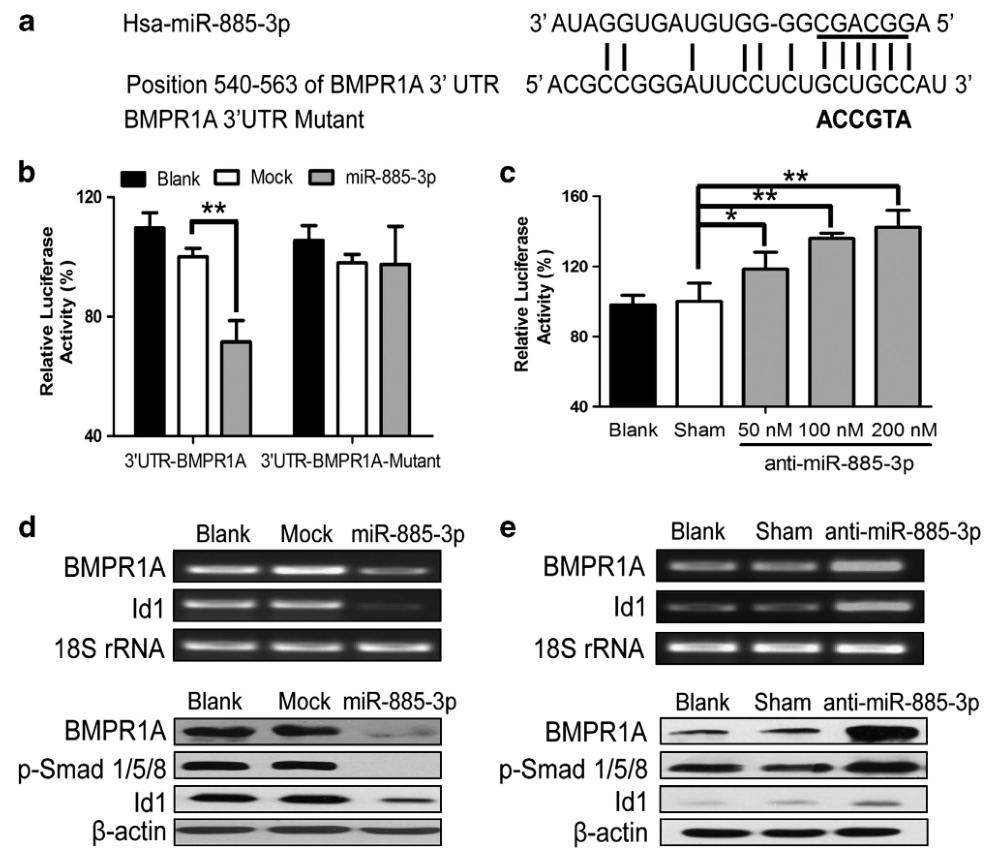
图3:miR-885-3p 直接靶向 BMPR1A 3'UTR 并在 HMEC-1 细胞中阻断 BMP/Smad/Id1 信号通路
该图通过序列比对发现 miR-885-3p 与 BMPR1A 3'UTR 存在部分互补结合位点;双荧光素酶报告实验显示,miR-885-3p 可显著抑制野生型 BMPR1A 3'UTR 报告载体的荧光素酶活性,对突变型则无影响,且 miR-885-3p 抑制剂可剂量依赖性促进野生型载体活性,证实 miR-885-3p 直接靶向结合 BMPR1A 3'UTR。RT-PCR 和 Western blot 结果显示,miR-885-3p 过表达可显著降低 HMEC-1 细胞中 BMPR1A 的 mRNA 和蛋白表达,同时抑制 Smad1/5/8 磷酸化和 Id1 表达;而沉默 miR-885-3p 则得到相反结果,在 HUVEC 细胞中也验证了该调控作用,明确 miR-885-3p 通过靶向 BMPR1A 阻断 BMP/Smad/Id1 信号通路。
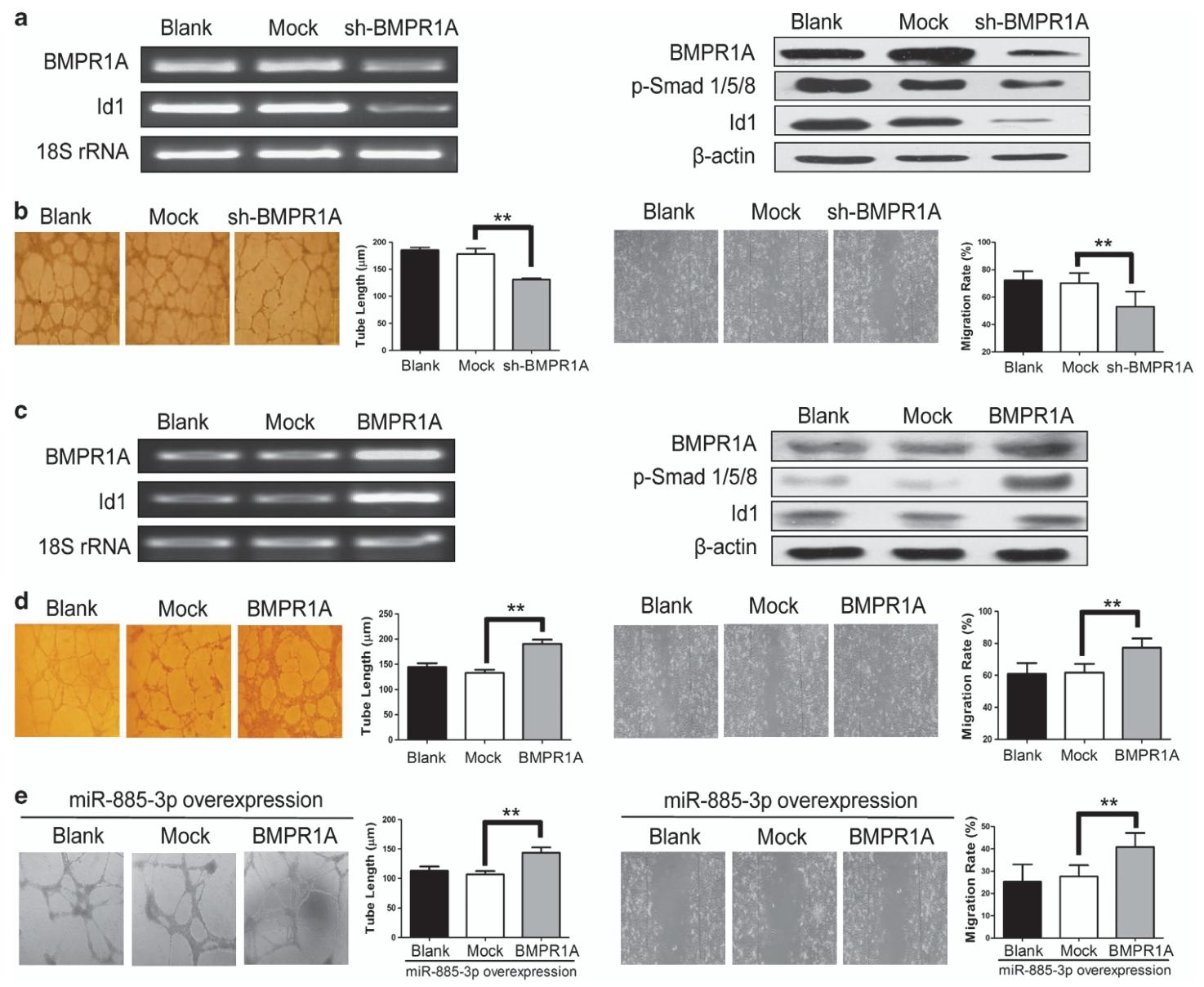
图4:BMPR1A 促进 HMEC-1 细胞的血管生成和 BMP/Smad/Id1 信号通路激活
该图显示 shRNA 敲低 BMPR1A 可显著降低 HMEC-1 细胞中 BMPR1A、Id1 表达及 Smad1/5/8 磷酸化,同时抑制细胞管形成和迁移;过表达 BMPR1A 则显著增强 BMP/Smad/Id1 信号通路激活,并促进内皮细胞管形成和迁移。回补实验表明,在 miR-885-3p 过表达的 HMEC-1 细胞中重新表达 BMPR1A,可显著恢复细胞的管形成和迁移能力,证实 miR-885-3p 对血管生成的抑制作用至少部分通过靶向 BMPR1A 介导。
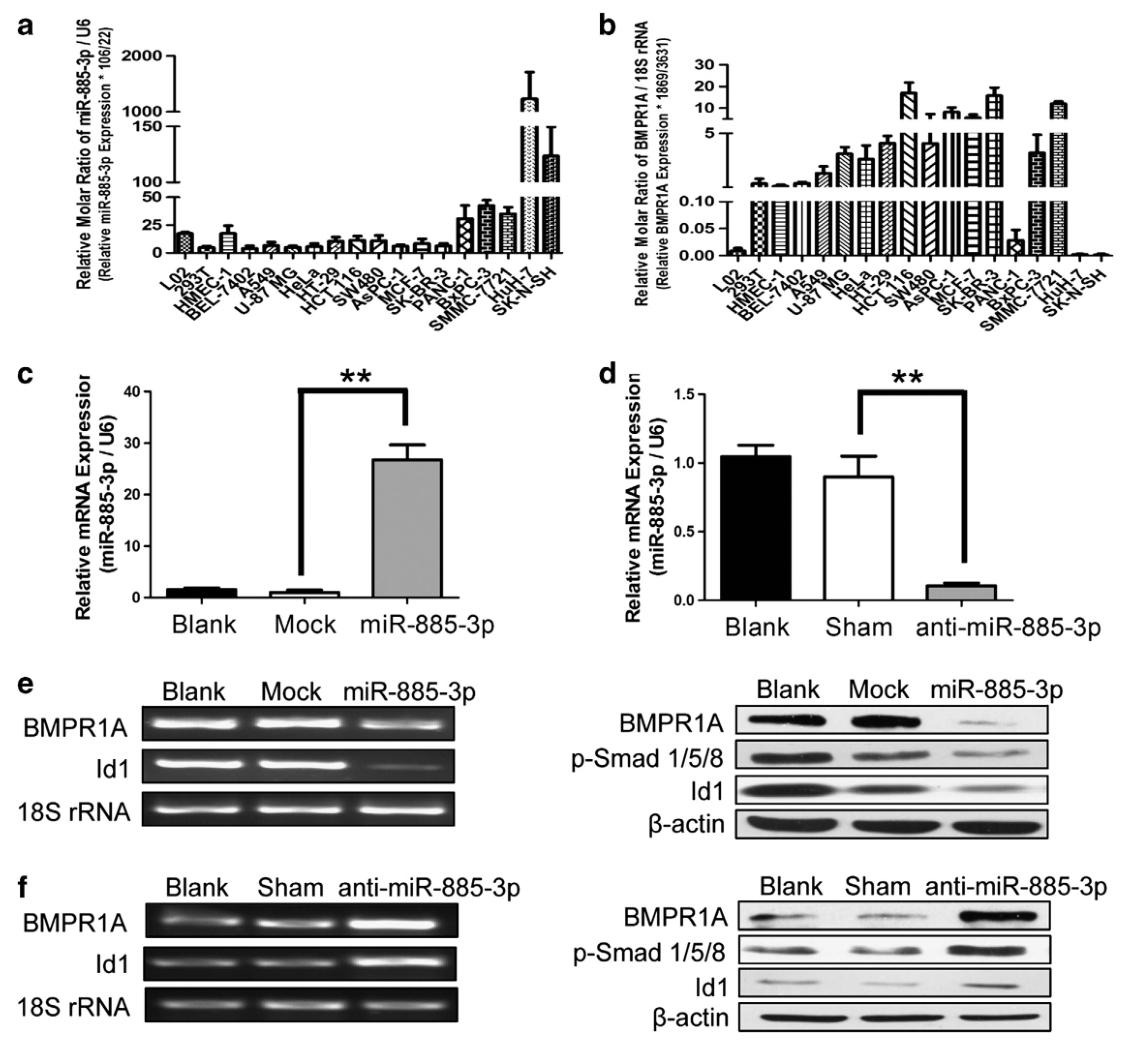
图5:miR-885-3p 与 BMPR1A 表达呈负相关,且在 HT-29 结肠癌细胞中抑制 BMPR1A 表达和 BMP/Smad/Id1 信号通路
该图通过检测多种肿瘤细胞系发现,在包括 HT-29 在内的多数肿瘤细胞中 miR-885-3p 表达水平与 BMPR1A 呈显著负相关,结肠癌细中 miR-885-3p 低表达、BMPR1A 高表达。qPCR 验证 HT-29 细胞中转染 miR-885-3p 可实现过表达,转染抑制剂则沉默其表达;RT-PCR 和 Western blot 结果显示,miR-885-3p 过表达可显著降低 HT-29 细胞中 BMPR1A、Id1 表达及 Smad1/5/8 磷酸化,沉默 miR-885-3p 则促进该信号通路激活,在 HCT 116 结肠癌细胞中也得到一致结果,证实 miR-885-3p 在结肠癌细胞中同样调控 BMPR1A 和 BMP/Smad/Id1 信号通路。
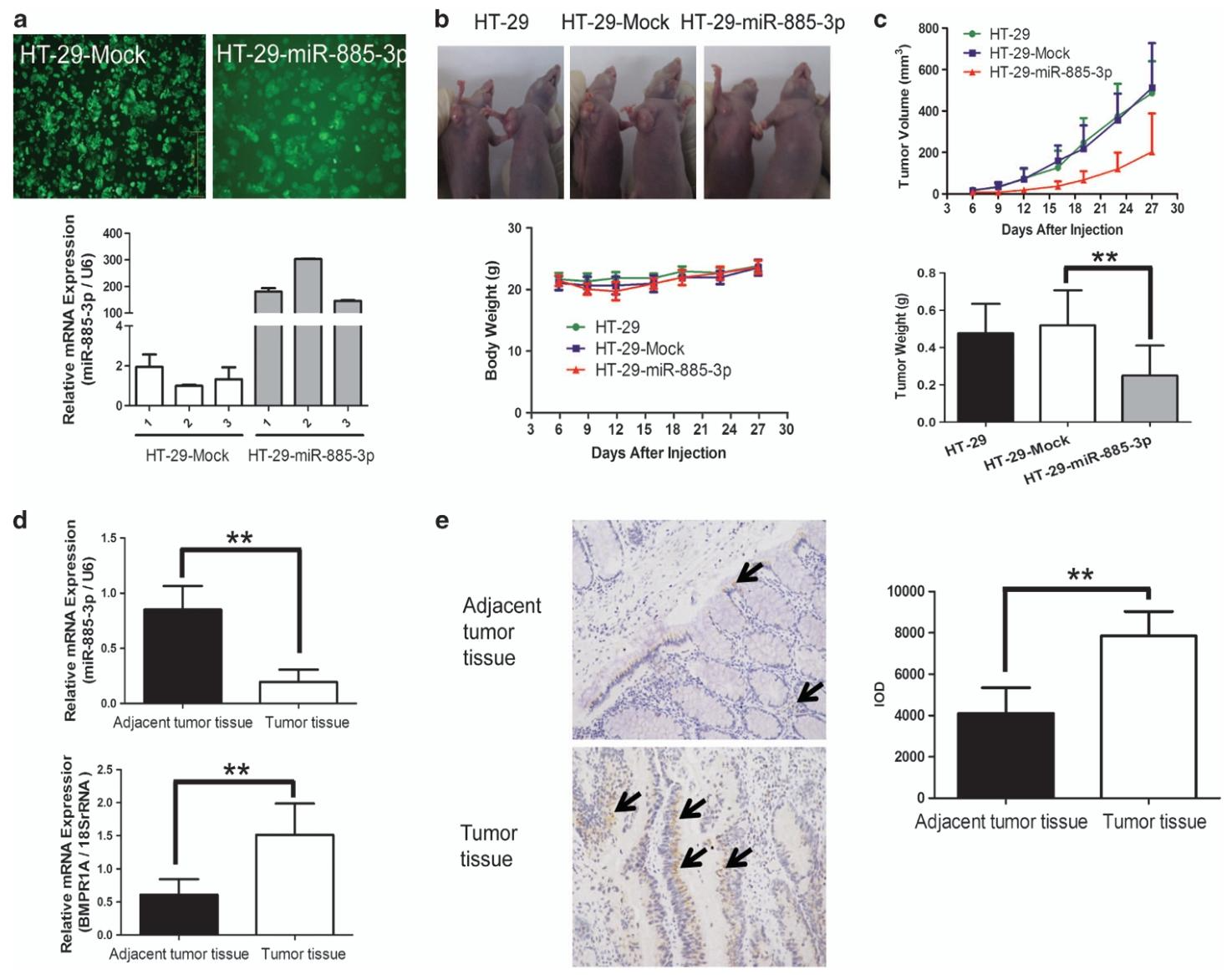
图6:miR-885-3p 抑制裸鼠中 HT-29 结肠癌异种移植物生长,且结肠癌临床标本中 miR-885-3p 低表达、BMPR1A 高表达
该图验证慢病毒感染可有效在 HT-29 细胞中过表达 miR-885-3p;裸鼠异种移植瘤实验显示,过表达 miR-885-3p 的 HT-29 细胞形成的肿瘤体积和重量显著小于对照组,小鼠体重无明显变化,miR-885-3p 的治疗效应约为 48%。qPCR 检测 8 例结肠癌临床配对标本发现,肿瘤组织中 miR-885-3p 表达显著低于癌旁组织,BMPR1A 表达则显著升高;免疫组化结果也证实肿瘤组织中 BMPR1A 的表达水平和光学密度显著高于癌旁组织,明确临床标本中 miR-885-3p 与 BMPR1A 表达呈负相关。
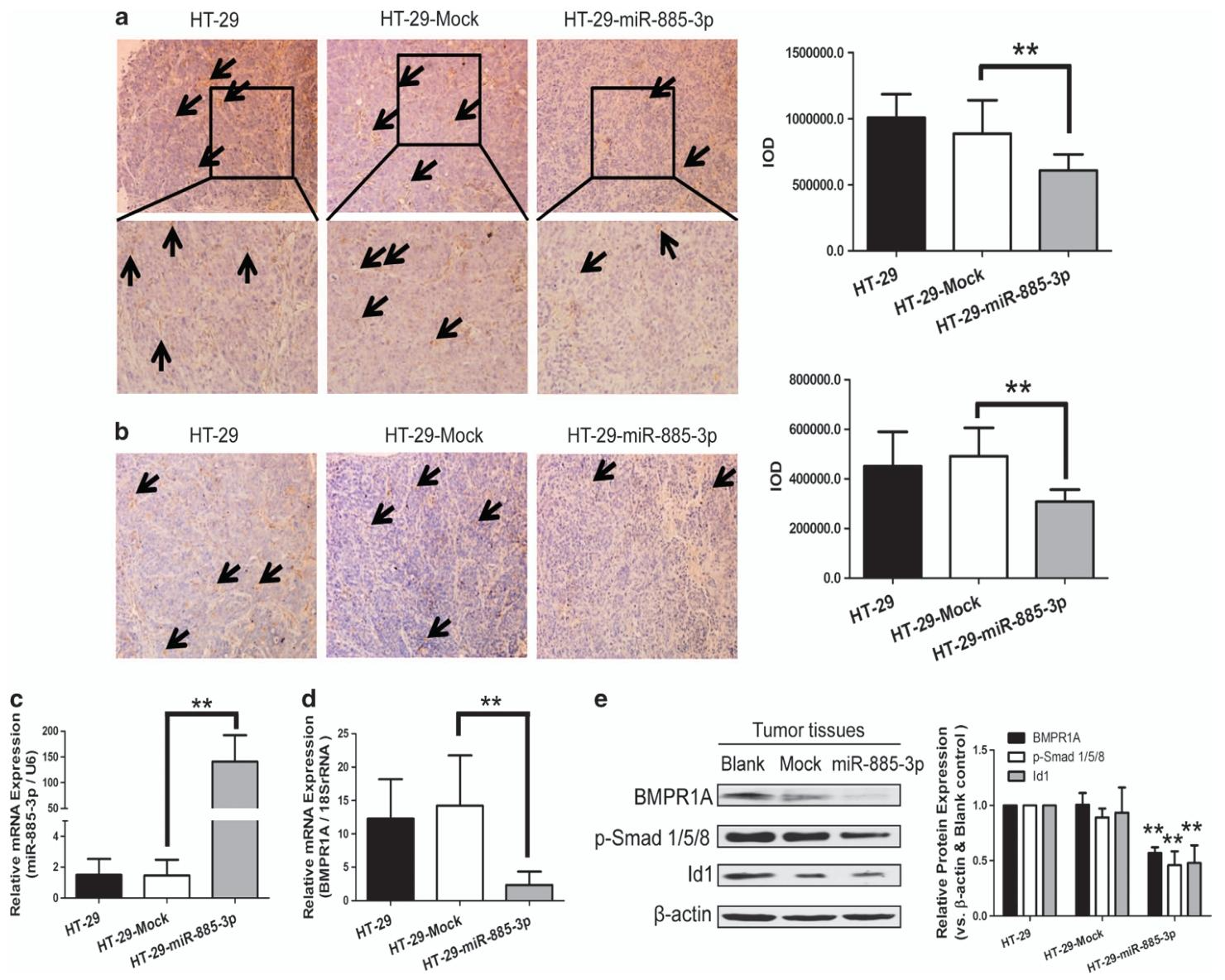
图7:miR-885-3p 在 HT-29 异种移植物中抑制血管生成并阻断BMP/Smad/Id1 信号通路
该图通过免疫组化检测发现,过表达 miR-885-3p 的移植瘤组织中 CD31 阳性血管数量和 BMPR1A 表达水平均显著低于对照组,光学密度定量分析验证了该差异。qPCR 结果显示,移植瘤组织中 miR-885-3p 表达显著升高,BMPR1A mRNA 表达显著降低;Western blot 结果证实,过表达 miR-885-3p 可显著降低移植瘤中 BMPR1A、Id1 蛋白表达及 Smad1/5/8 磷酸化,证实 miR-885-3p 在体内通过下调 BMPR1A、阻断 BMP/Smad/Id1 信号通路抑制结肠癌移植瘤的血管生成,进而抑制肿瘤生长。
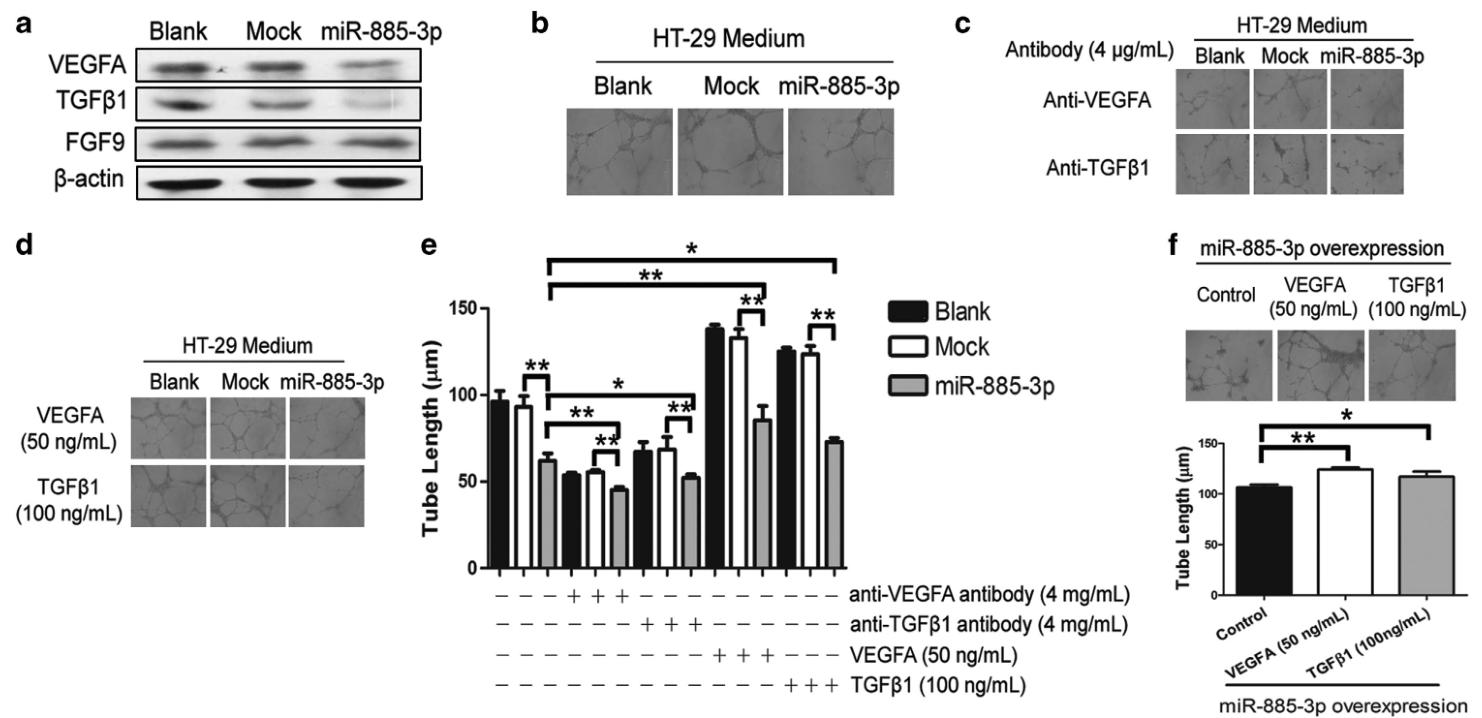
图8:miR-885-3p 通过阻滞 BMPR1A 和 BMP/Smad/Id1 信号通路介导的抗血管生成作用强于通过 VEGFA、TGFβ1 等细胞因子的作用
该图 Western blot 结果显示,miR-885-3p 过表达可降低 HT-29 细胞中 VEGFA、TGFβ1 表达,对 FGF9 无明显影响。条件培养基实验显示,miR-885-3p 过表达的 HT-29 细胞培养基可显著抑制 HMEC-1 细胞管形成,加入 VEGFA 或 TGFβ1 中和抗体后抑制作用增强,加入外源性 VEGFA 或 TGFβ1 则可部分恢复管形成;而在 miR-885-3p 过表达的 HMEC-1 细胞中加入外源性 VEGFA 或 TGFβ1,对管形成的恢复作用显著弱于回补 BMPR1A 的效果,证实 miR-885-3p 虽可调控 VEGFA、TGFβ1 等细胞因子,但通过靶向 BMPR1A 阻断 BMP/Smad/Id1 信号通路是其发挥抗血管生成作用的主要途径。
本研究首次阐明 miR-885-3p 在结肠癌血管生成和肿瘤生长中的作用及分子机制,证实 miR-885-3p 可在体内外直接抑制内皮细胞的血管生成相关功能,其通过直接靶向结合 BMPR1A 的 3'UTR,下调 BMPR1A 表达,进而阻断 BMP/Smad/Id1 信号通路的激活,抑制促血管生成因子 Id1 的表达,这是其发挥抗血管生成作用的核心机制;BMPR1A 作为促血管生成因子,其敲低可抑制血管生成,回补 BMPR1A 可逆转 miR-885-3p 的抗血管生成效应。在多种肿瘤细胞系及结肠癌临床标本中,miR-885-3p 与 BMPR1A 的表达呈显著负相关,结肠癌中 miR-885-3p 低表达、BMPR1A 高表达;过表达 miR-885-3p 可显著抑制裸鼠中 HT-29 结肠癌异种移植物的生长,该效应依赖于其对肿瘤血管生成的抑制,且对小鼠无明显毒性。此外,miR-885-3p 虽可调控 VEGFA、TGFβ1 等其他促血管生成因子的表达,但其通过阻滞 BMPR1A 和 BMP/Smad/Id1 信号通路介导的抗血管生成作用更为显著,同时 BMPR1A 可通过上调 VEGFA 促进肿瘤血管生成,揭示了肿瘤细胞与内皮细胞间的交叉调控机制。本研究证实 miR-885-3p 是结肠癌中重要的抑癌性 miRNA,为结肠癌的抗血管生成治疗提供了新的靶点,也为 miRNA 靶向治疗肿瘤提供了新的实验证据和理论依据。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:猪与啮齿类(小鼠 / 大鼠)支持细胞(SCs)分离、培养及肾被膜下移植的标准化实验方案