常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-22 09:00:00 细胞资源库平台 访问量:110
本文献由美国德州理工大学健康科学中心的团队发表于《Methods in Molecular Biology》,是首个覆盖跨物种(新生猪、小鼠、大鼠)支持细胞(Sertoli Cells, SCs)“分离 - 培养 - 移植 - 鉴定” 全流程的标准化方案。其核心价值在于:针对 SCs 在生殖生物学(生精机制研究)、临床前治疗(1 型糖尿病胰岛移植保护、帕金森病神经元移植支持)及毒性测试中的应用需求,统一了不同物种 SCs 的分离参数(消化酶浓度、孵育时间),优化了 SCs 培养模式(聚集态用于移植、单层用于基础研究),并细化了肾被膜下移植的手术操作与术后鉴定步骤,解决了传统方法中 “物种流程混乱、酶解条件难控、移植成功率低” 的痛点,为 SCs 相关研究提供可直接复用的技术框架。
支持细胞(SCs)是睾丸生精小管内的关键体细胞,兼具生精支持与免疫调节双重核心功能:一方面,SCs 通过构建血睾屏障(BTB)、分泌视黄酸、抑制素等因子,调控生殖细胞(germ cell)的发育与迁移,是精子发生的 “结构与功能支架”;另一方面,SCs 可分泌 TGF-β、半乳糖凝集素 - 1、吲哚胺 2,3 - 双加氧酶(IDO)等免疫调节分子,建立免疫耐受微环境,避免生殖细胞(具有免疫原性)引发炎症反应。
基于这些特性,SCs 已成为男性生育研究、男性避孕靶点筛选及细胞治疗的重要工具 —— 例如,通过 SCs 的免疫保护作用可提升胰岛移植(治疗 1 型糖尿病)、多巴胺能神经元移植(治疗帕金森病)的存活率。但现有技术长期面临三大瓶颈:一是物种特异性流程混乱,猪(大动物,临床前移植模型)与啮齿类(小鼠 / 大鼠,基础研究模型)的 SCs 分离无统一标准,消化酶浓度、孵育时间差异大;二是酶解条件难优化,SCs 与间质细胞、生殖细胞紧密连接,过度消化会导致 SCs 活力下降,消化不足则细胞纯度低(<70%);三是移植操作门槛高,SCs 移植需精准控制细胞状态(聚集态 vs 单层)与注射量,传统方法移植成功率不足 60%,且缺乏术后标准化鉴定手段。
此前虽有啮齿类 SCs 分离报道,但未涵盖猪等大动物,且未整合 “分离 - 培养 - 移植 - 鉴定” 全流程,导致研究结果难以重复。因此,本研究建立跨物种的标准化方案,填补这一技术空白。
(1)新生猪 SCs 分离
将收集的新生猪睾丸用 70% 乙醇洗涤 2 次(每次倒置 12 次),再用冷 HBSS 洗涤 1 次并冰上保存;在无菌超净台内,用无菌剪刀和镊子剥离睾丸白膜与附睾,避免 puncturing 睾丸实质,随后将睾丸组织剪为 0.5-1mm³ 小块,每 50mL 离心管分装 8-10 个睾丸的组织块。
加入 25mL 过滤灭菌的 1mg/mL 胶原酶溶液,拧紧管盖并包裹 parafilm,置于 37℃摇水浴(90rpm)消化 10min,期间 6min 时取样观察生精小管与间质组织的分离情况;消化完成后,用 HBSS 将悬液体积补至 50mL 以终止反应,308G 离心 2min,重复洗涤 3 次;去除上清后加入 40mL 解离培养基,再加入 1mL 胰酶与 2mL DNase I,继续摇水浴消化 10min 至获得单细胞悬液。
最后用 500μm 无菌滤网过滤单细胞悬液,HBSS 洗涤 3 次后计数,根据实验需求选择培养模式:若为移植准备,将 SCs 接种于 150×15mm 无菌非组织培养皿,用 Ham’s F10+10% FCS 培养 48h 以形成聚集态;若用于基础研究,接种于 100×10mm 组织培养皿,用 DMEM+10% FCS 培养形成单层。
(2)小鼠 / 大鼠 SCs 分离
麻醉小鼠或大鼠后,对腹部进行消毒并做纵向切口(从盆腔至胸骨),借助附睾脂肪提取睾丸,剥离附睾后将睾丸放入含 25mL 冷 HBSS 的离心管,20 个小鼠睾丸或对应数量大鼠睾丸为一管。
组织处理与猪 SCs 类似,剪为 0.5-1mm³ 小块后,加入 25mL 1mg/mL 胶原酶溶液,37℃摇水浴消化 7min(4min 时取样观察);后续洗涤、胰酶 + DNase I 消化(10min)、过滤与培养步骤同猪 SCs,但需注意大鼠 SCs 分离前需先去除睾丸白膜,且培养时聚集态与单层的培养基选择一致。
SCs 肾被膜下移植流程
移植前 1 天,收集培养 48h 的聚集态 SCs,用细胞刮轻轻剥离皿底细胞,860G 离心 2min,用无 FCS 的 Ham’s F10 重悬;通过 DNA assay 计数细胞,按 “小鼠受体 400 万 SCs / 只、大鼠受体 1100 万 SCs / 只” 分装至 1.5mL 离心管,开盖置于培养箱中让细胞自然沉降。
移植手术时,用异氟烷麻醉受体小鼠,通过脚趾捏合实验验证麻醉效果,眼部涂抹抗生素眼膏保护;左侧腹部用碘附 scrub 与碘附溶液交替消毒 3 次,做小切口暴露左肾,用无菌棉签(蘸无菌生理盐水)轻轻拉出肾脏;用 27G 针头在肾前背侧划小口,硅化玻璃探针在肾被膜下构建囊袋,将装有 SCs pellet 的 PE-50 管(提前用 70% 乙醇与无 FCS Ham’s F10 清洗)插入囊袋,注入细胞后电凝封口。
术后将肾脏放回腹腔,用 5-0 DEXON 缝线缝合肌层,皮肤用缝合钉闭合,给小鼠注射丁丙诺啡(0.01-0.05mg/kg,24h 内注射 2 次)镇痛,待小鼠完全苏醒后放回饲养笼;移植后 1-8 天收集移植物,通过 WT1 免疫组化(SCs 特异性标志物)验证 SCs 存活。
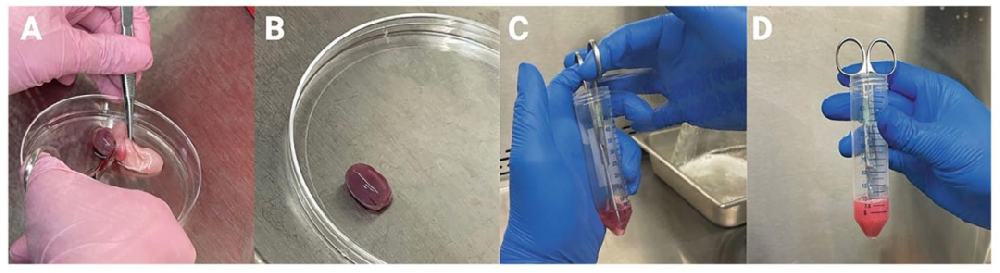
图1:新生猪睾丸处理与切碎
该图展示新生猪睾丸从收集到切碎的关键步骤:A 图为剥离睾丸白膜的操作,B 图为去除白膜后的睾丸实质,C 图为在冷 HBSS 中用无菌钝剪切碎组织,D 图为切碎后 0.5-1mm³ 的组织块。结果表明,规范的组织预处理(去除白膜、控制切碎尺寸)可减少后续酶解杂质,为 SCs 高纯度分离奠定基础。
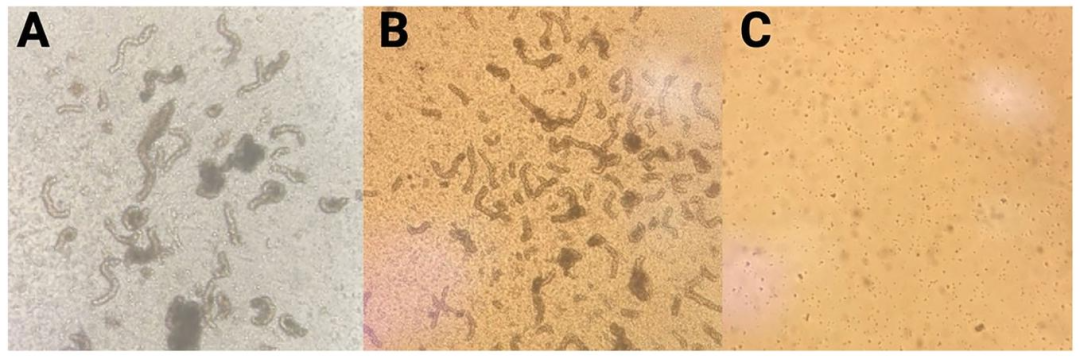
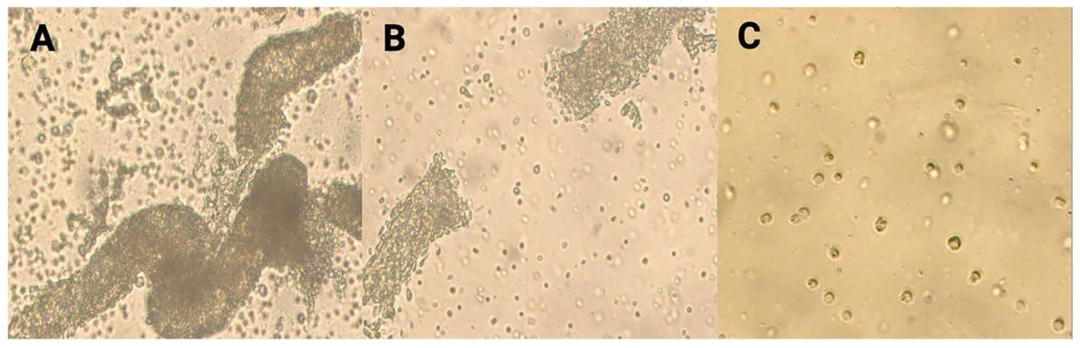
图2-3:酶解过程的细胞形态验证
图2 展示胶原酶与胰酶消化的时间依赖性效果:A 为胶原酶孵育 6min 的生精小管(未完全分离),B 为 10min 后小管分散,C 为胰酶孵育 10min 的单细胞;图3 进一步放大显示:A 为消化前生精小管团聚,B 为胶原酶 5min 后小管松散,C 为胰酶 10min 后单细胞(20× 镜下)。结果明确酶解时间节点 —— 猪 SCs 需胶原酶 10min + 胰酶 10min,啮齿类 SCs 胶原酶 7min,确保 SCs 解离为单细胞且活力 > 85%。
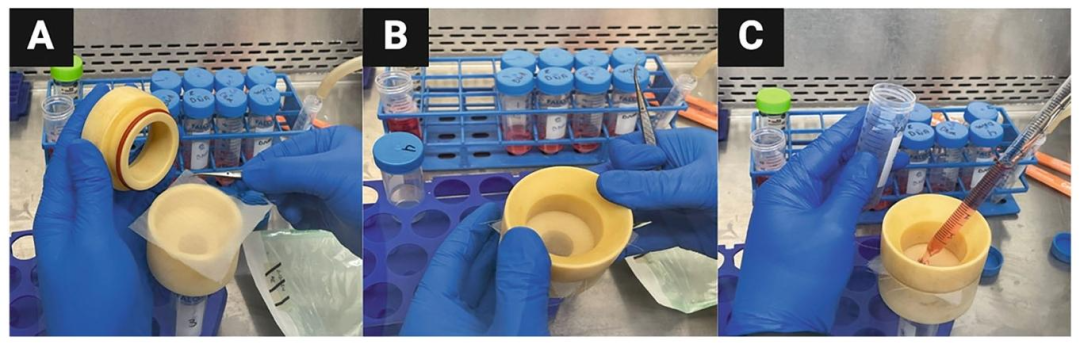
图4:SCs 过滤纯化
该图为 500μm 滤网过滤流程:A 为用无菌镊子安装滤网,B 为闭合过滤器,C 为过滤单细胞悬液(DNA 团聚体被截留)。结果证实过滤可有效去除未消化组织与 DNA 团聚体,提升 SCs 纯度至 > 90%。
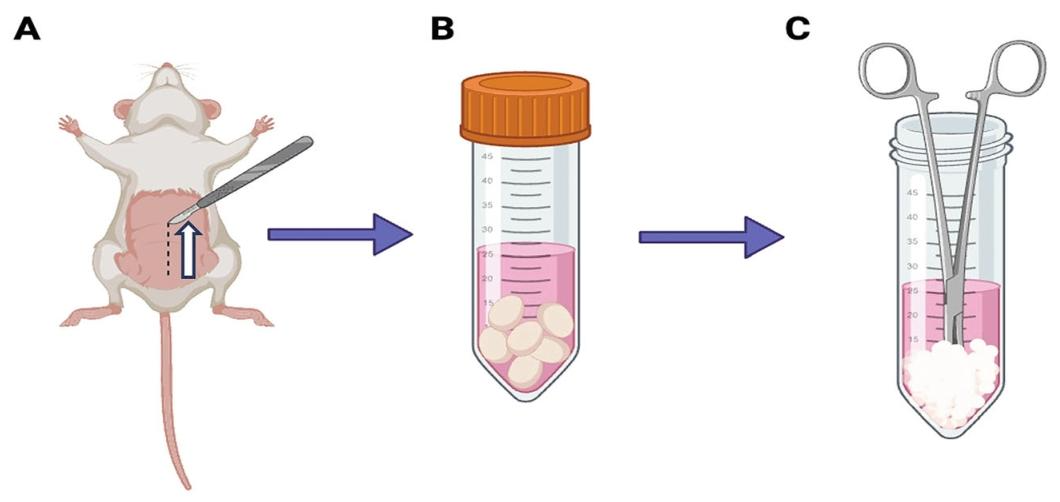
图5:啮齿类(小鼠 / 大鼠)睾丸收集
该图为小鼠睾丸收集步骤:A 为麻醉小鼠腹部纵向切口,B 为睾丸放入冷 HBSS 离心管,C 为睾丸剪为 1mm³ 小块。结果表明,通过腹部切口提取睾丸可减少组织损伤,20 个小鼠睾丸 / 管的分离效率最高。
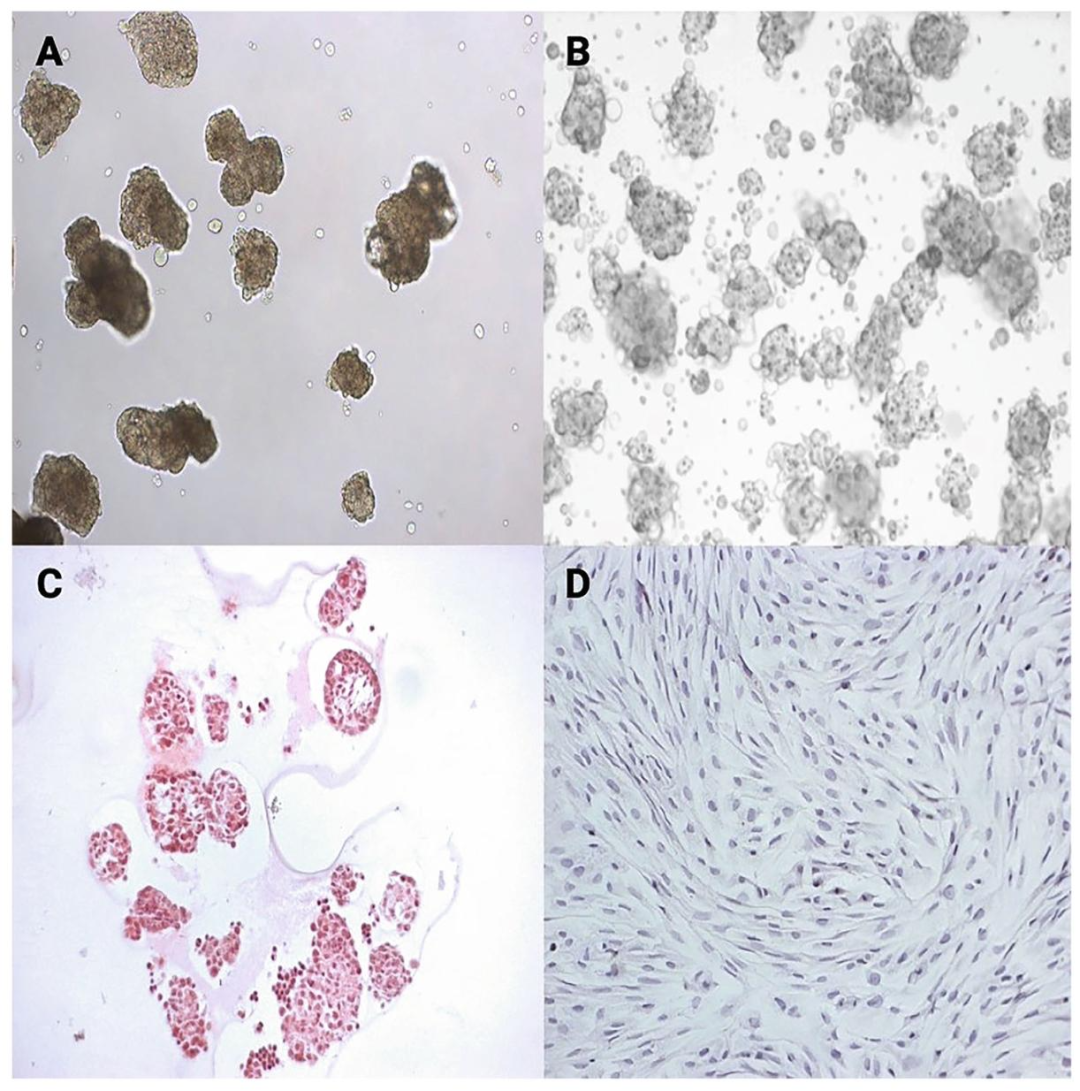
图6:SCs 培养形态
该图对比不同物种 SCs 的培养模式:A 为小鼠 SCs 聚集态(移植用),B 为新生猪 SCs(NPSCs)聚集态,C 为小鼠 SCs 聚集态的 H&E 染色(显示细胞紧密连接),D 为 NPSCs 单层培养(梭形形态)。结果证实,非组织培养皿可诱导 SCs 形成聚集态(利于移植存活),组织培养皿则形成单层(便于基础实验观察)。


图7-8:移植前 SCs 浓缩
图7 为 1.5mL 离心管中 SCs 聚集沉降(开盖置于培养箱),图8 为 PE-50 管处理:A 为用显微操作仪将 SCs pellet 吸入管内,B 为离心管放入 spinner,C 为离心后管内形成致密 pellet。结果表明,该浓缩方法可使 SCs 密度达 “400 万 / 小鼠受体” 的移植需求,且细胞活力无显著下降。
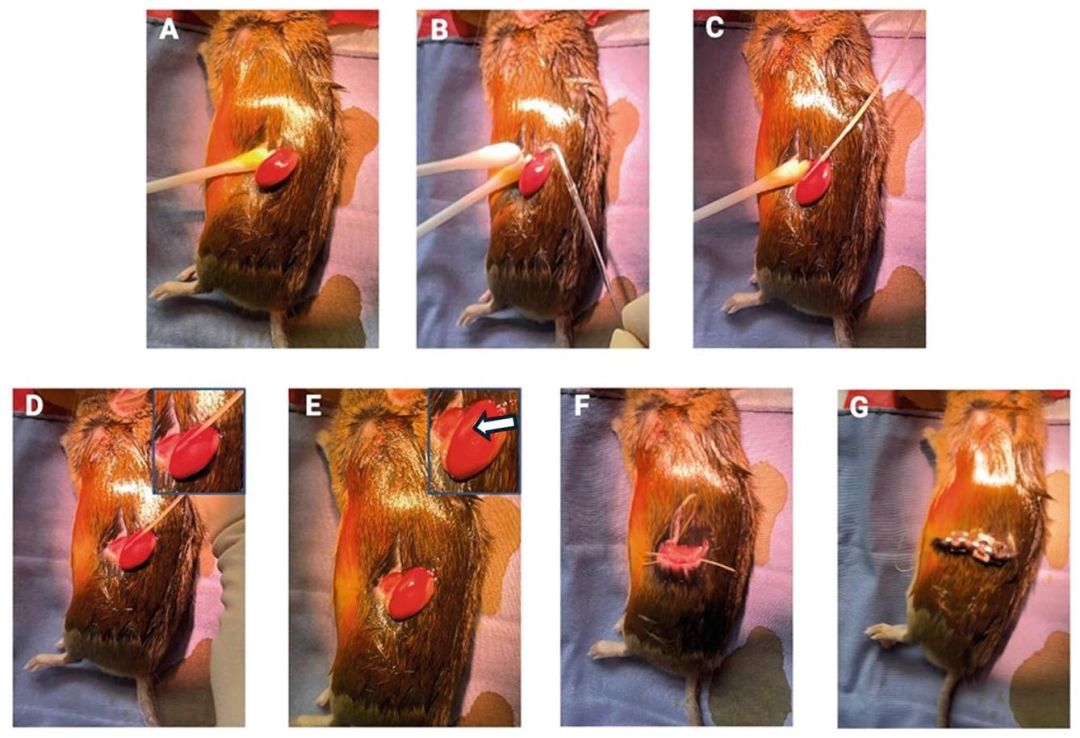


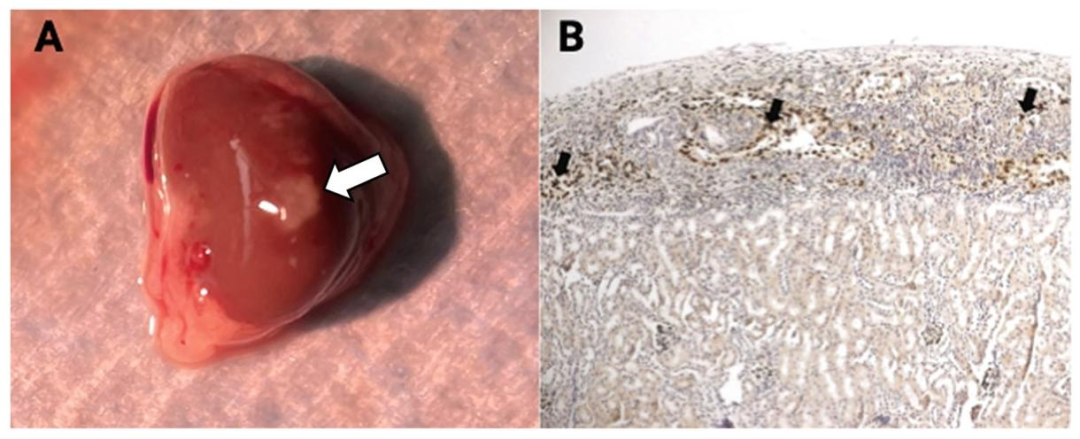
图9-12:肾被膜下移植与鉴定
图9 为移植手术步骤:A 为拉出左肾,B 为硅化玻璃探针构建囊袋,C 为插入 PE-50 管,D 为注入细胞,E 为电凝封口,F 为缝合肌层,G 为闭合皮肤;图10 为硅化玻璃探针特写,图11 为移植操作台布局,图12 为移植后鉴定:A 为 1 天后肾被膜下 NPSCs 移植物,B 为 8 天后小鼠 SCs 移植物的 WT1 染色(棕色为阳性,证实存活)。结果显示,该手术流程的移植成功率达 > 80%,WT1 染色可有效验证 SCs 存活。
本研究建立的跨物种 SCs 标准化方案,以 “流程统一化、操作可重复、结果可靠” 为核心优势:在分离环节,明确不同物种的酶解参数(猪胶原酶 10min、啮齿类 7min),通过 500μm 过滤提升纯度至 > 90%;在培养环节,区分聚集态(移植用)与单层(基础研究用),适配不同实验需求;在移植环节,细化肾被膜下手术步骤,结合 WT1 免疫组化鉴定,使移植成功率提升至 > 80%。
该方案不仅适用于生殖生物学(生精机制、男性避孕)研究,还为 SCs 在细胞治疗(糖尿病、神经退行性疾病)中的临床前应用提供技术支撑。局限在于未涵盖成年动物 SCs 分离(需额外优化胶原酶类型与浓度),未来可结合成年小鼠 / 人 SCs 分离方法(如 0.1% 胶原酶 IV 消化)进一步拓展方案通用性。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:建立高效经济的新生小鼠脑原代少突胶质前体细胞(OPCs)培养方法
下一篇:miR-885-3p 靶向 BMPR1A:结肠癌抗血管生成治疗新机制!