常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-19 17:02:16 细胞资源库平台 访问量:151
英文标题:Rothia mucilaginosa membrane vesicles stabilize labile iron to alleviate UVB-induced ferroptosis
中文标题:粘液罗斯菌膜囊泡稳定不稳定铁以减轻UVB诱导的铁死亡
发表期刊:《Cell Host & Microbe》
影响因子:18.7
作者单位:
空军军医大学口腔医院口腔预防科、口腔生物学教研室、组织工程中心;空军军医大学西京医院皮肤科;空军军医大学基础医学院医学微生物学与寄生虫学教研室等
作者信息:
Siyuan Fan, Xinyue Cai, Weiqi Wang, ..., Zihan Li, Kun Xuan, Shiyu Liu
1.临床问题: 紫外线B(UVB)照射是导致唇部光化性唇炎(AC)的主要原因,这是一种潜在的恶性疾病。唇红部因缺乏附属器和黑色素细胞,尤其易受UVB损伤。
2.共生菌群的角色: 共生微生物群在维持宿主屏障功能和抵御环境压力中发挥重要作用。然而,唇部共生菌是否能保护宿主免受UVB损伤尚不清楚。
3.研究切入点: 研究发现,在高原地区人群中,光化性唇炎患者唇部共生菌——粘液罗斯菌的丰度显著降低,且其丰度与唇部屏障功能(经皮水分流失)呈负相关,提示其可能具有保护作用。
4.研究创新点:
本研究揭示了UVB照射下,唇部共生菌粘液罗斯菌释放的膜囊泡(RMVs)被宿主角质形成细胞的内吞体/溶酶体摄取。RMVs携带的细菌源性的亚铁螯合酶(FECH) 在溶酶体这一非经典位点,催化过量的二价铁离子(Fe²⁺)和卟啉转化为血红素,从而稳定细胞内不稳定铁池,减轻氧化应激和铁死亡,最终缓解UVB引起的皮肤和唇部损伤。这项工作阐明了一种前所未有的跨界保护机制,即共生菌通过膜囊泡向宿主细胞输送功能性酶,调控宿主细胞代谢以抵御环境胁迫。
1.临床样本分析: 采集高原地区健康志愿者和光化性唇炎患者的唇部拭子,进行16S rRNA全长测序,分析微生物组成,并与临床指标(经皮水分流失,TEWL)进行关联分析。
2.细菌与膜囊泡(RMVs)制备与表征:
培养粘液罗斯菌,通过超速离心法提取并纯化其分泌的膜囊泡(RMVs)。
使用透射电镜(TEM)、扫描电镜(SEM)、纳米颗粒追踪分析(NTA)、Zeta电位分析等技术表征RMVs的形态、大小、表面电荷和内含物(蛋白、DNA、RNA)。
3.细胞实验:
使用人角质形成细胞系(HaCaT),评估HaCaT细胞对RMVs的摄取效率(共聚焦显微镜、流式细胞术)。
建立UVB照射诱导的细胞损伤模型,通过CCK-8、LDH释放、PI染色评估细胞活力与死亡。
通过特异性探针(FerroOrange, OxC11-BODIPY, 4HNE, 8-OHdG, DCFH-DA)和试剂盒检测细胞内铁离子水平、脂质过氧化、DNA氧化损伤、活性氧(ROS)和谷胱甘肽(GSH)水平,确定铁死亡的发生与缓解。
通过细胞器共定位(溶酶体、线粒体、内质网、高尔基体)、Western Blot、提取细胞器(溶酶体)检测等技术,探究RMVs的胞内定位及其对铁代谢、血红素合成的影响。
使用siRNA敲低细胞内源性FECH,验证RMVs中细菌FECH的功能。
4.动物实验:
SD大鼠唇部UVB照射模型和C57BL/6J小鼠背部皮肤UVB照射模型。
分组:空白凝胶组、粘液罗斯菌活菌组、RMVs组、铁死亡抑制剂(Fer-1)组等,局部给药。
评估指标:大体照片观察唇部/皮肤损伤,H&E染色观察组织病理学变化(上皮厚度、炎症浸润),Masson染色观察胶原沉积,免疫荧光染色(IL-1β, MPO, Ki67, K6, 4HNE, 8-OHdG等)检测炎症、增殖、氧化损伤,试剂盒检测SOD活性、MDA含量、细胞因子水平。
提取表皮组织和溶酶体,检测Fe²⁺、卟啉、血红素含量。
5.分子机制研究:
蛋白质组学分析: 对RMVs内容物进行LC-MS/MS质谱分析,鉴定关键功能蛋白。
分子克隆与建模: 克隆粘液罗斯菌亚铁螯合酶(命名为RmCpfC)基因,使用AlphaFold预测其3D结构,通过分子对接和动力学模拟分析其与底物(卟啉)的结合能力和在不同pH环境下的稳定性。
酶活性验证: 体外重构酸性环境(pH 5.0),加入RMVs、亚铁离子和卟啉,通过紫外-可见吸收光谱和荧光检测验证RmCpfC催化血红素合成的活性。
6.临床转化潜力评估:
评估冻干RMVs制剂的稳定性。
在小鼠模型中评估含RMVs药膏的长期应用生物安全性(血常规、肝肾功能、主要脏器病理)。
开展小规模随机对照临床试验(ChiCTR2500100015),初步评估含RMVs药膏对光化性唇炎患者的治疗效果。
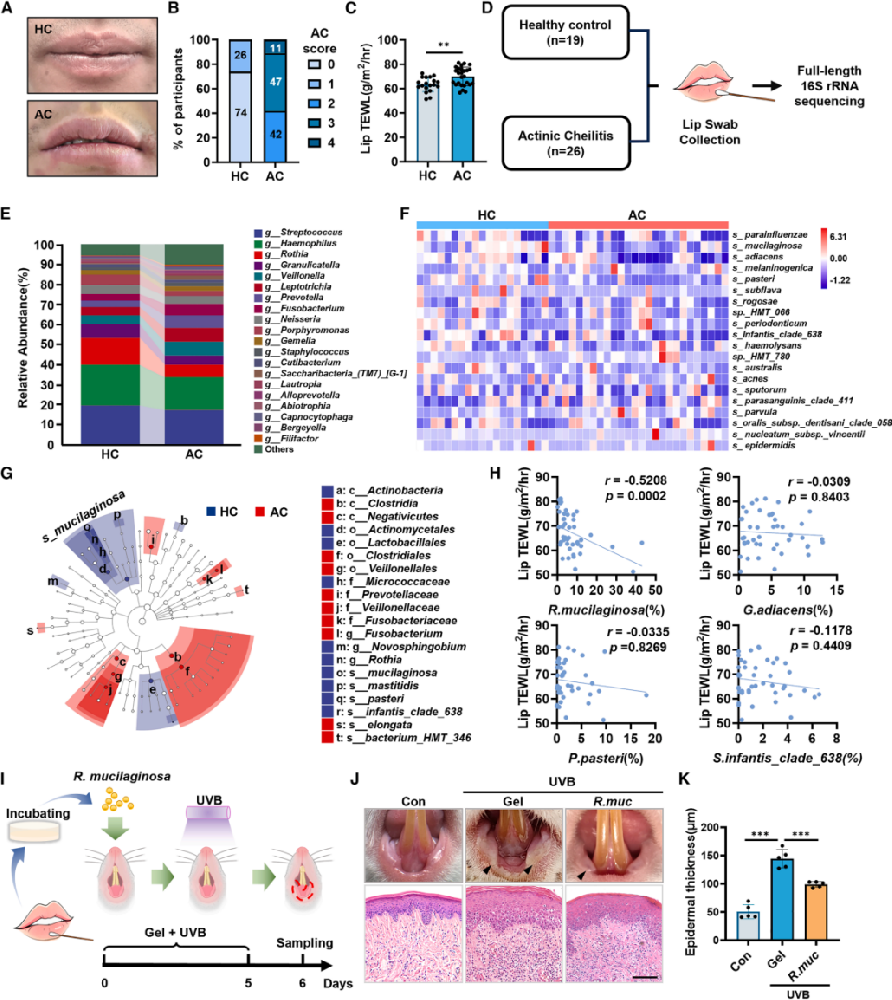
图1 | 人唇红部粘液罗斯菌丰度及其对UVB损伤的保护作用
(A)健康志愿者(HC)和光化性唇炎患者(AC)的代表性唇部图像。(B)参与者AC临床评分分布。(C)HC组和AC组的经皮水分流失(TEWL)水平。(D)唇部微生物样本采集与测序流程示意图。(E)排名前20的菌属相对丰度堆积条形图。(F)排名前20的菌种丰度模式热图。(G)LEfSe分析的进化分支图。(H)细菌种类相对丰度与参与者TEWL水平的Spearman相关性分析。
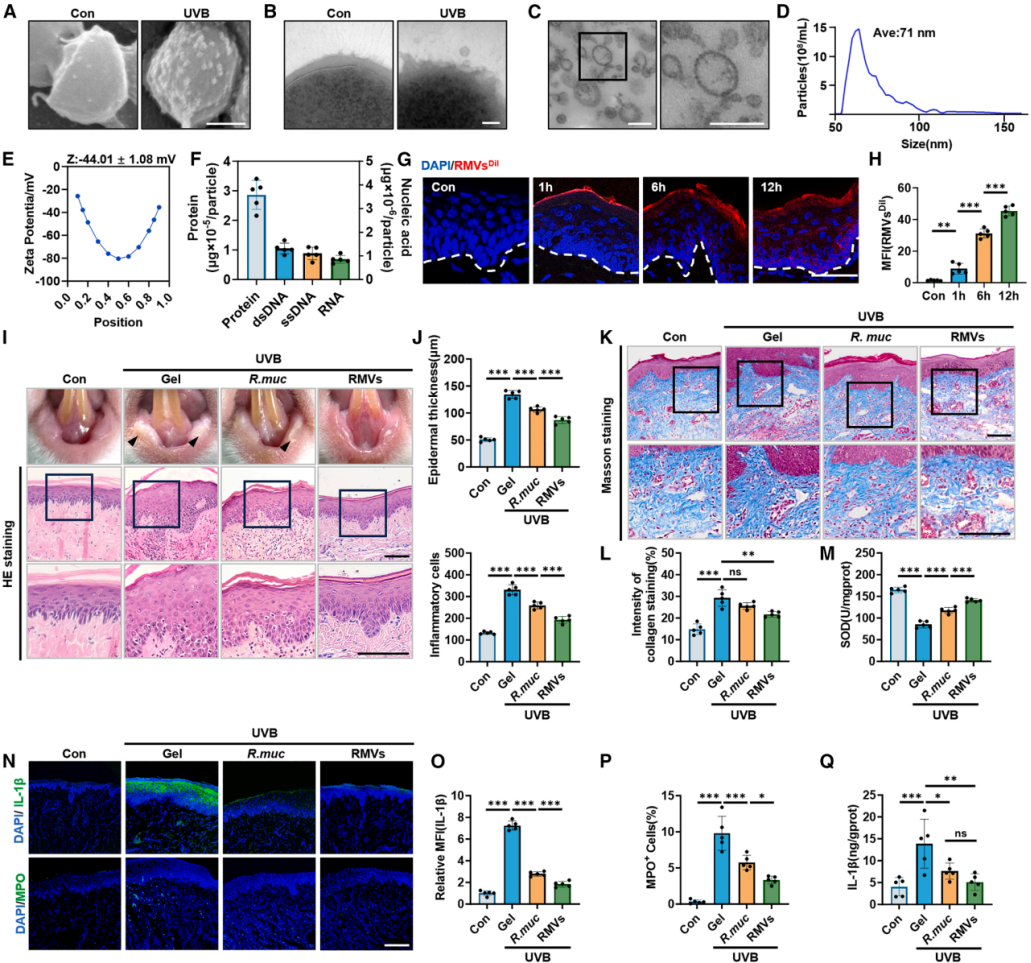
图2 | 粘液罗斯菌释放的RMVs减轻UVB诱导的黏膜损伤
(A-B)R. mucilaginosa的代表性SEM和TEM图像。(C)RMVs的代表性TEM图像。(D)RMVs粒径分布的NTA分析。(E)RMVs的平均Zeta电位。(F)RMVs内蛋白、dsDNA、ssDNA和RNA的浓度分析。(G-H)局部涂抹后,Dil标记的RMVs在唇组织中的代表性荧光图像及平均荧光强度(MFI)定量分析。(I-J)各组唇组织代表性大体图、H&E染色图像及表皮厚度和炎性细胞数量定量。(K-L)代表性Masson染色图像及胶原强度定量。(M)唇组织中SOD水平定量。(N-P)唇组织中IL-1β和MPO的代表性荧光图像及相对MFI和阳性细胞百分比定量。(Q)唇组织中IL-1β的ELISA分析。
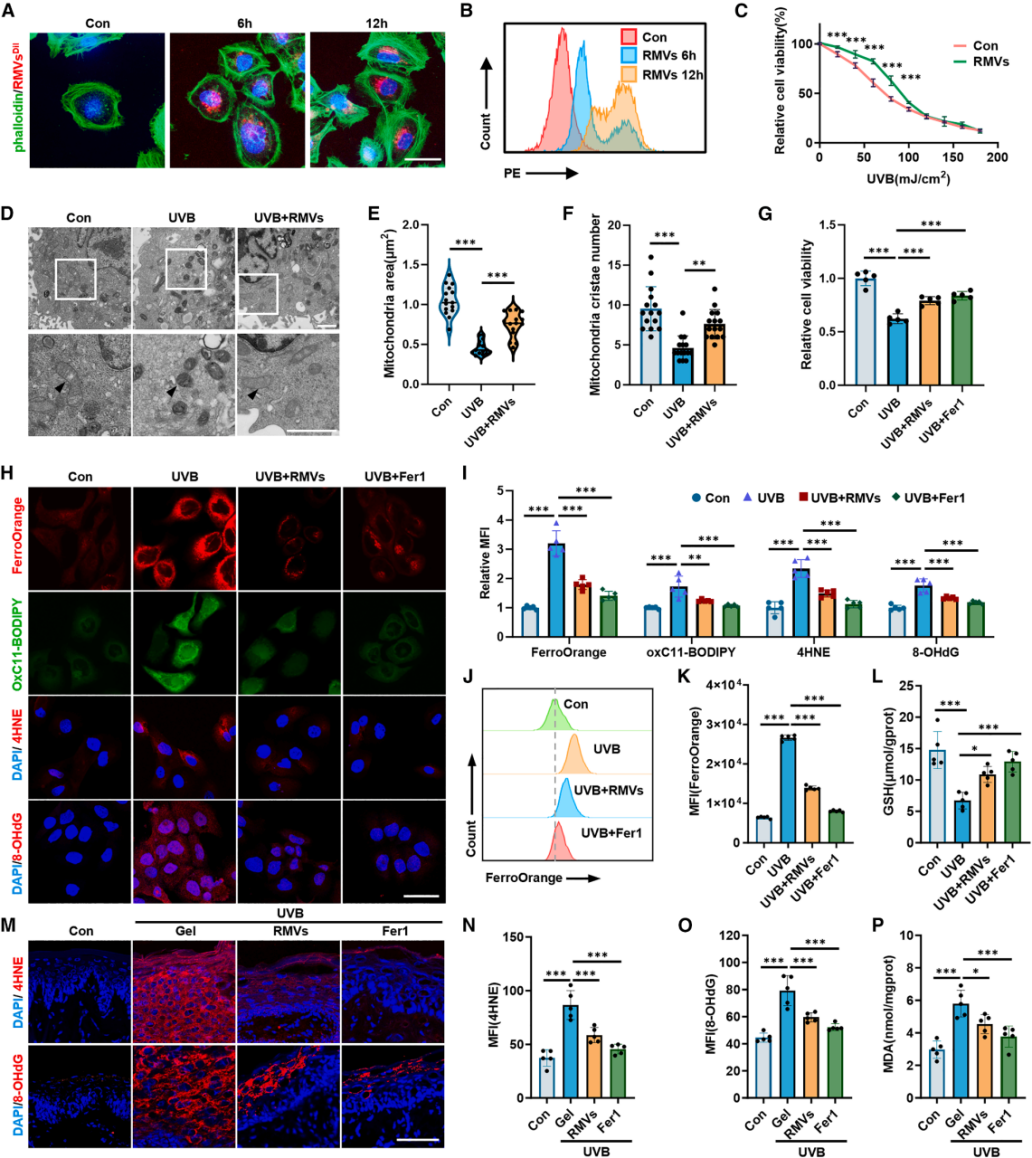
图3 | RMVs保护角质形成细胞免受UVB诱导的铁死亡
(A)Dil标记的RMVs在HaCaT细胞中的代表性荧光图像。(B)HaCaT细胞对Dil标记的RMVs时间依赖性摄取的流式细胞术分析。(C)不同剂量UVB照射下,RMVs处理对HaCaT细胞活力的影响(CCK-8法)。(D-F)HaCaT细胞代表性TEM图像及线粒体面积和嵴数量定量分析。(G)不同处理后HaCaT细胞活力分析。(H)HaCaT细胞中FerroOrange、OxC11-BODIPY、4HNE和8-OHdG的代表性荧光图像。(I-J)流式细胞术分析细胞内铁水平及平均荧光强度(MFI)定量。(K)GSH水平定量。(L-N)大鼠唇组织中4HNE和8-OHdG的代表性荧光图像及MFI定量。(O)MDA水平定量。
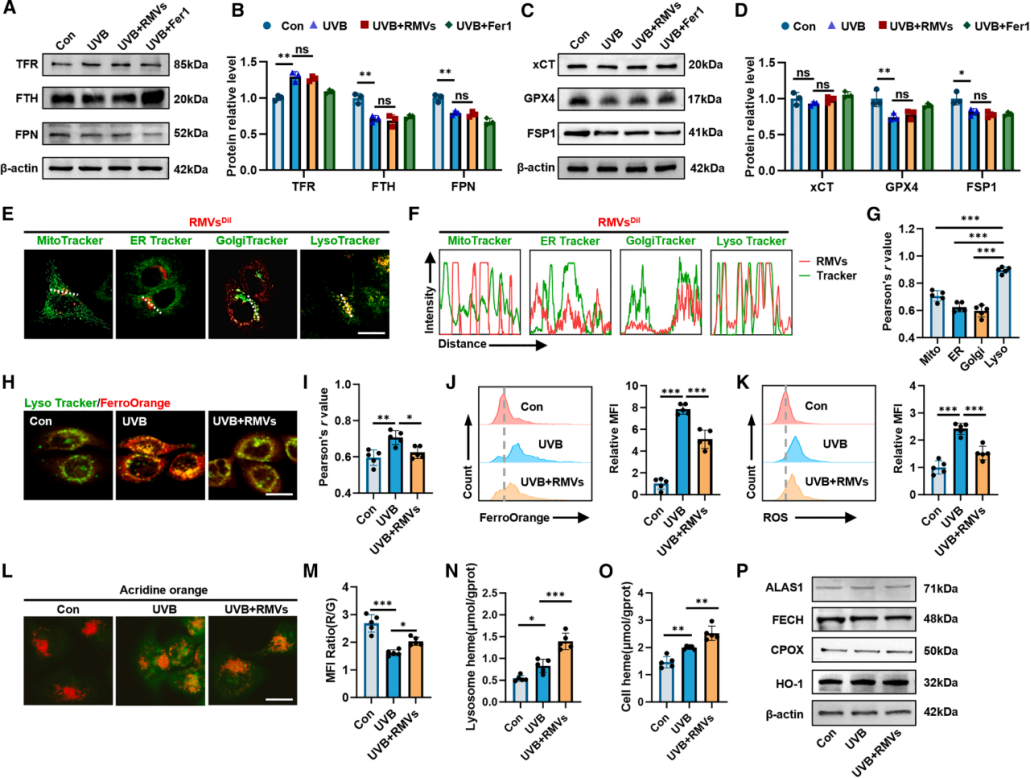
图4 | RMVs减少UVB诱导的溶酶体不稳定铁积累并提高HaCaT细胞的血红素水平
(A-B)Western blot检测HaCaT细胞中TFR、FTH和FPN的表达。(C-D)Western blot检测xCT、GPX4和FSP1的表达。(E)RMVs与线粒体、内质网、高尔基体和溶酶体在HaCaT细胞中的共定位荧光图像。(F)荧光强度与距离线图显示RMVs与不同细胞器的共定位模式。(G)RMVs与细胞器的皮尔逊共定位系数(PCC)分析。(H)溶酶体与不稳定铁在HaCaT细胞中的共定位荧光图像。(I)溶酶体与不稳定铁的PCC分析。(J)从HaCaT细胞提取的溶酶体中不稳定铁水平的流式细胞术分析及相对MFI定量。(K)溶酶体中ROS水平的流式细胞术分析及相对MFI定量。(L)吖啶橙染色的HaCaT细胞代表性荧光图像。(M)吖啶橙红/绿MFI比值定量分析。(N-O)溶酶体和HaCaT细胞内血红素水平定量分析。(P)Western blot检测ALAS1、FECH、CPOX和HO-1的表达。
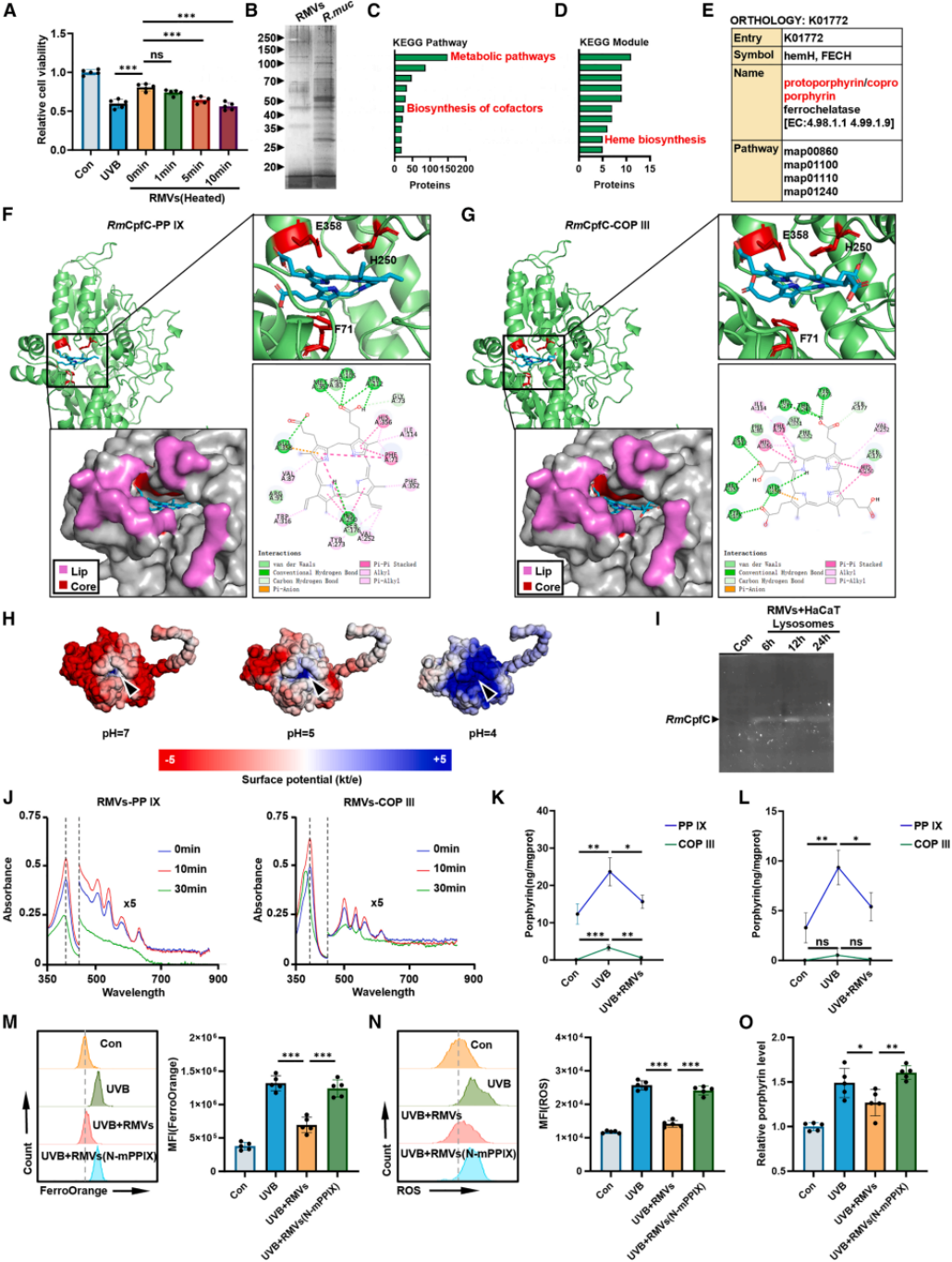
图5 | RMVs携带的RmCpfC具有血红素合成酶活性
(A)CCK-8法分析细胞活力。(B)RMVs和R. mucilaginosa蛋白的SDS-PAGE考马斯亮蓝染色分析。(C)从RMVs和R. mucilaginosa中鉴定出的FECH(原核型)质谱肽段。(D)RmCpfC蛋白结构建模及分子对接模拟。(E)RmCpfC与粪卟啉III(COP III)和原卟啉IX(PP IX)的分子对接模型。(F-G)RmCpfC的表面电荷分布和活性位点结构。(H)不同pH条件下RmCpfC的表面静电势图。(I)不同物种FECH与卟啉的分子对接结合能比较。(J)体外酶促反应体系中,不同处理后卟啉(PP IX)的紫外-可见吸收光谱变化。(K-L)RMVs催化Fe²⁺与COP III或PP IX反应后的荧光强度变化。(M)FECH敲低后,不同处理对HaCaT细胞内血红素水平的影响。(N)不同处理后HaCaT细胞内卟啉水平的LC-MS/MS分析。(O)不同细菌来源的MVs对UVB照射后HaCaT细胞活力的影响。(P)不同处理后HaCaT细胞中脂质过氧化水平。
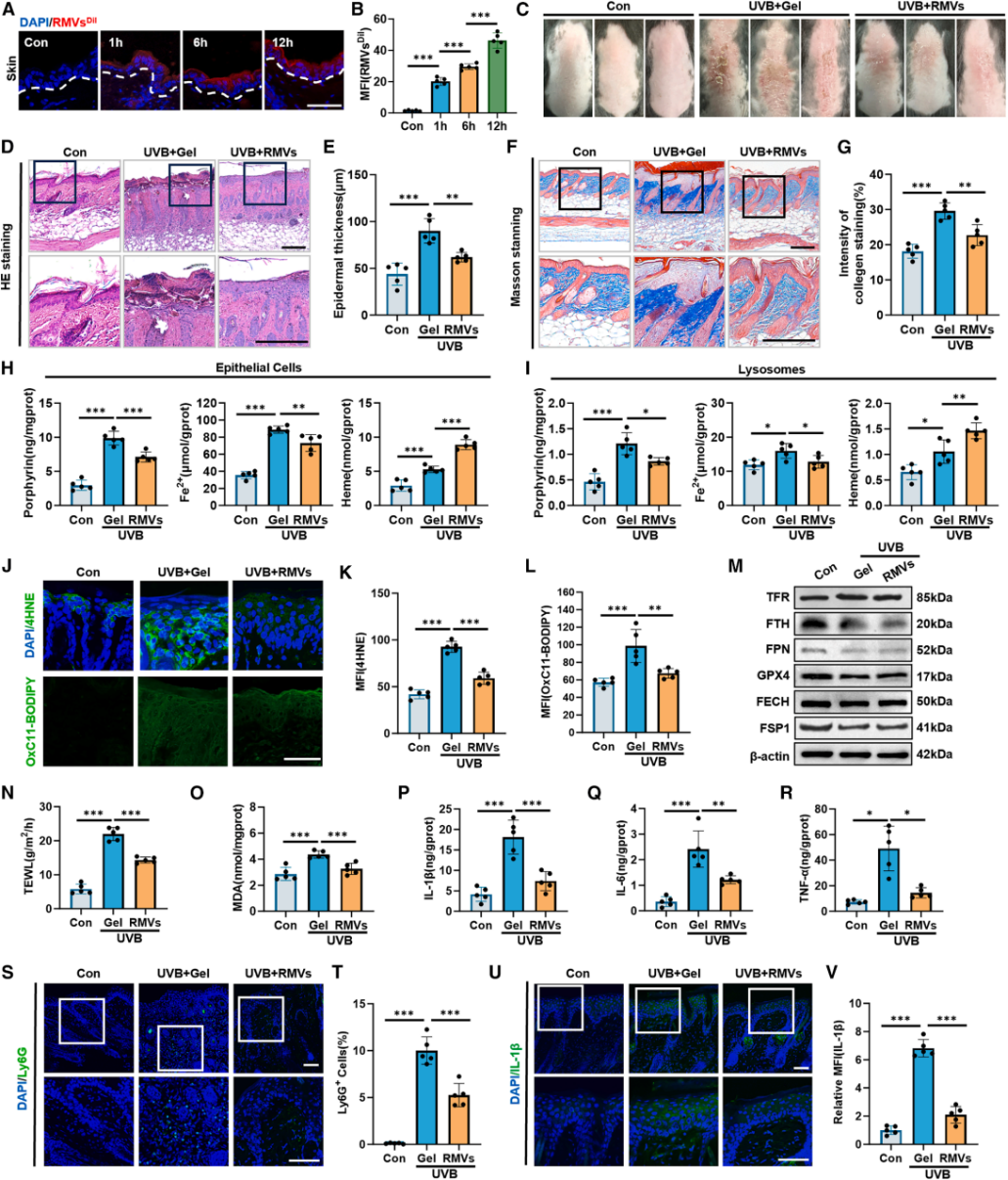
图6 | RMVs催化Fe²⁺和卟啉生成血红素以抑制铁死亡并减轻UVB诱导的皮肤损伤
(A-B)Dil标记的RMVs在小鼠皮肤中的代表性荧光图像及MFI定量。(C)各组皮肤代表性大体图。(D-E)皮肤组织代表性H&E染色图像及表皮厚度定量分析。(F-G)代表性Masson染色图像及胶原含量定量分析。(H-I)皮肤上皮细胞及分离的表皮溶酶体中卟啉、Fe²⁺和血红素水平的定量分析。(J-L)皮肤中4HNE和OxC11-BODIPY的代表性荧光图像及MFI定量。(M)Western blot检测上皮细胞中铁代谢及抗氧化相关蛋白的表达。(N)皮肤TEWL定量分析。(O)皮肤MDA水平定量分析。(P-R)ELISA分析皮肤中IL-1β、IL-6和TNF-α水平。(S-T)皮肤中Ly6G的代表性荧光图像及阳性细胞百分比定量。(U-V)皮肤中IL-1β的代表性荧光图像及相对MFI定量。
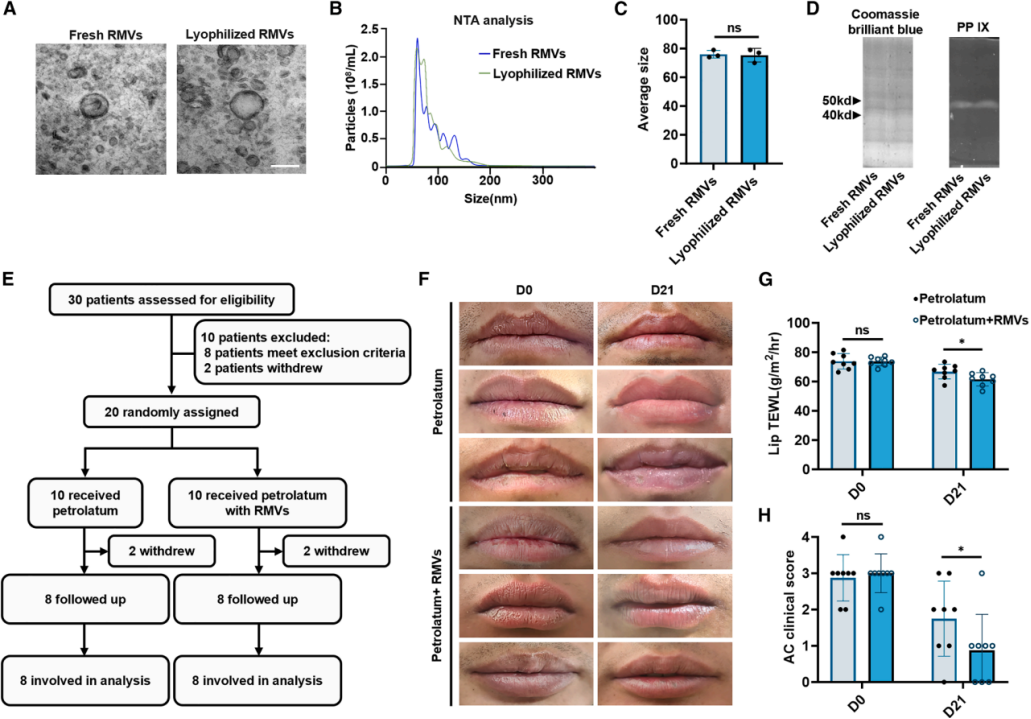
图7 | RMVs在临床前模型和临床试验中缓解慢性UV损伤
(A)冻干前后RMVs的TEM图像。(B-C)冻干前后RMVs的粒径分析。(D)冻干RMVs中RmCpfC与PP IX结合后的荧光凝胶图像。(E)临床试验的CONSORT流程图。(F)临床试验中代表患者的唇部图像。(G-H)临床试验中患者TEWL测量值和AC临床评分的变化。
1.关键菌群发现: 唇部共生菌粘液罗斯菌的丰度与光化性唇炎严重程度呈负相关,外源性补充该菌可减轻大鼠UVB诱导的唇部损伤。
2.作用载体: UVB照射刺激粘液罗斯菌释放膜囊泡(RMVs),RMVs可被角质形成细胞高效摄取并定位于溶酶体,其保护效果优于活菌。
3.核心机制: RMVs通过向宿主细胞溶酶体递送细菌源性的亚铁螯合酶(命名为RmCpfC),在溶酶体酸性环境中催化过量的Fe²⁺和卟啉转化为血红素,从而:
稳定不稳定铁池,减少游离Fe²⁺。
减轻氧化应激和脂质过氧化。
最终抑制UVB诱导的角质形成细胞铁死亡。
4.治疗潜力: 含RMVs的药膏在动物模型中能有效缓解UVB引起的急性和慢性皮肤/唇部损伤,并在初步的小规模临床试验中显示出改善光化性唇炎患者症状的潜力,且安全性良好。
5.概念创新: 本研究揭示了一种前所未有的跨界保护机制:共生细菌通过释放膜囊泡,向宿主细胞输送功能性酶,在非经典细胞器(溶酶体)中调控宿主细胞的代谢过程(铁代谢),以共同抵御环境胁迫。这拓展了我们对共生菌与宿主关系的理解。
文献意义:
本研究首次揭示了唇部共生菌粘液罗斯菌通过其分泌的膜囊泡(RMVs)保护宿主免受UVB损伤的全新机制。这一发现不仅解答了唇部微生态与光化性唇炎发病之间的关联,更重要的是,它阐明了一种跨界分子交流模式:原核生物(细菌)利用膜囊泡作为载体,向真核生物(宿主)细胞器(溶酶体)递送功能性酶(亚铁螯合酶),直接参与并调控宿主细胞的代谢通路(血红素合成与铁稳态),从而干预宿主细胞的命运(铁死亡)。该研究为理解宿主-共生菌互作提供了全新的视角,并为治疗日光相关性皮肤病(如光化性唇炎、光老化)以及其他与铁代谢紊乱和氧化应激相关的疾病,提供了一种基于天然细菌衍生物的原创性治疗策略和候选药物。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:新型生物发光细胞系助力 PNETs 小鼠模型构建,为研究带来新工具!
下一篇:靶向 HPV16 剪接!双荧光素酶报告系统助力病毒基因调控研究!